3 листопада, 2020
Клінічна ефективність препарату Антраль® у хворих на хронічний панкреатит
 Актуальність проблеми ведення пацієнтів із хронічним панкреатитом (ХП) останніми роками істотно зросла і продовжує зростати в силу багатьох причин [3, 6, 11, 18]. Сумація та потенціювання несприятливих ефектів чинників ризику та дія етіологічних факторів ХП сприяють зростанню захворюваності на ХП та його перебігу, що прогресує, із порушенням зовнішньосекреторної недостатності підшлункової залози (ПЗ), розвитку мальдигестії, мальабсорбції, трофологічної недостатності хворих із порушенням усіх видів обміну [3, 6, 10, 13, 14, 18, 22, 23]. Проведені дослідження ланок патогенезу ХП за умов ізольованого перебігу та різноманітної коморбідності доводять важливу роль системного запалення [8, 16, 17, 22, 23], дисбалансу про- та протизапальних цитокінів [8, 11, 14, 16, 17, 23], чинників протеїназо-інгібіторної системи зі зростанням негативного впливу системного протеолізу [1, 6, 11, 14, 15, 20], порушення оксидантно-антиоксидантного гомеостазу з активацією оксидативного та нітрозитивного стресу на тлі дефіциту природних антиоксидантів та агентів детоксикації [1, 2, 6, 12, 19, 21], що сприяє розвитку ендогенної інтоксикації, яка зростає на тлі супровідного дисбіозу товстої кишки [1, 6, 11, 22]; гіперглікемії на тлі формування панкреатогенного цукрового діабету (ЦД) 3 типу [3, 8], змін ліпідного та білкового спектра крові [6, 8, 11], дисбалансу білкових та вуглеводно-білкових компонентів позаклітинного матриксу [8, 15, 18, 19, 23], які в сукупності сприяють прискоренню апоптозу ацинарного епітелію, його цитолізу, гальмуванню репаративних процесів та активації процесів фіброзування ПЗ [1, 3, 8, 15, 22, 23].
Актуальність проблеми ведення пацієнтів із хронічним панкреатитом (ХП) останніми роками істотно зросла і продовжує зростати в силу багатьох причин [3, 6, 11, 18]. Сумація та потенціювання несприятливих ефектів чинників ризику та дія етіологічних факторів ХП сприяють зростанню захворюваності на ХП та його перебігу, що прогресує, із порушенням зовнішньосекреторної недостатності підшлункової залози (ПЗ), розвитку мальдигестії, мальабсорбції, трофологічної недостатності хворих із порушенням усіх видів обміну [3, 6, 10, 13, 14, 18, 22, 23]. Проведені дослідження ланок патогенезу ХП за умов ізольованого перебігу та різноманітної коморбідності доводять важливу роль системного запалення [8, 16, 17, 22, 23], дисбалансу про- та протизапальних цитокінів [8, 11, 14, 16, 17, 23], чинників протеїназо-інгібіторної системи зі зростанням негативного впливу системного протеолізу [1, 6, 11, 14, 15, 20], порушення оксидантно-антиоксидантного гомеостазу з активацією оксидативного та нітрозитивного стресу на тлі дефіциту природних антиоксидантів та агентів детоксикації [1, 2, 6, 12, 19, 21], що сприяє розвитку ендогенної інтоксикації, яка зростає на тлі супровідного дисбіозу товстої кишки [1, 6, 11, 22]; гіперглікемії на тлі формування панкреатогенного цукрового діабету (ЦД) 3 типу [3, 8], змін ліпідного та білкового спектра крові [6, 8, 11], дисбалансу білкових та вуглеводно-білкових компонентів позаклітинного матриксу [8, 15, 18, 19, 23], які в сукупності сприяють прискоренню апоптозу ацинарного епітелію, його цитолізу, гальмуванню репаративних процесів та активації процесів фіброзування ПЗ [1, 3, 8, 15, 22, 23].
Для корекції встановлених змін внаслідок згаданих вище і наразі ще не відомих механізмів логічним, на нашу думку, було б внесення до протоколу лікування хворих на ХП потужних антиоксидантів із протизапальними властивостями. Одним із вітчизняних препаратів, який володіє подібними ефектами, є Антраль® – оригінальний універсальний цитопротектор із вираженою мембраностабілізуючою, антиоксидантною, протизапальною та імуномодулювальною дією, широко апробований у клініці гастроентерології та гепатології [1, 4, 5, 7, 9, 11]. Зазначені в інструкції фармакологічні ефекти препарату Антраль® зумовлені його хімічною структурою. Він є сполукою алюмінію з похідною антранілової кислоти, що забезпечує виражені протизапальні властивості [1]. Водночас засіб не володіє жовчогінною дією, що дозволяє апробувати його в клініці панкреатології пацієнтам із ХП у фазі загострення.
Мета дослідження. Встановити ефективність застосування препарату Антраль® у лікуванні ХП у фазі загострення на підставі комплексної оцінки клінічного перебігу ХП та структурно-функціональних порушень ПЗ.
Матеріал та методи. Обстежено 52 хворих на ХП змішаної етіології у фазі загострення середньої тяжкості. Для визначення ефективності лікування за випадковою ознакою було сформовано дві репрезентативні групи пацієнтів. Їх середній вік становив 41,3±4,5 років. Групу порівняння склали 30 практично здорових осіб відповідного віку та статі. Група 1, контрольна, складалася з 24 осіб і отримувала адаптовану дієту 5п, реосорбілакт 400 мл в/в № 5, рабепразол (20 мг 2 рази на добу), платифіліну гідротартрат 0,2% 1 мл п/ш № 10, поліферментний препарат (креон 20 тис. ОД 2 рази на день) упродовж 10 днів у стаціонарі. На амбулаторному етапі пацієнти отримували спазмолітичний (мебеверину гідрохлорид) та поліферментний препарат (креон) упродовж 20 днів. Основна група 2 складалася з 28 осіб і крім наведеної вище терапії отримувала Антраль® (АО «Фармак», Київ) по 1 таблетці (200 мг) 3 рази на день упродовж 30 днів.
Діагноз ХП встановлювали на підставі скарг, анамнестичних даних, результатів клінічних, лабораторних та інструментальних досліджень згідно з наказом МОЗ України № 271 від 13.06.2005 р., який був оновлений наказом МОЗ України № 638 від 10.09.2014 р. Для класифікації та рубрикації випадків ХП використовувалася Міжнародна статистична класифікація хвороб та причин смерті 10‑го перегляду (К 86.1. Хронічний панкреатит). Дизайн досліджень передбачав клінічні, лабораторні, біохімічні дослідження крові (активність α-амілази у крові), імуноферментні (ІФА) методи (аналіз калу на вміст еластази‑1), біохімічний аналіз дуоденального вмісту (активність ферментів ПЗ), копрограму, ультрасонографію (УСГ) ПЗ.
Аналіз клінічних, УСГ проявів ХП, біохімічних (α-амілаза крові), лабораторних показників функціонального стану ПЗ проводили за загальноприйнятими методиками, які досліджували в динаміці через 30 днів лікування. Комплексне УСГ-дослідження виконували на ультразвуковому сканері AU‑4 Idea (Biomedica, Італія) конвексним датчиком із частотою 3,5 МГц, вміст С-реактивного протеїну в сироватці крові – латексним методом за допомогою набору НВЛ «Гранум» (Україна). Вивчалися також показники фекальної панкреатичної еластази‑1 методом ІФА на імуноферментному аналізаторі Labsystems Multiskan MS (Нідерланди).
Перед перевіркою статистичних гіпотез проведено аналіз нормальності розподілу величин у рандомізованих вибірках через визначення коефіцієнтів асиметрії та ексцесу за допомогою критерію Хана – Шапіро – Уілкі. Вірогідність змін варіацій у динаміці лікування в разі нормального розподілу у вибірках визначали за парним критерієм Стьюдента, в інших випадках – за непараметричним парним Т-критерієм Вілкоксона. Для виявлення ефективності застосування препарату Антраль® використовували методику розрахунку показника відношення шансів – Odds Radio (OR) та визначення його 95% довірчого інтервалу (ДІ). Математичну обробку отриманих даних проводили на комп’ютері на базі процесора AMD Athlon 64 за допомогою програми Primer of Biostatistics Version 4.03.
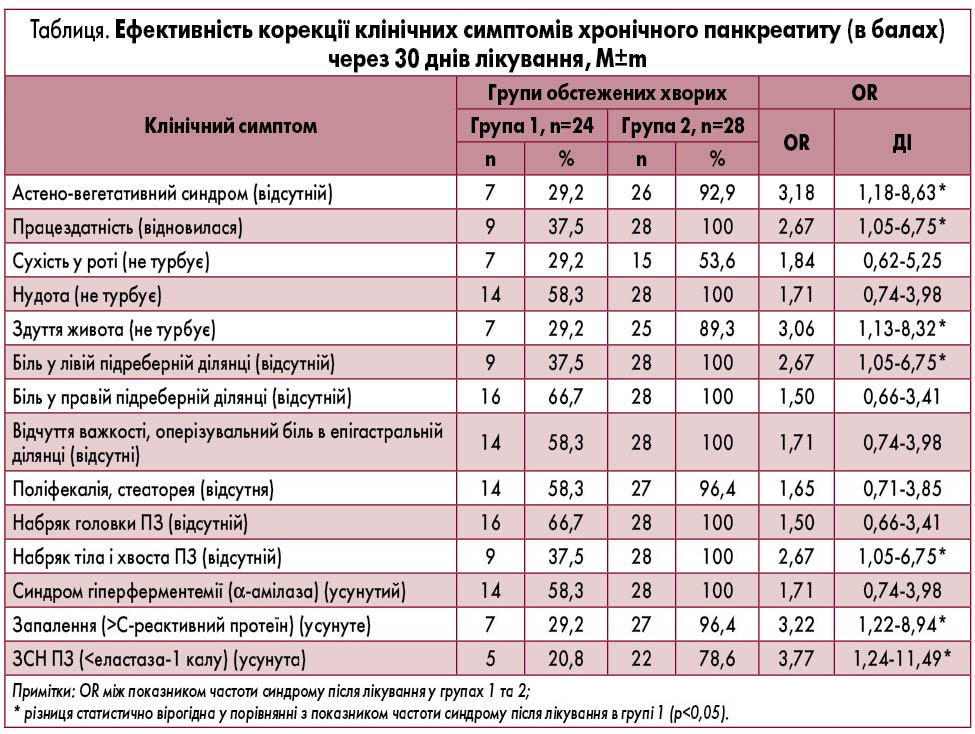
Результати дослідження та їх аналіз. Аналіз впливу запропонованої терапії хворим на ХП (група 2) на перебіг захворювання у порівнянні з групою 1 виявив наступні результати (табл.). Через 4 тижні від початку терапії астено-вегетативний синдром значно меншої інтенсивності зберігався лише у 2 осіб (7,1%) групи 2, тоді як у групі 1 він залишався у 17 хворих (70,8%) (OR=3,18, 95% ДІ 1,18‑8,63). У той же термін в усіх хворих групи 2 (100%) зникли біль та відчуття важкості в епігастральній ділянці (проти 14 осіб (58,3%) у групі 1 (OR=1,71, 95% ДІ 0,74-3,98), біль у лівій підреберній ділянці (100% проти 9 осіб (37,5%) (OR=2,67, 95% ДІ 1,05-6,75), біль у правій підреберній ділянці (100% проти 16 осіб (66,7%) (OR=1,50, 95% ДІ 0,66‑3,41), а також практично не турбувала нудота (28 хворих (100%) проти 14 (58,3%) відповідно у групі 1 (OR=1,71, 95% ДІ 0,74‑3,98), що спостерігалося й надалі у частини хворих групи 1 на 30-й день лікування. Порівняльна динаміка проявів диспепсичного синдрому (сухість у роті, здуття живота) вказує на те, що у хворих групи 2 ці прояви суб’єктивно зменшилися в більшої кількості пацієнтів, що відрізнялося від показника у групі 1 у межах 1,8 раза (OR=1,84, 95% ДІ 0,62-5,25) та 3,1 раза (OR=3,06, 95% ДІ 1,13-8,32) відповідно (р<0,05) (табл.). Позитивним проявом ефективності лікування було відновлення фізичної працездатності у 100% хворих групи 2 проти 9 осіб (37,5%) групи 1 (OR=2,67, 95% ДІ 1,05-6,75), що можна пояснити активними протизапальними та енерготонічними властивостями препарату Антраль®.
Усунення діарейного синдрому (у т. ч. поліфекалії, стеатореї) під час загострення ХП у групах 1 і 2 досягнуто із переважанням ефективності курсу лікування в групі 2 – в 1,7 раза (OR=1,65, 95% ДІ 0,71-3,85) (табл.).
Ультрасонографічні показники розмірів ПЗ також змінилися не рівнозначно: у групі 2 у 100% пацієнтів усунуто набряк ПЗ як у ділянці головки, так і ділянці тіла та хвоста ПЗ, у той час як у хворих із групи 1 зберігалися набряк та збільшення головки ПЗ у 8 осіб (33,3%) (OR=1,50, 95% ДІ 0,66-3,41), а у 15 осіб (62,5%) залишався набряк тіла та хвоста ПЗ (OR=2,67, 95% ДІ 1,05-6,75, р<0,05). За інтенсивністю зменшення запального набряку хвоста ПЗ у групах порівняння результат лікування у хворих з групи 2 перевищував показник у хворих з групи 1 у 2,7 раза (р<0,05). Таким чином, ми дійшли висновку про те, що Антраль® має потужні протизапальні, протинабрякові властивості, які модифікують структуру ПЗ, зменшують її запальну інфільтрацію, що потенціює вплив традиційної терапії ХП.
Аналізуючи показники, які характеризують фазу загострення ХП, слід зазначити вищу ефективність лікувальної програми у хворих групи 2 (табл.). Так, динамічні показники активності α-амілази в крові на тлі встановленої до лікування гіперферментемії у фазі загострення ХП після 30 днів лікування істотно знизилися в обох групах спостереження (табл.), однак у хворих групи 2 синдром відхилення ферментів у крові був усунутий у 100% пацієнтів, у той час як у групі 1 – лише у 58,3% (OR=1,71, 95% ДІ 0,74-3,98).
Динаміка показників синдрому запалення у хворих на ХП (за вмістом у крові С-реактивного протеїну) вказує на його повне усунення у 96,4% пацієнтів групи 2 проти 29,2% хворих групи 1 (OR=3,22, 95% ДІ 1,22‑8,94; р<0,05) (табл.). Це свідчить про вірогідний протизапальний ефект терапії, підсиленої додаванням препарату Антраль® упродовж 1 місяця лікування.
Аналіз динамічних показників вмісту еластази‑1 у випорожненнях пацієнтів із ХП, враховуючи встановлений переважний гіпосекреторний тип секреції ПЗ, на 30-й день лікування вказує на істотне зростання показника лише в групі спостереження (табл.). Встановлено відновлення секреторної здатності ПЗ у 78,6% хворих групи 2 проти 20,8% хворих групи 1 (OR=3,77, 95% ДІ 1,24‑11,49), що можна пояснити потужними протизапальними, антиоксидантними та регенераторними властивостями препарату Антраль® [1, 4, 5, 7].
Таким чином, застосування препарату Антраль® у комплексній терапії ХП є абсолютно доцільним і обґрунтованим, оскільки справляє протизапальний, протинабряковий ефекти, активно усуває синдром гіперферментемії без застосування інгібіторів протеїназ та аналогів соматостатину і водночас стимулює зовнішньо-секреторну функцію ПЗ.
Висновки
Терапія хворих на ХП із застосуванням препарату Антраль® на тлі комплексної терапії призвела до швидшого у порівнянні з лише традиційною терапією досягнення клінічної ремісії ХП: усунення запального набряку ПЗ (OR=2,67; р<0,05), гіперферментемії (OR=1,71), запалення (зниження вмісту С-реактивного протеїну; OR=3,22; р<0,05), відновлення зовнішньої секреції ПЗ (підвищення вмісту еластази‑1 у калі; OR=3,77; р<0,05), усунення клінічних синдромів (астено-вегетативного – OR=3,18; р<0,05), болю в лівій підреберній ділянці (OR=2,67; р<0,05), здуття живота (OR=3,06; р<0,05), відновлення працездатності (OR=2,67; р<0,05).
Перспективою подальших досліджень у цьому напрямку є дослідження впливу препарату Антраль® на стан чинників антиоксидантного захисту, інтенсивності процесів пероксидного окиснення ліпідів, окиснювальної модифікації білків, нітрозитивного стресу, інтенсивність нітрозитивного стресу у динаміці лікування хворих на ХП у фазі загострення.
Література
- Анохіна Г.А., Романенко М.С., Герасименко О.М., Копиловська Т.О. Патогенетичне обґрунтування застосування препарату Антраль® у лікуванні пацієнтів із хронічними захворюваннями підшлункової залози. // Медична газета «Здоров’я України». Тематичний номер «Гастроентерологія, гепатологія, колопроктологія». – 2016. – 3 (41): с. 54-55.
- Горбунов А.А. Інтенсифікація процесів ліпопероксидації як один із провідних патогенетичних механізмів ускладнень у хворих на хронічний панкреатит: залучення до патологічного процесу еритроцитів. // Науковий вісник Ужгородського університету. Серія: Медицина. – 2016. – № 2. – С. 56-59.
- Губергриц Н.Б., Беляева Н.В., Зубов А.Д. и др. Новости мировой панкреатологии (по материалам объединенной встречи Международной Ассоциации панкреатологов, Японского панкреатологического общества, Азиатско-Тихоокеанской ассоциации панкреатологов (Сендай, Япония, 2016). // Вестник клуба панкреатологов. – 2017. – № 1 (34). – С. 5-12.
…
23. Xue J., Sharma V., Hsieh M.H. et al. Alternatively activated macrophages promote pancreatic fibrosis in chronic pancreatitis. Nat Commun. – 2015; 6: 7158. doi: 10.1038/ncomms8158.
Повний список літератури знаходиться в редакції.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 3 (57) 2020 р.