25 листопада, 2020
Значення мікробіому кишечнику та пробіотиків у боротьбі з вірусними інфекціями, зокрема SARS-CoV‑2
 Коронавірусна хвороба (COVID‑19) дуже швидко досягла масштабів пандемії. Як один із можливих терапевтичних варіантів пропонується прийом пробіотиків. Продемонстровано деякі факти впливу COVID‑19 на мікробіом кишечнику, а пробіотики розглянуто щодо їхньої ефективності при лікуванні вірусних інфекцій дихальних шляхів. Це може бути обґрунтовано дедалі очевиднішим існуванням осі легені – кишечник, що передбачає модуляцію мікробіому кишечнику серед підходів до профілактики та лікування COVID‑19. У таких випадках можна використовувати Лактіалє® Мульті.
Коронавірусна хвороба (COVID‑19) дуже швидко досягла масштабів пандемії. Як один із можливих терапевтичних варіантів пропонується прийом пробіотиків. Продемонстровано деякі факти впливу COVID‑19 на мікробіом кишечнику, а пробіотики розглянуто щодо їхньої ефективності при лікуванні вірусних інфекцій дихальних шляхів. Це може бути обґрунтовано дедалі очевиднішим існуванням осі легені – кишечник, що передбачає модуляцію мікробіому кишечнику серед підходів до профілактики та лікування COVID‑19. У таких випадках можна використовувати Лактіалє® Мульті.
У грудні 2019 року з м. Ухань (Китай) було повідомлено про спалах вірусної хвороби, яка називається COVID‑19 [1]. Вірусний агент визнано зоонозним бетакоронавірусом (Severe Acute Respiratory Syndrome Coronavirus 2, SARS-CoV‑2), схожим на інші коронавіруси SARS і MERS (близькосхідний респіраторний синдром) [2]. COVID‑19 спричиняє тяжкий гострий респіраторний синдром (SARS) із летальністю від 2% у Китаї [3] до 12% у певних регіонах Італії [4]. SARS-CoV‑2 – одноланцюговий РНК-вмісний вірус, що належить до великого сімейства Coronaviridae, яке вражає птахів і ссавців. Розмір геному цих вірусів коливається від 26 до 32 кб [5]. Оболонку SARS-CoV‑2 утворюють 4 білки (як і в інших коронавірусів): білок шипа, нуклеокапсидний білок, мембранний білок, білок суперкапсиду. Білок шипа (або S-білок) має два домени S1 і S2. S1 зв’язується з пептидазним доменом ангіотензинперетворювального ферменту‑2 (ACE2), отже, називається рецептор-зв’язувальним доменом, тоді як S2 каталізує злиття мембран, вивільняючи так генетичний матеріал у клітини [6]. Усередині клітини РНК забезпечує шаблон для структурних білків, як-от репліказа (R1a/ab), оболонка (E), шип (S), мембрана (M), нуклеопротеїн (N) і кілька неструктурних білків (NS1-16), нехарактерний білок 14, білок 9b [7]. Із них, як передбачається, неструктурні білки беруть участь у взаємодіях «господар-білок» і модулюють сигнальні шляхи клітин господаря. Вважається, що інкубаційний період при SARS-CoV‑2 варіює від 2 до 14 днів. Сьогодні відомо, що шлях передачі вірусу – повітряно-крапельний. Типовими клінічними симптомами інфекції SARS-CoV‑2 є сухий кашель (67%), лихоманка (88%), втома (38%), міалгія (14,9%) та задишка (18,7%). Інші симптоми включають головний біль, біль у горлі, ринорею та шлунково-кишкові симптоми. Пневмонія, як видається, є найпоширенішим і найтяжчим проявом інфекції [8]. Наразі не існує конкретного препарату проти COVID‑19. Крім того, розробка нового противірусного препарату обумовлена низкою проблем і вимагає значного часу та зусиль. На сьогодні жодне дослідження не підтверджує ефективності використання будь-яких добавок як допоміжної терапії для лікування пацієнтів з COVID‑19. На додаток до SARS-CoV‑2, віруси пташиного грипу, Ебола, Денге та Зіка залишаються погано контрольованими у всьому світі [9].
Живі мікроорганізми, що несуть користь для здоров’я господаря при введенні у відповідній кількості, називаються пробіотиками, що включають певні роди бактерій і дріжджів. До пробіотиків належать: Lactobacillus, Bifidobacterium, Leuconostoc, Pediococcus та Enterococcus тощо. Нормальна мікрофлора шлунково-кишкового тракту (ШКТ) у людей заселена мікрофлорою, яка належить до роду Lactobacillus і Bifidobacterium; вони безпечні та широко використовуються в йогуртах й інших молочних продуктах [10]. Пробіотики відіграють певну роль у врівноваженні захисної імунної відповіді господаря, стимулюючи так бар’єрну функцію слизової оболонки та модулюючи імунну систему [11]. Цікавим є той факт, що кишкові бактерії також надають сприятливий ефект завдяки модуляції дії вітаміну D; через неї пробіотики можуть захистити цілісність бар’єра слизової оболонки та зменшити запалення слизової оболонки кишечнику [12]. Крім того, за допомогою модуляції дії вітаміну D пробіотики можуть регулювати як вроджену, так і набуту імунну відповідь. Ці ефекти включають зменшення Т-клітин Th1/Th17 і прозапальних цитокінів, як-от IL‑1, IL‑6, IL‑8, IFN-γ та TNF-α (на користь відповіді Th2), збільшення T-регулючих клітин (Treg), знижуючи продукцію IgG, зумовленого Т-клітинами, інгібуючи диференціювання дендритних клітин (DC) і допомагаючи підтримувати самотолерантність, одночасно посилюючи захисні вроджені імунні реакції [13]. Взаємодія осі кишечник-легені визначає роль пробіотиків при респіраторних захворюваннях, тому імунний діалог залишається двостороннім процесом. Легеневий мікробіом захищає від респіраторних інфекцій, продукуючи насамперед гранулоцити-макрофаги через стимуляцію IL‑17 і білок Nod2. При легеневих інфекціях мікробіом кишечнику відіграє вирішальну роль. Дослідження in vivo на безмікробних мишах показали підвищену захворюваність під час гострої легеневої інфекції [14]. Так само модуляція тяжкості інфекції, спричиненої Mycobacterium tuberculosis, у легенях корелює з мікробіомом кишечнику [15]. Мікроелементи, як-от цинк, відіграють важливу роль у нормальному зростанні та розвитку організму господаря. Цинк має значний вплив на кишкові бактеріальні популяції та імунну систему, посилюючи імунну відповідь через Th1. Основним механізмом гомеостазу цинку в організмі є шлунково-кишкове всмоктування поглинутого цинку, збалансоване секрецією ендогенного цинку в кишечнику й екскрецією з калом [16]. Порушення гомеостазу цинку в людини – критичний фактор впливу на противірусний імунітет. Дефіцит цинку зумовлює ризик зараження вірусними інфекціями, оскільки з’являється дисбаланс Th1 та Th2, що спричиняє дефект Th1 [17]. Leonardi та співавт. довели, що молочнокислі бактерії (LAB), збагачені цинком, можуть бути цінним джерелом цього елемента в їжі, оскільки є найкращою формою для засвоєння людиною [18].
Механізми дії пробіотиків на організм господаря й імунну систему є складними та все ще не з’ясованими до кінця. Ефективність вакцин проти вірусних захворювань обмежена високими показниками мутації вірусів, особливо РНК-вмісних. Саме тому в цьому огляді ми обговорюємо ефективність пробіотиків і їх значення у профілактиці вірусних інфекцій.
Кишковий мікробіом та імунна модуляція
Кишечник є ключовим середовищем існування, де більшість мікробів симбіотично живуть в організмі господаря; його мікробіота відіграє безцінну роль у підтримці кишкового гомеостазу [19]. Мікробіом кишечнику включає різні мікробні спільноти, не обмежуючись бактеріями, вірусами та грибами [20]. Він складається близько з 1000 різних видів мікробів, а їхня щільність варіює від 104 до 105 бактерій на міліметр ШКТ у тонкій кишці та 1011 бактерій на грам вмісту товстої кишки [21]. Склад мікробіому відрізняється в кожного індивідуума, що залежить від змін навколишнього середовища та генетики [22]. У здорових людей мікробіом переважно складається з чотирьох скупчень мікроскопічних організмів: Firmicutes, Bacteroidetes, Proteobacteria й Actinobacteria [23, 24], в яких два типи (Firmicutes і Bacteroidetes) становлять 90% кишкової мікробіоти. Крім того, здебільшого домінуючими типами кишечнику є Bacteroidetes і Firmicutes, а потім – Bacteroidetes й Actinobacteria [25]. Мікробіом використовує простір, поживні речовини та середовище кишечнику людини для розмноження [26]. Своєю чергою, мікрофлора кишечнику допомагає у ферментації вуглеводів, синтезує вітаміни та здійснює регуляцію проникності кишечнику [27]. Мікробіота кишечнику діє як захисний бар’єр і допомагає модифікувати імунну систему кишечнику. На мікробіом нижніх відділів ШКТ впливають різні фактори навколишнього середовища. Так, співпраця між мікробіомом і кишковою імунною системою є необхідною для збереження кишкового гомеостазу. Коли цей гомеостаз порушується, дисбіоз спричиняє кишкові захворювання [26]. Дослідження довели, що рання мікробна колонізація в ШКТ новонароджених має вирішальну роль у зростанні імунної системи кишечнику. Мікробіом кишечнику демонструє конкуренцію щодо зв’язування патогенів, їхньої колонізації, виживання та прямого знищення їх метаболітами (наприклад, органічною кислотою, антимікробними сполуками) та підвищує пов’язаний з кишечником імунітет. Пероральний прийом пробіотиків захищає від інфекції у віддалених до слизової кишки ділянках, як-от бронхи та слизова оболонка сечостатевих органів [28, 29]. Ризик зараження Salmonella enterica серовар Typhimurium можна мінімізувати шляхом перорального прийому пробіотиків, що зумовлюють фагоцитарну та мікробіцидну дію макрофагів [30]. За даними Galdeano та співавт. [30], цитокіни, що виділяються пробіотиком, діють на імунні клітини. Виробляючи специфічні антитіла, пробіотики можуть стимулювати системну імунну відповідь. Достатня кількість пробіотиків може стимулювати вроджений та набутий імунітет господаря. Мікробіота кишечнику також опосередковано впливає на здоров’я серця, печінки, нирок і легень [31, 32]. Імунна модуляція під час респіраторних захворювань опосередковується мікробіотою кишечнику. Здоровий мікробіом кишечнику може змінити його імунітет, а також імунітет легень через вісь кишечник-легеня [33]. Під час інфікування дихальних шляхів коменсальні організми стимулюють імунну відповідь, а мікробіота кишечнику модулює легеневу імунну систему [34]. Вісь «кишечник-легені» вважається двонаправленою (кров і лімфатична система). Мікробні метаболіти, ендотоксини можуть чинити вплив на легеню при виникненні запалення, що може впливати й на мікробіом кишечнику. Саме за цим механізмом є можливим вплив SARS-CoV‑2 на зміну мікробіому кишечнику [35]. Показано, що мікробіота кишечнику бере участь у модуляції багатьох захворювань легень [36]. Пробіотики продемонстрували значимі властивості щодо ліквідації мікробів, діючи через альвеолярні макрофаги, нейтрофіли, природні клітини-кілери та підвищений рівень прозапальних цитокінів, як-от TNF-α та IL‑6 у легенях [37, 38]. Протизапальні цитокіни (Treg та IL‑10) також зростають зі збільшенням прозапальних цитокінів у легенях інфікованих мишей [39]. Найважливіший спосіб реалізації дії пробіотиків полягає у тому, що лімфатична система знаходиться між легенями та кишечником. Коменсали, їхні частинки (наприклад, ліпополісахариди) та метаболіти (наприклад, коротколанцюгові жирні кислоти, SCFA) транслокуються через мезентеріальну лімфатичну систему з кишечнику в легені, використовуючи системний кровообіг для регуляції легеневого імунітету [40, 41]. Нещодавнє дослідження довело, що тканини для відновлення вроджених лімфоїдних клітин можуть мігрувати з кишечнику в легені у відповідь на запальну імунну відповідь на IL‑25 [42]. Було показано, що інфекція, спричинена K. pneumoniae в мишей, регулюється споживанням Bifidobacterium longum. Looft та Allen [43] дійшли висновку про зниження рівня Lactobacilli та Lactococci й підвищення рівня Enterobacteriaceae в просвіті кишечнику під час дослідження грипозної інфекції на клінічній моделі.
Імунна відповідь слизової оболонки
Дисбіоз може стимулювати імунну систему організму. Зв’язок між мікробіотою та факторами навколишнього середовища впливає на імунітет слизової оболонки [44]. Слизовий шар, який є на поверхні ШКТ, дихальних шляхів, вагінального тракту, відіграє першу лінію захисту, де IgА діє як перша ланка імунітету слизової оболонки [45]. Муцини є бар’єром. Сторонні частинки чи збудники, перетинаючи мукоциліарний бар’єр, здатні контактувати з кількома розчинними антимікробними пептидами, присутніми у слизі, як-от лізоцим, лактоферин, колектини й дефензини, що виробляються імунними клітинами дихальних шляхів. Ці антимікробні пептиди беруть участь у безпосередньому знищенні збудника чи його пригніченні шляхом опсонізації або рекрутингу інших запальних клітин [46, 47]. Патогенна інфекція клітин слизової епітелію виводить моноцити, макрофаги, гранулоцити, В-клітини, природні кілери та DC. Ініціювання цих клітин залежить від рецепторів розпізнавання патернів (PRR). PRR, включаючи Toll-подібні рецептори (TLR) і нуклеотидозв’язувальний білок‑2, що містить домен олігомеризації (NOD‑2), лектиноподібні рецептори С-типу й датчики цитозольної ДНК, активовані внутрішньоклітинною сигналізацією, індукують імунні відповіді через про- та/або прямі імуногенні реакції протизапальних чи регуляторних та/або противірусних хемокінів [48-51]. Знищення збудника через макрофаги та DC також бере участь у вродженій імунній відповіді слизової оболонки дихальної системи. Альвеолярний макрофаг негайно усуває збудника, виділяючи NO й активні форми кисню. DC відіграють значну роль в очищенні легень від вірусів, ініціюючи противірусну відповідь CD8+ цитотоксичних Т-клітин у лімфатичних вузлах [52]. DC ефективно фагоцитизують збудника через трансепітеліальні дендрити [53]. Вони також допомагають блокувати та трансцитозувати збудника через епітеліальні келихоподібні клітини й М-клітини. Антигени, що вторглися, трансцитуються через М-клітини до субепітеліальних антигенпрезентуючих клітин (АРС). APC відправляють сигнал до Т-клітинної ділянки лімфоїдної тканини слизової оболонки для подання обробленого антигена до В-клітини. В-клітини продукують поверхневі імуноглобуліни IgA. Антигеностимульовані Т-клітини та поверхневий клітинний імуноглобулін надходять у системний кровообіг через лімфатичні вузли. Під час внутрішньоклітинного транспорту, опосередкованого імуноглобуліном, вірус може бути знешкоджений [46]. Цитокіни, отримані з епітелію (TGF-β, IL‑25 та IL‑33), відіграють вирішальну роль в активації Th2 або T-регуляції імунної відповіді слизової оболонки. Сильне ушкодження легень за допомогою RSV збільшує інфільтрацію нейтрофілів і синтез TNF-α, IL‑13, що продукують клітини CD4+ в легені [54]. Інфекція RSV також посилює вироблення слизу через підвищений рівень IL‑17, прозапального цитокіну, що виділяється активованими Т-клітинами в легенях [55]. Пробіотичні організми також допомагають у дозріванні й активації імунної системи слизової за допомогою різних сигнальних мереж, опосередкованих через метаболіти, як-от SCFA [56, 57] та антимікробні сполуки, що називаються бактеріоцинами [58]. Пробіотичні бактерії також можуть зв’язуватися з вірусом, інгібуючи так приєднання вірусу до рецептора клітини-господаря [59]. Пробіотики допомагають зміцнити імунітет слизової оболонки та забезпечити стійкість до респіраторної вірусної інфекції [60].
Пробіотики як імуностимулятори
Пробіотики мають кілька корисних для здоров’я господаря ефектів, діючи через місцевий (підтримуючи еубіоз кишечнику та цілісність його стінок) і системний імунітет (шляхом посилення специфічної і неспецифічної імунної відповіді). Застосування пробіотиків є ефективним і виправданим за низки захворювань, зокрема при вірусних інфекціях [61]. Понад століття тому лауреат Нобелівської премії Ілля Мечников провів серію досліджень, які довели, що прийом мікроорганізмів, котрі продукують молочну кислоту, покращує перебіг розладів травлення та патології дихальних шляхів [62]. Пробіотики модулюють вроджену імунну систему господаря, посилюючи фагоцитарну активність, лейкоцити (поліморфноядерні та моноцити) й експресію деяких рецепторів (CR1, CR3, FccRI і FcaR), які пов’язані з фагоцитозом, та підвищують мікробіцидну функцію нейтрофілів [63]. Кількість й активність клітин природних кілерів (NK) також значно підвищується в крові [64]. Сигналізація TLR коменсальними організмами виявляє значний ефект для збереження кишкового гомеостазу господаря шляхом посилення бар’єрної функції кишечнику та покращення місцевої імунної відповіді [65].
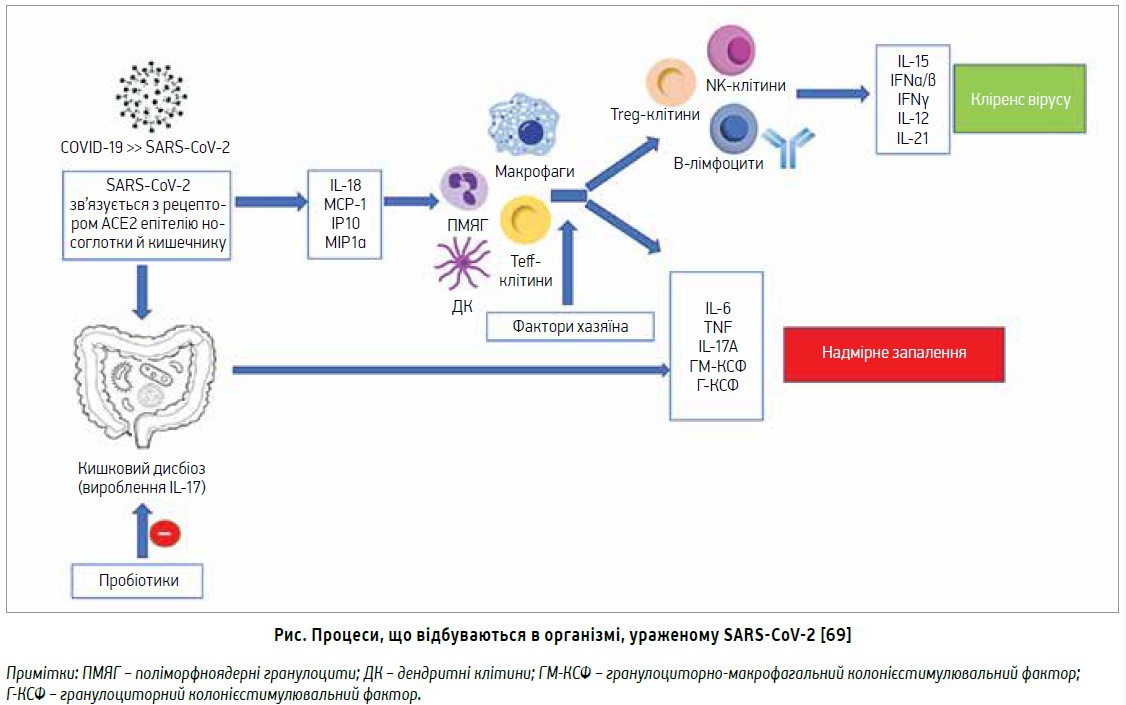
Пробіотики також можуть стимулювати вироблення APC про- та протизапальних цитокінів (наприклад, IL‑10, IL‑12, IL‑17, TNF, інтерферон-α) проти чужорідних частинок шляхом активації набутого імунітету. Протизапальні цитокіни, хемокіни та їхні рецептори, що регулюють запалення кишечнику, пригнічуються протизапальним цитокіном IL‑10, який продукується різними імуноактивованими клітинами [66]. Пробіотики забезпечують два різні імуномодулюючі ефекти: один активізує вироблення IL‑12, індукує клітини NK, Th1, Th2 та діє проти інфекції й алергії, а інший включає IL‑10 і Treg-клітинну активацію Th2, DC, B-клітинами та моноцитами для набутого імунітету господаря (рис.) [67].
Нещодавнє клінічне дослідження на тваринах і людях довело підвищення рівнів IFN-γ, IL‑2, фактора некрозу пухлини (TNF), IgA й IgA-секретуючих клітин у відповідь на прийом штамів Lactobacillus або Bifidobacterium [68].
Вивільняються прозапальні цитокіни й інтерферони, а трансляція вірусу пригнічується, щоб забезпечити очищення від нього клітин епітелію як частину імунної відповіді господаря. Очищення від вірусу відбувається в епітелії легень та кишечнику залежно від імунного статусу організму господаря. Вживання пробіотиків покращує запальний процес шляхом регуляції імунної відповіді в кишечнику за допомогою різних сигнальних шляхів і сприяє поліпшенню дисбіозу кишечнику, спричиненого SARS-CoV‑2, пришвидшує одужання в пацієнтів.
Прийом пробіотиків може також зменшити ризик або модифікувати перебіг інфекцій органів дихання [70]. Пробіотики стимулюють легеневий імунітет, посилюючи відповідь Т-клітинної ланки імунітету в дихальних шляхах. LAB безпосередньо потрапляють у кровообіг від кишечнику до легень та чинять імуномодулювальну дію. Пероральне вживання лактобактерій може модулювати профіль цитокінів [71]. Інше дослідження довело, що Lactobacillus GG, L. casei Shirota (LcS) і DN114001 можуть запобігати та лікувати грибкові інфекції ШКТ і дихальних шляхів [71]. Випробування серед літніх людей і дітей продемонструвало, що пробіотики L. paracasei, L. casei 431 та L. fermentum PCC можуть зменшити частоту виникнення, тривалість та симптоматику грипу й інших інфекцій дихальних шляхів, збільшуючи рівень IFN-γ в крові та sIgA в кишечнику [68]. IFN-γ індукує бактерицидну функцію макрофагів, опсонізуючу активність В-клітин і підвищує кількість комплементфіксованих антитіл [72]. Було встановлено, що вживання Bifidobacterium і Lactobacillus покращує перебіг інфекцій верхніх та нижніх дихальних шляхів у дітей і дорослих [73, 74]. Уживання Bifidobacterium breve чинить посилений протигрипозний ефект, може успішно захистити дихальні шляхи мишей від грипу [75].
Порівняно зі здоровими дорослими та людьми похилого віку населення з ослабленим імунітетом містить менше різновидів, а також меншу кількість родів Firmicutes, Bifidobacteria, Clostridium, Faecalibacterium prausnitzii та Blautia coccoides і вищі кількості Enterobacteriaceae й Bacteroidetes [76]. Firmicutes і Bacteroidetes становлять 93% загальної мікрофлори кишечнику здорової людини [77]. Якісний і кількісний склад організмів кишкового мікробіому зменшується з віком. Зміна мікробного складу відбувається внаслідок впливу середовища проживання, недоїдання, стану здоров’я та прийому лікарських засобів, як-от антибіотики та нестероїдні протизапальні препарати (НПЗП) [78]. Секвенування 16S ДНК 18-річних людей, які приймали НПЗП, показало зміни у складі мікробіому, зокрема знижену кількість Firmicutes і збільшену кількість Bacteroidetes [78]. Час пасажу їжі кишечником також залежить від віку та стану здоров’я. У випадку ослабленого імунітету час кишкового транзиту збільшується, а клітинна маса калових бактерій зменшується порівняно зі здоровими людьми [79]. Отже, зміна мікробного розташування в просвіті кишечнику може зумовити зниження функції імунної системи та більшу частоту шлунково-кишкових інфекцій у літніх людей, аніж у молодих. Основні імунологічні зміни, пов’язані зі старінням, включають зниження ефективності імунних відповідей, опосередкованих В- і Т-лімфоцитами [77], оскільки кількість лімфоцитів у периферичній крові зменшується з віком [80].
Уживання пробіотиків зменшує ризик появи респіраторних інфекцій у дітей [81], значно зменшує тривалість проявів інфекцій дихальних шляхів [82]. Окрім того, пробіотики показали важливу роль у конкурентній колонізації в кишечнику для виключення патогенних мікроорганізмів, модулюючи кишкову бар’єрну функцію та її проникність. Дослідження довело, що пробіотики модулюють експресію IL‑10 і зменшують експресію запальних цитокінів, як-от TNF, IL‑1β та IL‑8 [83], підвищують імуноглобулін A в слині й продукують бактеріоцини, що в підсумку проявляє антимікробну дію [84]. Метааналіз продемонстрував, що вживання L. rhamnosus GG запобігало появі респіраторних інфекцій [85]. Інший метааналіз оцінював ефективність пробіотиків (штами Lactobacillus і Bifidobacterium) щодо тривалості епізодів респіраторних захворювань у дітей та дорослих [86]. Tabbers і співавт. [87] довели можливість лікування внутрішньолікарняної інфекції за допомогою Bifidobacterium animalis subsp. lactis BB‑12. Показано, що штам L. reuteri DSM 17938 BioGaia захищає від інфекції верхніх дихальних шляхів і розладів ШКТ у дітей віком від 6 місяців до 3 років [88].
Пробіотики як інгібітори АСЕ
Вважається, що SARS-CoV‑2 (як й інші коронавіруси SARS) зв’язується з рецептором ACE2 для внутрішньоклітинної інвазії та використовує клітинну серинову протеазу TMPRSS2 для праймінгу й реплікації в інфікованих організмах [89-91]. З іншого боку, вважається, що механізм гострого ураження легень під час інфекції опосередковується шляхом активації системи ренін-ангіотензинової системи, при якій АСЕ2 виробляє кілька захисних ефектів [92]. Експресія АСЕ2 епітеліальними клітинами легень, кишечнику, нирок і судин суттєво збільшується в пацієнтів, які отримують інгібітори АСЕ [93]. Саме тому деякі дослідники припустили, що інгібітори АСЕ можуть бути корисними для пацієнтів з COVID‑19, зменшуючи запальний процес у легенях [94], хоча інші стверджували, що інгібітори АСЕ здатні посилити проникнення вірусів, регулюючи рівень АСЕ2. Повідомлялося, що кілька пробіотиків, зокрема LAB, можуть продукувати пептиди з інгібуючим АСЕ ефектом [95]. Після демонстрації некаталітичної ролі АСЕ2 у транспорті амінокислот у кишечнику було висловлено припущення, що терапевтичний ефект АСЕ2 може бути опосередкований, зокрема, його діями на ШКТ та/або мікробіом кишечнику. Це узгоджується з новими даними, які підтверджують існування зв’язку між кишечником і легенями та свідчать про те, що дисбіоз кишечнику й мікробіом легень пов’язані із серцево-легеневою патологією [96]. З огляду на це слід оцінити можливу роль пробіотиків у лікуванні SARS-CoV‑2 [97].
Зважаючи на ці дані, бактеріотерапія може бути додатковим ресурсом для профілактики ураження, а також відновлення ушкодження слизової оболонки кишечнику при SARS-CoV‑2 за рахунок модуляції мікробіому кишечнику та зменшення пов’язаного із цим запалення. За інших інфекцій (наприклад, ВІЛ), при яких запалення кишечнику та пов’язане із цим порушення мікробіому можуть впливати на бар’єрну функцію кишечнику, пробіотики пригнічують апоптоз, регулюють сигнальні шляхи для продукування цитокінів, підтримують гомеостаз кишкового епітелію, що дозволяє відновити здоров’я слизової оболонки кишечнику [98, 99].
Пробіотики та боротьба з вірусними інфекціями
Пацієнт з імуносупресією має дисбіоз кишечнику, що спричиняє накопичення патогенних мікроорганізмів у ШКТ. Інфекції, зумовлені кишковими бактеріями, є одними з найскладніших, зокрема й для лікування, тому вони можуть стати небезпечними для життя. У разі вірусних інфекцій у людей епітелій дихальних шляхів є вхідними воротами. Перший рівень захисту організму – мукоциліарний кліренс дихальних шляхів і sIgА в їхньому секреті. Вплив вірусної інфекції на DC спричиняє каскад реакцій з активацією клітин CD4+ та CD8+ і подальшим розвитком специфічного опосередкованого Т- й В-ланками імунного запального процесу [69].
Пробіотики мають противірусну активність; їх часто обирають як природні стимулятори імунітету [100]. Пробіотики і їхні метаболіти також можуть негативно впливати на вірус, ушкоджуючи його клітини та стимулюючи вроджений та/або набутий імунітет; вони проявляють противірусну активність шляхом прямої взаємодії «пробіотик-вірус», вироблення противірусних інгібуючих метаболітів і стимуляції імунної системи. LAB та їхні бактеріоцини є потужними противірусними агентами [101]. Відомо, що LAB синтезують екзополісахариди, які мають імуномодулюючу, протипухлинну, антиоксидантну активність, а також перешкоджають утворенню біоплівок. Один з таких штамів (L. plantarum CRL1506) при пероральному застосуванні продемонстрував противірусні властивості через зменшення опосередкованого ушкодження тканин [102]. Аналіз метаболітів L. plantarum довів наявність високого рівня цукрів, а це вказує на те, що основними противірусними діючими речовинами можуть бути полісахариди. Попередні дослідження також довели, що колонізація епітелію лактобактеріями перешкоджає адгезії вірусів до поверхні. Callahan і співавт. [103] повідомили, що сульфатовані екзополісахариди інгібують прилипання ВІЛ до клітин-мішеней, блокуючи так потрапляння вірусу. Так само було виявлено, що Bacillus subtilis OKB105 і сурфактин мають противірусну активність проти TGEV (вірус трансмісивного гастроентериту), що потрапляє в епітеліальні клітини кишечнику свиней шляхом адсорбції частинок вірусу та блокування прикріплення вірусу шляхом конкурентного інгібування [104].
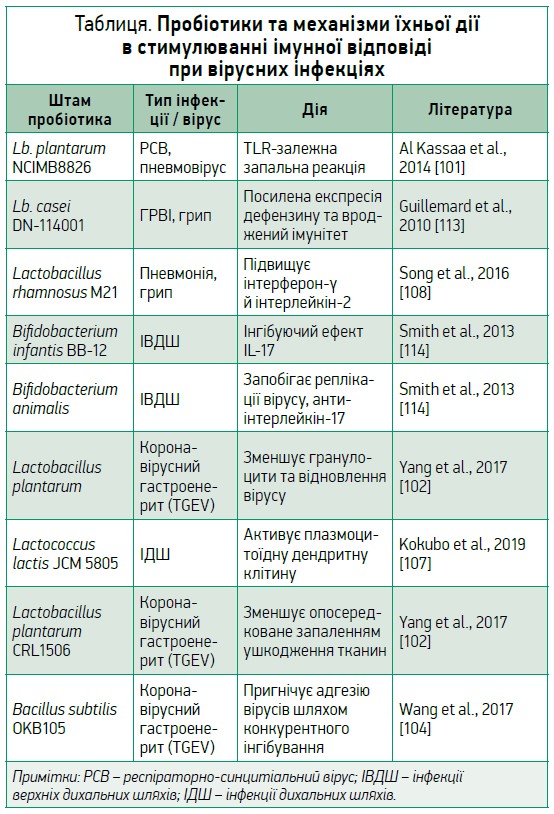 Пробіотики L. plantarum і L. reuteri при вірусній пневмонії знижують кількість гранулоцитів й експресію множинних прозапальних цитокінів, а також зменшують відновлення вірусу. Це вказує на те, що механізм дії може бути незалежним від TLR [105]. Уживання L. plantarum HEAL 9 і L. paracasei 8700:2 у здорових людей знижувало ризик зараження застудними інфекціями [106]. Дослідження, проведене Kokubo та співавт. [107] показало, що Lactococcus lactis LC впливає на активацію дендритних клітин. L. rhamnosus M21 при лікуванні пневмонії в мишей продемонстрував підвищений рівень інтерферону-γ й інтерлейкіну‑2, які є репрезентативними цитокінами Тh1 [108] (табл.). Застосування пробіотиків довело клінічний потенціал в експериментах на тваринах. Різні штами Lactobacillus spp. і Bifidobacterium spp. за допомогою перорального чи інтраназального введення показали придушення симптомів інфекції при вірусних інфекціях, зокрема грипі [109, 110]; вони зменшують титри навантаження вірусу та збільшують Т-хелпери в легеневій паренхімі. В іншому дослідженні одночасне введення L. rhamnosus і B. lactis збільшило рівні IFN-γ та IL‑4, IL‑10 й IL‑6 у бронхоальвеолярному секреті, а також активність фагоцитарних клітин [111, 112]. Отже, пробіотики можуть спричинити руйнування нуклеїнової кислоти вірусу й обмежити його реплікацію [69].
Пробіотики L. plantarum і L. reuteri при вірусній пневмонії знижують кількість гранулоцитів й експресію множинних прозапальних цитокінів, а також зменшують відновлення вірусу. Це вказує на те, що механізм дії може бути незалежним від TLR [105]. Уживання L. plantarum HEAL 9 і L. paracasei 8700:2 у здорових людей знижувало ризик зараження застудними інфекціями [106]. Дослідження, проведене Kokubo та співавт. [107] показало, що Lactococcus lactis LC впливає на активацію дендритних клітин. L. rhamnosus M21 при лікуванні пневмонії в мишей продемонстрував підвищений рівень інтерферону-γ й інтерлейкіну‑2, які є репрезентативними цитокінами Тh1 [108] (табл.). Застосування пробіотиків довело клінічний потенціал в експериментах на тваринах. Різні штами Lactobacillus spp. і Bifidobacterium spp. за допомогою перорального чи інтраназального введення показали придушення симптомів інфекції при вірусних інфекціях, зокрема грипі [109, 110]; вони зменшують титри навантаження вірусу та збільшують Т-хелпери в легеневій паренхімі. В іншому дослідженні одночасне введення L. rhamnosus і B. lactis збільшило рівні IFN-γ та IL‑4, IL‑10 й IL‑6 у бронхоальвеолярному секреті, а також активність фагоцитарних клітин [111, 112]. Отже, пробіотики можуть спричинити руйнування нуклеїнової кислоти вірусу й обмежити його реплікацію [69].
Безпека пробіотиків, включаючи лактобактерії та біфідобактерії, була продемонстрована численними клінічними дослідженнями. Сучасні факти свідчать, що пробіотики та їхні похідні сприяють здоров’ю організму господаря та регулюють його гомеостаз, зокрема імунний. Пробіотики мають багато позитивних ефектів за рахунок модуляції імунної відповіді господаря, підтримують гомеостаз кишечнику та виробляють інтерферон, пригнічуючи таким способом вірусний цитокіновий шторм. Хоча кілька рандомізованих контрольованих досліджень довели, що прийом пробіотиків (Lactobacillus rhamnosus GG, Bacillus subtilis і Enterococcus faecalis) може запобігти розвитку вентиляційної пневмонії [115, 116], зокрема в пацієнтів із COVID‑19, ефективність щодо зменшення смертності залишається невизначеною. Лактобактерії та біфідобактерії показали перспективний сприятливий ефект; їх введення може подолати дисбактеріоз кишечнику, спричинений інфекцією SARS-CoV‑2. Отже, доцільно впливати на мікрофлору застосуванням пробіотиків і так потенційно покращувати імунний статус. Однак імунна стимуляція й експресія цитокінів є специфічними для штаму та можуть змінюватися залежно від консорціумів пробіотичних бактерій. Імовірно, знадобиться новий та цілеспрямованіший підхід до модуляції мікробіоти кишечнику як один із терапевтичних підходів COVID‑19 і його супутніх захворювань.
На ринку України є мультиштамний пробіотик Лактіалє® Мульті, який включає 14 штамів пробіотичних бактерій із доведеною ефективністю (Lactobacillus casei, Lactobacillus plantarum, Lactobacillus rhamnosus, Bacillus subtilis, Bifidobacterium bifidum, Bifidobacterium breve, Bifidobacterium longum, Lactobacillus acidophilus, Lactococcus lactis, Streptococcus thermophilus, Bifidobacterium infantis, Lactobacillus delbrueckii ssp. bulgaricus, Lactobacillus helveticus, Lactobacillus salivarius) – сумарно 2,0×109 КУО пробіотичних мікроорганізмів в 1 капсулі. Усі штами мають розшифрований геном і код безпеки (PXN), а також тестовані на кислотостійкість, здатність до адгезії, інгібувальної дії щодо патогенів. Дія штамів Лактіалє® Мульті є доведеною, тому цю дієтичну добавку можна розглядати як варіант корекції мікробіому при SARS-CoV‑2.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» № 20 (489), 2020 р.