14 січня, 2021
Роль інгібіторів тирозинкінази Брутона у лікуванні пацієнтів з мантійноклітинною лімфомою
.jpg) Мантійноклітинна лімфома (МКЛ) – рідкісний підтип В-клітинних неходжкінських лімфом, який зазвичай класифікується як агресивна лімфома, що потребує хіміоімунотерапії з попередньою консервацією стовбурових клітин пацієнта. Частка МКЛ у структурі злоякісних лімфом складає 5-7%. Протягом останніх десятиріч щорічна частота діагностування цієї онкологічної патології у Західній Європі зросла до 1-2 випадків на 100 000 осіб (M. Dreyling et al., 2017). МКЛ залишається невиліковною хворобою, практично у всіх пацієнтів розвивається рецидив. Проте в останні десятиріччя довгострокові результати лікування покращилися переважно у молодих пацієнтів, у яких стандартна індукційна терапія включає режими на основі ритуксимабу та цитарабіну у високих дозах (HD-AraC), після чого проводиться аутологічна трансплантація стовбурових клітин (АТСК; J.N. Gerson et al., 2019). Після розвитку рецидиву МКЛ стандартної терапії не розроблено (M. Dreyling et al., 2017; N. Gerson et al., 2019; Р. McKay et al., 2012).
Мантійноклітинна лімфома (МКЛ) – рідкісний підтип В-клітинних неходжкінських лімфом, який зазвичай класифікується як агресивна лімфома, що потребує хіміоімунотерапії з попередньою консервацією стовбурових клітин пацієнта. Частка МКЛ у структурі злоякісних лімфом складає 5-7%. Протягом останніх десятиріч щорічна частота діагностування цієї онкологічної патології у Західній Європі зросла до 1-2 випадків на 100 000 осіб (M. Dreyling et al., 2017). МКЛ залишається невиліковною хворобою, практично у всіх пацієнтів розвивається рецидив. Проте в останні десятиріччя довгострокові результати лікування покращилися переважно у молодих пацієнтів, у яких стандартна індукційна терапія включає режими на основі ритуксимабу та цитарабіну у високих дозах (HD-AraC), після чого проводиться аутологічна трансплантація стовбурових клітин (АТСК; J.N. Gerson et al., 2019). Після розвитку рецидиву МКЛ стандартної терапії не розроблено (M. Dreyling et al., 2017; N. Gerson et al., 2019; Р. McKay et al., 2012).
Основні проблеми у лікуванні МКЛ пов’язані із наявністю декількох патофізіологічних варіантів хвороби, високою частотою прогресування та рецидивування, коротшими періодами без ознак хвороби, похилим віком пацієнтів і наявністю у них супутніх захворювань (А. Ladha et al., 2019). Порівняно з іншими неходжкінськими лімфомами для МКЛ характерні гірші показники тривалості відповіді (ТВ) на лікування, виживаності без прогресування (ВБП) та загальної виживаності (ЗВ). Більшість пацієнтів вже мають прогресуючу агресивну МКЛ, потребуючи системної терапії, часто – комбінованої хіміоімунотерапії (K.S. Hanna et al., 2019). Індукційна терапія з використанням агресивних режимів рекомендована тим пацієнтам, які є кандидатами на проведення високодозової терапії та на консервацію аутологічних стовбурових клітин. Лікування за допомогою менш агресивних режимів показане пацієнтам, котрі не є кандидатами на проведення високодозової терапії та на консервацію аутологічних стовбурових клітин.
Незважаючи на широке застосування агресивних режимів лікування, у теперішній час медіана ВБП при МКЛ залишається у діапазоні 3-4 роки. Тому оптимальний підхід до лікування пацієнтів з рецидивуючою або рефрактерною (р/р) МКЛ ще належить визначити.
Розуміння особливої ролі у патогенезі гемобластозів (і зокрема, МКЛ) тирозинкінази Брутона (ТКБ) – ферменту з родини протеїнкіназ, що має важливе значення у дозріванні та функціонуванні В-лімфоцитів – вже посприяло створенню специфічних інгібіторів її кіназної активності та їх подальшого клінічного застосування. Наразі у пацієнтів з р/р МКЛ переконливо продемонстровано хороший профіль переносимості й ефективності таких інгібіторів ТКБ, як ібрутиніб, акалабрутиніб і занубрутиніб. Перший представник класу інгібіторів ТКБ – ібрутиніб – 13 листопада 2013 р. був схвалений Управлінням з контролю якості харчових продуктів і лікарських препаратів (FDA) США для лікування МКЛ у пацієнтів, які вже отримали як мінімум один курс попередньої терапії. Загалом впровадження інгібіторів ТКБ у клінічну практику стало дуже значним досягненням, яке істотно розширило можливості лікування пацієнтів з МКЛ. При цьому на сьогодні саме ібрутиніб є найбільш вивченим інгібітором ТКБ, який визнаний одним із кращих стандартів лікування пацієнтів з р/р МКЛ і застосовується 1 раз на добу (C. Visco et al., 2020).
Ібрутиніб: клінічна фармакологія
Ібрутиніб – низькомолекулярний інгібітор ТКБ. Механізм дії ібрутинібу полягає в утворенні ковалентного зв’язку з цистеїновим залишком в активній ділянці ТКБ, що призводить до інгібування її ферментативної активності. Доклінічні дослідження продемонстрували, що ібрутиніб інгібує проліферацію та виживаність злоякісних В-клітин in vivo, а також міграцію клітин та їх адгезію до субстрату in vitro. У пацієнтів з рецидивуючою В-клітинною лімфомою зайнятість >90% активних ділянок ТКБ у мононуклеарах периферичної крові спостерігалася протягом майже 24 год після додавання ібрутинібу у дозі 2,5 мг/кг маси тіла на добу (175 мг/добу для особи з середньою масою тіла 70 кг).
У пацієнтів з В-клітинними злоякісними новоутвореннями ефективність лікування ібрутинібом зростає при підвищенні дози до 840 мг (що у 1,5 разу вище за максимальну схвалену рекомендовану дозу). Середня рівноважна площа під кривою концентрація – час (AUC; % коефіцієнту варіації), що спостерігалася у пацієнтів з МКЛ при застосуванні ібрутинібу в дозі 560 мг, складає 865 (69%) нг×год/мл. У здорових людей абсолютна біодоступність ібрутинібу натще становила 2,9% (95% довірчий інтервал – ДІ – 2,1-3,9). Ібрутиніб абсорбується після перорального прийому, при цьому медіана Тmax складає 1-2 год. Показано, що у разі вживання висококалорійної їжі або їжі з високим вмістом жирів Cmax ібрутинібу збільшується у 2-4 рази, а AUC – приблизно у 2 рази порівняно з прийомом препарату після нічного голодування. Зворотне зв’язування ібрутинібу з білками плазми крові людини in vitro складало 97,3%, без залежності від концентрації у діапазоні від 50 до 1000 нг/мл.
Ібрутиніб метаболізується з утворенням декількох метаболітів переважно за допомогою CYP3A і меншою мірою – за допомогою CYP2D6. Активний метаболіт – PCI‑45227 – метаболіт дигідродіолу з інгібіторною активністю щодо ТКБ, яка приблизно у 15 разів нижча за таку в ібрутинібу.
Застосування ібрутинібу у лікуванні МКЛ: доказова база
Початково безпека й ефективність ібрутинібу були встановлені у ході міжнародного багатоцентрового відкритого дослідження II фази (Study 1104), результати якого стали підставою для прискореного схвалення застосування препарату при р/р МКЛ (M.L. Wang et al., 2012). Включені до цього дослідження пацієнти мали підтверджений діагноз МКЛ з наявністю транслокацій t(11;14) або гіперекспресії цикліну D1 та вимірюваних проявів захворювання (визначених як розмір лімфатичних вузлів ≥2 см). Вони отримали щонайменше одну (проте не більше 5) попередню лінію терапії (без часткової або кращої відповіді на застосування останнього режиму або з прогресуванням захворювання після отримання останнього режиму лікування). Пацієнти не повинні були мати функціональних порушень органів. Оцінка функціонального статусу за шкалою Східної об’єднаної онкологічної групи (ECOG) мала становити ≤2 бали, абсолютна кількість нейтрофілів щонайменше 0,75×109/л і кількість тромбоцитів щонайменше 50×109/л. Учасники дослідження (n=115), які відповідали зазначеним критеріям включення, були розподілені на дві групи: ті, що отримали ≥2 циклів попереднього лікування бортезомібом (n=50) та <2 циклів лікування бортезомібом або взагалі не отримували цього препарату (n=65). Пацієнтам призначали монотерапію ібрутинібом у добовій дозі 560 мг до прогресування захворювання або до появи неприйнятних проявів токсичності. Чотири пацієнти були виключені з дослідження через швидке прогресування захворювання або адміністративні причини. Загалом 111 учасників дослідження отримали щонайменше одну дозу ібрутинібу, при цьому розрахована медіана тривалості періоду подальшого спостереження склала 15,3 міс. Загальна частота відповіді (ЗЧВ) у всіх пацієнтів становила 68%, при цьому у 21% осіб відзначалася повна відповідь (ПВ), а у 47% – часткова відповідь. Попереднє лікування бортезомібом та вихідні характеристики не впливали на ЗЧВ. Медіана ТВ дорівнювала 17,5 міс (95% ДІ 15,8 – не досягнуто). Медіана часу до розвитку відповіді на лікування становила 1,9 міс (діапазон 1,4-13,7). Медіана часу до досягнення ПВ становила 5,5 міс (діапазон 1,7-11,5). Оцінена медіана ВБП складала 13,9 міс (95% ДІ 7,0 – не досягнуто). Медіана ЗВ не була досягнута. Оцінена частота ЗВ через 18 міс дорівнювала 58%.
Небажані явища, що спостерігалися у дослідженні, переважно були оцінені як 1 або 2 ступеня вираженості; найчастішими з них були діарея (50%), втомлюваність (41%), нудота (31%), периферичні набряки (28%), задишка (27%), запор (25%), інфекції верхніх дихальних шляхів (23%), блювання (23%) та зниження апетиту (21%). Гематологічні небажані явища 3 ступеня вираженості реєструвалися нечасто і включали нейтропенію (16%), тромбоцитопенію (11%) та анемію (10%).
Дані тривалого спостереження за учасниками цього дослідження, яке проводилося з метою оцінювання безпеки й ефективності ібрутинібу (медіана тривалості періоду спостереження – 26,7 міс), продемонстрували стабільну перевагу терапії цим препаратом (M.L. Wang et al., 2015). Медіана тривалості лікування складала 8,3 міс, при цьому 46% пацієнтів отримували лікування протягом >12 міс, а 22% – протягом ≥2 років. Результати включали медіану ВБП, що становила 13 міс (95% ДІ 7,0-17,5), ЗВ – 22,5 міс (95% ДІ 13,7 – не оцінено) та медіану ТВ – 17,5 міс (95% ДІ 14,9 – не оцінено). Це узгоджується з даними реєстраційного дослідження та додатково підтверджує профіль ефективності ібрутинібу. Крім того, оцінена дослідниками ЗЧВ у всіх пацієнтів складала 67% (95% ДІ 57,1-75,3) з частотою досягнення ПВ 23% (95% ДІ 15,1-31,4). У пацієнтів, які отримували попередню терапію бортезомібом (n=48), ЗЧВ дорівнювала 65% (95% ДІ 49,5-77,8), а у тих, хто отримував попереднє лікування леналідомідом (n=27), – 59% (95% ДІ 38,8-77,6). 24-місячна ВБП становила 31% (95% ДІ 22,3-40,4), а ЗВ – 47% (95% ДІ 37,1-56,9). Аналіз безпеки також продемонстрував, що найбільш частими небажаними явищами прогнозовано були діарея, втомлюваність, нудота та задишка; прояви гематологічної токсичності виявилися аналогічними встановленим у основному дослідженні.
У рандомізованому дослідженні III фази порівнювали ібрутиніб (n=139) і темсиролімус (n=141) у пацієнтів з р/р МКЛ (S. Rule et al., 2018). Його результати засвідчили, що ЗЧВ становила 77% у групі ібрутинібу та лише 47% у групі темсиролімусу (P<0,0001). Після завершення періоду подальшого спостереження, медіана тривалості якого дорівнювала 39 міс, медіана ВБП була достовірно більшою при лікуванні ібрутинібом (16 проти 6 міс). Крім того, також відзначалася тенденція до збільшення ЗВ у пацієнтів, рандомізованих у групу лікування ібрутинібом (30 проти 24 міс; Р=0,06).
В іншому дослідженні II фази за участю 50 пацієнтів з р/р МКЛ після попередніх курсів терапії (медіана кількості – 3) та завершення періоду подальшого спостереження, медіана тривалості якого складала 47 міс, застосування ібрутинібу у комбінації з ритуксимабом забезпечувало досягнення ПВ у 58% пацієнтів, а медіана ВБП склала 43 міс (P. Jain et al., 2018).
Таким чином, на сьогодні інгібітор ТКБ ібрутиніб переконливо продемонстрував загалом сприятливий терапевтичний профіль у пацієнтів з МКЛ. У рекомендаціях Національної онкологічної мережі США ібрутиніб (± ритуксимаб) віднесений до категорії доказовості 2А як варіант другої лінії терапії у пацієнтів з МКЛ. Інші варіанти другої лінії терапії включають рекомендовані режими категорії доказовості 2В: ібрутиніб, леналідомід та ритуксимаб або венетоклакс та ібрутиніб.
Нині рекомендована доза ібрутинібу при лікуванні МКЛ становить 560 мг перорально 1 раз на добу. Препарат приймають до прогресування захворювання або до виникнення проявів неприйнятної токсичності. Терапію ібрутинібом слід припинити при будь-яких проявах негематологічної токсичності 3 ступеня та нейтропенії з інфекцією чи лихоманкою або при проявах гематологічної токсичності 4 ступеня. Прийом ібрутинібу можна відновити у стартовій дозі одразу після повернення початкового стану здоров’я пацієнта або усунення симптомів токсичності. У разі подальшого виникнення токсичності доза ібрутинібу може бути знижена до 140 мг/добу. Прийом ібрутинібу має бути припинений, якщо прояви токсичності зберігаються або виникають після двох зменшень дози. При супутньому застосуванні інгібіторів CYP3A рекомендується зниження дози ібрутинібу. У пацієнтів із легким порушенням функції печінки (клас А за класифікацією Чайльда – П’ю) рекомендується знизити дозу ібрутинібу до 140 мг/добу, із помірним порушенням (клас В за класифікацією Чайльда – П’ю) – до 70 мг/добу. Пацієнти з тяжким порушенням функції печінки (клас С за класифікацією Чайльда – П’ю) мають уникати прийому ібрутинібу. У разі порушення функції нирок корекція дози ібрутинібу не потрібна.
Дані 2020 р.: у фокусі уваги – результати дослідження MANTLE-FIRST
У серпні 2020 р. на онлайн-сторінках журналу Leukemia група італійських онкологів (C. Visco et al., 2020) представила дані міжнародного ретроспективного дослідження MANTLE-FIRST. У ньому були оцінені результати лікування загалом 261 пацієнта з МКЛ (медіана віку – 58 років), котрий мав прогресуюче захворювання або перший рецидив на тлі попередньої індукційної терапії цитарабіном у високих дозах (HD-AraC) у рамках підготовки до АТСК. Лікування цієї категорії хворих є особливо складним, оскільки не розроблено стандартної терапії. ЗВ та ВБП у цьому дослідженні оцінювали від початку терапії порятунку. Попередньо визначене порогове значення у 24 міс використовувалося для віднесення учасників дослідження до групи пацієнтів з раннім прогресуванням захворювання (РПЗ, ≤24 міс) або з пізнім прогресуванням захворювання (ППЗ, >24 міс). Застосовувані режими другої лінії терапії включали комбінацію ритуксимабу та бендамустину (R-B; 21%), R-B та цитарабін (R-BAC; 29%), монотерапію ібрутинібом (19%) та інші режими лікування (31%). При корекції за віком та РПЗ/ППЗ пацієнти, що отримували режим R-BAC, достовірно частіше досягали повної ремісії (63%), ніж хворі, які отримували інші порівнювані режими. Загалом монотерапія ібрутинібом та застосування режиму R-BAC були асоційовані зі значущим збільшенням медіани ВБП (24 та 25 міс відповідно) порівняно з режимом R-B (13 міс) або іншими режимами лікування (7 міс; рис. 1).
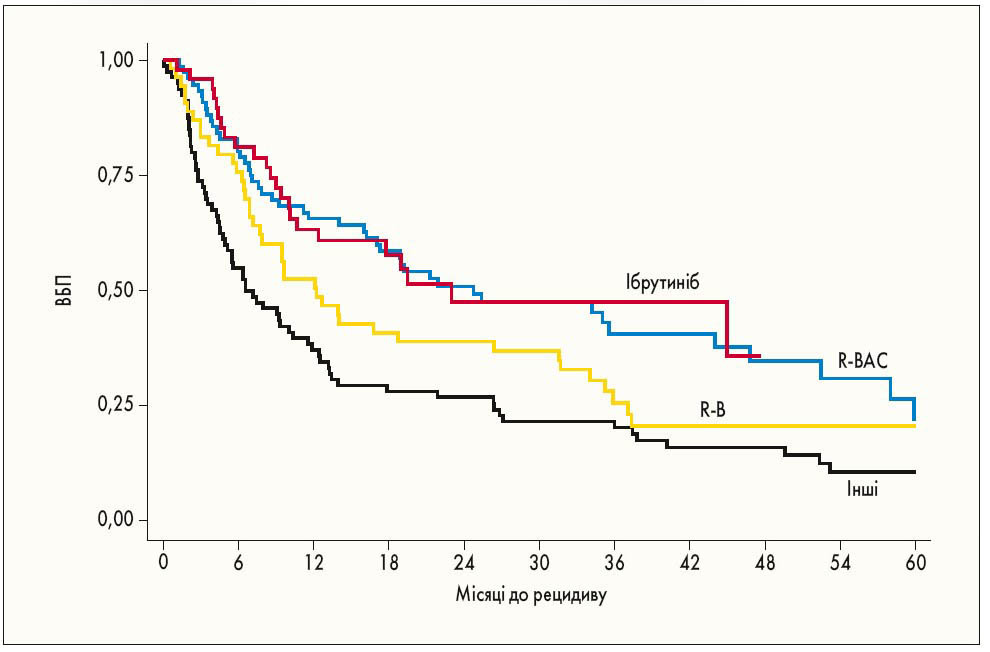 Рис. 1. Криві ВБП залежно від застосовуваного режиму другої лінії терапії.
Рис. 1. Криві ВБП залежно від застосовуваного режиму другої лінії терапії.
P=0,001 між групами ібрутинібу та інших режимів; P=0,002 між групами R-BAC та інших режимів; P=0,11 між групами R-BAC та R-B; P=0,07 між групами ібрутинібу та R-B; P=0,86 між групами ібрутинібу та R-BAC; P=0,06 між групами R-B та інших режимів
У пацієнтів з РПЗ (n=127) застосування ібрутинібу асоціювалося з нижчим ризиком настання смерті порівняно з референтними режимами (відношення шансів 2,41 для режиму R-B; 2,17 – для інших режимів; 2,78 – для режиму R-BAC; рис. 2). Медіана ЗВ у пацієнтів з РПЗ, які отримували лікування ібрутинібом, склала 29,7 міс (ДІ 15,7 – не досягнуто). У цьому контексті ібрутиніб мав перевагу порівняно з режимом R-BAC (медіана ЗВ – 10,3 міс; 95% ДІ 7,7-22,1; Р=0,02), режимом R-B (медіана ЗВ – 11,9 міс; 95% ДІ 5,3-28,7; Р=0,02) або іншими підходами до лікування (медіана ЗВ – 12,8 міс; 95% ДІ 6,9-16,6; Р=0,02).
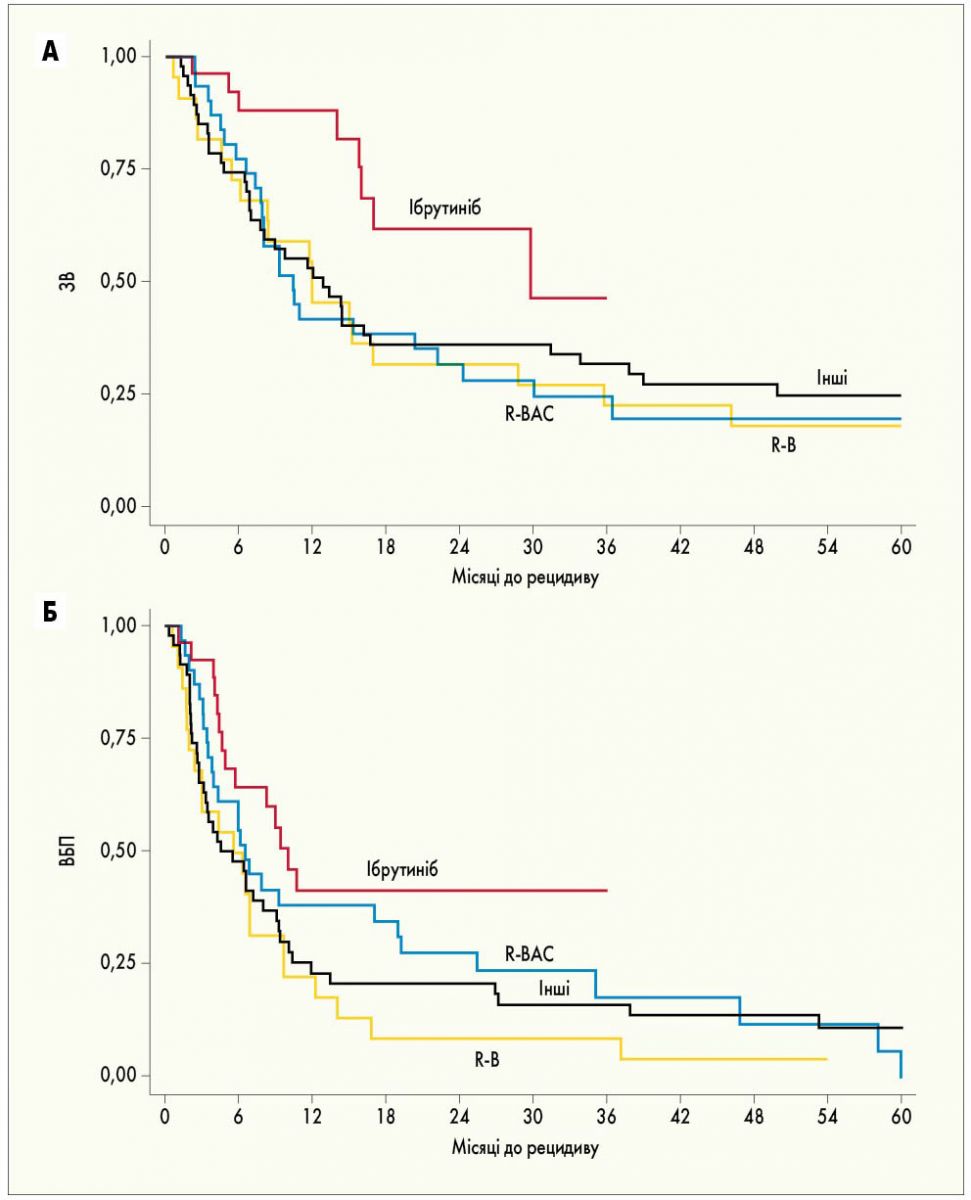 Рис. 2. Криві виживаності у пацієнтів з РПЗ залежно від застосовуваного режиму другої лінії терапії. А – ЗВ при використанні ібрутинібу порівняно з режимами R-B та R-BAC (P=0,02), а також ібрутинібу порівняно з іншими режимами (P=0,03). Б – ВБП при введенні ібрутинібу порівняно з режимом R-B (P=0,01), ібрутинібу порівняно з іншими режимами (P=0,02), ібрутинібу порівняно з режимом R-BAC (P=0,23)
Рис. 2. Криві виживаності у пацієнтів з РПЗ залежно від застосовуваного режиму другої лінії терапії. А – ЗВ при використанні ібрутинібу порівняно з режимами R-B та R-BAC (P=0,02), а також ібрутинібу порівняно з іншими режимами (P=0,03). Б – ВБП при введенні ібрутинібу порівняно з режимом R-B (P=0,01), ібрутинібу порівняно з іншими режимами (P=0,02), ібрутинібу порівняно з режимом R-BAC (P=0,23)
У пацієнтів з ППЗ (n=134) не спостерігалося достовірної різниці між лікуванням ібрутинібом та режимами на основі бендамустину. Застосування ібрутинібу у пацієнтів з р/р МКЛ асоціювалося із покращенням результатів лікування у підгрупі пацієнтів із РПЗ.
Отже, результати дослідження MANTLE-FIRST дозволили зробити висновки, важливі для клінічної практики (C. Visco et al., 2020):
- режим R-BAC і монотерапія ібрутинібом асоціюються з досягненням аналогічних показників ВБП;
- пацієнти з РПЗ (рецидив або прогресування захворювання через ≤2 роки після діагностування МКЛ) мали достовірно кращі результати лікування ібрутинібом за ВБП та ЗВ; при цьому жоден пацієнт не отримував бендамустин як компонент режиму попередньої індукційної терапії, що додатково підсилює значення зроблених висновків на користь ібрутинібу;
- у пацієнтів із ППЗ застосування режимів R-B та R-BAC характеризувалося показниками виживаності, аналогічними з такими при застосуванні ібрутинібу;
- у пацієнтів, які отримували другу лінію терапії з використанням інших режимів, були продемонстровані достовірно гірші результати.
Хоча когортне дослідження MANTLE-FIRST і є ретроспективним за дизайном, його безсумнівною перевагою є порівняння найбільш часто застосовуваних на практиці режимів другої лінії терапії. Його результати чітко вказують на перспективність і доцільність призначення ібрутинібу пацієнтам із рецидивами та прогресуванням МКЛ.
CP-199299
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 6 (67) 2020 р.



