29 грудня, 2015
Применение азитромицина при инфекционном обострении бронхиальной астмы
Бронхиальная астма (БА) – это хроническая воспалительная респираторная патология. Обострение БА связано с усилением выраженности воспаления дыхательных путей и может быть обусловлено нарушением режима проведения базисной терапии, агрессивным воздействием провоцирующих факторов, инфицированием вирусами или бактериальными патогенами. Важным моментом в лечении БА является своевременная помощь при обострении, что предполагает усиление противовоспалительной и бронхолитической терапии. Известно, что патогенные микроорганизмы могут не только вызывать обострения БА, но и усугублять ее течение. Большинство обострений БА обусловлены респираторными вирусами (рино- и аденовирусы, респираторно-синцитиальный вирус, возбудители гриппа и парагриппа) и не требуют назначения антибактериальных препаратов.
Весьма распространенным внутриклеточным бактериальным патогеном, часто вызывающим поражение дыхательных путей и легких, является Chlamydophila pneumoniae. Результаты сероэпидемиологических исследований свидетельствуют о том, что первичное инфицирование чаще происходит у детей и подростков в возрасте от 5 до 15 лет, а реинфицирование может наблюдаться в течение всей жизни человека. С возрастом количество в популяции лиц, инфицированных C. pneumoniae, возрастает. Инфекция, вызванная атипичными микроорганизмами, в частности C. pneumoniae, не является артефактом выборочных наблюдений, а закономерно присутствует в качестве одного из звеньев патогенеза. По данным различных авторов, от 5 до 30% всех обострений БА связано с влиянием атипичных возбудителей – C. pneumoniae (СР-инфекция) и Mycoplasma pneumoniae (MP-инфекция).
Убедительными представляются результаты, свидетельствующие о пусковой роли СР-инфекции в развитии обострения заболевания. Недавние исследования продемонстрировали не только связь инфекции и обострения БА, но и влияние С. pneumoniae на тяжесть обострения. Такие выводы были сделаны после выявления четкой корреляции между маркерами острой СР-инфекции и выраженностью функциональных нарушений у пациентов с обострением БА [1-3].
К препаратам, воздействующим на атипичную флору, относятся новые макролиды, фторхинолоны, доксициклин. В клинической практике именно эти средства наиболее часто используются при инфекционном обострении БА. Данные об улучшении течения БА на фоне применения макролидов появились более 40 лет назад, когда было отмечено значительное снижение потребности в системных стероидах, уменьшение гиперреактивности бронхов, сокращение частоты госпитализаций, а также повышение функции внешнего дыхания (ФВД) у пациентов, получавших олеандомицин. Антибактериальная терапия при БА показана только в случае подтверждения этиологической роли бактериальных патогенов на основании следующих критериев:
• повышение температуры тела, которое сохраняется >3 дней;
• характер мокроты слизисто-гнойный, выявление в мокроте полиморфноядерных нейтрофилов, а не эозинофилов;
• отсутствие эффекта после коррекции базисной терапии;
• появление воспалительных изменений в периферической крови (лейкоцитоз, повышенная скорость оседания эритроцитов – СОЭ).
Применение антибиотиков у пациентов с аллергическими заболеваниями, в частности при аллергическом рините и БА, является довольно серьезной проблемой, что связано с аллергизирующими свойствами антибиотиков.
В научной литературе представлены результаты исследования по применению макролидов в лечении БА. Использование антибиотиков данного класса обусловлено как активностью в отношении бактерий, играющих важную роль в патогенезе БА, так и наличием неантибактериальных эффектов, обеспечивающих ряд терапевтических преимуществ [4, 5]. Противовоспалительные свойства макролидов наряду с низкой природной аллергенностью позволяют широко использовать средства этого класса при аллергических заболеваниях, в т. ч. при БА. Успех применения макролидов в терапии БА обеспечивают их многочисленные эффекты, среди которых угнетение продукции провоспалительных цитокинов, активация секреции противовоспалительного интерлейкина-10, уменьшение трансэндотелиальной миграции нейтрофилов, эозинофилов, моноцитов и т. д. При оценке эффективности лечения макролидами пациентов с БА и риносинуситом некоторые исследователи фокусируют внимание на способности этих средств воздействовать на эозинофилы, в частности стимулировать клеточный апоптоз, уменьшать продукцию ими хемокинов и молекул адгезии [6].
Положительное влияние макролидов при обострении БА, обусловленном бактериальной инфекцией, определяют несколько составляющих: прямой антибактериальный эффект; неспецифическое противовоспалительное действие; нормализация мукоцилиарного клиренса; снижение гиперреактивности бронхов; улучшение их проходимости и, как следствие, более раннее разрешение симптомов [7].
Высокую эффективность макролидов при хламидийной или легионеллезной инфекции связывают с тем, что эти препараты, особенно кларитромицин и азитромицин, хорошо накапливаются в тканях, в т. ч. в полиморфноядерных лейкоцитах, и длительно сохраняются в крови и очагах воспаления. Именно современные макролиды (кларитромицин, азитромицин) наиболее широко применяются в клинической практике.
Азитромицин – первый и на сегодня единственный антибактериальный препарат, официально разрешенный для применения в виде коротких 3-дневных курсов терапии при инфекциях нижних дыхательных путей и ряде других заболеваний бактериальной этиологии. Азитромицин относится к 15-членным полусинтетическим макролидам, в то же время наличие атома азота в ядре антибиотика дает возможность считать его представителем подкласса азалидов. Механизм микробного действия препарата заключается в нарушении синтеза белка клетками чувствительных микроорганизмов путем связывания с 50S-субъединицей рибосом. Хотя макролиды обеспечивают преимущественно бактериостатический характер действия, азитромицин, создающий высокие концентрации в тканях, проявляет бактерицидную активность в отношении ряда возбудителей: H. influenzae, M. catarrhalis, N. gonorrhoeae, S. pneumoniae, S. pyogenes, S. agalactiae, Campylobacter spp., H. pylori, B. pertussis, C. diphtheriae. Эффективность азитромицина зависит не только от его бактерицидного/бактериостатического действия, но и от присущих ему постантибиотического и суб-МПК действием. Под постантибиотическим эффектом подразумевается персистирующее ингибирование жизнедеятельности бактерий после их кратковременного контакта с антибактериальным препаратом. В основе эффекта лежат необратимые изменения в рибосомах микроорганизма, следствием чего является стойкий блок транслокации и размножения бактерий, потенцирующий и пролонгирующий общее антибактериальное действие.
Клинически значимый постантибиотический эффект азитромицина отмечен в отношении S. pneumoniae, H. influenzae, S. pyogenes, L. pneumophila. Суб-МПК эффект заключается в подавлении роста микроорганизмов антибиотиком, уровень которого ниже, чем МПК. Установлено, что данный эффект приводит к утрате отдельными штаммами стрептококков, стафилококков и гемофильной палочки адгезивных свойств и факторов вирулентности. Было обнаружено, что даже в концентрации ниже МПК, азитромицин угнетает образование биопленки синегнойной палочкой. Препарат накапливается преимущественно внутриклеточно, в особенно больших количествах содержится в фосфолипидном слое мембран лизосом альвеолярных макрофагов, нейтрофильных гранулоцитов, моноцитов и фибробластов. Азитромицин обладает преимуществами перед другими макролидами в отношении накопления в указанных клетках: попав внутрь лизосомы, антибиотик как бы «запирается» там и очень медленно выводится. Этим и объясняется уникальность фармакокинетики азитромицина, предоставляющая возможность проводить короткие (3-дневные) курсы лечения при некоторых инфекционных заболеваниях [7].
Азитромицин, как и некоторые другие макролиды, обладает иммуномодулирующим и противовоспалительным действием [1, 7, 9]. Противовоспалительное влияние отмечается даже при субтерапевтических концентрациях макролидов и сравнимо с таковым нестероидных противовоспалительных препаратов. Считается, что именно благодаря данному свойству макролиды уменьшают выраженность гиперреактивности дыхательных путей, сопровождающей бронхолегочные инфекции [4, 8-12].
Для оценки клинической эффективности и безопасности применения азитромицина в терапии инфекционных обострений БА были обследованы 26 пациентов с данным заболеванием. Участники были включены в группу наблюдения при условии их согласия с целями и объемом запланированных исследований, необходимостью назначения антибактериальной терапии и возможным риском возникновения побочных эффектов.
Дизайн исследования предусматривал включение в испытание больных с персистирующей БА легкой и средней степени тяжести с наличием признаков инфекционного обострения. Критерии включения: отсутствие контроля БА по тесту для контроля над астмой (АСТ <15), наличие кашля с выделением мокроты слизисто-гнойного и гнойного характера, повышение температуры тела, отсутствие тяжелых сопутствующих заболеваний.
В испытании приняли участие 16 женщин и 10 мужчин. Средний возраст пациентов составил 38 лет (от 18 до 69 лет). БА была установлена в среднем 6,7±2,6 года назад. Средняя длительность обострения составляла 10 дней, среднее количество обострений в течение года – 3, продолжительность пребывания в стационаре – 9,2±2,9 дня. На момент включения в исследование у всех больных отмечались клинические признаки инфекционного обострения: повышенная температура тела (в пределах 37,8-38,5 °C), вязкая мокрота желтого или зеленого цвета, нарушение физической активности, сна, ослабление везикулярного дыхания и сухие свистящие или гудящие хрипы в легких при аускультации.
До момента госпитализации антибактериальные препараты не применялись; на амбулаторном этапе была назначена усиленная противовоспалительная и бронхолитическая терапия, которая включала, согласно приказу МЗ Украины № 128 от 19.03.2007 г., β2-адреномиметики и кортикостероиды. За время пребывания в стационаре пациенты были обследованы 3 раза: на 1-2-й (визит 1), 4-5-й (визит 2) и 9-10-й день (визит 3).
Всем участникам при первом визите проводили электрокардиографию и рентгенологическое исследование органов грудной клетки. В рамках первого и третьего визита исследовали ФВД на основе анализа кривой форсированного выдоха. С надлежащими показателями сравнивали жизненную емкость легких, форсированную жизненную емкость легких, объем форсированного выдоха за 1-ю секунду (ОФВ1).
Степень контроля БА оценивали по АCТ, гнойный характер и эозинофилию мокроты – на основании данных общего анализа мокроты. В общем анализе крови определяли неспецифические признаки воспаления – лейкоцитоз, сдвиг лейкоцитарной формулы влево, СОЭ.
Выраженность кашля оценивали в баллах: от 0 (отсутствие кашля) до 4 (сильный постоянный надсадный кашель) с/без наличия мокроты.
Лечение начинали с 1-го дня госпитализации после подписания пациентом информированного согласия. Всем больным, находившимся под наблюдением, назначали эмпирическую антибиотикотерапию азитромицином 500 мг (Азибиот®, KRKA, Словения) 1 р/сут в течение 3 дней. Кроме того, пациенты получали ингаляционную базисную терапию, муколитические и бронхолитические средства в соответствии с действующим приказом по лечению БА.
Эффективность назначенной терапии определяли согласно рекомендациям Европейского консенсуса по клинической оценке противомикробных препаратов на основании результатов анализа комплекса клинических, функциональных и лабораторных показателей. Клинически эффективным считалось лечение, которое позволяло достичь ликвидации бактериального обострения БА. Результаты наблюдения представлены в таблице.
Полученные в процессе исследования результаты были обработаны с помощью статистического пакета Microsoft Office Professional 2000. Расчетные формулы рабочего листа Exсel были запрограммированы в соответствии с рекомендациями С.М. Лапача и соавт. Статистическую обработку полученных данных проводили параметрическими методами с применением критериев Стьюдента.
Длительность пребывания в стационаре составила 9,2±2,9 дня. Результаты проведенного лечения указывали на статистически достоверную (р<0,01) положительную динамику всех клинических показателей у наблюдаемых больных.
Контроль течения БА у всех пациентов был достигнут к визиту 3. Показатель АСТ составлял 21,8±2,4 балла. Частота кашля снижалась к 3-му дню лечения, на визите 3 данный признак сохранялся у 5 больных. Отмечена положительная аускультативная симптоматика – уменьшение свистящих хрипов практически у всех больных.
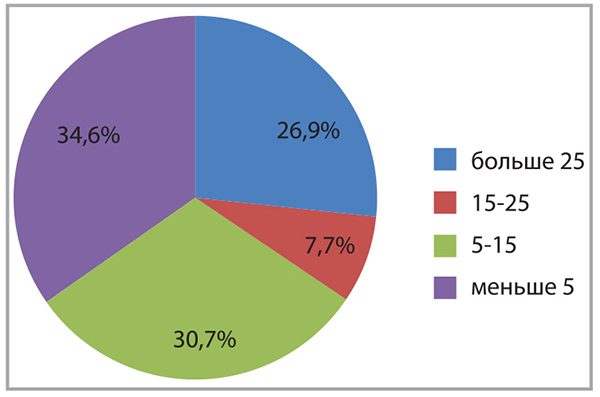
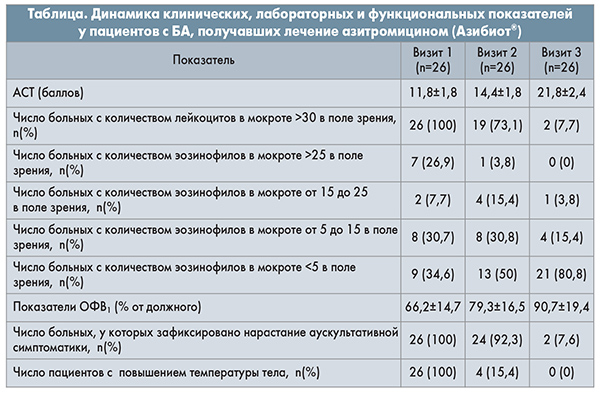
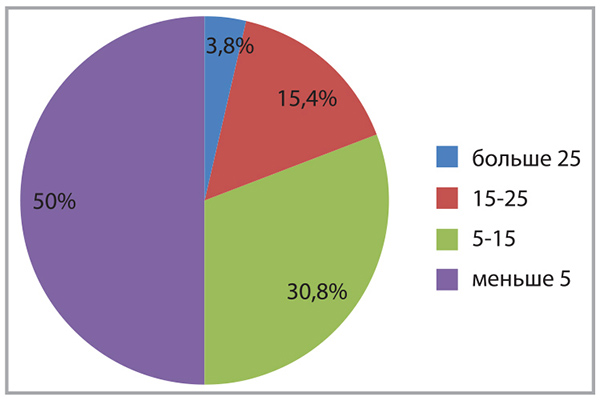
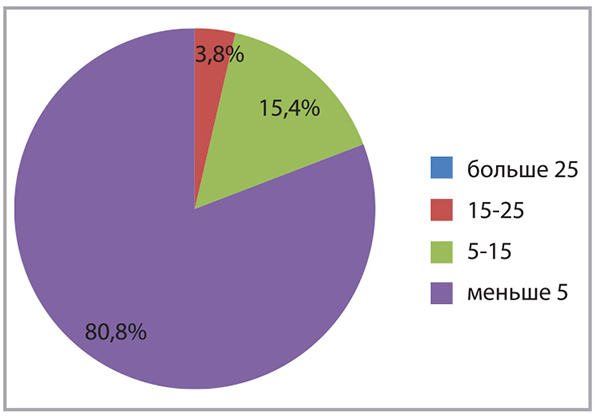
Регрессу клинических симптомов БА сопутствовали изменения лабораторных и функциональных показателей. Одним из методов оценки степени воспаления дыхательных путей при БА является определение выраженности эозинофильного и нейтрофильного воспаления посредством изучения мокроты. Доказана взаимосвязь между атопией и инфекцией. Атопический статус влияет на реактивность дыхательных путей при инфекционном поражении, а инфекция нижних дыхательных путей способствует сенсибилизации пациента. В рамках первого визита у 65,4% пациентов наблюдалась эозинофилия мокроты (>5 эозинофилов в поле зрения при микроскопии); при этом у 26,9% больных эозинофилия классифицировалась как выраженная (>25 эозинофилов в поле зрения), наблюдались кристаллы Шарко-Лейдена (рис. 1). В рамках второго визита зафиксирована положительная динамика в отношении уменьшения эозинофилии мокроты (рис. 2), при третьем посещении количество эозинофилов в поле зрения не превышало 5 ни у кого из участников. У пациентов уменьшились количество мокроты и выраженность проявлений атопии, статистически достоверно снизилось количество нейтрофилов в мокроте (рис. 3).
При первом визите выделение мокроты гнойного или слизисто-гнойного характера (≥30 лейкоцитов в поле зрения) наблюдалось у 100% участников, к третьему визиту у 92,3% пациентов содержание лейкоцитов снизилось до нормальных значений.
Как видно из полученных данных, количество эозинофилов и лейкоцитов в мокроте статистически достоверно уменьшилось, что свидетельствовало о снижении выраженности как аллергического, так и инфекционного воспаления дыхательных путей у наблюдаемых пациентов.
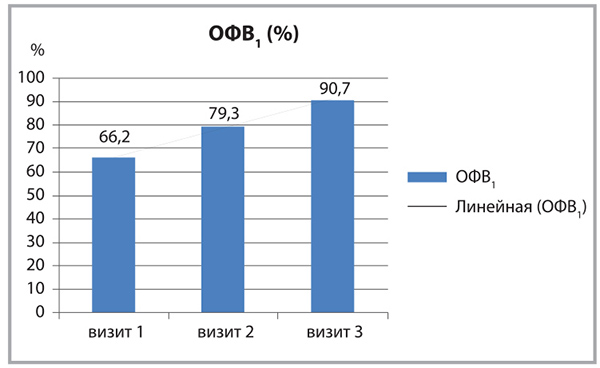
Положительная динамика показателей ФВД и снижение количества эозинофилов в мокроте, уменьшение гнойного характера мокроты сочетались с клиническим улучшением. Уровень ОФВ1 у всех пациентов третьем визите был достоверно выше, чем при первичном осмотре, и демонстрировал стойкую тенденцию к улучшению (рис. 4).
Существенное уменьшение интенсивности интоксикационного синдрома подтверждается данными общего анализа крови (снижение лейкоцитоза, СОЭ, восстановление баланса клеточного состава), нормализацией температуры тела и аускультативной картины.
Об эффективности применения азитромицина (Азибиот®) у пациента с БА свидетельствует клинический пример.
Больная М., 38 лет, на протяжении 16 лет страдает тяжелой персистирующей БА. Лечилась нерегулярно, самостоятельно прекращала назначенную специалистом базисную терапию и использовала бронхолитики короткого действия. Обострения наблюдались приблизительно 3 раз в год.
Обратилась с жалобами на постоянное затруднение дыхания в дневное время, частые ночные симптомы, ухудшение физической активности, приступообразный кашель с выделением незначительного количества мокроты слизисто-гнойного характера, свистящее дыхание, одышку, слабость.
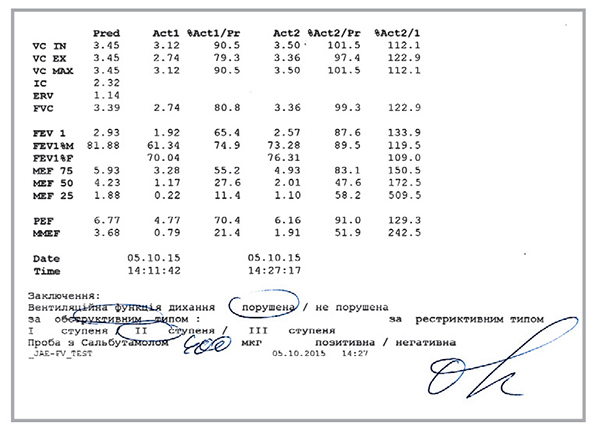
При объективном обследовании отмечались субфебрильная температура тела (37,4 °С), аускультативно на фоне жесткого дыхания выслушивались двусторонние свистящие и гудящие сухие хрипы. Общий анализ крови: лейкоциты – 12,6×109/л, эритроциты – 5,4×1012/л, лимфоциты – 16%, нейтрофилы – 68%, миелоциты – 2%, палочкоядерные нейтрофилы – 8%, эозинофилы – 6%, СОЭ – 18 мм/ч. При рентгенологическом исследовании отмечались фиброзные изменения в области корня легких, эмфизематозные признаки. При исследовании ФВД ОФВ1 составил 65,4% от должных величин. Обратимость бронхообструкции после приема 400 мкг сальбутамола была на уровне 33,9% (рис. 5). Средний астма-счет – 5,2 балла, среднее количество ингаляций сальбутамола в сутки – 2,8.
Было назначено лечение: сальбутамол 2,0 мл 2 р/сут, флутиказон по 2,0 мг 2 р/сут через небулайзер и сальбутамол по необходимости. Учитывая инфекционный характер обострения БА, в схему терапии был добавлен азитромицин (Азибиот®, KRKA, Словения) 500 мг 1 р/сут курсом 3 дня.
Рис. 5. Показатели ФВД у пациентки М. при первичном осмотре
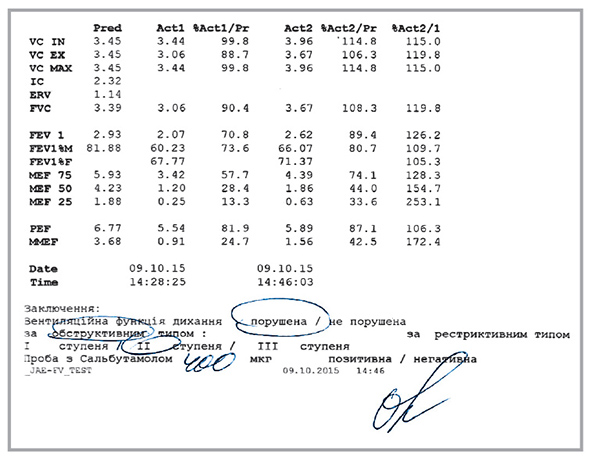
Через 3 дня лечения у больной уменьшился кашель, изменились характер и количество мокроты, нормализовалась температура тела, снизились частота и интенсивность ночных и дневных симптомов. Показатели ФВД улучшились, ОФВ1 возрос до 70,8% от должных величин (рис. 6).
Рис. 6. Показатели ФВД у пациентки М. при повторном осмотре
Через 10 дней на фоне базисной терапии обострения БА у больной нормализовалась температура тела, кашель стал редким, мокрота приобрела слизистый характер, практически исчезли ночные симптомы, значительно уменьшилась интенсивность дневных проявлений. В общем анализе крови отмечалось уменьшение количества нейтрофилов. Средний астма-счет на фоне назначенного лечения составил 2,5 балла, пациентка перестала использовать сальбутамол по требованию. Наблюдалось увеличение ОФВ1 до 84,6%, обратимость бронхообструкции – 15,3% (рис. 7).
Анализируя полученные результаты, следует отметить, что клиническая эффективность азитромицина в лечении больных с инфекционным обострением БА сочеталась с положительной динамикой ОФВ1, обеспечением ликвидации гнойного характера мокроты, достоверным снижением признаков атопии.
Рис. 7. Показатели ФВД у пациентки М. при выписке
Результаты оценки клинической эффективности азитромицина (Азибиот®, KRKA, Словения) 500 мг 1 р/сут курсом 3 дня при инфекционном обострении БА позволяют рекомендовать его более широкое применение с указанной целью. Препарат обладает хорошей переносимостью (побочный эффект в виде кратковременной тошноты наблюдался лишь у 1 пациента и не требовал прекращения лечения) и характеризуется удобным режимом приема (возможность назначения 1 р/сут коротком курсом), что оптимально для пациента и улучшает комплайенс.
Список литературы находится в редакции.