22 грудня, 2015
Негоспитальная пневмония: диагностика, тактика ведения и рациональная антибактериальная терапия с использованием препарата Фромилид® уно
 Этиологическая структура инфекционных болезней человека подвержена определенным изменениям во времени. Например, за последние десятилетия отмечен сдвиг в сторону гнойно-воспалительных заболеваний смешанной этиологии как во внутрибольничных, так и во внебольничных условиях. При этом возбудителями выступают не только классические, но и атипичные, а также условно-патогенные микроорганизмы (в ряде случаев обладающие множественной лекарственной устойчивостью).
Этиологическая структура инфекционных болезней человека подвержена определенным изменениям во времени. Например, за последние десятилетия отмечен сдвиг в сторону гнойно-воспалительных заболеваний смешанной этиологии как во внутрибольничных, так и во внебольничных условиях. При этом возбудителями выступают не только классические, но и атипичные, а также условно-патогенные микроорганизмы (в ряде случаев обладающие множественной лекарственной устойчивостью).
Если ведущая роль в этиологической структуре в 1950-1960 гг. принадлежала грамположительным бактериям, в 1970-1980 гг. – грамотрицательным и атипичным, то с конца 1990-х гг. и по настоящее время возрастает значение грамположительных полирезистентных кокков (стафило-, энтеро- и пневмококков). Отмечается увеличение количества метициллин- и ванкомицинрезистентных штаммов стафилококков, а также возбудителей, устойчивых ко всем известным на сегодня антибиотикам. Таким образом, несмотря на достоверную доказательную базу антибактериальных препаратов, их рациональный выбор остается сложной клинико-фармакологической задачей.
Трудности в данном вопросе обусловлены не только разнообразием этиологических патогенов и их возможной резистентностью, но и большим количеством классов антибиотиков, особенностями практического применения в рамках одной классификационной группы, недостаточным уровнем знаний в области клинической фармакологии и, наконец, ненадлежащим внедрением в практическую деятельность согласительных документов, протоколов и стандартов. Сложность выбора антибиотиков обусловлена также тем, что они демонстрируют отличия фармакокинетики и фармакодинамики в конкретных клинических ситуациях. По мнению экспертов, 75% антибиотиков применяются нерационально.
Так или иначе большинство антимикробных препаратов (АМП) проникают в очаг инфекции путем простой диффузии, и их концентрация там пропорциональна таковой свободного препарата в плазме или во внеклеточной жидкости. В то же время концентрация кларитромицина (14-членный макролидный антибиотик) в слизистой оболочке бронхов в 240 раз, а в альвеолярной жидкости – в 80 раз превышает сывороточную; соответствующий уровень сохраняется в течение 7 дней после отмены терапии. Это связано с тем, что по сравнению с другими макролидами кларитромицин в наименьшей степени связывается с белками плазмы (7-51%), что позволяет ему быстро поступать из сосудистого русла в ткани (в силу указанных свойств препарат называют тканевым антибиотиком). В целом связывание с белками снижает концентрацию лекарственного средства в очаге инфекции и препятствует реализации его терапевтических эффектов.
Неизбежное следствие широкого применения антимикробных средств – появление устойчивых (резистентных) возбудителей, что заставляет искать все новые и новые антибиотики, а также ведет к удорожанию медицинской помощи. За последние десятилетия темпы разработки АМП резко сократились, поэтому для успешного лечения бактериальных инфекций необходимо более рационально и избирательно подходить к назначению существующих антибиотиков, что требует от врача клинического мышления и достаточных знаний в области клиники, фармакологии и микробиологии.
В то же время врачебная деятельность с ее последовательной ориентацией на эмпирические данные является необходимой и существенной чертой любой диагностической и лечебной гипотезы, то есть эмпиризм – это не всегда деятельность вслепую. Правильно спланированный и четко проведенный эксперимент, в том числе клинический, – пожалуй, самая объективная модель, позволяющая рационально использовать АМП в практической деятельности врача.
Известно, что существует три вида антимикробной терапии (АМТ): эмпирическая, направленная против определенного возбудителя и профилактическая. В современных рекомендательных эмпирических моделях (консенсусах, приказах) при лечении негоспитальной пневмонии (НП) у больных III и IV групп лидирующее место занимают защищенные аминопенициллины, цефалоспорины III и IV поколений в сочетании с макролидом (данная комбинация улучшает прогноз заболевания, уменьшает летальность, а также сокращает сроки пребывания больных в стационаре). В схемах терапии НП у больных I и II групп также используются макролиды. Респираторные фторхинолоны (III и IV поколений) рассматриваются только как альтернатива в силу опасности развития к ним резистентности, высокой стоимости и большей вероятности возникновения нежелательных явлений, в особенности аритмий.
В современных рекомендациях по НП как основные классы АМП рассматриваются β-лактамные антибиотики (амоксициллин, амоксициллин/клавуланат; цефалоспорины II-IV поколений (цефуроксим, цефотаксим, цефтриаксон, цефепим; карбапенемы), макролиды (азитромицин, кларитромицин), фторхинолоны III и IV поколений (левофлоксацин, моксифлоксацин, гатифлоксацин), тетрациклины (доксициклин), препараты других классов (гликопептиды – ванкомицин, тейкопланин; оксазолидиноны – линезолид).
Клиническая картина, например, пневмоний предопределяется видом возбудителя (их около 100), причем разнообразие проявлений обусловливается особыми свойствами как микроорганизма (например, его вирулентностью), так и макроорганизма (например, резистентностью). В этой связи сохраняет свою принципиальность подразделение пневмоний на негоспитальную и госпитальную по этиологии и лечению, что, собственно, и заложено в современной классификации пневмоний.
В целом основанием для таких рекомендаций послужили выводы ряда исследований. Например, E. Garcia Vazquez и соавт. проанализировали исходы НП у 1391 больного. В 270 случаях предпочтение было отдано монотерапии β-лактамами, а в 918 – их комбинации с макролидным антибиотиком. Летальность в группе больных, получавших монотерапию β-лактамами, составила 13,3%, тогда как в группе сочетанного приема β-лактама и макролида – 6,9% (р=0,001). Результаты исследования показали, что сочетанное применение β-лактамного антибиотика и макролида приводило к снижению летальности больных НП независимо от степени тяжести заболевания.
В 2007 г. были опубликованы результаты когортного исследования, включавшего 2209 госпитализированных пациентов с доказанной бактериемией на фоне пневмонии. Многофакторный анализ позволил выявить влияние стартовой антибактериальной терапии на исход заболевания. Назначение макролидов (кларитромицина, азитромицина) в качестве стартовой терапии снижало госпитальную летальность (OR=0,59; 95% доверительный интервал 0,43-0,87; р=0,007). Возможно, важную роль в этом играют их иммуномодулирующий и противовоспалительный эффекты. Применение фторхинолонов или препаратов тетрациклинового ряда не имело преимуществ перед терапией другими классами антибиотиков.
В международные рекомендации включены такие представители класса макролидов, как кларитромицин, азитромицин и эритромицин. В то же время применение последнего актуально лишь в силу его низкой стоимости, ведь частота развития нежелательных реакций при использовании эритромицина наиболее высока по сравнению с таковой на фоне терапии другими макролидами. При сочетанном приеме эритромицина с верапамилом и дилтиаземом риск внезапной смерти увеличивается в 5 раз, с противогрибковыми препаратами – в 2 раза. Показано, что у новорожденных, матери которых принимали эритромицин, развивалась гипертрофия привратника.
Между тем 80-летний опыт использования антибиотиков не смог сдержать прогрессирование инфекционных процессов, не ликвидировал летальность от сепсиса, не сократил сроки лечения гнойных ран. Более того, огромные масштабы применения АМП привели к широкому распространению внутрибольничных и внебольничных инфекций, обусловленных штаммами патогенов с множественной устойчивостью.
В конечном счете в этих сложных условиях терапия бронхолегочных инфекций назначается, как и прежде, эмпирически. Поэтому в клинической практике следует исходить из консенсуального учета потенциальных возбудителей и необходимости применения эффективных препаратов с широким антимикробным спектром действия. То есть при лечении негоспитальных инфекций нижних дыхательных путей выбор АМП необходимо осуществлять по таким критериям, как спектр антимикробного действия, охватывающий предполагаемых возбудителей; особенности фармакокинетики, позволяющие обеспечить концентрации в тканях дыхательных путей, достаточные для эрадикации возбудителей; наличие таблетированной формы с хорошей биодоступностью; оптимальная переносимость. Выбранный нами препарат кларитромицина (Фромилид® уно) соответствовал вышеуказанным требованиям.
Основу всех макролидов составляет макроциклическое лактонное кольцо, связанное с одним или несколькими углеводными остатками. В зависимости от числа атомов углерода макролидные антибиотики подразделяются на классы, кларитромицин является 14-членным макролидом. Макролиды считаются средствами выбора при лечении заболеваний дыхательных путей, вызванных микоплазменной, хламидийной и легионеллезной инфекциями, хотя спектр их антибактериальной активности гораздо шире и при этом неоднороден. Так, кларитромицин превосходит другие макролиды по действию на пиогенный стрептококк и золотистый стафилококк. Согласно данным Bauerifeind (1993), по сравнению с другими препаратами этого класса кларитромицин также наиболее активен в отношении стрептококков группы В (S. agalactiae). Он демонстрирует значительную эффективность в отношении гемофильной палочки и анаэробных кокков.
Механизм антибактериального действия макролидов обусловлен торможением синтеза белка в микробной клетке за счет связывания с 50S-субъединицей рибосомы. По фармакокинетическим и микробиологическим показателям кларитромицин, 14-членный полусинтетический макролид, признан одним из лучших представителей класса. Активность препарата in vitro обусловлена образованием активного метаболита – 14-гидроксикларитромицина.
Одним из недостатков, за который в свое время критиковали кларитромицин, был двукратный режим приема, что негативно влияло на приверженность пациентов к лечению. В исследовании P. Cardas продемонстрировано влияние частоты применения препарата на комплайенс: при однократном суточном приеме АМП данный показатель составлял 97,6%, тогда как при двукратном – лишь 64,9%. Этот недостаток был нивелирован созданием лекарственной формы кларитромицина с пролонгированным высвобождением – препарата Фромилид® уно (фармакокинетические и фармакодинамические характеристики остались прежними, при этом обеспечивается однократный режим дозирования, способствующий повышению приверженности к лечению).
Нами проведено открытое неконтролированное исследование клинической и бактериологической эффективности препарата Фромилид® уно в монотерапии или в комбинированной схеме лечения у больных НП I-IV групп. В исследовании участвовали 78 больных: 53 (67,9%) – мужчины, 25 (32,05%) – женщины с подтвержденным диагнозом НП, которые по шкале PORT с интегральным индексом тяжести пневмонии (Pneumonia Severity Index, PSI) ≤90 баллов соответствовали I-IV группам: I группа – 10 пациентов, II группа – 32, III группа – 31, IV группа – 5. Средний возраст участников составил 49,7±5,4 года. В исследование не включали беременных и ВИЧ-инфицированных.
Клиническое обследование больных НП (рентгенография органов грудной клетки – ОГК, электрокардиография, клинический и биохимический анализ крови, определение уровня С-реактивного белка, исследование мочи и мокроты) были проведены до начала терапии и при выписке (на 7-14-й день). В этот же период выполняли бактериологическое исследование мокроты и идентификацию микроорганизмов из гемокультуры с оценкой их чувствительности к АМП (диско-диффузионный метод). Перед началом лечения определяли наличие пневмококкового антигена в крови и моче больных методом иммуноэлектрофореза, а также осуществляли серологический тест для выявления Chlamydоphila pneumoniae, C. psittaci, Mycoplasma pneumoniae, Legionella pneumophila, Coxiella burnetii.
Для микробиологического исследования использовалась утренняя мокрота, полученная при соответствующей подготовке. С целью определения пригодности образца мокроты для посева проводили бактериоскопию мазков, окрашенных по Граму. Материал рассматривали как качественный при наличии >25 полиморфноядерных лейкоцитов и <10 эпителиальных клеток в поле зрения при малом увеличении (+100) – V и VI классы по P.R. Murray, J.A. Washington.
Согласно результатам бактериологического исследования, возбудитель НП был выделен у 34 (43,5%) больных. Основными причинными патогенами оказались S. pneumoniae (14 штаммов), H. influenzae (5 штаммов) и K. pneumoniae (5 штаммов). Все выделенные штаммы S. pneumoniae сохраняли высокую чувствительность к защищенным аминопенициллинам, цефалоспоринам III поколения и кларитромицину. В одном случае был выявлен штамм S. pneumoniae, умеренно резистентный к пенициллину (МПК 0,12 мг/л) и устойчивый к эритромицину. Выделенные штаммы гемофильной палочки были чувствительны к аминопенициллинам, кларитромицину, азитромицину и цефтриаксону. Штаммов K. pneumoniae, не чувствительных к кларитромицину и азитромицину, не обнаружено. Необходимо отметить, что макролиды являются одной из тех групп АМП, которые наиболее требовательны к соблюдению условий определения чувствительности для получения корректных результатов, причем основными факторами, влияющими на результаты, являются рН питательной среды и атмосфера инкубации (повышенное содержание CO2), что в конечном итоге также приводит к изменению рН агара.
Все пациенты I группы получали Фромилид® уно по 500 мг 1 р/сут и были выписаны на 5-7-й день лечения с клинико-рентгенологическим выздоровлением. Больные II группы поступили в стационар с диагнозом пневмонии после отсутствия клинического эффекта на амбулаторном этапе на фоне приема триметоприма/сульфаметоксазола, офлоксацина, норфлоксацина, гентамицина, цефтриаксона без макролидов, иногда аминопенициллинов в таблетках. Анализируя назначенную амбулаторную терапию (кроме аминопенициллинов), можно сделать вывод, что она не соответствует современным стандартам. Можно предположить, что причиной 5 случаев клинической неэффективности защищенных аминопенициллинов при НП могла быть атипичная этиология заболевания, так как назначение препарата Фромилид® уно (по 500 мг 1 р/сут) обеспечило хороший результат (клинико-рентгенологическое и бактериологическое выздоровление).
Длительность антибиотикотерапии в первых двух группах составила в среднем 7 дней. Продолжительность рентгенологического разрешения пневмонии у больных І группы – 6,9±3,4 дня, ІІ – 8,7±5,4 дня, средняя длительность пребывания больного в стационаре – 10,8±2,5 койко-дня. Клинико-рентгенологическая и бактериологическая эффективность препарата Фромилид® уно в монотерапии или в сочетании с цефалоспоринами III поколения (при неэффективности таблетированных аминопенициллинов) составила 100%. При повторном бактериологическом исследовании возбудитель был выявлен у 2 пациентов (бактериологическая эффективность – 62,5%).
У 2 больных было отмечено умеренное и транзиторное повышение активности трансаминаз, что не явилось поводом для отмены препарата. У одного пациента на 7-й день лечения увеличилась частота стула. Динамика клинических и лабораторных данных у этого пациента была расценена как позитивная, на основании чего принято решение отменить антибиотик. В целом препарат хорошо переносился. Наиболее часто встречающиеся нежелательные явления включали преходящую боль в животе и тошноту у 2 (2,5%) больных, головную боль у 2 (2,5%) участников; однократная диарея/обстипация имела место у 1 (1,2%) пациента, кожная сыпь – у 1 (1,2%) больного. В ходе статистической обработки данных не выявлены различия в клиническом эффекте между возрастным группами больных, принимавших Фромилид® уно.
Антибактериальная терапия у пациентов III группы (n=31) соответствовала современным стандартам: парентерально аминопенициллин (преимущественно защищенный) + макролид (Фромилид® уно) по 1 таблетке 1 р/сут или цефалоспорин III поколения + макролид (Фромилид® уно) по 1 таблетке 1 р/сут.
Больные IV группы (n=5) начинали лечение в палате интенсивной терапии. Все участники этой группы, кроме цефалоспоринов III и IV поколения, получали Фромилид® уно по 1000 мг однократно утром в течение 7-10 дней. Показатель по шкале CRB-65 у них равнялся 3 баллам.
Комплексный подход к определению целесообразности антибактериальной терапии предполагает взаимосвязанную оценку последствий (результатов) и стоимости медицинских вмешательств. Речь идет не просто о сравнении затрат, а об оценке соотношения между затратами и полученными результатами. Согласно данным современных фармакоэкономических исследований, стоимость лечения больного НП в стационаре составляет 70-80% прямых затрат. В то же время уменьшение длительности пребывания больного в стационаре на 1 койко-день позволяет снизить затраты в среднем на 3-5%. В связи с этим сокращение продолжительности стационарного лечения за счет оптимизации и повышения эффективности антибиотикотерапии – потенциальный способ уменьшения затрат на ведение больных НП. Хотя данное исследование проведено в стационарных условиях, препарат Фромилид® уно (как в монотерапии, так и в сочетании с другими классами АМП) может обеспечить столь же выраженный положительный эффект и экономические выгоды в амбулаторных условиях.
Клинический случай 1
Больной Д., 38 лет. Заболел остро. Появились сухой кашель, слабость, температура тела 38,6 °С. К врачу не обращался, принимал жаропонижающие средства в течение 3 дней, однако состояние ухудшилось: температура тела повысилась до 39,4 °С, усилилась слабость, появилась боль в левой половине грудной клетки при кашле. Осмотрен терапевтом на дому. Диагностирована ОРВИ, назначены защищенный аминопенициллин в таблетках и отхаркивающие средства. Сохранялись слабость, кашель с мокротой серого цвета, лихорадка до 39,6 °С, боли в левой половине грудной клетки при кашле и глубоком вдохе. Через 4 дня в связи с выраженным болевым синдромом в области грудной клетки слева с иррадиацией в живот вызвана бригада неотложной помощи.
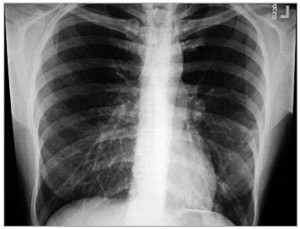 Рис. 1. Рентгенограмма больного Д.: негомогенное затемнение в нижних сегментах левого легкого; инфильтрация выражена неярко, не исключен интерстициальный тип заболевания
Рис. 1. Рентгенограмма больного Д.: негомогенное затемнение в нижних сегментах левого легкого; инфильтрация выражена неярко, не исключен интерстициальный тип заболеванияБольной госпитализирован в хирургическое отделение, где была произведена рентгенограмма ОГК (рис. 1). Диагностирована сегментарная левосторонняя пневмония, больной переведен в пульмонологическое отделение. В силу неэффективности предшествующей терапии защищенным аминопенициллином, а также ввиду того, что на рентгенограмме предположительно имеется интерстициальный компонент легочного рисунка, назначен Фромилид® уно 500 мг 1 р/сут + цефалоспорин III поколения внутривенно. Также выполнена компьютерная томография (КТ) ОГК (рис. 2), подтвердившая пневмонию нижней доли (поражение сегмента S9) левого легкого.
Проводимая терапия оказалась эффективной: через 3 дня нормализовалась температура тела, купирован синдром интоксикации, перестала беспокоить боль в левой половине грудной клетки; сохранялись локальные мелкопузырчатые хрипы. Контрольная рентгенограмма ОГК через 7 дней: очаговые и инфильтративные изменения отсутствуют.
Можно предположить, что пациент перенес атипичную пневмонию (факторы риска иммунодефицита отсутствуют), так как на КТ ОГК определяется смешанный тип инфильтрации (интерстициальный и альвеолярный); защищенный аминопенициллин не обеспечил эрадикацию возбудителя, а терапия препаратом Фромилид® уно по 1 таблетке в сутки и цефалоспорином III поколения сопровождалась клинико-рентгенологическим выздоровлением.
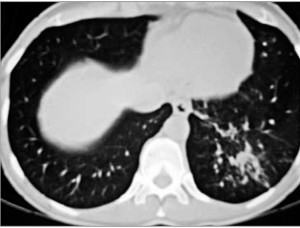 Рис. 2. КТ ОГК больного Д.: очаговая сливная инфильтрация в S9 левого легкого с участками «матового стекла»
Рис. 2. КТ ОГК больного Д.: очаговая сливная инфильтрация в S9 левого легкого с участками «матового стекла»В целом о пневмонии следует думать при наличии как минимум 2 из 3 факторов: респираторного (кашель, мокрота, одышка, боль в груди при дыхании или кашле, мелкопузырчатые хрипы в легких или крепитация); интоксикационного (озноб, температура тела >38 °С, тахикардия, полиорганные нарушения) синдрома и легочного инфильтрата. В то же время следует помнить, что сходные клинические проявления могут быть обусловлены различными возбудителями.
Разновидность инфильтрации легких имеет значение при проведении дифференциальной диагностики. В данном случае можно добавить, что возбудитель пневмонии не может быть точно установлен только на основании оценки клинических данных.
Клинический случай 2
Больной С., 22 лет, студент. Вечером появились сухой кашель, слабость, лихорадка 38,6 °С; принимал таблетированные жаропонижающие средства. Через 2 дня температура тела повысилась до 39,6 °С, появились умеренная боль в правой половине грудной клетки при кашле и слизисто-гнойная мокрота, ухудшилось общее самочувствие. Осмотрен участковым терапевтом.
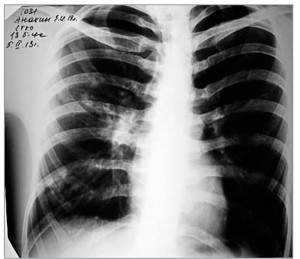 Рис. 3. Рентгенограмма ОГК больного С.: негомогенное очаговое затемнение (выраженное уплотнение) в области корня правого легкого
Рис. 3. Рентгенограмма ОГК больного С.: негомогенное очаговое затемнение (выраженное уплотнение) в области корня правого легкогоДиагностирована ОРВИ с трахеобронхитом. Назначены комбинированный жаропонижающий препарат, тилорон, амброксол. Несмотря на это на следующий день усилилась слабость, появилась умеренная одышка, сохранялись боль в правой половине грудной клетки при кашле, лихорадка 39,5 °С. Бригадой скорой помощи пациент был доставлен в стационар с диагнозом абсцесса легкого.
На обзорной рентгенограмме ОГК выявлен легочный инфильтрат в S3 справа (рис. 3). У больного диагностирована правосторонняя НП в верхней доле, I группа, дыхательная недостаточность I ст. К I группе больной отнесен из-за отсутствия сопутствующей патологии и указаний на прием антибиотикотерапии в течение последних 3 мес.
Этиологическая структура пневмонии имеет различия в зависимости от возраста: у детей и молодых людей возбудителями преимущественно выступают микоплазмы или вирусы; в то время как у лиц пожилого возраста, новорожденных или в случаях, когда пневмония является осложнением другого заболевания, ее причиной чаще бывают типичные бактериальные патогены. В I группе (легкое течение) этиологическое значение имеют стрептококк, микоплазма, хламидия, гемофильная палочка.
Учитывая вышесказанное, пациенту был назначен Фромилид® уно по 500 мг 1 р/сут. Через 48 ч от начала лечения выраженность респираторного и интоксикационного синдромов значительно уменьшилась, температура тела снизилась до 37,6 °С. К 8-му дню лечения жалобы исчезли. На обзорной рентгенограмме ОГК очаговые и инфильтративные изменения отсутствовали (рис. 4). Больной выписан с клинико-рентгенологическим выздоровлением.
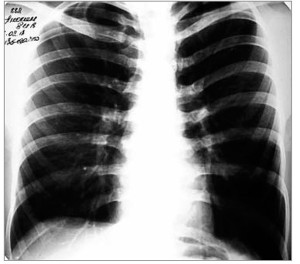 Рис. 4. Рентгенограмма ОГК больного С. после проведенного лечения: очаговые и инфильтративные изменения отсутствуют
Рис. 4. Рентгенограмма ОГК больного С. после проведенного лечения: очаговые и инфильтративные изменения отсутствуютУ больных с верифицированной НП, не имеющих других факторов риска, отмечаются хороший прогноз в плане выздоровления и низкие показатели летальности. Оценка эффективности антибактериального лечения проводится в течение 48-72 ч от начала терапии. Критериями являются уменьшение респираторного и интоксикационного синдромов, снижение температуры тела больного, уменьшение плевральной боли и признаков дыхательной недостаточности.
Показания для внутривенного введения антибиотиков – исходно тяжелое течение пневмонии, измененное сознание, нарушение глотательного рефлекса, недостаточность питательных веществ вследствие нарушения их всасывания в тонкой кишке (мальабсорбция) или анатомических дефектов / функциональной патологии; III или IV группа НП.
Рекомендованная длительность антибактериальной терапии при легком неосложненном течении НП составляет 3-5 дней; при легком (в сочетании с факторами риска) и среднетяжелом течении – 7-10 дней; при тяжелом течении с неустановленной этиологией – 10 дней; при микоплазменной или хламидийной этиологии – 10-14 дней. НП, вызванная S. aureus, Enterobacteriaceaе (тяжелые инфекции) и P. aeruginosa, требует лечения в течение ≥14 дней; легионеллезная НП – 14-21-дневной терапии.
В итоге мы пришли к выводу, что клиническая и бактериологическая эффективность Фромилида уно позволяет рассматривать данный препарат в ряду первостепенных средств при лечении I-IV групп пациентов с НП. Немаловажно, что в нынешней сложной клинико-микробиологической ситуации чувствительность патогенов к препарату Фромилид® уно сохраняется на высоком уровне. Это доказано как собственной клинической практикой, так и многочисленными адекватно контролируемыми испытаниями с участием десятков тысяч больных.
Список литературы находится в редакции.



