22 грудня, 2015
Антибиотики при остром бронхите: от предубеждений к рациональной терапии
Хороший врач знает, какие есть антибиотики.
Отличный врач знает, когда можно применить антибиотики.
Самый лучший врач знает, когда не надо назначать антибиотик.
Л.С. Страчунский
Довольно часто перед врачом общей практики возникает дилемма: необходимо ли назначать антибиотик (АБ) при остром бронхите (ОБ)? В большинстве случаев применение антибактериального препарата терапевт аргументирует опасением вовремя не распознать тяжелое заболевание, например пневмонию. Нередко в качестве основания для назначения АБ рассматривается наличие кашля, субфебрильной температуры тела и двусторонних сухих свистящих хрипов при аускультации легких.
 Вопросам рационального применения АБ при лечении пациентов с ОБ был посвящен доклад доцента кафедры фтизиатрии и пульмонологии Национальной медицинской академии последипломного образования им. П.Л. Шупика, кандидата медицинских наук Людмилы Владимировны Юдиной, представленный в рамках VII Национального конгресса «Человек и лекарства – Украина».
Вопросам рационального применения АБ при лечении пациентов с ОБ был посвящен доклад доцента кафедры фтизиатрии и пульмонологии Национальной медицинской академии последипломного образования им. П.Л. Шупика, кандидата медицинских наук Людмилы Владимировны Юдиной, представленный в рамках VII Национального конгресса «Человек и лекарства – Украина».
– В настоящее время до 75% всех назначений АБ в терапевтической практике можно считать необоснованными, и это одна из главных причин возникновения и распространенности антибиотикорезистентности. Еще одной актуальной проблемой является преодоление стереотипов относительно пути введения АБ. К сожалению, пациентам, которые получают лечение в амбулаторных условиях, все еще назначают АБ с внутримышечным путем введения, что обусловлено ошибочным мнением о более высокой эффективности парентеральных форм.
Рациональная антибиотикотерапия – одна из основных задач современной медицины. Следует помнить, что АБ не являются жаропонижающими средствами, не заменяют санитарно-эпидемиологических мероприятий и не должны использоваться как «транквилизаторы» для больных, их родственников и администрации больницы.
ОБ можно рассматривать как случай острой респираторной инфекции (ОРИ), сопровождающейся кашлем, который наблюдается в течение не более 3-4 нед после исчезновения других респираторных симптомов. Более чем в 90% случаев этиологическим фактором ОБ являются вирусы: возбудители гриппа А и В, парагриппа, риновирусы, респираторно-синцитиальный вирус и др. Следовательно, при установлении диагноза ОБ безотлагательное назначение антибиотикотерапии не требуется; АБ нужно применять только при отсутствии положительной динамики заболевания в течение 3-7 дней.
В случае ОБ бактериальной природы (отмечается в <10% случаев) необходимо принимать во внимание следующий факт: у каждого четвертого пациента причиной заболевания являются атипичные микроорганизмы (Mycoplasma pneumoniae, Chlamydophila pneumoniaе) и Bordetella pertussis, которые устойчивы к воздействию β-лактамов, но чувствительны к макролидам.
Ключевое условие рационального использования АБ – выбор препарата, спектр активности которого охватывает максимальное число предполагаемых возбудителей заболевания. Одной из групп препаратов, неоднократно продемонстрировавших эффективность и безопасность в терапии респираторных инфекций, включая ОБ бактериальной этиологии, являются макролиды.
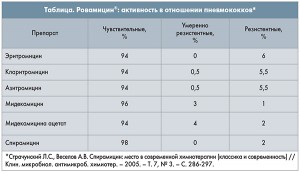 Наряду с макролидами, синтезированными в 1980-1990-х гг. (азитромицин, рокситромицин, кларитромицин), в клинической практике используются и так называемые ранние макролиды, среди которых следует отметить спирамицин (оригинальная молекула представлена на рынке под торговым названием Ровамицин® производства Санофи). Спирамицин является 16-членным макролидом, который активен в отношении ряда возбудителей (в том числе грамположительных кокков), резистентных к 14- и 15-членным представителям этой группы препаратов (табл.).
Наряду с макролидами, синтезированными в 1980-1990-х гг. (азитромицин, рокситромицин, кларитромицин), в клинической практике используются и так называемые ранние макролиды, среди которых следует отметить спирамицин (оригинальная молекула представлена на рынке под торговым названием Ровамицин® производства Санофи). Спирамицин является 16-членным макролидом, который активен в отношении ряда возбудителей (в том числе грамположительных кокков), резистентных к 14- и 15-членным представителям этой группы препаратов (табл.).
Согласно результатам российского проспективного многоцентрового микробиологического исследования ПеГАС-II (2004-2005 гг.), количество умеренно резистентных и резистентных штаммов Streptococcus pneumoniae к спирамицину составляет всего 4,5% (рис.).
Следует отметить так называемый парадокс спирамицина: несмотря на относительно низкую активность in vitro, которая основана на определении минимальной подавляющей концентрации, препарат проявляет высокую активность in vivo. Механизм антибактериального эффекта данного средства, как и других макролидных АБ, обусловлен торможением синтеза белка в микробной клетке за счет связывания с 50S-субъединицей рибосомы. Спирамицин способен соединяться не с одним, а сразу с тремя доменами 50S-субъединицы рибосомы, что обеспечивает более длительный антибактериальный эффект. Как в исследованиях in vitro, так и in vivo продемонстрирована способность АБ накапливаться внутри фагоцитов (в альвеолярных макрофагах, нейтрофилах и др.). Уровни спирамицина в них в 20-30 раз превышают внеклеточные значения. Препарат также создает высокие концентрации как в верхних (миндалины, синусы), так и в нижних дыхательных путях (бронхиальный секрет, легочная ткань).
Также спирамицину присущ постантибиотический эффект, под которым подразумевают персистирующее ингибирование жизнедеятельности бактерий после их кратковременного контакта с АБ. В основе указанного эффекта лежат необратимые изменения в рибосомах патогена, следствием чего является стойкий блок транслокации. За счет этого антибактериальное действие препарата пролонгируется, сохраняясь в течение срока, необходимого для ресинтеза новых функциональных белков микробной клетки.
Следует отметить суб-МПК эффект спирамицина: ингибирующее влияние на размножение бактерий сохраняется после снижения уровня препарата в сыворотке крови и очаге инфекции ниже минимальной подавляющей концентрации. Считается, что суб-МПК эффект обусловлен возможностью блокировать рибосомальную транслокацию даже при невысокой концентрации макролидов и ассоциируется со снижением вирулентности микрофлоры, а также c повышением чувствительности бактерий к влиянию иммунных факторов.
Спирамицин отличается хорошим профилем безопасности; в наименьшей степени в сравнении с другими представителями макролидов ингибирует цитохром Р450; оказывает минимальное влияние на метаболизм лекарственных препаратов. Благодаря перечисленным преимуществам спирамицин можно рассматривать как препарат выбора у пациентов с сопутствующими заболеваниями. В отличие от 14-членных макролидов для спирамицина не характерен прокинетический эффект (способность усиливать моторику желудочно-кишечного тракта, которая клинически проявляется нежелательными реакциями в виде боли в животе, тошноты, диареи).
Имеются данные об иммуномодулирующем эффекте спирамицина, основанном на способности антибиотика угнетать образование интерлейкина-2, гиперпродукция которого может играть роль в аутоиммунном поражении тканей.
Ровамицин® выпускается в форме таблеток, покрытых оболочкой, по 1,5 и 3 млн МЕ. Рекомендуемая доза препарата для взрослых составляет 6-9 млн МЕ/сут в 2 приема, детям весом более 20 кг назначают 1,5 млн МЕ на 10 кг массы тела в сутки в 2-3 приема.
Спирамицин (Ровамицин®) отличают:
• удобство приема (его биодоступность не зависит от приема пищи);
• высокая результативность благодаря достижению оптимальных концентраций препарата в тканях;
• широкий спектр активности (в том числе против некоторых возбудителей, устойчивых к 14- и 15-членным макролидам);
• хорошая переносимость (нежелательные реакции развиваются редко).
Спирамицин – один из немногих природных антибиотиков, которые выдержали испытание временем и сохраняют свое клиническое значение в новом тысячелетии на фоне увеличения резистентности микроорганизмов и появления на фармацевтическом рынке новых препаратов. Следует отметить высокую активность этого АБ в отношении атипичных возбудителей и его «неуязвимость» для β-лактамаз.
Подготовила Елена Молчанова