24 січня, 2021
Предіабет і цукровий діабет: стратегії, що допомагають зупинитися вчасно
За даними, наведеними в IDF Diabetes Atlas (2019), станом на 2019 рік один з 11 дорослих віком 20-79 років (загалом 463 млн осіб), мав цукровий діабет (ЦД). У кожного 2-го хворого (приблизно 232 млн осіб) діабет не діагностовано. Порівняно з показниками 2017 року кількість дорослих, які мають підвищений ризик виникнення ЦД 2 типу, зросла на 22 млн. 10% глобальних витрат у системі охорони здоров’я – 760 млн доларів – припадає на ЦД. Тому з упевненістю й сумом можна констатувати, що епідемія коронавірусної інфекції, в умовах якої ми наразі живемо, не єдина глобальна проблема системи охорони здоров’я. Ускладнює ситуацію й те, що 3 з 4 пацієнтів із ЦД мешкають у країнах із низьким/середнім рівнем економічного розвитку, де своєчасній діагностиці та лікуванню перешкоджають фінансові причини й особливості менталітету.
Підступність ЦД – у високій частоті ускладнень: ризик серцево-судинних захворювань (ССЗ) у пацієнтів із ЦД зростає приблизно вдвічі; також спостерігається суттєве збільшення ймовірності термінальних стадій хронічної ниркової недостатності.
Фахівцями першого контакту для пацієнтів із ЦД 2 типу та станами, котрі йому передують, є лікарі загальної практики – сімейної медицини, що підкреслює надзвичайно важливу роль їхньої обізнаності в питаннях класифікації, діагностики й терапії порушень вуглеводного обміну.
Досвідом із фахівцями первинної ланки активно діляться спеціалісти-ендокринологи. Зокрема, в рамках Школи ендокринології для лікарів загальної практики – сімейної медицини (науково-освітнього проєкту, що відбувається у форматі онлайн) прозвучало кілька цікавих доповідей, присвячених цій темі. Пропонуємо ознайомитися з ключовими тезами, представленими у виступах.
Предіабет і ЦД: як не перейти межу
.jpg) На питаннях скринінгу, діагностики предіабету та ЦД 2 типу докладно зупинилася завідувачка науково-консультативного відділу амбулаторно-профілактичної допомоги хворим з ендокринною патологією ДУ «Інститут ендокринології та обміну речовин ім. В. П. Комісаренка НАМН України» (м. Київ), кандидат медичних наук Валерія Леонідівна Орленко.
На питаннях скринінгу, діагностики предіабету та ЦД 2 типу докладно зупинилася завідувачка науково-консультативного відділу амбулаторно-профілактичної допомоги хворим з ендокринною патологією ДУ «Інститут ендокринології та обміну речовин ім. В. П. Комісаренка НАМН України» (м. Київ), кандидат медичних наук Валерія Леонідівна Орленко.
– Порушення толерантності до глюкози та порушення глікемії натще (ПГН) – це стани, за яких рівень глюкози в крові вищий за нормальний діапазон, але нижчий за рекомендований поріг для діагностики ЦД. Терміни «предіабет», «недіабетична гіперглікемія», «проміжна гіперглікемія» використовують як альтернативні.
Основні документи, на які орієнтуються фахівці під час діагностики й лікування предіабету, – Стандарти надання медичної допомоги при ЦД (Standards of Medical Care in Diabetes, 2020), Рекомендації Європейського товариства кардіологів із діабету, предіабету та ССЗ, розроблені спільно з Європейською асоціацією з вивчення діабету (2019 ESC Guidelines on diabetes, pre-diabetes and cardiovascular diseases in collaboration with EASD).
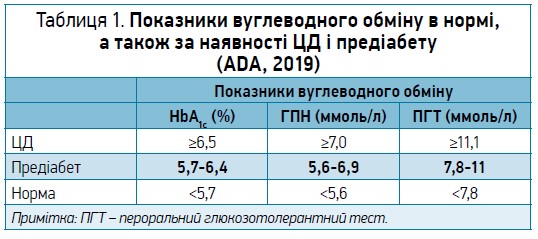 Предіабет – порушення вуглеводного обміну, що асоціюється з високим ризиком розвитку ЦД при значеннях глюкози плазми, недостатніх для встановлення діагнозу діабету (табл. 1). Цей стан характеризується ПГН та/або порушенням толерантності до глюкози, є незалежним фактором ризику виникнення ССЗ.
Предіабет – порушення вуглеводного обміну, що асоціюється з високим ризиком розвитку ЦД при значеннях глюкози плазми, недостатніх для встановлення діагнозу діабету (табл. 1). Цей стан характеризується ПГН та/або порушенням толерантності до глюкози, є незалежним фактором ризику виникнення ССЗ.
У разі предіабету від початку метаболічних змін до клінічної маніфестації ЦД минає в середньому 5 років. На момент встановлення діагнозу ЦД 2 типу приблизно 20% пацієнтів уже мають мікро- та макросудинні ускладнення.
До патофізіологічних порушень за наявності предіабету відносять інсулінорезистентність (ІР), або порушення чутливості до дії інсуліну; втрату β-клітин; дисфункцію ендотелію; артеріальну ригідність; підвищений ліполіз; зниження рівня інкретинів; підвищення продукції глюкози в печінці; порушення рівня глюкагону; дисбаланс цитокінів; гіперглікемію та зумовлений нею феномен глюкозотоксичності. Нині у фокусі уваги – процеси, що перешкоджають надходженню до клітин адекватної кількості інсуліну, зокрема порушення ремоделювання позаклітинного матриксу. Його провокують запальні процеси, як наслідок, виникають дисфункція ендотелію, капілярна регресія, підвищення взаємодії елементів позаклітинного матриксу з рецепторами клітин, включаючи сімейство інтегринів. Важливо, що описаний механізм є одним із небагатьох, на який можна вплинути та знизити ІР. За даними D. H. Wasserman і співавт. (2018), зменшення доступу інсуліну до скелетних м’язів і впливу на них вважається одним із ключових механізмів розвитку предіабету. Порушення мікроциркуляції, що спостерігаються при ожирінні, – бар’єр для проникнення інсуліну в скелетні м’язи. Діяти на цю ланку рекомендується першочергово.
Невидима загроза
Чим загрожує пацієнту наявність предіабету? На тлі предіабету зростає ризик виникнення ЦД, ССЗ (ішемічної хвороби серця, ішемічного інсульту – приблизно вдвічі), а також рівень загальної смертності – в 1,6 раза. Збільшується ймовірність мікросудинних уражень, зокрема ретинопатії, особливо якщо HbA1c >5,5% (Gheng Y. J., Gregg E. W. et al., 2009).
У спостереженні, котре тривало 11 років, було встановлено, що за наявності порушення толерантності до глюкози ЦД 2 типу виникав у 46% пацієнтів, у разі ПГН – у 38%. Результати роботи S. M. Twigg (2004) продемонстрували, що через 10 років після діагностики предіабету, незважаючи на превентивні заходи, у 50% пацієнтів відбулося прогресування порушень вуглеводного обміну в ЦД 2 типу.
Якщо HbA1c зберігається в діапазоні 6,0-6,4%, ризик розвитку ЦД 2 типу протягом 5 років максимальний: він сягає 25-50% (Zhang X., Gregg E. et al., 2010). У дослідженні TOPICS визначили, що в разі поєднання в пацієнта HbA1c 6,0-6,4% і ПГН 6,0-6,9 ммоль/л поява ЦД 2 типу через 5 років практично гарантована – майже 100% (Heianza Y. et al., 2012). Зазначена категорія пацієнтів потребує обов’язкової й активної корекції способу життя та постійного спостереження.
Різні діагностичні критерії предіабету мають зіставну прогностичну значущість стосовно ССЗ і рівня загальної смертності. На думку окремих дослідників, дещо точнішим вважається HbA1c.
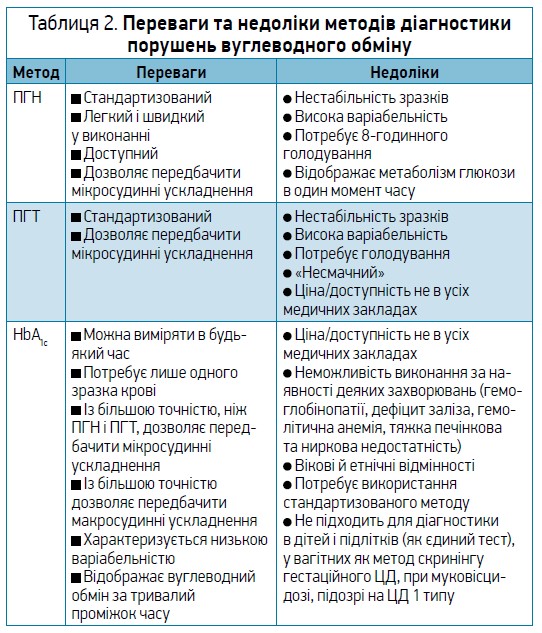 Методи діагностики порушень вуглеводного обміну докладно описано в таблиці 2.
Методи діагностики порушень вуглеводного обміну докладно описано в таблиці 2.
Скринінг у дорослих
Згідно з рекомендаціями ADA (2020), можливість обстеження на предіабет і ЦД 2 типу слід розглянути в безсимптомних дорослих із факторами ризику (ФР) і всіх осіб віком від 45 років.
Тестування на предіабет і ЦД 2 типу варто проводити дорослим будь-якого віку, котрі мають надмірну вагу / ожиріння (індекс маси тіла (ІМТ) >25 кг/м2) і ≥1 додаткових ФР діабету, а також жінкам, які планують вагітність і мають надмірну вагу / ожиріння та ≥1 додаткових ФР діабету.
Якщо результати скринінгу в межах норми, його повторюють через ≥3 роки (або частіше, залежно від початкових показників і ФР). За наявності предіабету тестування проводять щорічно, а жінок із гестаційним діабетом в анамнезі тестують на предіабет кожні 3 роки.
Критерії скринінгу предіабету / ЦД 2 типу в безсимптомних дорослих (ADA, 2020)
- Низька фізична активність
- Наявність діабету в родичів першого ступеня
- Раса / етнічна група високого ризику
- Жінки, котрі народили дитину вагою понад 4 кг або мали гестаційний ЦД
- Артеріальна гіпертензія (≥140/90 мм рт. ст.) або застосування антигіпертензивної терапії
- Рівень холестерину ліпопротеїнів високої щільності <0,9 ммоль/л та/або рівень тригліцеридів (ТГ) >2,82 ммоль/л (їх значення важливіше, ніж рівня холестерину ліпопротеїнів низької щільності)
- Інші клінічні стани, пов’язані з ІР (наприклад, ожиріння, синдром полікістозних яєчників)
- Анамнез ССЗ
! Зафіксовано, що в деяких пацієнтів після COVID‑19 реєструється підвищення рівня HbA1c до 6,2-6,4%. Оптимальна тактика лікаря в такій ситуації – визначити HbA1c кілька разів протягом тривалого часу. Існують гіпотези, що COVID‑19 провокує розвиток ЦД; також зростання концентрації HbA1c може виникати як відповідь на застосування глюкокортикоїдів.
Скринінг у дітей
Скринінг у дітей на предіабет і ЦД 2 типу слід розглянути після досягнення статевої зрілості чи 10-річного віку (залежно від того, що настане раніше), в дітей і підлітків із надмірною вагою / ожирінням, які мають ≥1 додаткових ФР діабету.
До ФР належать:
- обтяжений сімейний анамнез (наявність ЦД у родичів першої чи другої лінії);
- раса / етнічна група високого ризику;
- ознаки ІР або стани, пов’язані з ІР;
- гестаційний діабет у матері.
Скринінг здійснюють із періодичністю раз на 3 роки. В осіб молодого віку рекомендують застосовувати визначення концентрації глюкози в плазмі крові натще, через 2 год під час проведення ПГТ і визначення рівня HbA1c.
Гестаційний діабет
Діагноз гестаційного ЦД встановлюється на 24-28-му тижні вагітним, у яких раніше не виявляли ЦД. Також потрібно проводити діагностику предіабету та ЦД на 4-12-му тижні після пологів за допомогою ПГТ і клінічних критеріїв.
Жінки, котрі мають в анамнезі гестаційний діабет, повинні проходити довічний скринінг предіабету та ЦД щонайменше кожні 3 роки. Пацієнтки з обтяженим анамнезом гестаційного ЦД, у яких після пологів виявили предіабет, мають дотримуватися активного способу життя та/або застосовувати метформін із профілактичною метою.
Здоровий спосіб життя: довготривалі зміни, а не «разова акція»
Як показали результати Diabetes Prevention Program (DPP, 2002), пацієнти з предіабетом повинні модифікувати спосіб життя, досягати зниження маси тіла на 7% від початкової та зберігати її на цьому рівні, збільшувати тривалість фізичної активності середньої інтенсивності (наприклад, швидка ходьба) мінімум до 150 хв на тиждень, дотримуватися дієтичного режиму зі зменшенням добової калорійності на 20-30% від звичної.
Дітям і підліткам із ЦД 1 або 2 типу чи предіабетом варто приділяти ≥60 хв на добу аеробній активності середньої чи високої інтенсивності з активним зміцненням м’язів і кісток не менше 3 днів на тиждень.
Більшість дорослих із ЦД 1 та 2 типу повинні виконувати аеробні вправи середньої чи високої інтенсивності ≥150 хв на тиждень (щонайменше 3 заняття, максимум із 2-денними інтервалами). Коротша тривалість (мінімум 75 хв занять на тиждень) енергійних або інтервальних тренувань допускається як достатня для молодших і фізично підготовлених осіб.
Відповідно до результатів DPP, дотримання здорового способу життя протягом 4 років допомогло запобігти 58% випадків предіабету та ЦД, а застосування метформіну – 31%. Проте подальше спостереження, DPP Outcomes Study, показало, що втримати нормальні показники вуглеводного обміну після активної зміни способу життя й додержуватися жорстких обмежень протягом тривалого часу вдалося менш ніж 25% пацієнтів.
Фінське дослідження DPS регламентувало такі вимоги до зміни способу життя та дієти: споживання ≤30% від денної кількості загальних жирів, ≤10% від денної кількості насичених жирів, ≥15 г / 1000 ккал становила клітковина, ≥30 хв фізичної активності щодня, ≥5% зниження маси тіла. І тільки пацієнти, котрі чітко дотримувалися всіх 5 (!) вимог, змогли уникнути розвитку ЦД 2 типу.
Місце фармакотерапії в лікуванні предіабету
Препаратом із доведеною ефективністю, рекомендованим для лікування предіабету, є метформін. Терапію метформіном для профілактики ЦД 2 типу слід розглянути у хворих із предіабетом й ожирінням, в осіб віком від 60 років і жінок із гестаційним діабетом в анамнезі.
Метформін знижує рівень HbA1c, зменшує показник систолічного артеріального тиску в осіб із предіабетом та/або ожирінням, що, своєю чергою, забезпечує зниження ризику ССЗ.
У дослідженні MET-REMODEL довели кардіопротекторну дію метформіну: його застосування в дозі 2000 мг зменшувало вираженість гіпертрофії лівого шлуночка в пацієнтів із предіабетом без супутньої артеріальної гіпертензії. У випробуванні DPPOS використання метформіну супроводжувалося зменшенням розповсюдженості та вираженості коронарного атеросклерозу в чоловіків із предіабетом.
Тривале застосування метформіну здатне призводити до дефіциту вітаміну В12, тому періодично слід визначати його концентрацію в крові, особливо в пацієнтів з анемією чи периферичною нейропатією.
Метформін пролонгованого вивільнення (Глюкофаж XR) рекомендується для зниження ризику та профілактики ЦД 2 типу в дорослих пацієнтів із надмірною вагою й порушенням толерантності до глюкози та/або ПГН та/або підвищенням рівня HbA1c, в яких:
- високий ризик розвитку ЦД 2 типу;
- ЦД 2 типу прогресує, незважаючи на активну зміну способу життя протягом останніх 36 міс.
! У дослідженні DPP було зроблено висновок, що терапія метформіном у дозі 1700 мг/добу не спричиняла гіпоглікемії в осіб із предіабетом.
Лікування предіабету: надмірність або необхідність?
 Чи варто розпочинати фармакотерапію предіабету? І якщо так, то коли? Міркуваннями на тему та переконливими доказовими даними поділилася керівник відділу діабетології ДУ «Інститут ендокринології та обміну речовин ім. В. П. Комісаренка НАМН України» (м. Київ), доктор медичних наук Любов Костянтинівна Соколова.
Чи варто розпочинати фармакотерапію предіабету? І якщо так, то коли? Міркуваннями на тему та переконливими доказовими даними поділилася керівник відділу діабетології ДУ «Інститут ендокринології та обміну речовин ім. В. П. Комісаренка НАМН України» (м. Київ), доктор медичних наук Любов Костянтинівна Соколова.
– Виділяють декілька типів ЦД:
- ЦД 1 типу виникає через автоімунну деструкцію β-клітин, що зазвичай призводить до абсолютного дефіциту інсуліну;
- ЦД 2 типу (понад 90% випадків) розвивається внаслідок прогресуючого зниження секреції інсуліну β-клітинами (часто на тлі ІР);
- гестаційний ЦД – діабет, діагностований під час II-III триместрів вагітності, що не був виявлений до гестації;
- специфічні типи діабету, зумовлені іншими причинами, зокрема моногенними синдромами діабету (діабет у новонароджених, діабет MODY), захворюваннями екзокринної частини підшлункової залози (панкреатит, муковісцидоз) або індуковані наркотичними/хімічними речовинами (наприклад, у разі застосування глюкокортикоїдів, при лікуванні ВІЛ/СНІД, після трансплантації органів).
Критерій встановлення діагнозу ЦД – ПГН ≥7 ммоль/л (через 8 год після останнього прийому їжі); якщо таке значення було отримано двічі з інтервалом 5-7 днів, встановлюємо діагноз ЦД. Додаткове виконання ПГТ не потрібне, оскільки може спровокувати декомпенсацію. Оцінка рівня HbA1c не є обов’язковою умовою для встановлення діагнозу, проте допомагає вибрати стратегію лікування: якщо HbA1c ≥7%, варто призначити пероральну цукрознижувальну терапію (чи навіть інсулінотерапію, коли показник дуже високий).
Якщо ПГН ≥5,6, але <7 ммоль/л, потрібно виконати ПГТ. Якщо через 2 год після навантаження глюкозою її рівень перевищує 11,1 ммоль/л, можна стверджувати, що в пацієнта ЦД, навіть якщо її концентрація натще не досягала 7 ммоль/л. Показник HbA1c оцінюють, щоб обрати терапевтичну тактику.
Визначення лише рівня HbA1c достатнє для верифікації ЦД у тому випадку, коли показник становитиме ≥6,5%. Якщо в пацієнта HbA1c <6,5%, а ПГН >7 ммоль/л або ПГТ >11,1 ммоль/л, таку ситуацію трактують як ЦД 2 типу.
! Рівень HbA1c <6,5% не є гарантією відсутності порушень вуглеводного обміну.
Предіабет vs діабет
Предіабет – стан, який наразі жодним чином не класифікується в МКХ‑10, проте потребує активного втручання фахівця, рекомендацій щодо зміни способу життя та навіть призначення медикаментозної терапії.
Критерії встановлення діагнозу предіабету (Standards of Medical Care in Diabetes, 2020): ПГН 5,6-6,9 ммоль/л, або ПГТ 7,8-11,0 ммоль/л, або HbA1c 5,7-6,4%.
- Поєднання ПГН 5,6-6,9 ммоль/л і ПГТ 7,8-11,0 ммоль/л класифікується як предіабет.
- ПГН 5,6-6,9 ммоль/л і ПГТ >11,0 ммоль/л – як ЦД.
- ПГН 5,6-6,9 ммоль/л і ПГТ <7,8 ммоль/л – як ізольована гіперглікемія (критерій предіабету).
Скринінг на наявність ЦД 2 типу
Скринінг слід здійснювати в усіх пацієнтів віком понад 45 років і тих, кому до 45 років, але вони мають щонайменше 1 ФР.
Для скринінгу достатньо вимірювання ПГН за допомогою глюкометра, а для встановлення діагнозу необхідно проводити дослідження в умовах лабораторії із застосуванням біохімічного аналізатора.
У рамках діагностики ЦД виконують такі дослідження:
- рівень глюкози крові натще;
- HbA1c;
- тест на визначення толерантності до глюкози;
- С-пептид;
- імунореактивний інсулін;
- фруктозамін;
- глюкозурія;
- індекс НОМА;
- антитіла до клітин підшлункової залози (GADA, ICA, IA‑2).
У більшості випадків можна обмежитися першими 3 дослідженнями, лише вони є обов’язковими для скринінгу.
Як уже зазначала Валерія Леонідівна, в дорослих пацієнтів із предіабетом потрібно щороку проводити скринінг ЦД 2 типу, а для профілактики появи діабету – модифікувати спосіб життя відповідно до результатів програми DPP, а саме досягти зниження маси тіла на 7% від початкової та зберігати її на цьому рівні, збільшити тривалість фізичної активності середньої інтенсивності мінімум до 150 хв на тиждень. Хочу підкреслити, що протягом 5 днів лежати на дивані й ласувати смаколиками, а у вихідні безперервно «гарувати» в спортзалі – не варіант, фізична активність має бути системною та регулярною, 30-45 хв щодня.
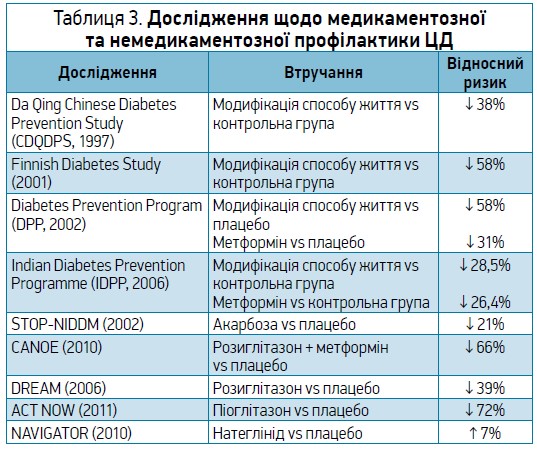 Призначати метформін на тлі ІР за відсутності порушень вуглеводного обміну, згідно з інформацією в інструкції до препарату, рекомендаціями ADA та EASD, не дозволено. Проте пацієнтам, у яких присутні хоча би початкові порушення вуглеводного обміну (ПГН, порушення толерантності до глюкози), метформін з огляду на його ефективність у запобіганні ЦД 2 типу (табл. 3) краще призначити, ніж не призначити.
Призначати метформін на тлі ІР за відсутності порушень вуглеводного обміну, згідно з інформацією в інструкції до препарату, рекомендаціями ADA та EASD, не дозволено. Проте пацієнтам, у яких присутні хоча би початкові порушення вуглеводного обміну (ПГН, порушення толерантності до глюкози), метформін з огляду на його ефективність у запобіганні ЦД 2 типу (табл. 3) краще призначити, ніж не призначити.
Результати DPP продемонстрували, що найдієвіший спосіб профілактики ЦД – модифікація способу життя (ризик прогресування предіабету в ЦД знижувався на 58%, а на тлі терапії метформіном у дозі 850 мг 2 р/добу цей показник становив -31%). Як показує власний практичний досвід, призначення метформіну допомагає збільшити у хворого мотивацію дотримуватися суворих вимог зі зміни способу життя.
! Вчасно призначивши адекватну терапію метформіном, вдається відтермінувати розвиток ЦД 2 типу в середньому на 10 років.
- Метформін є кращим варіантом стартової фармакотерапії для лікування ЦД 2 типу.
- Прийом метформіну слід продовжувати, доки пацієнт добре переносить лікування та не має протипоказань; до метформіну варто додавати інші засоби, включаючи інсулін.
- Раннє введення інсуліну можна обговорювати, якщо спостерігається втрата ваги, наявні симптоми гіперглікемії чи рівень HbA1c >10% або рівень глюкози >16,7 ммоль/л.
 Метформін – базисне лікування назавжди. Це ефективний, дешевий, дієвий варіант терапії, що добре переноситься та має вагому доказову базу. Якнайшвидше призначення метформіну пацієнтам із предіабетом та ЦД 2 типу є виправданим.
Метформін – базисне лікування назавжди. Це ефективний, дешевий, дієвий варіант терапії, що добре переноситься та має вагому доказову базу. Якнайшвидше призначення метформіну пацієнтам із предіабетом та ЦД 2 типу є виправданим.
Цукрознижувальний ефект метформіну є дозозалежним: мінімальний – у разі застосування в дозі 500 мг/добу, максимальний – 2000-2500 мг/добу. У пацієнтів із дуже вираженою ІР, ожирінням можна використовувати дозування 3000 мг/добу, проте нетривалий час – у подальшому необхідні модифікація способу життя та зниження дозування.
 Якщо в пацієнта стабільна хронічна серцева недостатність, метформін може призначатися за умови регулярного моніторингу функції серця та нирок. Гостра й нестабільна хронічна серцева недостатність є протипоказаннями до застосування препарату. Підходи до застосування метформіну в разі порушень із боку нирок відображено в таблиці 4.
Якщо в пацієнта стабільна хронічна серцева недостатність, метформін може призначатися за умови регулярного моніторингу функції серця та нирок. Гостра й нестабільна хронічна серцева недостатність є протипоказаннями до застосування препарату. Підходи до застосування метформіну в разі порушень із боку нирок відображено в таблиці 4.
Переваги, недоліки й особливості застосування метформіну описано в таблиці 5.
Терапію порушень вуглеводного обміну рекомендують розпочинати з метформіну звичайного вивільнення. Якщо в пацієнта присутня його непереносимість, віддають перевагу метформіну пролонгованого вивільнення (наприклад, препарату Глюкофаж XR). Якщо існують протипоказання до прийому метформіну, лікування розпочинають з інгібіторів дипептидилпептидази‑4, піоглітазону, препаратів сульфонілсечовини.
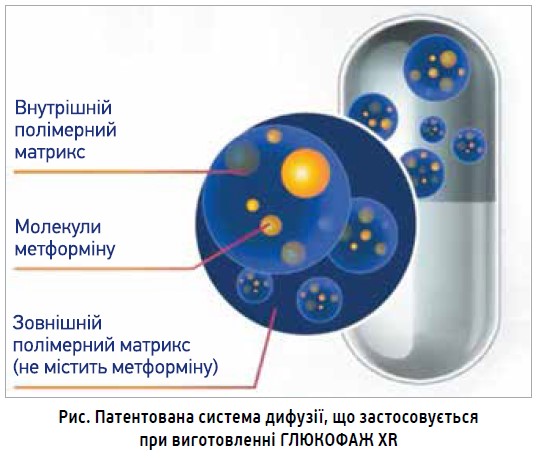 Глюкофаж XR застосовується 1 р/добу (вся доза одномоментно у вечірній час). Патентована система дифузії крізь гелевий бар’єр GelShield (рис.) забезпечує поступове й рівномірне вивільнення метформіну з таблетки, завдяки чому зменшується ймовірність несприятливих гастроінтестинальних ефектів і покращується комплаєнс.
Глюкофаж XR застосовується 1 р/добу (вся доза одномоментно у вечірній час). Патентована система дифузії крізь гелевий бар’єр GelShield (рис.) забезпечує поступове й рівномірне вивільнення метформіну з таблетки, завдяки чому зменшується ймовірність несприятливих гастроінтестинальних ефектів і покращується комплаєнс.
Варто зауважити: нещодавно форма препарату Глюкофаж XR змінилася з двоопуклих капсул на двоопуклі круглі таблетки. Також зменшилася маса таблетки. Вона містить ту саму кількість метформіну, але тепер до складу таблетки входить менше допоміжних речовин, як-от стеарат магнію, карбоксиметилцелюлоза натрію, гіпромелоза; відсутня мікрокристалічна целюлоза. Завдяки цьому таблетки легше та зручніше ковтати.
Підсумовуючи сказане, ще раз хочу наголосити, що предіабет вимагає призначення активних стратегій: зміни способу життя, збільшення тривалості фізичних навантажень, дотримання дієти (харчування невеличкими порціями продуктами з низьким глікемічним індексом 5-6 разів на добу), терапії метформіном.
Глюкофаж XR – єдиний метформін в Україні, дозволений для профілактики розвитку ЦД 2 типу в разі неефективності дієтотерапії й активної зміни способу життя. Глюкофаж і Глюкофаж XR можуть призначатись як стартове лікування при ЦД 2 типу як у режимі монотерапії, так і в комбінації з іншими цукрознижувальними засобами.
Підготувала Олександра Марченко
UA-GLUC-PUB-122020-065
Медична газета «Здоров’я України 21 сторіччя» № 24 (493), 2020 р.



