27 січня, 2021
GINA-2020: що нового? Global Initiative for Asthma, перегляд 2020 р.
 Бронхіальна астма (БА) – гетерогенне захворювання, що зазвичай характеризується хронічним запаленням дихальних шляхів. Діагностується за наявності в анамнезі респіраторних симптомів, таких як свистячі хрипи, задишка, стиснення в грудях і кашель, які змінюються з часом та за інтенсивністю, а також нестійкого обмеження повітряного потоку на видиху.
Бронхіальна астма (БА) – гетерогенне захворювання, що зазвичай характеризується хронічним запаленням дихальних шляхів. Діагностується за наявності в анамнезі респіраторних симптомів, таких як свистячі хрипи, задишка, стиснення в грудях і кашель, які змінюються з часом та за інтенсивністю, а також нестійкого обмеження повітряного потоку на видиху.
БА – поширене хронічне респіраторне захворювання, на яке хворіють 1–18% населення різних країн. Для астми характерні мінливі симптоми хрипів, задишки, стиснення в грудях і/або кашлю, а також нестійке обмеження повітряного потоку на видиху.
Як симптоми, так і обмеження потоку повітря змінюються з часом та за інтенсивністю. Часто вони спричинюються такими факторами, як фізичне навантаження, вплив алергенів або подразників, зміна погоди або вірусні респіраторні інфекції.
Симптоми та обмеження повітряного потоку можуть зникати спонтанно або після прийому препаратів, іноді вони відсутні впродовж декількох тижнів або місяців. З іншого боку, у пацієнтів можуть виникати епізодичні загострення БА, які загрожують життю та зумовлюють значний тягар для пацієнтів і суспільства (див. Додаток до розділу 1). Зазвичай БА пов’язана з гіперреактивністю дихальних шляхів на прямі або непрямі подразники, а також із хронічним запаленням дихальних шляхів. Ці ознаки зберігаються навіть за відсутності симптомів або в разі нормальної функції легень, але можуть нормалізуватись у процесі лікування.
Фенотипи астми
БА – гетерогенне захворювання з різними механізмами розвитку. Розрізнювані групи демографічних, клінічних і/або патофізіологічних ознак часто називають фенотипами астми [5-7]. Для пацієнтів із більш тяжкою БА доступні певні методи лікування, спрямовані на фенотип захворювання. Однак не було виявлено сильного взаємозв’язку між певними патологічними проявами та клінічними закономірностями або відповіддю на лікування. Потрібні додаткові дослідження, аби зрозуміти клінічну цінність класифікації БА за фенотипами.
Виявлено багато клінічних фенотипів астми [5-7]. Найпоширенішими є:
- Алергічна астма: це найлегше розпізнаваний фенотип астми, який часто дебютує в дитячому віці і пов’язаний з анамнезом і/або сімейним анамнезом алергічних захворювань, таких як екзема, алергічний риніт, харчова або лікарська алергія. Під час дослідження індукованого мокротиння перед лікуванням в таких пацієнтів часто виявляють еозинофільне запалення дихальних шляхів. Пацієнти з цим фенотипом БА зазвичай добре реагують на лікування інгаляційними кортикостероїдами (ІКС).
- Неалергічна астма: у деяких пацієнтів розвивається БА, не пов’язана з алергією. Клітинний профіль мокротиння таких пацієнтів може бути нейтрофільним, еозинофільним або містити незначну кількість запальних клітин (пауцигранулоцитарним). У пацієнтів із неалергічною БА часто спостерігають слабшу найближчу (короткострокову) реакцію на ІКС.
- Астма в дорослих (пізня): у деяких дорослих, особливо жінок, БА вперше виникає в дорослому віці. Такі пацієнти, як правило, не мають алергії, часто потребують вищих доз ІКС або є відносно стійкими до КС-терапії. У пацієнтів із пізньою БА необхідно виключати професійну астму.
- Астма зі стійким обмеженням потоку повітря: у деяких пацієнтів із тривалим перебігом БА розвивається стійке, або повністю незворотне, обмеження повітряного потоку. Вважають, що воно пов’язане з реорганізацією стінок дихальних шляхів.
- Астма з ожирінням: у деяких хворих з ожирінням і БА спостерігають виражені респіраторні симптоми й незначне еозинофільне запалення дихальних шляхів.
Дані про природний перебіг БА після встановлення діагнозу обмежені, але в одному дослідженні було показано, що приблизно в 16% дорослих із недавно діагностованою БА може спостерігатися ремісія вродовж 5 років [8].
COVID‑19 і БА
Радьте пацієнтам із БА продовжувати приймати протиастматичні препарати, особливо ІКС і пероральні КС (ПКС), якщо їх було призначено.
- Прийом протиастматичних лікарських засобів треба продовжувати як зазвичай. Відміна ІКС часто призводить до потенційно небезпечного погіршення перебігу БА.
- Для пацієнтів із тяжкою БА: продовжувати біологічну терапію і не припиняти раптово прийом ПКС, якщо їх було призначено.
Переконайтесь, що всі пацієнти мають письмовий план дій щодо БА з інструкціями стосовно:
- підвищення дози контролювальних і допоміжних препаратів у разі погіршення перебігу БА;
- застосування короткого курсу ПКС у разі тяжких загострень БА;
- того, в яких випадках звертатись по медичну допомогу.
Див. Звіт GINA‑2020, щоб отримати додаткову інформацію про варіанти лікування згідно з планом дій при БА.
Уникайте за можливості застосування небулайзерів:
- небулайзери збільшують ризик поширення вірусу серед пацієнтів і медичних працівників;
- дозувальний інгалятор під тиском зі спейсером є найкращим вибором у разі тяжких загострень, з використанням мундштука або щільно прилягаючої лицьової маски, якщо потрібно.
Уникайте спірометрії в пацієнтів із підтвердженим/підозрюваним COVID‑19:
- спірометрія може призвести до поширення вірусних частинок і створювати ризик зараження персоналу та пацієнтів;
- поки у вашому регіоні відбувається передача вірусу в популяції, відкладіть проведення спірометрії та пікфлоуметрії в закладах охорони здоров’я, якщо в цих дослідженнях немає нагальної потреби;
- дотримуйтеся запобіжних заходів щодо контактного та крапельного механізмів передачі.
Дотримуйтеся суворих заходів із контролю інфекції, якщо потрібні процедури, що супроводжуються утворенням аерозолю:
- наприклад: небулізація, киснева терапія (у тому числі з використанням назальних канюль), індукція мокротиння, ручна вентиляція, неінвазивна вентиляція та інтубація;
- рекомендації Всесвітньої організації охорони здоров’я (ВООЗ) щодо боротьби з інфекцією наведено тут: www.who.int/publications-detail/infection-prevention-and-control-during-health-care-when-novel-coronavirus-(ncov)-infection-is-suspected‑20200125
Дотримуйтеся місцевих медичних рекомендацій щодо гігієнічних стратегій і використання засобів індивідуального захисту, щойно нова інформація стане доступною у вашій країні чи вашому регіоні.
GINA-2019: знакові зміни в лікуванні БА
З міркувань безпеки GINA більше не рекомендує застосовувати монотерапію БАКД на 1-му Кроці лікування.
- Це рішення базувалося на доказах того, що монотерапія БАКД збільшує ризик тяжких загострень, а додавання будь-якого ІКС значно його зменшує.
Тепер GINA для зменшення ризику тяжких загострень рекомендує всім дорослим і підліткам із БА застосовувати як контролювальний препарат ІКС.
- ІКС може призначатися на регулярній основі (щодня) або, у разі легкої астми, за потреби – у вигляді низьких доз ІКС-формотеролу.
Стратегія зменшення популяційного ризику:
- інші приклади: статини, антигіпертензивні засоби;
- в окремих пацієнтів можуть не спостерігатись (або вони можуть не знати про них) найближчі (короткострокові) клінічні переваги;
- метою є зменшення ймовірності серйозних несприятливих наслідків на популяційному рівні.
Персоналізоване ведення пацієнтів із БА
Початкове лікування БА: з чого починати?
Чи допомагає визначення рівня FeNO у вирішенні питання про початкове призначення ІКС?
У дослідженнях, переважно за участю пацієнтів, які не палять, вміст FeNO >50 млрд‑1 асоціювався з хорошою найближчою реакцією на IКС [163, 172]. Однак у цих дослідженнях не вивчали віддалений ризик загострень. Отже, такі докази не означають, що безпечно щодо загострень утримуватися від призначення ІКС пацієнтам із низьким початковим вмістом FeNO. Зовсім недавно у двох 12-місячних дослідженнях легкої БА частота серйозних загострень була меншою в разі застосування за потреби ІКС-формотеролу порівняно із застосуванням за потреби БАТД і підтримувальною терапією ІКС, незалежно від вихідних показників запалення, зокрема FeNO [173, 174].
Отже, у пацієнтів із БА або підозрою на неї вимірювання FeNO може підтвердити рішення про початкове призначення ІКС, але не може використовуватися для рішення проти лікування ІКС. На основі минулих і сучасних даних GINA рекомендує призначення щоденних низьких доз ІКС або, якщо потрібно, низьких доз ІКС-формотеролу всім пацієнтам із легкою БА для зменшення ризику тяжких загострень [175].
ІКС-формотерол за потреби – якою має бути максимальна добова доза?
Низькі дози будесоніду–формотеролу за потреби:
- призначають для підтримувальної та полегшувальної терапії (Кроки 3-5), або лише за потреби (Кроки 1, 2), або в рамках плану дій щодо БА;
- згідно з інструкцією до препарату, максимальна рекомендована добова доза – 72 мкг формотеролу (12 інгаляцій будесоніду–формотеролу Турбухалер 200/6 мкг).
Низькі дози беклометазону–формотеролу за потреби:
- призначають для підтримувальної та полегшувальної терапії (Кроки 3-5) або в рамках плану дій щодо БА;
- згідно з інструкцією до препарату, максимальна рекомендована добова доза становить 48 мкг формотеролу (6 інгаляцій беклометазону–формотеролу у формі дозованого інгалятора під тиском (pMDI) 100/6 мкг).
Оцінка контролю симптомів
Оцінюючи контроль симптомів, враховують частоту використання БАКД:
- частіше вживання БАКД асоціюється з гіршими результатами, навіть у пацієнтів, які приймають ІКС.
На нашу думку, частота застосування ІКС-формотеролу не має враховуватися під час оцінки контролю симптомів, особливо в пацієнтів, які не приймають ІКС для підтримувальної терапії:
- IКС-формотерол за потреби забезпечує контролювальну терапію;
- очікуються додаткові дані: це питання буде повторно розглянуто наступного року.
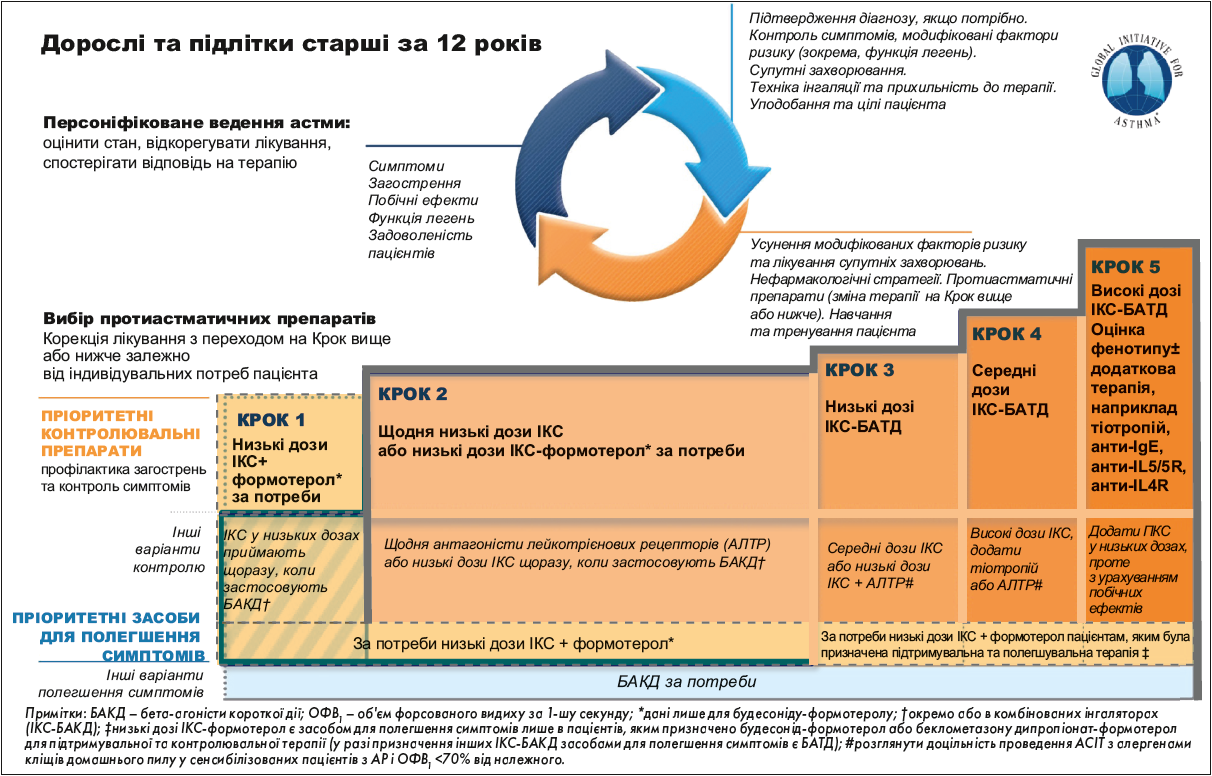
Кроки терапії БА
Крок 1: Пріоритетний засіб для контролю симптомів: комбінація низьких доз IКC–формотеролу за потреби (дорослі та підлітки; рис.)
Рис. Рекомендована початкова контролювальна терапія для дорослих і підлітків із діагностованою БА
Пріоритетний засіб для контролю симптомів на 1-му Кроці терапії для дорослих і підлітків: комбінація низьких доз IКС-формотеролу за потреби для усунення симптомів і, якщо потрібно, перед фізичними навантаженнями.
Крок 1, згідно з рекомендаціями GINA, призначений:
- для початкового лікування БА в пацієнтів із частотою симптомів <2 разів на місяць і відсутністю факторів ризику загострення; є групою, що рідко вивчається;
- зміна лікування на Крок нижче в пацієнтів, в яких БА добре контролюється на 2-му Кроці.
Застосування низьких доз ІКС-формотеролу за потреби для усунення симптомів на 1-му Кроці в дорослих і підлітків (РД В) підтверджується непрямими даними масштабного подвійного сліпого дослідження, що порівнює цей режим із монотерапією БАКД і з регулярним прийомом низьких доз ІКС+БАКД за потреби в пацієнтів із легкою БА, що відповідають критеріям 2-го Кроку (див. нижче) [177]. Ці результати підтверджуються 2 відкритими рандомізованими контрольованими дослідженнями (РКД), що представляють спосіб застосування пацієнтами з легкою БА ІКС-формотеролу за потреби в реальних умовах [173, 174]. У цих дослідженнях пацієнти застосовували БАКД від 2 разів на місяць до 2 разів на день.
Найважливішими міркуваннями GINA щодо прийому низьких доз ІКС-формотеролу за потреби на 1-му Кроці були:
- Докази того, що пацієнти з нечастими симптомами БА мають ризик тяжких або смертельних загострень [178]. GINA рекомендує оцінювати фактори ризику загострень, а також контролювати симптоми.
- Зниження на дві третини частоти тяжких загострень у дослідженні застосування на 2-му Кроці низьких доз будесоніду–формотеролу за потреби проти монотерапії БАКД і той факт, що це було досягнуто за допомогою <20% середньої дози ІКС відносно щоденного їх прийому [177]. У відкритому РКД також спостерігали зменшення на 60% частоти тяжких загострень порівняно з монотерапією БАКД [173].
- Докази того, що в пацієнтів із нечастими симптомами прихильність до щоденної терапії ІКС є дуже низькою [179], що наражає їх на ризики, пов’язані з монотерапією БАКД.
- Важливо уникати суперечливих повідомлень під час навчання пацієнта. Раніше на початку лікування БА пацієнтам призначали лише БАКД для полегшення симптомів, але пізніше, незважаючи на те що це лікування було ефективним у хворих, їм сказали, що потрібно приймати контролювальний препарат щодня, навіть коли немає симптомів, щоб зменшити використання БАКД. Рекомендація щодо забезпечення всіх пацієнтів засобом для контролю симптомів від початку терапії (зокрема, при легкій БА ІКС-формотерол за потреби) дає можливість послідовно інформувати про необхідність як зменшення симптомів, так і ризиків, і може запобігти формуванню в пацієнта залежності від БАКД як основного лікувального засобу.
Максимальна рекомендована добова доза будесоніду–формотеролу для використання за потреби відповідає 72 мкг формотеролу. Однак у РКД при легкій БА рідко спостерігали таке високе дозування, у середньому використовували приблизно 3-4 дози на тиждень [173, 177, 180].
Поки що всі докази застосування за потреби ІКС-формотеролу при легкій БА стосувалися низьких доз будесоніду–формотеролу, але можна призначати і беклометазон–формотерол. Обидва препарати добре зарекомендували себе при застосуванні за потреби в рамках підтримувальної та полегшувальної терапії Кроків 3-5 за GINA [181]; у чотирьох дослідженнях із застосуванням за потреби будесоніду–формотеролу при легкій БА не виявлено нових сигналів небезпеки.
Не проводилося досліджень використання за потреби ІКС-формотеролу в дітей віком 6-11 років. Однак занепокоєння щодо монотерапії БАКД стосується й дітей і має враховуватися під час призначення 1-го Кроку лікування.
Інші варіанти контролювальної терапії на 1-му Кроці для дорослих і підлітків
Прийом низьких доз ІКС щоразу, коли приймають БАКД (РД В): докази ефективності цієї стратегії на 1-му Кроці є непрямими, з досліджень з окремими або комбінованими інгаляторами ІКС і БАКД у пацієнтів, які відповідали критеріям 2-го Кроку лікування [184-187]. Ця рекомендація покликана зменшити ризик тяжких загострень і труднощі досягнення належної прихильності до регулярного прийому ІКС у пацієнтів із нечастими симптомами. Застосування IКC щоразу, коли приймають БАКД, може бути доцільним у країнах, де IКC-формотерол недоступний або дорогий.
Крок 2. Пріоритетні варіанти контролювальної терапії: щодня низька доза IКC плюс БАКД за потреби (дорослі, підлітки та діти) АБО низька доза IКC–формотеролу за потреби (дорослі та підлітки)
Пріоритетний засіб для контролю симптомів на 2-му Кроці терапії (дорослі, підлітки та діти): щодня низькі дози IКC плюс БАКД за потреби
Є велика кількість доказів, отриманих під час РКД і обсерваційних досліджень, які демонструють істотне зниження ризику тяжких загострень, госпіталізацій і смерті в разі регулярного застосування низьких доз ІКС; також зменшуються вираженість симптомів і бронхоконстрикція, спричинена фізичним навантаженням (РД A) [182, 188, 190, 199, 200]. У разі прийому низьких доз ІКС частота тяжких загострень зменшується вдвічі навіть у пацієнтів з частотою симптомів 0-1 день на тиждень [160].
Для цієї рекомендації найважливішим фактором було зменшення ризику важких загострень. Призначаючи щоденний прийом ІКС пацієнтам із легкою БА, клініцисти мають пам’ятати про ймовірність поганого комплаєнсу, що наражає пацієнтів на ризики, пов’язані з монотерапією БАКД.
Пріоритетний препарат для контролю симптомів на 2-му Кроці терапії (дорослі та підлітки): низька доза ІКС-формотеролу за потреби для купірування симптомів і, якщо потрібно, перед фізичними навантаженнями.
Під час розробки цієї рекомендації найважливішими міркуваннями GINA було запобігання тяжким загостренням і уникнення необхідності щоденного прийому ІКС у пацієнтів із легкою БА, які в клінічній практиці часто погано дотримуються призначеного лікування ІКС.
Як свідчить інструкція до препарату, максимальна рекомендована добова доза IКC-формотеролу становить 48 мкг формотеролу для беклометазону–формотеролу та 72 мкг формотеролу для будесоніду–формотеролу. Однак у РКД при легкій БА рідко можна було спостерігати таке високе дозування, а середня частота застосування ІКС-формотеролу за потреби становила приблизно 3-4 дози на тиждень [173, 174, 177, 180].
У пацієнтів із легкою БА одне дослідження показало, що будесонід–формотерол, вжитий за потреби та перед фізичним навантаженням, був так само корисний щодо зменшення бронхоконстрикції, спричиненої фізичним навантаженням, як щоденне застосування ІКС із БАКД за потреби чи перед тренуванням [183]. Потрібні додаткові дослідження, але це свідчить про те, що пацієнти з легкою БА, яким призначають IКC-формотерол за потреби для запобігання загостренням і контролю симптомів, можуть застосовувати ті самі ліки перед фізичним навантаженням, і їм не потрібно призначати БАКД перед тренуваннями (РД B).
Інші варіанти контролювальної терапії на 2-му Кроці для дітей і підлітків
Якщо IКC-формотерол за потреби недоступний, іншим варіантом є прийом низьких доз IКC щоразу, коли пацієнт приймає БАКД. Докази, отримані в ході досліджень з окремими або комбінованими інгаляторами ІКС і БАКД [184-186, 201], продемонстрували відсутність різниці в частоті загострень порівняно з щоденним прийомом ІКС.
Антагоністи лейкотрієнових рецепторів (АЛР) менш ефективні, ніж IКC [202], особливо щодо загострень (РД A). Їх можна призначати для початкової контролювальної терапії деяким пацієнтам, які не можуть або не хочуть використовувати IКC; пацієнтам, в яких розвивалися серйозні побічні ефекти на тлі прийому ІКС; або пацієнтам із супутнім АР (РД B) [203, 204]. Перш ніж призначати монтелукаст, медичні працівники мають врахувати його переваги та ризики, а пацієнтів потрібно проінформувати про ризик розвитку нервово-психічних подій. Нещодавно Управління із санітарного контролю якості харчових продуктів і медикаментів США (FDA) зробило особливе попередження про ризик серйозних негативних наслідків для психічного здоров’я при застосуванні монтелукасту [205].
Побічні ефекти монтелукасту
У березні 2020 р. FDA зробила особливе попередження про зумовлений монтелукастом ризик серйозних нервово-психічних подій, у тому числі суїцидальної поведінки:
- суїцидальність у дорослих і підлітків;
- кошмари та розлади поведінки в дітей.
Перш ніж призначати монтелукаст, медичні працівники мають зважувати переваги та ризики, необхідно інформувати пацієнтів про ризик нервово-психічних подій.
Для дорослих або підлітків, які раніше не застосовували контролювальну терапію, регулярне щоденне використання низьких доз IКC-БАТД як початкового підтримувального лікування зменшує симптоми та покращує функцію легень порівняно з низькими дозами IКC [206]. Однак це лікування дорожче і додатково не зменшує ризик загострень проти монотерапії ІКС (РД А) [206].
У пацієнтів із сезонною алергічною БА, наприклад на пилок берези, з постійними симптомами БА треба розпочинати регулярний щоденний прийом ІКС або ІКС-формотеролу за потреби відразу після появи симптомів і продовжувати впродовж 4 тиж після закінчення сезону пилкування (РД D).
Не рекомендовано для рутинного застосування
Теофілін із пролонгованим вивільненням є малоефективним при БА [207-209] (РД B), його побічні ефекти є поширеними і можуть загрожувати життю в разі застосування високих доз (РД А) [213]. Кромони (недокроміл натрію та кромоглікат натрію) мають сприятливий профіль безпеки, але низьку ефективність (РД А) [211-213], а інгалятори, що їх містять, потребують обтяжливого щоденного промивання для уникнення закупорки.
Крок 3. Пріоритетні варіанти контролювальної терапії: підтримувальне застосування низьких доз IКC-БАТД плюс БАКД за потреби, АБО низькі дози IКC-формотеролу для підтримувальної та полегшувальної терапії (дорослі та підлітки)
Перш ніж розглянути зміну терапії на Крок угору, перевірте наявність таких поширених проблем, як неправильна техніка інгаляції, низька прихильність до лікування, вплив факторів довкілля, а також переконайтеся, що симптоми зумовлені БА.
Пріоритетна контролювальна терапія на Кроці 3 у дорослих і підлітків
Для дорослих і підлітків на Кроці 3 є два пріоритетні варіанти лікування:
- комбінація низьких доз IКC-БАТД для підтримувального лікування та БАКД за потреби як засіб для полегшення симптомів;
- низькі дози IКC-формотеролу для підтримувального та полегшувального лікування.
У пацієнтів, які отримують підтримувальне лікування ІКС і БАКД за потреби, додавання БАТД у комбінованому інгаляторі забезпечує додаткове поліпшення симптомів і функції легень зі зниженням ризику загострень порівняно з тією самою дозою ІКС (РД А) [214, 215], але лише незначне зменшення використання допоміжного засобу для полегшення симптомів [216, 217]. На сьогодні схвалені комбіновані інгалятори з ІКС-БАТД для підтримувальної терапії БА на Кроці 3, що містить низькі дози флутиказону пропіонату–формотеролу, флутиказону фуроату–вілантеролу, флутиказону пропіонату–сальметеролу, беклометазону–формотеролу, будесоніду–формотеролу і мометазону–формотеролу. Ефективність флутиказону фуроату–вілантеролу, якщо порівняти зі стандартним лікуванням, щодо контролю симптомів БА була продемонстрована в масштабному дослідженні в реальних умовах, проте щодо ризику загострень різниці виявлено не було [69, 218].
ІКС-формотерол для підтримувальної та полегшувальної терапії може призначатись у вигляді низьких доз беклометазону–формотеролу або будесоніду–формотеролу. У дорослих і підлітків з ≥1 загостренням за минулий рік призначення ІКС-формотеролу для підтримувальної та полегшувальної терапії значно зменшує частоту загострень і при відносно низьких дозах ІКС забезпечує такі самі рівні контролю БА, як і фіксовані дози ІКС-БАТД для підтримувального лікування або більші дози ІКС, в обох випадках у поєднанні з БАКД за потреби (РД А) [219-224].
Інші варіанти контролювальної терапії на Кроці 3 для дорослих і підлітків
Для дорослих пацієнтів з АР і сенсибілізацією до кліщів домашнього пилу (КДП) із субоптимально контрольованою БА, незважаючи на застосування від низьких до високих доз ІКС, розгляньте можливість проведення сублінгвальної алергенспецифічної імунотерапії (АСІТ) за умови, що ОФВ1 >70% від прогнозованого [225, 226].
Варіантом лікування для дорослих і підлітків є збільшення дози ІКС до середньої [130], але на груповому рівні це менш ефективно, ніж додавання БАТД (РД A) [227, 228]. Іншими менш ефективними варіантами є призначення низьких доз IКC + АЛР [229] (РД A) або низьких доз теофіліну з тривалим вивільненням (РД B) [230]. Див. Примітку вище про попередження FDA стосовно монтелукасту [205].
Крок 4. Пріоритетний засіб для контролю симптомів: низькі дозі ІКС-формотерол для контролювальної та полегшувальної терапії (дорослі та підлітки), АБО середні дози ІКС-БАТД для контролю симптомів і БАКД за потреби (дорослі, підлітки та діти)
Хоча на груповому рівні більшість терапевтичних переваг ІКС зазначають у разі використання низьких доз, індивідуальна відповідь на ІКС-терапію може варіювати, і деякі пацієнти з неконтрольованою БА в разі використання низьких доз ІКС-БАТД, незважаючи на хорошу прихильність до лікування та правильну техніку інгаляції, можуть мати користь від підвищення підтримувальної дози ІКС до середньої. Високі дози ІКС більше не рекомедовані на Кроці 4.
Рекомендовані варіанти контролювальної терапії на Кроці 4 для дорослих і підлітків
Вибір терапії на Кроці 4 залежить від варіанту лікування на Кроці 3. Перш ніж перейти на Крок вище, перевірте наявність таких поширених проблем, як неправильна техніка використання інгалятора, низька прихильність до терапії, впливи навколишнього середовища, і переконайтесь, що симптоми зумовлені БА.
Для дорослих і підлітків з ≥1 загостренням за минулий рік комбінація низьких доз ІКС-формотеролу для підтримувальної та додаткової терапії ефективніша щодо зменшення ризику загострень у порівнянні з такими самими дозами ІКС-формотеролу для підтримувальної терапії чи вищими дозами ІКС (РД А) [223]. Такий режим може призначатись у вигляді низьких доз будесоніду–формотеролу або беклометазону–формотеролу, як на Кроці 3; підтримувальну дозу за необхідності можна підвищити до середньої. Згідно з інструкцією до препарату, максимальна рекомендована добова доза формотеролу становить 48 мкг (для беклометазону–формотеролу) або 72 мкг (для будесоніду–формотеролу).
Як альтернатива в піцієнтів, що застосовують низькі дози ІКС-БАТД та БАКД за потреби і БА в яких лишається неконтрольованою, можна перейти до терапії середніми дозами ІКС-БАТД (РД В) [158]; комбінації ІКС-БАТД, як на Кроці 3.
Інші варіанти контролювальної терапії на Кроці 4 для дітей і підлітків
Тіотропій, антагоніст мускаринових рецепторів тривалої дії, у формі аерозольного інгалятора можна призначати для додаткової терапії пацієнтів ≥6 років, він помірно покращує функцію легень (РД А) [235, 236] і помірно зменшує частоту загострень [235-237]. Немає достатньої кількості доказів переваг комбінації ІКС-тіотропій у порівнянні з ІКС-БАТД [237].
У дорослих пацієнтів з АР і сенсибилізацією до КДП із субоптимально контрольованою БА, незважаючи на застосування від низьких до високих доз ІКС, розглянути доцільність проведення сублінгвальної АСІТ за умови, якщо ОФВ1 >70% від прогнозованого [225, 226].
У разі призначення середніх або високих доз будесоніду ефективність можна збільшити, застосовуючи препарат 4 рази на добу (РД В) [238, 239], проте проблемним моментом може бути прихильність до лікування. У разі використання інших ІКС прийнятним є застосування двічі на добу (РД D). У дорослих і підлітків іншими варіантами, які можуть бути додатково призначені до середніх або високих доз ІКС, але з меншою ефективністю, ніж БАТД, є АЛР (РД А) [240-244] або низькі дози теофіліну з повільним вивільненням (РД В) [208]. Див. Примітку вище про попередження FDA щодо монтелукасту [205].
Крок 5. Пріоритетний варіант: оцінка фенотипу та розгляд необхідності призначення додаткового лікування (дорослі, підлітки та діти)
Пацієнти будь-якого віку зі стійкими симптомами або загостреннями, незважаючи на правильну техніку використання інгалятора та належну прихильність до лікування на Кроці 4, і щодо яких розглядались інші варіанти контролювальної терапії, мають були направлені до фахівця, в якого є досвід в обстеженні та лікуванні тяжкої БА (РД D) [138].
У разі тяжкої форми БА, як при астмі легкого та середньотяжкого перебігу [245], учасники РДК можуть бути нерепрезентативними для пацієнтів, яких спостерігають у клінічній практиці. Наприклад, реєстрове дослідження показало, що понад 80% пацієнтів із тяжкою БА були б виключені з останніх досліджень, що оцінювали біологічну терапію [246].
Кишенькове керівництво GINA та алгоритм із діагностики та лікування тяжкої БА та БА, що важко лікується, у підлітків і дорослих наведені в розділі 3E. Варіантами лікування, які можуть бути розглянуті після оптимізації поточної терапії, можуть бути (завжди перевіряйте місцеві вимоги та критерії відповідності для платника):
- Комбінація високих доз IКC-БАТД: можна розглядати в дорослих і підлітків, але збільшення дози IКC, як правило, забезпечує незначну додаткову користь (РД A) [122, 230, 228]; крім того, є підвищений ризик розвитку побічних ефектів, зокрема пригнічення надниркових залоз [247]. Високі дози ІКС рекомендують лише на дослідній основі впродовж 3-6 міс, коли хорошого контролю БА не вдається досягти за допомогою середніх доз ІКС-БАТД і/або третього контролювального засобу (наприклад, АЛР або теофілін із пролонгованим вивільненням (РД B) [208, 243].
- Додавання тіотропію (антагоніст мускаринових рецепторів тривалої дії; АМТД) у пацієнтів віком ≥6 років, в яких БА погано контролюється IКC-БАТД. Додаткове призначення тіотропію (переважно в дозі 5 мкг один раз на добу за допомогою аерозольного інгалятора) помірно покращує функцію легень (РД А) і помірно подовжує час до тяжкого загострення, що потребуватиме ПКС (РД В) [236, 237]. Очікуються результати стосовно інших препаратів АМТД [236].
- Додавання азитроміцину (тричі на тиждень) у дорослих пацієнтів зі стійкими симптомами БА, незважаючи на середні/високі дози ІКС-БАТД, зменшувало частоту загострень у разі еозинофільної [248] та нееозинофільної БА [248, 249] (РД B) і покращувало якість життя, пов’язану з БА (РД В) [248, 249]. Діарея була більш поширеною [248]. Оскільки макроліди, такі як азитроміцин, можуть спричиняти ототоксичність і серцеву аритмію, хворих на БА з порушеннями слуху [248] або аномальним подовженням скорегованого інтервалу QT [248, 249] було виключено з досліджень. Перш ніж розглядати можливість додаткової терапії азитроміцином у дорослих пацієнтів із неконтрольованою або тяжкою БА, варто провести ЕКГ з визначенням тривалості інтервалу QTc, дослідження мокротиння на наявність атипових мікобактерій, а також враховувати ризик підвищення антимікробної резистентності на популяційному рівні. Рекомендована тривалість лікування становить щонайменше 6 міс, оскільки явної користі не спостерігали через 3 місяці. Немає чітких даних щодо того, як довго треба продовжувати лікування.
- Додаткова анти-IgE-терапія (омалізумаб): для пацієнтів віком ≥6 років із помірною або тяжкою алергічною БА, яка не контролюється на Кроці 4-5 (РД A) [250, 251].
- Додаткова анти-IL‑5/5R-терапія (підшкірно меполізумаб пацієнтам віком ≥6 років; внутрішньовенне введення реслізумабу пацієнтам віком ≥18 років) або анти-IL‑5R-терапія (підшкірно бенралізумаб пацієнтам віком ≥12 років) у разі тяжкої еозинофільної БА, яка не контролюється за допомогою лікування на Кроці 4-5 (РД A) [252-256]. Дані про ефективність меполізумабу в дітей віком 6-11 років обмежені одним дуже невеликим відкритим неконтрольованим дослідженням.
- Додаткова анти-IL‑4Rα-терапія (підшкірно дупілумаб) у пацієнтів віком ≥12 років із тяжкою БА типу 2 або в тих, хто потребує підтримувального лікування ПКС (РД A) [258-260].
- Лікування на основі аналізу мокротиння: для дорослих із постійними симптомами та/або загостреннями, незважаючи на високі дози IКC або IКC-БАТД, лікування може бути скореговане на основі еозинофілії (>3%) індукованого мокротиння. При тяжкій БА ця стратегія забезпечує зменшення загострень і/або зниження дози IКC (РД A) [161].
- Додаткове лікування за допомогою бронхіальної термопластики: може бути розглянуто для деяких дорослих пацієнтів із тяжкою БА (РД B) [138, 261]. Докази обмежені та у вибраних пацієнтів. Довгострокові ефекти в порівнянні з контрольними пацієнтами, у тому числі щодо функції легень, невідомі.
- Додавання низьких доз ПКС (≤7,5 мг/добу в перерахунку на преднізолон): може бути ефективним у деяких дорослих із тяжкою БА (РД D) [138], але часто асоціюється зі значними побічними ефектами (РД A) [262, 263]. Їх призначення необхідно розглядати лише в дорослих пацієнтів із поганим контролем симптомів і/або частими загостреннями, незважаючи на правильну техніку використання інгалятора та хорошу прихильність до лікування на Кроці 4, а також після виключення інших провокувальних факторів та додаткових методів лікування, у тому числі біологічної терапії, де це доступно. Пацієнтів потрібно інформувати про можливі побічні ефекти [263]. Необхідно оцінювати стан хворих і контролювати стосовно ризику КС-індукованого остеопорозу, а пацієнтам, яким лікування призначається на період ≥3 міс, треба надати відповідні консультації щодо способу життя та призначити засоби для профілактики остеопорозу (де це доречно) [264].
Інші види терапії
Алергенспецифічна імунотерапія
АСІТ може бути варіантом лікування в разі помітної ролі алергії, у тому числі коли БА супроводжується алергічним ринокон’юнктивітом [282, 283]. Сьогодні застосовують два підходи: підшкірна та сублінгвальна АСІТ. Раніше в небагатьох дослідженнях за участю пацієнтів із БА порівнювали АСІТ з фармакотерапією або використовували стандартизовані результати, такі як загострення, і більшість досліджень проводили за участю хворих на легку БА. Алергенами, які найчастіше використовували в дослідженнях АСІТ, були КДП і пилок трав. Недостатньо доказів безпеки та ефективності АСІТ у пацієнтів, сенсибілізованих до цвілі [284].
Підшкірна АСІТ полягає в ідентифікації та використанні клінічно значущих алергенів, введенні їх екстрактів з поступовим збільшенням дози з метою формування десенсибілізації та/або толерантності. Лікарі європейських країн зазвичай, віддають перевагу АСІТ одним алергеном, тоді як у Північної Америці часто призначають для лікування кілька алергенів [285]. В осіб із БА та алергічною сенсибілізацією АСIT асоціюється зі зменшенням бальної оцінки симптомів і потреби в ліках, а також з алергенспецифічною та неспецифічною гіперреактивністю дихальних шляхів [285].
Щодо підшкірної АСІТ, аналіз об’єднаних даних відносно безпеки, отриманих із клінічних випробувань і постмаркетингового нагляду за алергічними респіраторними захворюваннями, зумовленими КДП, свідчить про те, що частота побічних реакцій на лікування становить приблизно 0,5% [286]. Результати останніх досліджень показують, що серйозні побічні ефекти АСІТ є рідкісними, але можуть проявлятись у вигляді анафілактичних реакцій, що загрожують життю.
Сублінгвальна АСІТ (СЛІТ)
У систематичному огляді було виявлено помірний вплив СЛІТ на БА в дорослих і дітей [283, 287, 288], але є сумніви щодо дизайну багатьох досліджень [289], в яких кілька досліджень, які порівнювали СЛІТ з фармакотерапією БА [290]. Нещодавнє дослідження СЛІТ з використанням алергенів КДП у пацієнтів із БА та АР, спричиненим КДП, продемонструвало помірне зменшення дози ІКС при високих дозах алергену в СЛІТ [226]. В іншому дослідженні в пацієнтів із БА та АР, спричиненим КДП, АСІТ, додана до низьких або середніх доз ІКС, подовжувала час до загострення зі зменшенням ІКС при субоптимально контрольованій БА.
Побічні ефекти [291-293] СЛІТ з інгаляційними алергенами переважно обмежуються оральними та шлунково-кишковими симптомами.
Щеплення
Грип зумовлює значну захворюваність і смертність у загальній популяції та стає причиною загострень БА. Ризик грипозної інфекції можна зменшити завдяки щорічній вакцинації. Систематичний огляд плацебо-контрольованих РКД із вакцинації проти грипу не виявив зменшення частоти загострення БА [294], але такі дослідження не проводили з 2001 року. Однак нещодавні систематичний огляд і метааналіз, що вивчали обсерваційні дослідження з широким спектром дизайну, припустили, що вакцинація проти грипу зменшує ризик загострення БА, хоча для більшості досліджень не можна виключати упередженості [295]. Немає доказів збільшення частоти загострень БА після щеплення від грипу порівняно з плацебо [295]. Є обмежена кількість даних щодо безпеки та ефективності живої атенуйованої інтраназальної вакцини для дітей; більшість наявних доказів обмежується дітьми віком ≥3 роки.
Пацієнти з БА, передусім діти та особи похилого віку, мають вищий ризик розвитку пневмококової інфекції [296], але недостатньо доказів, щоб рекомендувати рутинну пневмококову вакцинацію пацієнтам із БА [297].
Бронхіальна термопластика
Бронхіальна термопластика в деяких країнах є потенційним варіантом лікування на Кроці 5 у дорослих пацієнтів, в яких БА залишається неконтрольованою, незважаючи на оптимізовані терапевтичні схеми та направлення до спеціалізованого центру з астми (РД B).
Під час бронхіальної термопластики на дихальні шляхи в ході 3 бронхоскопій здійснюють локальний радіоімпульсний вплив [115]. Лікування значною мірою пояснюється ефектом плацебо [115]. У пацієнтів, які приймають високі дози IКC-БАТД, бронхіальна термопластика була пов’язана зі збільшенням частоти загострень БА впродовж 3 міс лікування з наступним її зменшенням, але не було виявлено ніякого сприятливого впливу на функцію легень або симптоми БА порівняно з контрольними пацієнтами [115]. Тривале спостереження за деякими пацієнтами, які отримували лікування, виявило стійке зменшення частоти загострень порівняно з попереднім лікуванням [298]. Необхідне більш тривале спостереження за більшими когортами, яке порівнювало б ефективність і безпеку, зокрема функцію легень, у досліджуваних і контрольних пацієнтів.
Вітамін D
Кілька крос-секційних досліджень показали, що низький рівень вітаміну D у сироватці крові пов’язаний з порушенням функції легень, більшою частотою загострень і зниженою відповіддю на КС-терапію [299]. Добавки з вітаміном D можуть зменшувати частоту загострень БА, що потребуватимуть застосування системних КС, у хворих на БА з вихідним рівнем 25(OH)D <25 нмоль/л [300]. У ході метааналізу в деяких дослідженнях було виявлено користь у разі прогресуючої БА, але досі немає жодних переконливих доказів того, що добавки з вітаміном D поліпшують контроль БА або зменшують частоту загострень [301-303]. Потрібні додаткові дослідження.
Пацієнти з ознаками БА та ХОЗЛ
Також називається «астми-ХОЗЛ-перехрест-синдром» або «астма + ХОЗЛ» (табл.).
- НЕ окреме захворювання, а описова назва для пацієнтів, з якими часто стикаються лікарі у своїй клінічній практиці.
Астма та ХОЗЛ є гетерогенними станами, що накладаються один на одний.
- Діагнози астми та ХОЗЛ не є взаємовиключними.
- Кожне захворювання має кілька фенотипів, імовірно, з різними механізмами розвитку.
- Зростає інтерес до можливостей високоточної терапії.
Однак поняття «астма» та «ХОЗЛ» досі є клінічно важливими, оскільки дані підтверджують відмінності в рекомендаціях із лікування, заснованих на безпеці.
- Астма: ніколи не лікуйте лише бронходилататорами (ризик смерті, госпіталізації, тяжких загострень).
- ХОЗЛ: розпочати лікування з БАТД і/або антагоністів мускаринових рецепторів тривалої дії (АМТД) без ІКС.
- Пацієнти з діагнозом БА та ХОЗЛ частіше помирають або госпіталізуються, якщо отримують лікування БАТД у порівнянні з ІКС-БАТД (Gershon et al., JAMA, 2014; Kendzerska et al., Annals ATS, 2019).
- Високі дози ІКС можуть знадобитись і в разі тяжкої БА, але їх не варто застосовувати при ХОЗЛ (ризик пневмонії).
Розділ 5 для клінічної користі було перероблено з акцентом на клінічній діагностиці та безпечному початковому лікуванні.
Друкується в скороченні.
Реферативний огляд підготувала Євгенія Канівець
Повну версію дивіться на сайті www.ginasthma.org.
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 4 (53), 2020 р.