17 листопада, 2016
Синдром нарушения толерантности к гистамину: этиология, патогенез, клиника, современные подходы к диагностике и лечению
В последние годы в клинической практике все чаще встречаются пациенты с проявлениями двух и более гистамин-индуцированных симптомов. В первую очередь такие пациенты могут обращаться к аллергологу или дерматологу с жалобами на периодические высыпания, которые сопровождаются зудом, особенно после приема пищи или ряда медикаментов. При детализации анамнеза выясняется, что у пациентов также часто бывают боли в животе, метеоризм, диарея, головные боли и др. Обычно консультация заканчивается назначением диеты, антигистаминных препаратов, пробиотиков, спазмолитиков, локально – эмольентов и т. д. На фоне данных рекомендаций состояние больного, конечно, улучшается, но после отмены терапии пациент снова обращается к врачу, а часто просто учится жить с данной проблемой.
Как улучшить качество жизни пациента? Что должен знать клиницист о синдроме низкой толерантности к гистамину?
В 1910 г. Henry Daleand и соавт. с Wellcome Laboratories впервые описали биогенный амин – гистамин (2-[4-имидазолил] этиламин), выделенный ими с Claviceps purpurea [7]. Впоследствии, в 1927 г. Best и соавт. доказали, что гистамин – это естественный компонент человеческого организма, который синтезируется из аминокислоты гистидина путем декарбоксилирования при участии фермента L-гистидиндекарбоксилазы, коферментом которой является пиридоксальфосфат (витамин В6) [24].
Гистамин производится во многих клетках организма (мастоциты, базофилы, желудочные энтерохроматофильные клетки, гистаминергические нейроны и др.), сохраняется внутриклеточно в везикулах и выделяется при стимуляции клеток, инициируя значительное количество физиологических и патологических процессов. В частности, гистамин способствует спазму гладкой мускулатуры бронхов и кишечника, расширению сосудов и увеличению их проницаемости, усилению желудочной секреции, развитию тахикардии и аритмии, влияет на артериальное давление, нейропередачу, иммунокоррекцию и т. д. [15]. Гистамин также может синтезироваться в клетках эпидермиса, слизистой оболочке желудка и в нейронах. В этих клетках скорость его обмена довольно высокая, поэтому он почти не депонируется и выделяетсяпостоянно [12]. Многообразие эффектов гистамина связано с его способностью влиять на мембранные рецепторы различных клеток, которых в настоящее время описано четыре типа: H1-, Н2-, Н3- и Н4-гистаминорецепторы [19].
Знания о клинических эффектах гистамина необходимы многим практикующим врачам. К примеру, аллергологам, дерматологам, клиническим иммунологам важно знать, что дегрануляция тучных клеток с высвобождением гистамина может быть результатом связывания специфического антигена (в частности, аллергена) с FcωRI-рецептором на их поверхности. Активация тучных клеток также может происходить за счет неиммунных механизмов, а именно: стимулируют дегрануляцию нейропептиды (субстанция Р), компоненты системы комплемента (C3a и C5a), ряд цитокинов (интерлейкин-1 (IL-1), IL-3, IL-8, гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF), фактор активации тромбоцитов, липопротеиды, гиперосмолярность, состояние гипоксии, некоторые физические и химические факторы (экстремальная температура, травмы, вибрация, употребление алкоголя, ряд продуктов питания, медикаментов и т. д.) [16].
Катаболизм гистамина происходит двумя путями:
• путем окислительного дезаминирования с образованием имидазолацетальдегида с участием фермента диаминооксидазы (DAO, ранее «гистаминаза») – внеклеточно;
• путем метилирования имидазольного ядра к N4-метилгистамину при участии гистамин-N-метил трансферазы (HNMT) – внутриклеточно.
Фермент DAO накапливается в мембраноассоциированных везикулярных структурах эпителиальных клеток и высвобождается из них при стимуляции. DAO отвечает за уровень внеклеточного гистамина, который может повышаться после употребления богатой гистамином пищи или активации тучных клеток [21]. С другой стороны, фермент HNMT является цитозольным протеином, действие которого проявляется только во внутриклеточном пространстве [23]. Поэтому данные ферменты не конкурируют между собой за субстрат.
Синдром нарушения толерантности к гистамину (СНТГ) – это патологический процесс, который возникает вследствие дисбаланса между потреблением гистамина и способностью организма элиминировать его. Избыточное накопление гистамина приводит к развитию симптоматики, возникающей за счет связывания его с упомянутыми выше гистаминорецепторами. Определено, что указанный синдром имеют более 1% людей (в основном женщины среднего возраста). Однако существует мнение, что данный показатель значительно занижен из-за гиподиагностики СНТГ [14].
У здоровых людей ферментативный барьер клеток эпителия тонкой кишки обеспечивает DAO, противодействуя чрезмерному всасыванию в кровь гистамина внешнего происхождения. Нарушение толерантности к гистамину (НТГ), то есть увеличение уровня гистамина в плазме, может возникать в условиях недостаточности фермента или его ингибирования. В таких случаях развитие симптомов возможно даже при поступлении небольшого количества гистамина (например, с продуктами питания), который обычно хорошо переносится здоровыми людьми [22].
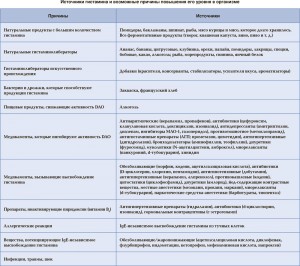
Причины снижения активности DAO могут быть разными: генетическая предрасположенность, заболевания желудочно-кишечного тракта (ЖКТ; воспалительные заболевания кишечника, болезнь Крона, неспецифический язвенный колит, инфекции, паразитарные инвазии, мальабсорбция, дисбактериоз), хронические заболевания почек, вирусные гепатиты, цирроз печени, хроническая крапивница и др. [4]. Возможно угнетение активности DAO другими биогенными аминами, алкоголем или медикаментами (см. таблицу) [2]. Также активность DAO может уменьшаться при недостаточности кофакторов: витамина В6, С, микроэлементов Cu и Zn [8]. Некоторые вещества-гистаминолибераторы способны вызвать высвобождение гистамина из эндогенных источников организма [10]. Гормоны, которые выделяются во время стресса, способны как непосредственно активизировать мастоциты и высвобождать гистамин, так и негативно влиять на эпителий тонкой кишки, инициируя уменьшение синтеза DAO [3].
Что касается роли генетических факторов, то сегодня определены разные генетические варианты фермента DAO. Ген, кодирующий DАО, находится во фрагменте 7-й хромосомы (7q34-Q36) генома человека, состоит из 5 экзонов и 4 интронов. Выявлена значительная взаимосвязь между активностью DAO и 7 единичными нуклеотидными полиморфизмами (SNP). Считается, что только один из этих семи SNP, расположенный в третьем экзоне, непосредственно связан с низкой активностью DAO [20].
Установлено, что при концентрации гистамина в плазме от 0,3 до 1 нг/мл не возникает никаких клинических признаков [17]. СНТГ характеризуется дозозависимым эффектом [5]. Даже у здоровых людей может развиться сильная головная боль или приливы из-за употребления большого количества продуктов, содержащих гистамин [9]. Типичные симптомы НТГ включают гастроинтестинальные расстройства, чихание, ринорею, заложенность носа, головную боль, дисменорею, гипотонию, аритмию, крапивницу, приливы и пр. В большинстве случаев на вероятность СНТГ указывает наличие двух и более типичных симптомов [6].
Нервная система: неврологические симптомы НТГ проявляются головными болями. Было обнаружено, что у пациентов с диагностированной мигренью наблюдается повышенный уровень гистамина не только во время приступов, но и в асимптомный период. У многих пациентов этой группы причиной НТГ была сниженная активность DAO. Продукты, содержащие гистамин, были триггерами головной боли.
В настоящее время известно, что гистамин может вызывать, поддерживать и усиливать головную боль, хотя механизмы этого установлены пока не полностью. Считают, что при некоторых патологических состояниях (мигрень, кластерные головные боли, рассеянный склероз) количество тучных клеток в головном мозге увеличивается. Хотя гистамин не проникает через гематоэнцефалический барьер (ГЭБ), он может влиять на активность гипоталамуса. Исследование Levy et al. подтвердили, что дегрануляция тучных клеток в твердой мозговой оболочке активирует болевой путь, лежащий в основе мигрени [3, 25]. Однако большинство АГП неэффективны при остром приступе мигрени.
С другой стороны, гистамин играет важную роль нейромодулятора путем воздействия на Н3-рецепторы, расположенные в центральной нервной системе (ЦНС) на уровне базальных ганглиев, гипокампа и коры головного мозга. Определено, что гистамин влияет на процессы корковой возбудимости (сон–бодрствование), возникновение мигрени, головокружения, тошноты или рвоты центрального происхождения, изменения температуры тела, памяти, восприятия информации и регуляции аппетита. Было доказано, что независимо от времени суток активность приступов мигрени уменьшалась, что коррелировало с уменьшением уровня центрального гистамина. В свою очередь, избыток гистамина приводил к перевозбуждению некоторых участков ЦНС, что вызывало различные нарушения сна, в том числе затрудненное засыпание [26]. Известно также, что снотворное действие некоторых АГП I поколения, проникающих через ГЭБ (например, димедрола), связано с блокирующим влиянием на гистаминовые рецепторы, расположенные в ЦНС [11, 27].
ЖКТ: важными симптомами НТГ являются диффузная боль в животе, колики, метеоризм, диарея или запоры, часто возникающее уже через 30 мин после приема пищи, содержащей высокие дозы или стимулирующей выброс гистамина. Рост концентрации гистамина и снижение активности DAO было обнаружено также при других заболеваниях ЖКТ (болезнь Крона, язвенный колит, аллергическая энтеропатия, колоректальный рак). У пациентов с пищевой аллергией слизистая оболочка кишечника кроме низкой активности DAO характеризуется еще и низкой активностью HNMT. Ферменты DAO и HNMT при таких условиях не могут компенсировать друг друга, поэтому общая способность к катаболизму гистамина значительно снижается [28]. Уровень DAO уменьшается также у пациентов с нервной анорексией вследствие недоедания, что влечет за собой атрофические повреждения слизистой оболочки кишечника. С другой стороны, симптоматика НТГ может быть схожа с таковой при нервной анорексии (снижение массы тела, диарея, боль в животе и др.). Точный диагноз и диета с исключением продуктов, содержащих гистамин, у таких больных могут привести к увеличению массы тела и уменьшению выраженности всех симптомов.
Следует отметить, что соблюдение строгой безгистаминовой диеты является непростой задачей и фактически лишает пациентов нормального сбалансированного питания. Особенно если идет речь о пациентах детского возраста, людях пожилого возраста или больных с сопутствующей патологией, где рациональное питание нужно рассматривать как главный источник поступления в организм большинства необходимых макро- и микронутриентов, витаминов и прочих веществ [36].
Важно также отметить, что уровень гистамина в пище можно определить только специальными лабораторными методами, он зависит от сроков и условий хранения продуктов. Заморозка или горячая обработка не уменьшает содержание гистамина в пище. Чем дольше хранится пища, тем больше в ней образуется гистамина. Одни и те же продукты могут содержать разное количество гистамина и, соответственно, вызывать (или нет) разную степень проявления симптомов, что усложняет диагностику СНТГ [30].
Дыхательные пути: СНТГ может проявляться у пациентов с атопическими аллергическими заболеваниями и без таковых. Во время или после употребления алкоголя либо пищевых продуктов, богатых гистамином, у пациентов с НТГ могут возникать такие симптомы, как ринорея, заложенность носа, кашель, одышка, бронхоспазм, приступы бронхиальной астмы [35]. Именно такие случаи представляют большой дифференциальный интерес для грамотной и своевременной верификации диагноза. Нужно также помнить, что течение сезонной, круглогодичной аллергии может быть более тяжелым при сопутствующем СНТГ. Что касается бронхиальной астмы, то имеются данные, что у пациентов с данной патологией обнаружена сниженная активность HNMT, которая является основным ферментом катаболизма гистамина в эпителии бронхов [41].
Кожа: чаще всего СНТГ на коже проявляется в виде крапивницы различной локализации и степени тяжести, что связано с естественным уровнем DAO на фоне поступления пищи, богатой гистамином, или сниженной концентрацией фермента при употреблении диетической пищи или медикаментов, усиливающих метаболизм гистамина. Наличие СНТГ – одна из причин псевдоаллергической пищевой реакции. На основании двойного слепого плацебо-контролируемого исследования с помощью провокационных тестов с пищевыми добавками, проведенного Di Lorenzo и соавт., было показано, что в 3% случаев у пациентов с хронической идиопатической крапивницей причиной патологии был СНТГ [37].
Снижение активности DAO было установлено у пациентов с атопическим дерматитом. В большинстве описанных в литературе клинических случаев такое сочетание сопровождалось усилением тяжести течения дерматита, особенно в детском возрасте. При соблюдении диеты с ограничением гистамина или приеме препаратов заместительной терапии наблюдалось облегчение симптомов атопического дерматита [45]. Заметим также, что во всех этих случаях диагноз был верифицирован только спустя 2–3 года на фоне неэффективной терапии. Наличие СНТГ не позволяет также добиться желаемого эффекта от аллерген-специфической иммунотерапии (АСИТ) у пациентов с установленным аллергеном, например, при аллергии на пыльцу весенних деревьев или к клещам домашней пыли. Таким пациентам были рекомендованы препараты заместительной терапии, что со временем улучшило клинические эффекты АСИТ [18, 31].
Сердечно-сосудистая система: избыток гистамина влияет на сердечно-сосудистую систему по-разному, что связано с гиперактивацией Н1- и Н2-рецепторов, расположенных в сердце и сосудах. Это приводит к развитию множества разнообразных клинических симптомов, которые вуалируют стандартное представление о данном заболевании. В частности, через взаимодействие с Н1-рецепторами сосудов гистамин опосредует расширение их оксидом азота и простагландинами (через эндотелиальные клетки); увеличивает проницаемость посткапиллярных венул, в результате чего формируется отек; влияет на сокращение сосудов сердца. Через взаимодействие с Н2-рецепторами вызывает расширение сосудов, опосредованное цАМФ (гладкомышечные клетки сосудов) [40]. Кроме того, гистамин способствует снижению атриовентрикулярной проводимости через взаимодействие с Н1-рецепторами в сердечной ткани, а также увеличивает хронотропию и инотропию посредством влияния на Н2-рецепторы сердца [53].
Репродуктивная система: женщины с НТГ часто страдают от дисменореи в сочетании с циклической головной болью. Данные симптомы объясняются взаимодействием гистамина и женских половых гормонов, в частности способностью гистамина поддерживать сокращение матки. Это связывают с тем, что гистамин, в зависимости от дозы, стимулирует синтез эстрадиола и незначительно – прогестерона [39]. Эстрадиол, в свою очередь, обладает способностью ингибировать образование прогестерона F2α, который отвечает за болезненные сокращения матки при дисменорее. Интенсивность симптомов НТГ может варьировать в зависимости от фазы менструального цикла, в частности при лютеиновой фазе уменьшаются проявления, что обусловлено высокой активностью DAO [44].
Баланс между гистамином и DAO необходим для неосложненного течения беременности. Благодаря способности стимулировать рост и пролиферацию клеток гистамин играет важную роль во взаимодействии между маткой и эмбрионом, участвуя в созревании плаценты. В свою очередь, плацента продуцирует большое количество фермента DAO, который играет роль своеобразного барьера, препятствующего попаданию в кровоток эмбриона избытка гистамина от матери. Таким образом, концентрация DAO у беременных женщин почти в 500 раз выше [50]. Благодаря высокой плацентарной продукции DAO у беременных женщин с НТГ наблюдается уменьшение клинической симптоматики [45].
Таким образом, указанные клинические симптомы часто требуют дифференцированного подхода к диагностике патологических нарушений со стороны различных органов и систем и, соответственно, осведомленности клиницистов в отношении данного синдрома.
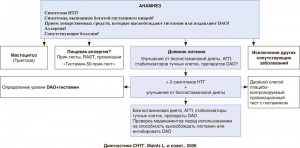
Алгоритм диагностики СНТГ, предложенный Maintz L. и соавт. (2006), представлен на рисунке. До недавнего времени использовали несколько различных методов определения DАО, однако некоторые из них были признаны недостаточно информативными (метод деградации утресцина, меченного радиоактивной меткой), с определенными ограничениями (исследование биоптата участка кишечника) или дорогостоящими [11].
В последнее время широкое применение получил кожный прик-тест с 1% раствором гистамина, описанный в литературе как Histamin 50-Skin-Prick Test. Суть теста заключается в определении размера папулы через 50 мин после скарификации. Размер папулы более 5 мм указывает на пониженную активность DАО. Данный тест является простым в исполнении и абсолютно безопасным [13].
Удобство и безопасность использования Histamin 50-Skin-Prick Test, а также необходимость диагностики СНТГ продемонстрированы на примере клинического случая.
Пациент М., 28 лет, обратился с жалобами на заложенность носа, ринорею и слезотечение, чихание, зуд, которые отмечал в течение последних 4 лет четко в период с марта до начала июня.
По данным анамнеза стало известно, что у больного периодически появлялся дискомфорт в ротовой полости (ощущение отека и онемение языка, губ, зуд) после употребления в пищу косточковых. Была проведена этапная диагностика в соответствии с консенсусом по молекулярной аллергодиагностике [1]. По результатам аллергодиагностики определено: кожные прик-тесты: гистамин (++), тест-контроль (–), береза (> 5 мм), ольха (> 5 мм), лещина (++++), граб (+++), яблоко (–), персик (++++). Аллергокомпонентная диагностика: rBet v 1 (PR-10) – 31,07 kU/l, rBet v 2–4 – 0,03 kU/l, rPru p 1 (PR-10) – 12,04 kU/l, rPru p 4 – 0,03 kU/l, rPru p 3 (nsLTP) – 0,02 kU/l.
Диагноз: «Аллергический ринит, интермиттирующее течение, сенсибилизация к пыльце весенних деревьев. Перекрестная пищевая аллергия к фруктам семейства Розоцветных».
Пациенту рекомендовано проведение АСИТ смесью пыльцы деревьев. Исключить из употребления фрукты в сыром виде и употреблять их только после термической обработки.
Через год лечения (на этапе поддерживающей терапии) пациенту провели мониторинг уровня специфических аллергенов для оценки эффективности АСИТ. Получили результат ImmunoCAP (Phadia AB): rBet v 1 – 15,02 kU/l, rBet v 2–4 – 0,03 kU/l, что указывало на хорошую эффективность выбранного лечения. Однако пациента продолжала беспокоить заложенность носа, причем независимо от периода палинации и на фоне предложенной диеты.
Кроме того, периодически появлялись кожные высыпания, метеоризм. В связи с этим пациенту предложено проведение 50-минутной гистаминовой пробы, результат которой оказался положительным.
Таким образом, пациенту верифицирован диагноз: «Аллергический ринит, интермиттирующее течение, сенсибилизация к пыльце весенних деревьев. Перекрестная пищевая аллергия к фруктам семейства Розоцветных. Синдром нарушения толерантности к гистамину». Было рекомендовано продолжение АСИТ, соблюдение указанной выше диеты, ограничение продуктов-гистаминолибераторов или обогащенных гистамином. При необходимости приема других медикаментов следует проконсультироваться с врачом относительно возможного влияния данного средства на метаболизм гистамина. Заместительная терапия препаратами диаминоксидазы (HistDAO).
Подходы к лечению СНТГ
Увеличение уровня DAO в крови пациентов с СНТГ возможно при комплексном лечении препаратами, которые содержат данный фермент. При низком уровне DAO в крови эти препараты могут быть использованы в комплексном лечении на фоне антигистаминной диеты и в случае употребления медикаментов, которые увеличивают уровень гистамина в крови. В настоящее время в Украине зарегистрирован препарат HistDAO, представляющий собой пищевую добавку для разрушения внеклеточного гистамина и содержащий фермент DAO, который полностью идентичен человеческому и повышает уровень DAO в ЖКТ. HistDAO не имеет побочных реакций, поскольку не всасывается в кровь, его действие ограничено только в тонком кишечнике. Согласно рекомендациям, возможно применение у детей с 6 лет и взрослых с CНТГ; не содержит гистамин, лактозу, глютен [46].
Положительные результаты применения фермента DAO в качестве пищевой добавки были представлены на XXI Всемирном конгрессе по неврологии (WCN) профессором Joan Izquierdo из Каталонского медицинского университета (Испания, 2013) [52]. Проводили двойное слепое плацебо-контролируемое исследование использования пищевой добавки DAO у пациентов с мигренью. По данным исследования, у 87% пациентов (в большинстве случаев – женщин) с мигренями, диагностированными в соответствии с критериями Международного общества головной боли, выявлен СНТГ. На основании результатов лечения был сделан вывод, что использование пищевой добавки DAO показало значительное снижение продолжительности приступа мигрени и тенденцию к уменьшению количества приступов. Кроме того, лечение не вызывало каких-либо побочных эффектов.
Особенно важна заместительная терапия препаратами DAO для пациентов, которые в силу лечения сопутствующих заболеваний вынуждены регулярно принимать медикаментозные препараты, влияющие на метаболизм гистамина. Что касается педиатрической практики, то все чаще появляются описания клинических случаев пациентов с СНТГ и преобладанием гастроэнтерологических проблем, у которых эффективность лечения была достигнута на фоне заместительной терапии [48].
Таким образом:
• СНТГ является важным для практической медицины, поэтому требует более глубокой осведомленности врачей различных специальностей;
• понимание патогенеза СНТГ, изучение вопроса диагностики недостаточности DAO дает широкие возможности для выбора эффективных подходов в лечении пациентов;
• проба Histamin 50-Skin-Prick Test с 1% гистамином является альтернативной, безопасной и доступной для выполнения и эффективной для диагностики CНТГ;
• использование АГП – блокаторов Н1- и Н2- носит временный характер и не влияет на основную причину заболевания. Избыток гистамина влияет на Н3- и Н4-гистаминовые рецепторы, инициируя развитие разнообразной патологической симптоматики со стороны ЦНС;
• заместительная терапия пищевой добавкой, содержащей DAO (препарат HistDAO), может рассматриваться как основа в сочетании с безгистаминовой диетой в комплексной терапии пациентов с СНТГ, воздействуя при этом на причину возникновения заболевания, понижая общий уровень гистамина.
Список литературы находится в редакции
Статья опубликована в журнале "Клінічна імунологія. Алергологія. Інфектологія." № 7 (96) 2016