27 березня, 2021
Дисбіоз, мікробіота і пробіотики при синдромі подразненого кишечнику
 20 лютого 2021 р. відбувся III Міжнародний конгрес для лікарів, присвячений темі корисних мікроорганізмів, PRO/PREBIOTIC 2021. Захід щороку збирає декілька тисяч відвідувачів, найвідоміших міжнародних та українських доповідачів і отримує безліч позитивних відгуків. У рамках конгресу було розглянуто надзвичайно актуальні питання пробіотикотерапії та мікробіоценозу.
20 лютого 2021 р. відбувся III Міжнародний конгрес для лікарів, присвячений темі корисних мікроорганізмів, PRO/PREBIOTIC 2021. Захід щороку збирає декілька тисяч відвідувачів, найвідоміших міжнародних та українських доповідачів і отримує безліч позитивних відгуків. У рамках конгресу було розглянуто надзвичайно актуальні питання пробіотикотерапії та мікробіоценозу.
Одним зі спікерів конгресу із доповіддю «Дисбіоз, мікробіота і пробіотики при синдромі подразненого кишечнику» виступив старший консультант-гастроентеролог, координатор досліджень Іспанського товариства шлунково-кишкової ендоскопії Vicente Lorenzo-Zuniga.
– Вагоме значення у підтримці адекватної проникності кишечнику має кишковий бар’єр, представлений мікробіотою, слизовим шаром та епітеліальними клітинами. Зміна будь-якого компоненту може призвести до порушення проникності стінки кишечнику.
Кишковий бар’єр можна умовно поділити на 2 складові:
- фізичний бар’єр, який запобігає втраті рідини, електролітів та проникненню антигенів і мікроорганізмів;
- функціональний бар’єр, що забезпечує обмін молекул між організмом та середовищем, а також всмоктування поживних речовин, що надходять із їжею.
Мікробіота кишечнику (МК) – це комплексна динамічна екосистема, представлена тисячами різноманітних бактерій. Відомо, що склад МК змінюється з віком. Це може проявлятися зменшенням кількості Actinobacteria, аж до повного їх зникнення у людей похилого віку, та зростанням кількості Firmicutes, Proteobacteriа і Bacteroidetes. Ці зміни можуть бути пов’язані з відмінностями у харчовій поведінці та різноманітністю раціону людей різних вікових груп, що підтверджують слова Гіпократа: «Ми є тим, що ми їмо». Збалансоване харчування є запорукою здорової МК та, навпаки, незбалансоване харчування є однією з причин розвитку дисбіозу.
Окрім неправильного харчування, до факторів, що зумовлюють розвиток дисбіозу, належать сидячий спосіб життя, вживання лікарських засобів, дефіцит сну та фізіологічний і психологічний стрес. Сукупність цих чинників у сучасному світі призвела до того, що сьогодні ми спостерігаємо тенденцію до зменшення бактеріального різноманіття кишечнику, що, відповідно, має свої наслідки.
? Яка роль МК у пацієнтів із синдромом подразненого кишечнику (СПК)?
СПК є функціональним поліетіологічним захворюванням, в основі якого лежать порушення моторики шлунково-кишкового тракту (ШКТ), МК, вісцеральна гіперчутливість, системне запалення низької інтенсивності та зміни з боку центральної нервової системи, зумовлені існуванням двонаправленої вісі «кишечник – головний мозок» (рис. 1). Нещодавні дослідження продемонстрували тісний взаємозв’язок між кишечником та головним мозком, який модулюється саме МК. Отож, за допомогою модифікації МК можна впливати на якість життя пацієнтів із СПК.
 Рис. 1. Вісь «кишечник – головний мозок»
Рис. 1. Вісь «кишечник – головний мозок»
Сучасні дослідження, проведені з використанням нових методик кількісного визначення МК, виявили відмінності МК пацієнтів із СПК порівняно зі здоровими особами. Зокрема, було продемонстровано зростання кількості Bacteroidetes, Firmicutes, Enterobacteriaceae, Enterobacter та Ruminococcus, у той час як кількість Bifidobacterium була зниженою (M. Rajilic-Stojanovic et al., 2015). Окрім зміни кількісних показників, описана також знижена активність Lactobacilli та Bifidobacteria в осіб із СПК (M. Bellin et al., 2014) і негативна кореляція між типом МК та вираженістю симптомів СПК (J. Tap et al., 2017). Існують також і відмінності між МК у чоловіків та жінок. При цьому саме жінки більш схильні до розвитку дисбіозу і СПК (A. Zhernakova et al., 2016).
Сьогодні активно вивчається можливість модуляції МК за допомогою пробіотиків, які можуть мати сприятливий вплив на перебіг СПК. Вибір найбільш ефективного пробіотика залежить від того, які специфічні типи бактерій характерні для того чи іншого стану. Так, наприклад, у пацієнтів із СПК здебільшого домінують Firmicutes, менше – Bacteroidetes, а у хворих із запальними захворюваннями кишечнику – навпаки (A.V. Vila, 2018). Окрім цього, при призначенні пробіотиків особливу увагу необхідно звертати на дотримання пацієнтами режиму лікування, адже доведено, що більш суворе дотримання режиму зумовлює вищу ефективність (C. Meydan et al., 2020).
? Який пробіотик є ефективним у лікуванні пацієнтів із СПК?
– Розробка пробіотика для застосування у пацієнтів із СПК базується на патофізіології захворювання та механізмі дії самого пробіотика. СПК – це багатофакторна патологія, в основі якої лежать кілька механізмів: підвищена проникність кишечнику, збільшення активності запальних клітин слизової оболонки, а особливо мастоцитів, розвиток дисбіозу та порушення газоутворення за участю бактерій (CH4 та H2S), наявність гастроентериту в анамнезі, молодий вік та інші соціально-психологічні фактори, стрес. Все це призводить до підвищення вісцеральної чутливості, тобто посиленої відповіді на нормальні подразники у кишечнику (B.E. Lacy et al., 2016; W.D. Chey et al., 2015; I.B. Jeffery et al., 2012; J.S. Labus et al., 2017). Для об’єктивізації даних щодо підвищеної вісцеральної чутливості може бути визначений індекс гіперчутливості (Visceral Sensitivity Index –VSI) або оцінений кишковий транзит екзогенних газових навантажень зі сцинтиграфічною візуалізацією. Було продемонстровано, що введення фіксованого об’єму газу в кишечник пацієнтів із СПК спричиняє більш болючі відчуття та більше здуття у порівнянні зі здоровими особами контрольної групи у тих же умовах (A.C. Hernando-Harder et al., 2010).
Застосування пробіотиків при СПК має доведені клінічні переваги, зокрема у пацієнтів, у яких домінуючим симптомом є діарея. Однак невирішеними залишаються питання механізму дії окремих штамів, відбору штамів та/або комбінації штамів, безпеки та стабільності, оптимального дозування і тривалості терапії, а також ефективності, продемонстрованої у клінічних дослідженнях (K. Hod, 2016). Отож пріоритетом залишається розробка мікробіологічної терапії в залежності від захворювання – таргетної терапії.
? Чому саме Пробіолог СПК?
– Пробіолог СПК («Лабораторія Майолі Спіндлер», Франція) – єдиний засіб на ринку, пробіотичний штам якого виробляє поліфосфати (ПФ), що підтверджено лабораторними методами. Відомо, що гранули ПФ підсилюють бар’єрну функцію кишкового епітелію та підтримують кишковий гомеостаз, що призводить до зменшення проникності кишечнику та, відповідно, нормалізації випорожнень. Вироблення ПФ-гранул залежить від гена ppk та є штамспецифічною особливістю. Такі штами, як L. plantarum, зокрема CECT7484, продукують велику кількість ПФ (C. Alcаntara et al., 2014; C. Alcаntara et al., 2018; S. Segawa et al., 2011). Протизапальний ефект пробіотиків можна оцінити шляхом визначення рівня утворення коротколанцюгових жирних кислот (КЖК), таких як ацетат, бутират і пропіонат. КЖК сприяють абсорбції натрію і води, що допомагає зменшити частоту дефекації. Ацетат має виражений протизапальний ефект та стимулює утворення слизу (K. Ishiguro et al., 2014; L. Wrzosek et al., 2013). Пробіолог СПК сприяє продукції великої кількісті КЖК, в основному ацетату (J.E. Mazo et al., 2016). Окрім цього, протизапальний ефект також можна оцінити, вимірюючи рівень утворення ацетилхоліну (АХ), який є важливим регулятором запалення слизової оболонки (для макрофагів та тучних клітин) через нікотинові ацетилхолінові рецептори nAChR-a7F (F. Guzmаn-Mejіa et al., 2018). У цьому напрямку найкращі результати продемонстрували штами Pediococcus acidilactici CECT7483, Lactobacillus plantarum CECT7484 і CECT7485, які й увійшли до складу Пробіолог СПК. Пробіолог СПК сприяє утворенню більшої кількості ацетилхоліну, ніж Bifidobacterium infantis 35624 (D.A. Drossman et al., 2016).
Ще однією проблемою, з якою стикаються пацієнти із СПК, є метеоризм, зумовлений надмірним виробленням газу бактеріями. Було продемонстровано, що вироблення МК CH4 асоціюється із запором, а H2S – із діареєю та підвищеною чутливістю. Тому при виборі пробіотика слід обирати штами з потужною окислювальною активністю, що допомагає зменшити кількість CH4 та H2S (M. Pimentel et al., 2012; M. Pimentel et al., 2018).
Як зазначено вище, СПК асоціюється з вісцеральною гіперчутливістю. При цьому у деяких пацієнтів із СПК підвищені рівні Enterobacteriaceae та Pseudomonas, які можуть збільшувати кишкову чутливість внаслідок виділення ендотоксину або H2S, що активує Toll-подібні рецептори TLR4 на мембранах тучних клітин та макрофагів, і нейрональні Cav3.2-канали відповідно. Кожен штам, що входить у Пробіолог СПК, має унікальний профіль протимікробної дії на ці бактерії (I.B. Jeffery et al., 2012; A.H. Sachdev et al., 2013).
Отож, штами, що входять до складу засобу Пробіолог СПК, є ефективними при вісцеральній гіперчутливості, зміні моторики ШКТ, збільшенні кишкової проникності та порушенні імунної функції.
? Чи здатен Пробіолог СПК покращити якість життя пацієнтів із СПК?
– Беззаперечно, важливим аспектом у лікуванні пацієнтів із СПК є не лише нормалізація вісцеральної чутливості, що є основою цієї проблеми, але й покращення якості життя пацієнтів. З метою оцінки ефективності застосування засобу Пробіолог СПК для вирішення цих проблем було проведене подвійне сліпе плацебо-контрольоване рандомізоване дослідження. У ньому брали участь 84 пацієнта зі встановленим діагнозом СПК із діареєю та СПК переміжного типу (за Римськими критеріями ІІІ). Пробіолог СПК пацієнти застосовували впродовж 6 тижнів, адже, як відомо, тривале застосування пробіотиків (>8 тижнів) може призвести до зниження їх ефективності. З метою підбору найкращої дози було оцінено 2 варіанти дозування засобу Пробіолог СПК: низька доза – 1 капсула (1-4×109 КУО), висока доза – 1 капсула (3-6×109 КУО) на добу після сніданку. Якість життя, пов’язану зі здоров’ям (HRQоL), оцінювали за допомогою опитувальника, розробленого саме для людей із СПК (IBS-QоL). Хорошою якість життя вважалася при покращенні на ≥15 балів, низькою – при покращенні на 10-15 балів, а покращення на <10 балів розцінювалося як відсутність відповіді. Для оцінки вісцеральної чутливості використовували шкалу індексу вісцеральної чутливості VSI. Окрім цього, оцінювали вісцеральні симптоми. Оцінку параметрів проводили через 3 та 6 тижнів прийому. У ході дослідження було отримано значне покращення якості життя (IBS-QоL) пацієнтів, що приймали Пробіолог СПК, порівняно з тими, хто приймав плацебо (р<0,05 для обох доз, із поправкою на множинність). При застосуванні засобу Пробіолог СПК спостерігалася висока частота позитивної відповіді на лікування порівняно із плацебо (р=0,009). Різниці між високими та низькими дозами у впливі на IBS-QoL не спостерігалося.
При оцінці VSI також було зафіксовано суттєве покращення вісцеральної чутливості (р<0,05 для обох доз, із поправкою на множинність). Варто зауважити, що хоча оцінка VSI через 3 тижні не показала переваги того чи іншого дозування, через 6 тижнів спостерігалося більш виражене покращення вісцеральної чутливості у тих пацієнтів, які отримували нижчі дози пробіотика (приріст склав 14±2 бали; р=0,015 у порівнянні з плацебо, у той час як для низьких доз 10±2 бали; р=0,033 у порівнянні з плацебо; рис. 2А). Спостерігалася значна кореляція покращення VSI та IBS-QoL (р<0,001; рис. 2Б; V. Lorenzo-Zuniga et al., 2014).
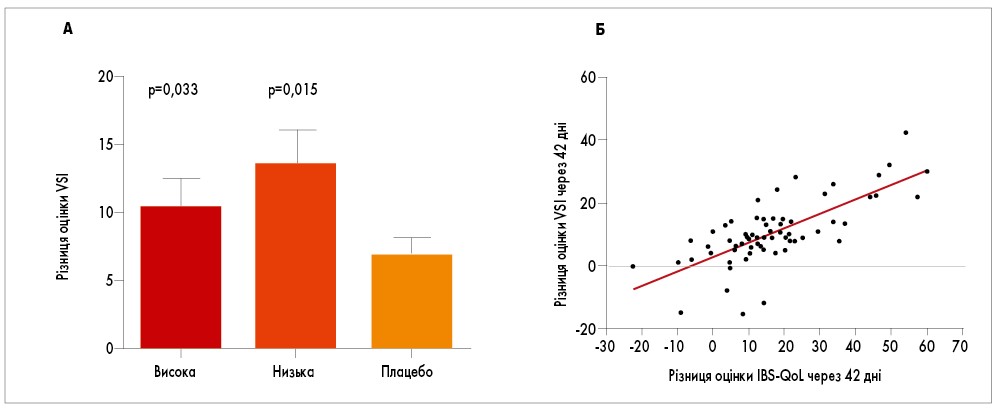 Рис. 2. Оцінка VSI при застосуванні різних доз засобу Пробіолог СПК у порівнянні з плацебо (А). Кореляція VSI та IBS-QoL (Б)
Рис. 2. Оцінка VSI при застосуванні різних доз засобу Пробіолог СПК у порівнянні з плацебо (А). Кореляція VSI та IBS-QoL (Б)
Потрібно пам’ятати, що дія пробіотиків розвивається поступово, тому для досягнення найкращого та швидкого ефекту рекомендується використовувати комбіноване лікування із включенням спазмолітиків (альверину цитрату) та симетикону (T. Wittmann et al., 2010).
Таким чином, Пробіолог СПК є засобом, розробленим саме для застосування у пацієнтів із СПК. Штами бактерій, що входять до складу засобу Пробіолог СПК, чинять протизапальний ефект, зменшують проникність кишкового бар’єра та протидіють розвитку дисбіозу. Пробіолог СПК є унікальним пробіотиком, який впливає на вісцеральну гіперчутливість та суттєво покращує якість життя пацієнтів із СПК.
Підготувала Ольга Нестеровська
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 1 (59) 2021 р.



