27 листопада, 2016
Стимулирующий фактор роста – ценный прогностический маркер при сердечно-сосудистых заболеваниях
Стимулирующий фактор роста (ST2) – это новый маркер, использующийся для прогнозирования и стратификации риска развития сердечной недостаточности (СН), опредления вероятности неблагоприятных исходов и смерти пациентов с подтвержденным диагнозом СН, возникновения сердечно-сосудистых заболеваний (ССЗ) в будущем, а также для мониторинга и подбора наиболее эффективной терапии больных СН.
ST2 экспрессируется в сердце в ответ на патологические изменения, вызванные хроническими заболеваниями и/или острыми повреждениями. Данный маркер отражает ремоделирование желудочков и фиброз сердца. ST2 (Grows STimulation expressed gene 2, стимулирующий фактор роста, экспрессирующийся геном 2, также известный как Т1, IL1RL1 или FIT1) – член семейства рецепторов интерлейкина-1 (IL-1), который был обнаружен в 1989 г. на хромосоме 2q12 (рис. 1).
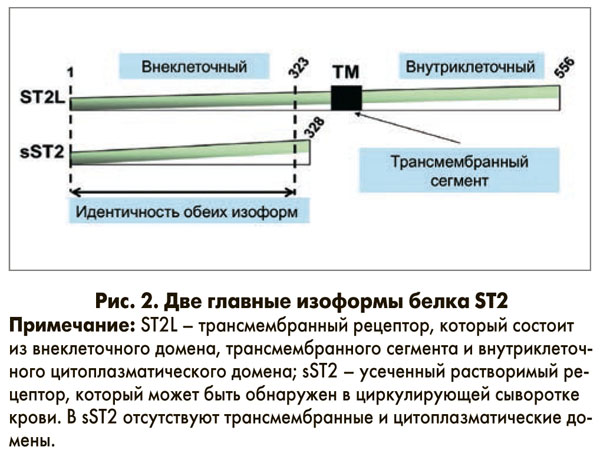
Связь между ST2 и биомеханической деформацией в сердце была обнаружена в 2002 г. Weinberg и соавт., которые установили, что в кардиомиоцитах среди 7 тыс. генов значительно экспрессированы были именно гены ST2. Ген ST2 кодирует белок, который относится к семейству генов иммуноглобулиновых рецепторов (особенно IL-1). ST2 имеет две изоформы: IL1RL1-β, или ST2L, – мембранный рецептор, который относится к семейству IL-1 рецепторов; IL1RL1-α, или sST2, – секреторная растворимая форма. Относительно большая трансмембранная форма – ST2 лиганд (ST2L) – имеет три внеклеточные домена иммуноглобулина G и один трансмембранный внутриклеточный домен (рис. 2).
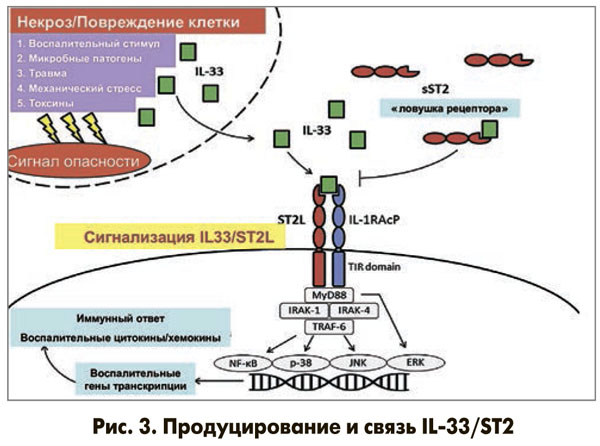
Функциональным лигандом ST2L является IL-33, который высвобождается из клеток преимущественно в момент их повреждения или некротической гибели и связывается с ST2L на мембранах клеток. Это связывание стимулирует митогенактивированные протеинкиназы (MAПK), а также приводит к активации ядерного фактора κВ (NF-κB), вызывая провоспалительные эффекты. Растворимая sST2 проявляет себя как «ловушка- рецептор» для IL-33. Растворимый sST2 связывает IL-33 и удаляет этот белок, не позволяя ему связаться с ST2L. Связывание sST2 с IL-33 ограничивает экспрессию и активацию NF-κB, что способствует уменьшению воспалительного ответа (рис. 3).
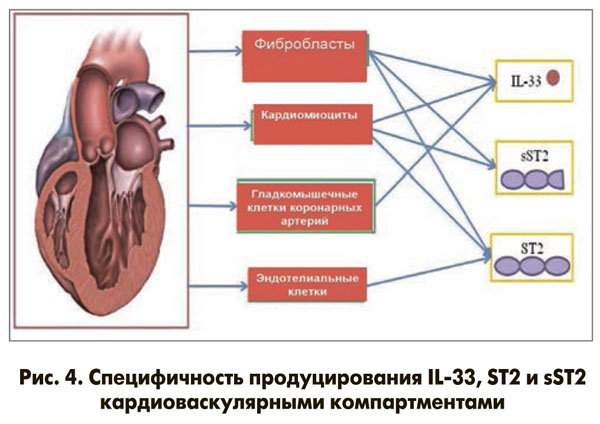
IL-33 экспрессируется из кардиомиоцитов, фибробластов и гладкомышечных клеток коронарных артерий человека, а sST2 и ST2 индуцируются из кардиомиоцитов, фибробластов и эндотелиальных клеток после биомеханического стресса, при этом преобладает растворимая форма sST2 (рис. 4).
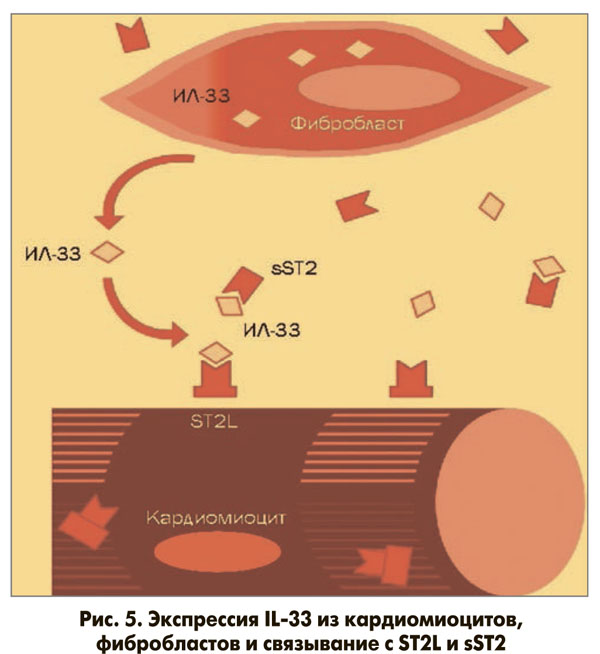
Установлено, что ST2L опосредует эффекты IL-33, тогда как избыточное содержание sST2 приводит к гипертрофии желудочков сердца, активации процессов фиброзирования, нарушению функции желудочков сердца (рис. 5).
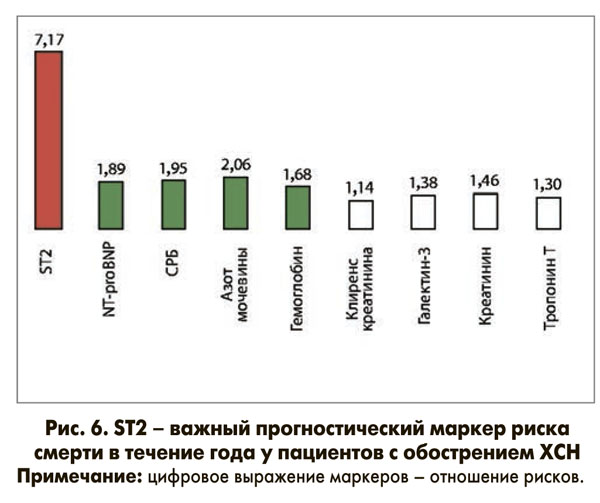
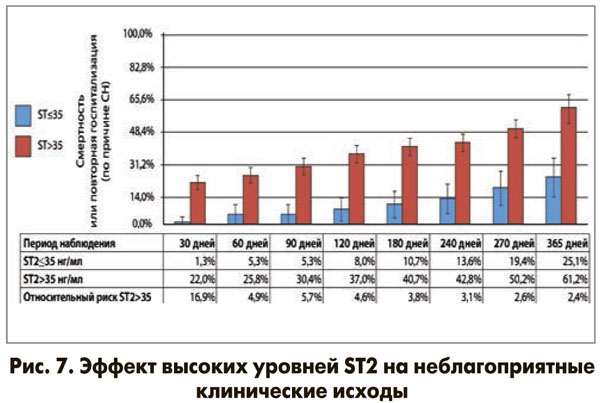
Физиологическая роль ST2 заключается в двух важных механизмах: он действует как кардиопротектор (обратимый процесс ремоделирования (фиброза) и гипертрофии), а также осуществляет иммунный ответ на воспаление. Теоретическая концепция кардиопротекторной роли ST2 заключается в том, что перегрузка давлением способствует повышенному синтезу IL-33, который, в свою очередь, через механизм лигандрецепторного взаимодействия с ST2L оказывает защитное действие, выражающееся в сдерживании процессов гипертрофии и фиброза миокарда. В противоположность ST2L активация sST2-рецептора не обладает кардиопротекторным действием ввиду того, что последний не имеет ни транс-мембранного, ни внутриклеточного домена, способного индуцировать какой-либо биологический эффект. Предполагается, что сигнализация IL-33-ST2L/sST2 играет важную роль в регуляции ответа миокарда на биомеханическую перегрузку. При увеличении концентрации ST2 происходит изменение внеклеточного матрикса, что приводит к повышению степени фиброза, прогрессированию гипертрофии и/или дилатации полостей сердца, тем самым обеспечивая снижение сократительной способности миокарда. Ответ здоровой сердечной ткани на повреждение или механический стресс включает продукцию и связывание IL-33 с ST2L, что запускает кардиозащитный сигнальный каскад предотвращения фиброза, ремоделирования сердца и СН. IL-33 является антагонистом гипертрофии кардиомиоцитов. Кроме того, ST2 вовлекается в процессы регуляции провоспалительной активации при широком спектре заболеваний, в том числе при хронической СН (ХСН), инфаркте миокарда, легочной артериальной гипертензии, выступая как маркер напряженности этой системы. Установлено, что циркулирующий пул ST2 хорошо и позитивно ассоциируется с величиной риска кардиоваскулярной смерти в популяции пациентов с обострением ХСН и дисфункцией миокарда (рис. 6, 7).
Референтные значения
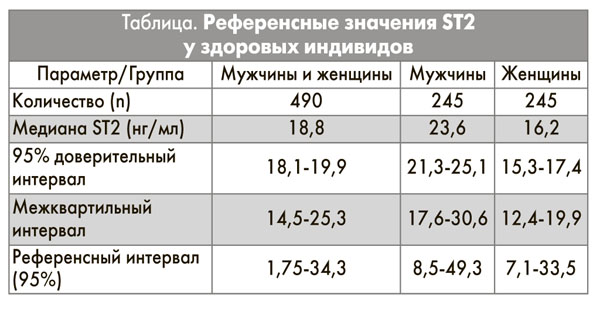
Основываясь на анализе 95 перцентиль, референсный интервал у здоровых нормальных мужчин составляет 8,5-49,3 нг/мл (медиана 23,6 нг/мл), у женщин этот показатель равняется 7,1-33,5 нг/мл (медиана 16,2 нг/мл) и внутри группы 1,75-34,3 (медиана 18,8 нг/мл) (табл.). Пороговое значение для ST2 равняется 35 нг/мл независимо от пола, возраста, расы и иных факторов.
ST2 и натрийуретические пептиды
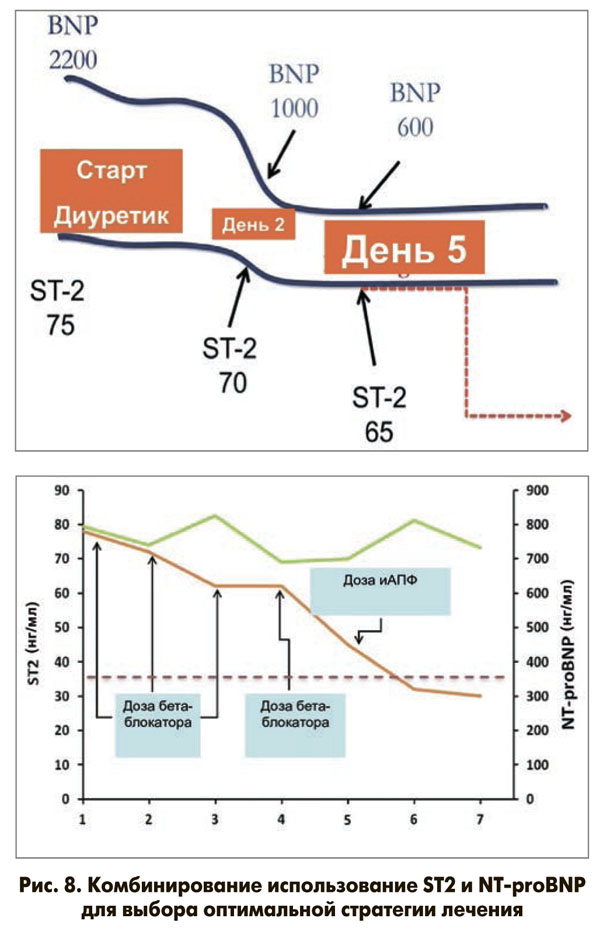
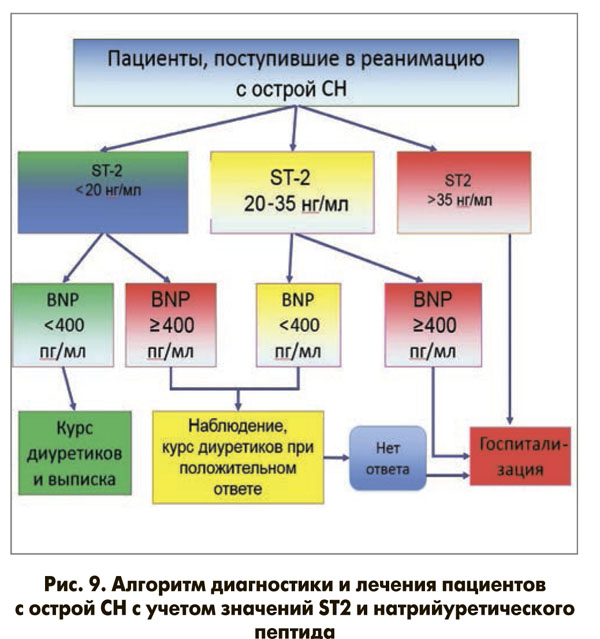
Комбинированное использование ST2 и мозгового натрийуретического пептида (BNP) повышает прогностическую ценность этих показателей в сравнении с таковой их изолированного определения. Смертность в течение 1 года была максимальной среди пациентов, имевших наиболее высокие концентрации обоих биомаркеров (42 против 28% в группе). В. Ky и соавт. (2010) в течение длительного времени наблюдали амбулаторных больных с ХСН. Работа этих авторов стала наиболее крупным исследованием, в котором изучалась предсказательная значимости уровня ST2 при стабильном течении ХСН. В данном испытании показана высокая диагностическая значимость ST2 при ХСН, а также то, что комбинированное измерение концентраций ST2 и NT-proBNP оказалось более информативным (на 14,9%) для определения риска, чем изолированное определение указанных маркеров. Эти данные подтверждает исследование B.D. Lori и соавт., опубликованное в 2010 г., целью которого являлось определение взаимосвязи между уровнем ST2 и структурно-функциональным состоянием миокарда. В этой работе, как и в исследовании В. Ky и соавт., было подтверждено, что сочетание повышенных концентраций ST2 и BNP имело большую прогностическую значимость по сравнению с соответствующим показателем в случае увеличения активности лишь одного маркера. Так, у пациентов, имевших одновременное увеличение концентрации ST2 и BNP, риск смерти в течение года (11%) был соответственно в 2,6 и в 5,5 раза выше, чем у лиц с повышением активности только одного из этих маркеров (5%) или с нормальными значениями указанных пептидов (2%). Таким образом, сочетанное использование ST2 и натрийуретических пептидов улучшает стратификацию риска и клиническое ведение пациентов, помогая определить оптимальную профилактическую стратегию лечения (рис. 8, 9).
ST2 и галектин-3
Относительно недавно опубликованы результаты исследования, в ходе которого проводилось прямое сравнение долгосрочной прогностической значимости ST2 и галектина-3 у пациентов со стабильным течением СН. Согласно результатам данной работы, ST2 превзошел галектин-3 и продемонстрировал независимую связь с сердечно-сосудистой смертностью. Более того, в отличие от галектина-3 включение ST2 в полную модель с поправкой на смертность от всех причин сопровождалось достоверным улучшением точности прогноза больных ХСН.
Анализаторы и наборы для определения ST2
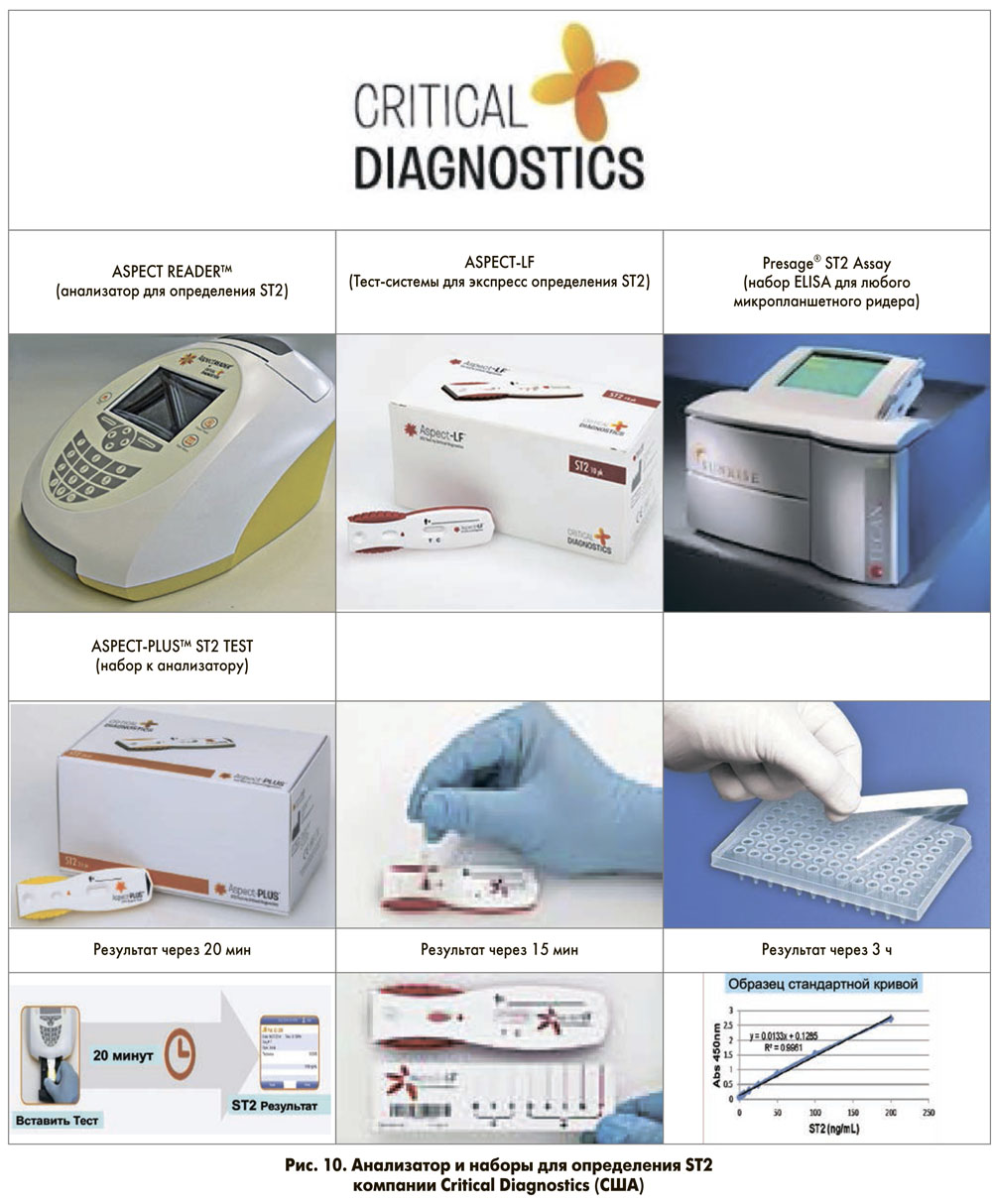
Для определения концентрации ST2 в сыворотке/плазме компания Critical Diagnostics (CША) выпускает оборудование и наборы в 3 форматах: анализатор ASPECT READER™ и набор тест-систем ASPECT-PLUS™ ST2 TEST; тест-системы для экспресс-диагностики ASPECT-LF; набор для исследования методом ELISA Presage® ST2 Assay (рис. 10).
Основные преимущества ST2 и его применение в различных клинических ситуациях
• ST2 позволяет поставить диагноз СН у больных еще на бессимптомной стадии в отличие от BNP и NT-proBNP, при использовании которых необходимо наличие симптомов заболевания.
• В отличие от натрийуретических пептидов уровень ST2 не зависит от возраста пациента, массы тела, образа жизни, наличия сопутствующих заболеваний (в т. ч. почечной дисфункции).
• Информация об уровне ST2 может быть полезна при выборе тактики лечения у пациентов с кардиоваскулярной патологией, а также позволяет облегчить принятие решений в критических ситуациях.
• Является маркером отторжения трансплантата при пересадке сердца.
• Используется при обследовании лиц, обратившихся за медицинской помощью по поводу острой боли в груди, у пациентов с острым инфарктом миокарда и больных с терминальной стадией СН.
• Определение ST2 позволяет прогнозировать ответ на лечебную физкультуру при ХСН.
• ST2 имеет четкое пороговое значение, которое составляет 35 нг/мл.
• ST2 является предиктором риска развития СН в общей популяции. С 2013 г. тест ST2 включен в Руководство по ведению сердечной недостаточности ACCF/AHA.
Список литературы находится в редакции.
Медична газета «Здоров’я України 21 сторіччя» № 20 (393), жовтень 2016 р.