11 липня, 2016
Діагностичні можливості імунного блотингу при бореліозі
Як відомо, бореліоз (хвороба Лайма) є полісистемним інфекційним захворюванням, спричиненим спірохетою Borrelia burgdorferi, що передається людям через укуси кліщів. Це захворювання широко розповсюджене, проте найвищий рівень захворюваності спостерігається в певних географічних зонах, зазвичай у літні місяці.
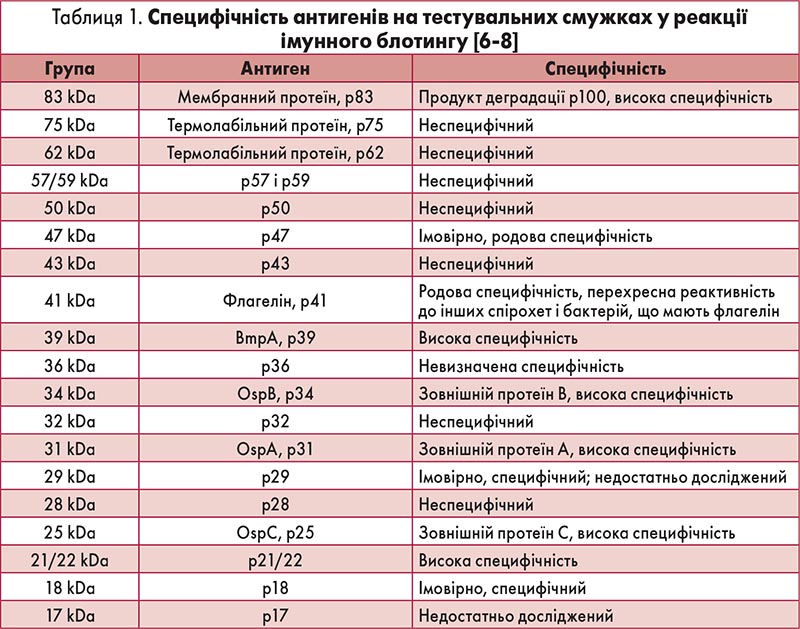
Для лабораторної діагностики цієї хвороби сьогодні здебільшого використовують серологічний метод – імуноферментний аналіз (ІФА, ELISA/IIFT), непряму реакцію імунофлюоресценції (нРІФ) та реакцію імунного блотингу (вестерн-блот). У літературі наведено різні дані щодо чутливості та специфічності ІФА в разі кліщового бореліозу. Зокрема, за оцінками деяких авторів, специфічність ІФА-тестування антитіл до B. burgdorferi нині сягає 95% (тобто неспецифічні реакції, перехресне реагування з антигенами інших бактерій приблизно в 5% випадків можуть давати псевдопозитивні результати) [1, 2]. Широкий спектр думок щодо переваг і недоліків різних серологічних методів став причиною розроблення й затвердження певного алгоритму специфічної діагностики у випадку бореліозу. Відповідно до рекомендацій Центрів з контролю та профілактики хвороб США (CDC), затверджено двоетапну схему [3]. На першому етапі за наявності клініко-анамнестичних показань проводиться тестування з допомогою ІФА або нРІФ. За результатами першого етапу дослідження зразки крові із сумнівними й позитивними результатами мають бути підтверджені з використанням методу імунного блотингу (табл. 1) [4, 5]. Останній дозволяє виділяти низку борелійних антигенів, що характеризуються різною специфічністю. Антигени B. burgdorferi загалом можна поділити на 3 категорії [9] (табл. 2). Результати імунного блотингу на виявлення IgM проти B. burgdorferi можуть бути негативними, граничними (так звана сіра зона) та позитивними.
У ранній фазі інфікування бореліями IgM, що можуть виявлятися в 50-90% пацієнтів у стадії I, зазвичай спрямовані проти зовнішнього протеїну C – OspC (p25) [10]. За умови недавнього інфікування IgM проти інших специфічних антигенів борелій зазвичай ще не виявляються. Частота знаходження специфічних IgG у цій фазі хвороби також дуже низька [11, 12].
IgM проти флагеліну (p41) є початковою відповіддю організму на B. burgdorferi. Проте не можна виключити й неспецифічну реакцію, оскільки зазначені антитіла перехресно реагують і з іншими мікроорганізмами. Тому єдиний позитивний тест на флагелін (p41) при виявленні IgM не може бути доказом недавнього інфікування B. burgdorferi. У таких випадках необхідно повторити тест через кілька тижнів.
Антитіла класу IgM часто бувають хибнопозитивними, причому іноді їх можна виявляти протягом багатьох років після перенесеного (лікованого чи нелікованого) бореліозу. Отже, виявлення зазначених антитіл не обов’язково вказує на свіже інфікування. Водночас і відсутність протибореліозних IgM не виключає нещодавньої інфекції, оскільки відомі випадки виявлення специфічних імуноглобулінів класу G без синтезу відповідних Ig M. Щоб уникнути цієї проблеми, у реакції імунного блотингу ідентифікують VlsE, що може розглядатися як головний антиген для серологічної діагностики бореліозу. Понад 85% IgG-позитивних сироваток можна ідентифікувати тільки шляхом оцінки VlsE. Цей антиген є специфічним для усіх різновидів борелій. Ризик хибнопозитивної реакції практично виключається [13].
У пізній стадії бореліозу позитивний тест на IgM не має жодного значення у зв’язку з можливістю постійної персистенції інфекційних агентів, про що йшлося раніше. Причина таких хибнопозитивних тестів на IgM часто залишається неясною. Так, нерідко вони мають місце при інфекційному мононуклеозі, герпетичних інфекціях і різних аутоімунних недугах [14].
Для діагностики свіжого інфікування бореліями позитивний результат IgM треба підтвердити виявленням протибореліозних IgG через 3-6 тиж (табл. 3).
У більшості гострих випадків бореліозу, які супроводжуються мігруючою еритемою на місці присмоктування кліща, клінічна діагностика не становить труднощів. Проте в 20-40% пацієнтів перебіг хвороби має безеритемну форму [15], що значно ускладнює діагностику хвороби. При цьому можуть спостерігатися ураження нервової системи, суглобів, серця, очей. Є підстави вважати, що значна кількість безеритемних випадків хвороби Лайма не діагностується, вони маскуються як прояви багатьох неврологічних, ревматологічних і кардіологічних синдромів, тож хворі не отримують вчасного належного протимікробного лікування. Результати проведених досліджень свідчать про високу частку серопозитивних осіб серед пацієнтів неврологічних стаціонарів. Так, серед мешканців (n=61) Львова, які з різними діагнозами госпіталізувалися в неврологічне відділення, протиборелійні антитіла класу IgG виявлені в 10 пацієнтів, що становить 16,4% обстежених, натомість серед донорів крові (n=60) було лише 3 (5%) серопозитивні особи (р<0,05) [16].
Через кілька тижнів або місяців після укусу кліща може розвинутися низка інших симптомів. Передусім це неврологічні прояви: менінгіт, енцефаліт, асиметричний поліневрит, парез черепномозкових нервів, лімфоцитарний менінгорадикулоневрит (II стадія). Часто можуть спостерігатися артрити, особливо колінних суглобів, і нелокалізовані болі кісток, суглобів і м’язів. Рідше відзначаються кардіологічні прояви, такі як міокардит і перикардит. Антитіла проти B. burgdorferi можуть бути виявлені в 50-90% пацієнтів у II стадії [13]. На ранній фазі цієї стадії знаходять переважно антитіла класу IgM, а в пізній фазі часто присутні тільки антитіла класу IgG, проте рівні специфічних IgM можуть зберігатися протягом тривалого часу [17]. Визначаючи IgG проти VlsE, можна підвищити серологічний коефіцієнт до 20-30%.
Типовими проявами борелійної інфекції на стадії III є хронічний рецидивний ерозивний артрит, хронічний атрофічний акродерматит і прогресуючий енцефаломієліт, перебіг якого може бути подібним до такого в разі множинного склерозу. За відсутності лікування ІІІ стадія може розвиватися протягом декількох років або десятиліть після первинного інфікування. На цій стадії рівні специфічних IgG-антитіл значно підвищені в 90-100% пацієнтів, водночас антитіла класу IgM виявляються дуже рідко [13].
Таким чином, перебіг бореліозу, особливо його підгострих і хронічних форм, може супроводжуватися ураженням багатьох органів і систем, а значна частота безеритемних випадків хвороби помітно ускладнює вчасну діагностику хвороби. Відтак створюються умови для прогредієнтного перебігу патології з розвитком несприятливих наслідків, у тому числі неврологічних синдромів. Для запобігання дисемінації збудника й розвитку органних уражень важливою є вчасна адекватна протимікробна терапія, для чого хворим з відповідною клінічною симптоматикою за наявності анамнестичних даних про присмоктування кліщів необхідно проводити специфічні серологічні дослідження [18].
Зрозуміло, що негативний результат найчастіше використовуваного ІФА із сироваткою крові пацієнта не виключає нещодавно перенесену інфекцію. Якщо у хворого є клінічні ознаки бореліозу, рекомендується проведення тесту на виявлення IgM-антитіл. Якщо обидва тести негативні, слід повторити ІФА через 10-14 діб для виключення уповільненої імунної відповіді з продукцією антитіл.
Зазвичай IgM з’являються першими у відповідь на інфікування чи реактивацію збудника, що дозволяє виявити гостру стадію первинної інфекції (коли ще немає IgG) або реактивацію хронічної (на тлі виявлення IgG). IgG у типових випадках з’являються через 2-3 тиж після інфікування, є суворо специфічними для збудника, зберігаються довічно, але їх рівень не відображає активності процесу [19].
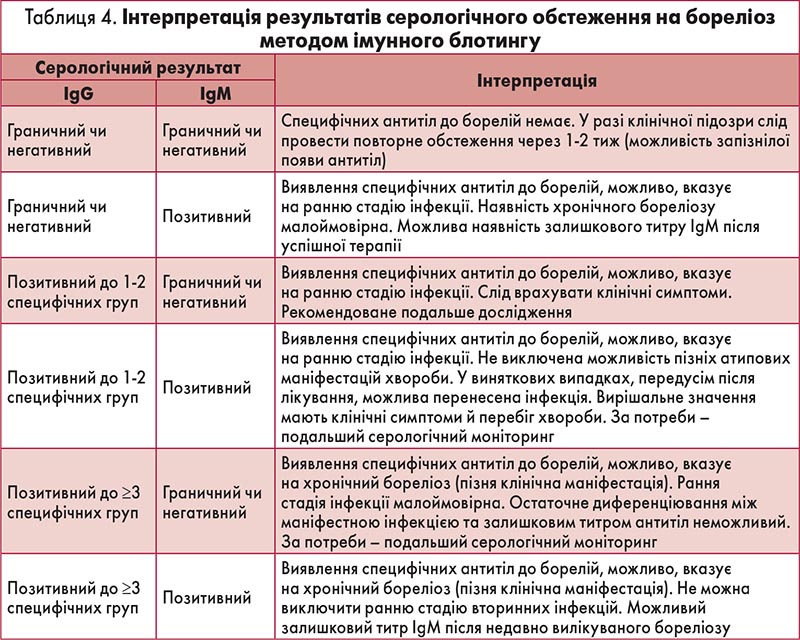
Діагностика бореліозу, особливо на стадії неврологічних уражень, може викликати труднощі не лише через відсутність патогномонічних проявів, а й через можливість хибних серологічних тестів. Так, оскільки специфічні сироваткові антитіла виявляються лише у 20-50% пацієнтів на I стадії захворювання (мігруюча еритема), у 50-90% – на II стадії (нейробореліоз) і майже в 100% – лише на III стадії (акродерматит, Лайм-артрит), то негативний результат не виключає діагнозу захворювання (табл. 4).
Труднощі своєчасного виявлення бореліозу зумовлені також можливістю інапарантного перебігу хвороби без помітних клінічних ознак як у ранній період, так і в період дисемінації збудника [20]. У віддалені терміни в частини інфікованих відбувається активація інфекційного процесу з маніфестацією клінічних проявів, розвитком серйозних органних уражень, які визначають симптоматику хронічної стадії хвороби через місяці й навіть роки після присмоктування кліща. Зрозуміло, що через тривалий час після інфікування інколи буває важко пов’язати ураження тих чи інших органів з присмоктуванням кліщів у минулому та запідозрити бореліоз, тим більше що такі пацієнти в більшості випадків перебувають поза увагою інфекціоністів, лікуються в інших спеціалістів терапевтичного профілю [18].
Обговорювана реакція імунного блотингу дає унікальну можливість визначати всі 3 види B. burgdorferi sensu lato: B. burgdorferi sensu stricto, B. afzelii та B. garinii. Іноді бувають ситуації, коли причиною хвороби Лайма стає не один вид борелій, а їх поєднання. Так, обстеживши 330 працівників лісового господарства Тернопільщини, у 7 з них за допомогою методу імунного блотингу ми виявили чіткі серологічні ознаки бореліозу, зумовленого комбінацією одразу 3 видів збудників (табл. 5). Очевидно, виконуючи професійні обов’язки, ці люди багаторазово зазнавали укусів кліщів, що й зумовило ко- чи суперінфікування. У кожного пацієнта на підставі епідеміологічних, клінічних і серологічних даних діагностовано еритемну чи безеритемну форму хвороби Лайма, хронічний перебіг з переважним ураженням нервової системи та суглобів.
Як видно з таблиці, у більшості пацієнтів виявлено IgM до антигену p41, що, однак, не є специфічним маркером до борелій. Адже зазначений білок-флагелін p41 міститься в багатьох бактеріях, передусім у спірохетах, і навіть в окремих тканинах людського організму. Тому знаходження тільки цього маркера не дає змоги верифікувати IgM та IgG проти борелій. Крім того, згідно з рекомендаціями Другої національної конференції зі серологічної діагностики хвороби Лайма [3] про виявлення IgM при блот-аналізі можна говорити лише тоді, коли присутні щонайменше 2 з перерахованих далі 3 антигенів: 24 kDa (OspC), 39 kDa (BmpA) і 41 kDa (Fla) [21]. Таким вимогам відповідають лише аналізи хворого С., у якого, крім IgM до p41, були знайдені ще й IgM до OspC Ba (B. afzelii). Це може свідчити або про недавнє інфікування B. afzelii, або про залишковий титр IgM, які, як згадувалося раніше, іноді можуть виявлятися протягом багатьох років.
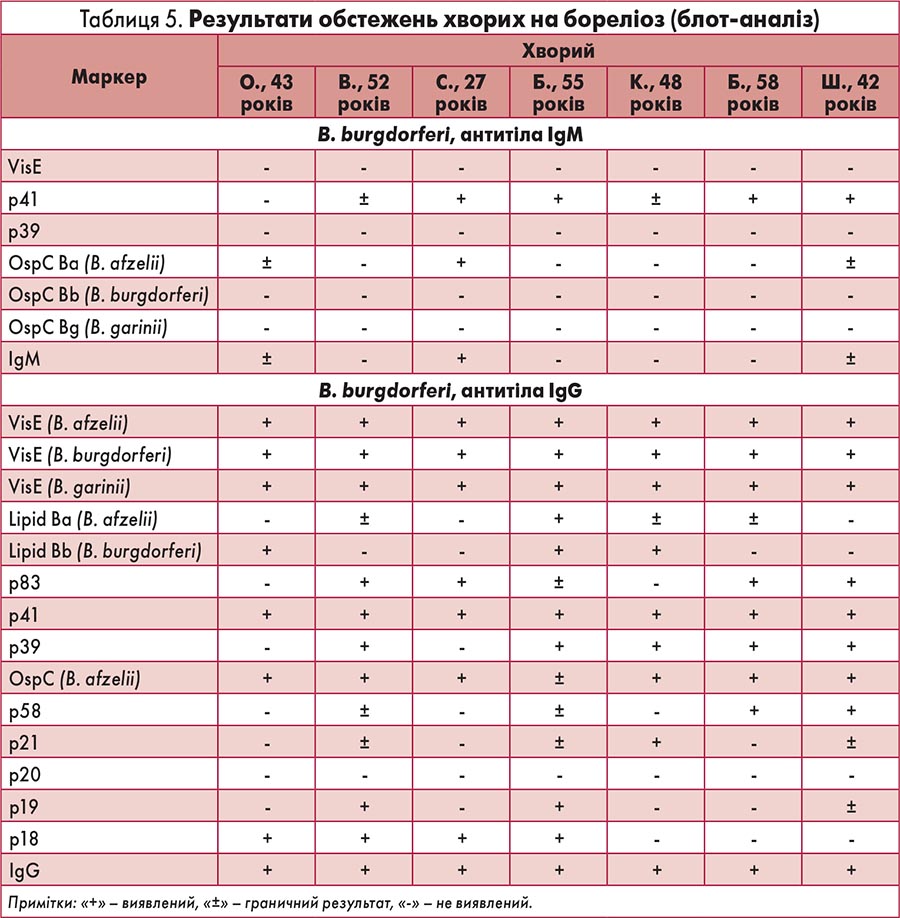
Натомість IgG при блот-аналізі наявні в тому випадку, коли визначаються 5 з 10 таких антигенів: 18 kDa, 21 kDa (OspC), 28 kDa, 30 kDa, 39 kDa (BmpA), 41 kDa (Fla), 45 kDa, 58 kDa (не GroEL), 66 kDa і 93 kDa [22]. В усіх хворих виявили IgG до високоспецифічних VisE B. afzelii, B. burgdorferi та B. garinii, неспецифічного p41, а також характерні для нещодавнього інфікування OspC (B. afzelii). У кожному випадку були знайдені IgG до як мінімум 5 різних антигенів борелій, що дало можливість ідентифікувати специфічність зазначених антитіл.
Обговорюється різна техніка виявлення антитіл проти B. burgdorferi [14, 23]: Elisa, нРІФ, пасивна гемаглютинація та імуноблотинг. Як було зазначено раніше, згідно з директивами регуляторних органів США та Німеччини, серологічна діагностика має здійснюватися за принципом двокрокової процедури: спочатку скринінг сироваток за допомогою ELISA або непрямої імунофлюоресценції (IIFT), а далі зразки крові зі сумнівними й позитивними результатами мають бути підтверджені за допомогою методу імунного блотингу. При свіжому інфікуванні рекомендовано паралельно виконувати ELISA/IIFT і вестерн-блот, оскільки останній метод дає можливість виявити деякі слабкі реакції, недосяжні для ІФА [13]. Найчутливішим антигеном для виявлення IgM є OspC, а для IgG – VlsE відповідно [24].
Варто звернути увагу на винятково важливу роль у таких випадках достовірності лабораторних тестів. Наш досвід дозволяє стверджувати, що на сьогодні перевіреною лабораторією, яка гарантовано забезпечує високу стабільність і відтворюваність результатів, а отже, заслуговує на довіру, є «Сінево» – європейська мережа медичних лабораторій в Україні.
Список літератури знаходиться в редакції.