15 листопада, 2021
Дослідження GRADE: очевидні та неочевидні висновки
GRADE – одне з найбільш усеосяжних досліджень у діабетології останніх років.
Воно було присвячене оцінюванню цукрознижувальних препаратів із чотирьох основних груп, які додавали до метформіну пацієнтам із цукровим діабетом (ЦД) 2 типу.
Для порівняння відібрали, напевно, найцікавіші представники своїх класів з оптимальним співвідношенням ефективності та безпеки: препарат сульфонілсечовини глімепірид, агоніст рецепторів глюкагоноподібного пептиду-1 ліраглутид, інгібітор дипептидилпептидази-4 ситагліптин і базальний аналог інсуліну гларгін. Який режим терапії виявився найефективнішим і які практичні висновки дає змогу зробити це випробування?
Мета, методи та результати дослідження GRADE
На той час, коли було сплановане та розпочалося дослідження GRADЕ, метформін був основою лікування ЦД 2 типу, а от для обґрунтованого вибору терапії другої лінії за недостатньої ефективності метформіну наукових даних було замало. Метою випробування GRADE як раз і стало визначення оптимального компаньйона для метформіну.
GRADE (Glycemia Reduction Approaches in Diabetes – a Comparative Effectiveness) – багатоцентрове інтервенційне рандомізоване відкрите клінічне випробування в паралельних групах. Для участі в ньому було відібрано понад 5 тис. пацієнтів із ЦД 2 типу з тривалістю захворювання менш як 10 років (медіана – 4,2 року), віком не менш як 30 років на момент встановлення діагнозу (середній вік – 57,2 року) та рівнем глікозильованого гемоглобіну (HbA1c) 6,8-8,5%, які отримували монотерапію метформіном у дозі не менш ніж 500 мг/добу на час скринінгу. Дозу метформіну збільшували протягом 6-12-тижневого ввідного періоду (до цільової дози 2000 мг/добу залежно від переносимості, але мінімально 1000 мг/добу на початок дослідження). Потім пацієнтів випадковим чином розподілили на чотири групи для лікування глімепіридом, ситагліптином, ліраглутидом та інсуліном гларгін на додаток до метформіну.
Первинною та вторинною кінцевими метаболічними точками дослідження було досягнення рівня HbA1c ≥7 та >7,5% відповідно. Після досягнення вторинної кінцевої метаболічної точки пацієнтам, які раніше не отримували інсулін гларгін, ініціювали інсулінотерапію. Час від початку лікування інсуліном гларгін до досягнення показника HbA1c >7,5% вважався третинною кінцевою метаболічною точкою. Вторинними кінцевими точками також були випадки мікроваскулярних ускладнень, серцево-судинних захворювань і побічних ефектів. Мікросудинні кінцеві точки включали помірну (≥30 мг/г) або тяжку (>300 мг/г) альбумінурію, швидкість клубочкової фільтрації <60 мл/хв/1,73 м2 та дистальну сенсорну полінейропатію. Серцево-судинні кінцеві точки включали випадки будь-яких серцево-судинних захворювань, загальну смертність, серйозні несприятливі серцево-судинні події (інфаркт міокарда, інсульт або серцево-судинна смерть) і менш значущі несприятливі серцево-судинні події (серцева недостатність, яка потребувала госпіталізації, нестабільна стенокардія, що потребувала госпіталізації або реваскуляризації). Загалом 93,7% учасників завершили дослідження. Середня тривалість спостереження становила 5 років.
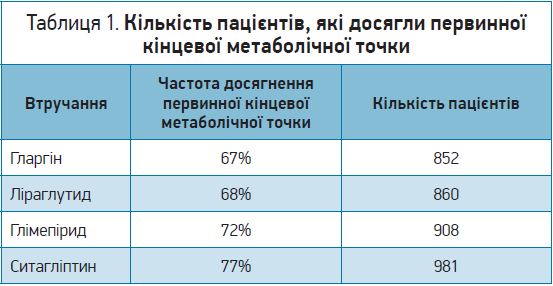
Серед пацієнтів, які були розподілені на прийом ліраглутиду й інсуліну гларгін, менша кількість учасників досягли первинної кінцевої метаболічної точки (67 і 68% відповідно) порівняно з пацієнтами, які отримували глімепірид (72%) або ситагліптин (77%) (табл. 1).
Відносне зниження ризику досягнення первинної кінцевої метаболічної точки в групі інсуліну гларгін було більшим, аніж у групі глімепіриду, на 11% (р=0,016), у групі ситагліптину – на 29% (р<0,001) і було подібним до такого в групі ліраглутиду (р=0,611). Відносне зниження ризику в групі ліраглутиду було більшим, аніж у групі глімепіриду, на 13% (р=0,007) і в групі ситагліптину – на 31% (р<0,001).
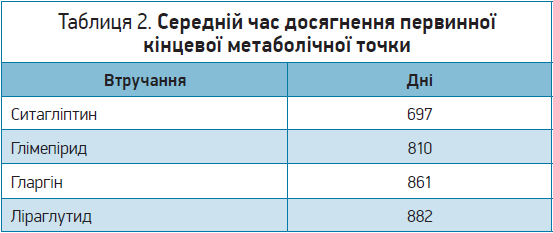
Протягом першого року дослідження ліраглутид і глімепірид виявилися найефективнішими щодо утримання рівня HbA1c <7%. Однак на четвертому році дослідження всі групи вийшли за межі первинної кінцевої метаболічної точки. Час досягнення первинної кінцевої метаболічної точки виявився найбільшим у групах ліраглутиду й інсуліну гларгін на відміну від глімепіриду та ситагліптину (табл. 2).
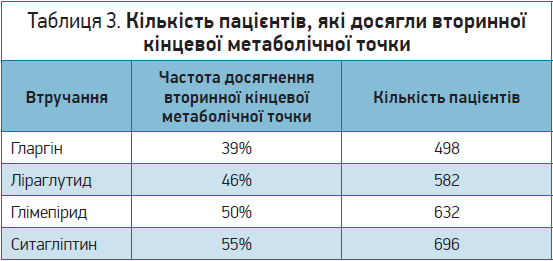
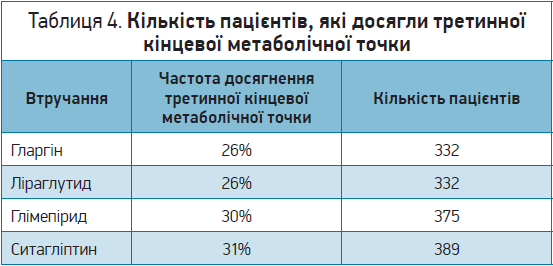
Виявилося, що ефективність гларгіну, глімепіриду та ліраглутиду зростала зі збільшенням вихідного рівня HbA1c. Отримані результати дали змогу зробити висновок, що ситагліптин був найменш ефективним втручанням. Інсулін гларгін виявився найбільш ефективним щодо вторинної кінцевої метаболічної точки, а ліраглутид за цим критерієм посідав друге місце (табл. 3). Зрештою, менша кількість учасників груп ліраглутиду й інсуліну гларгін досягли третинної кінцевої метаболічної точки порівняно з глімепіридом і ситагліптином (табл. 4).
Результати дослідження не показали відмінностей за частотою мікросудинних ускладнень залежно від виду втручання. Не було виявлено також істотних відмінностей щодо ризику розвитку серйозних несприятливих серцево-судинних подій, менш значущих несприятливих серцево-судинних подій, а також смертності в досліджуваних групах. Загалом ліраглутид продемонстрував нижчу кумулятивну серцево-судинну захворюваність порівняно з іншими втручаннями (р=0,048).
Частота виникнення серйозних побічних явищ достовірно не відрізнялася між групами (р=0,139). Тяжка гіпоглікемія спостерігалася частіше в разі застосування глімепіриду порівняно з іншими препаратами (р=0,003). У групі ліраглутиду була зафіксована найвища втрата ваги протягом 4 років (р<0,001), як і найвищий ризик розвитку гастроінтестинальних побічних ефектів (р<0,001).
Які очевидні висновки зробили автори дослідження?
За висновками дослідників, ліраглутид та інсулін гларгін виявилися найефективнішими препаратами другої лінії в лікуванні ЦД 2 типу. Відзначають також додаткову користь ліраглутиду щодо втрати ваги протягом перших 4 років, хоча визнають, що побічні ефекти з боку шлунково-кишкового тракту виникали при лікуванні цим препаратом значно частіше порівняно з іншими групами.
…і які неочевидні висновки можна зробити?
Сучасний підхід до лікування ЦД 2 типу є не тільки глюкозо-, а й кардіоцентричним. Це означає, що основною метою є подовження життя пацієнта та покращення її якості. Чи була отримана достовірна різниця між групами щодо ризику розвитку мікросудинних ускладнень, серйозних несприятливих серцево-судинних подій, смертності? Ні, не була.
Дійсно, ліраглутид та інсулін гларгін забезпечували дещо триваліший контроль глікемії, але якою ціною? Вартість такого лікування значно вища, що не можна ігнорувати в поточній економічній ситуації в нашій країні. Стосовно якості життя, то обидва препарати є ін’єкційними, а отже, є певні питання щодо цього та прихильності до лікування.
У перший рік лікування найефективнішими були глімепірид і ліраглутид. Отже, з огляду на співвідношення ефективності, безпеки, вартості та зручності застосування, а також відсутності суттєвих відмінностей між різними препаратами щодо впливу на жорсткі кінцеві точки, найраціональнішим вбачається додавання до метформіну глімепіриду. А згодом, у міру погіршення глікемічного контролю, варто розглядати дорожчі та складніші в застосуванні ін’єкційні методи терапії.
Якщо похідні сульфонілсечовини, то глімепірид
Залежно від фармакодинамічних характеристик препарати сульфонілсечовини можна умовно поділити на три покоління. Представниками першого є толбутамід, карбутамід, хлорпропамід і деякі інші лікарські засоби, які сьогодні вже не використовуються в клінічній практиці. До препаратів другого покоління належать глібенкламід, гліпізид, гліклазид і гліквідон. Третє покоління представлене молекулою глімепіриду.
Порівняно з іншими похідними сульфонілсечовини глімепірид має низку унікальних властивостей. Першою з них є подвійний механізм дії – м’яка стимуляція секреції інсуліну та зменшення інсулінорезистентності за рахунок покращення транспорту глюкози в клітину.
Другою важливою перевагою є менший ризик гіпоглікемії та відсутність збільшення маси тіла. Такий ефект пояснюється блокуванням диференціації адипоцитів, що робить глімепірид препаратом вибору у хворих на ЦД 2 типу, асоційований з ожирінням.
Окрім того, глімепірид має низку корисних позапанкреатичних ефектів: антиагрегантний (інгібує агрегацію тромбоцитів більш виражено, ніж гліклазид і глібенкламід; відновлює фібринолітичну активність судинного ендотелію); антихолестеринемічний (зменшує зростання атеросклеротичної бляшки; підвищує рівень адипонектину); антиішемічний (не впливає негативно на ішемічне прекондиціювання міокарда).
Ефективність, безпека, плейотропність і доступна вартість дають змогу розглядати глімепірид як один з основних варіантів лікування ЦД у разі непереносимості чи недостатньої ефективності метформіну.
Підготував В’ячеслав Килимчук
Медична газета «Здоров’я України 21 сторіччя» № 19 (512), 2021 р.