10 грудня, 2021
Хирургическое лечение редких осложнений желчнокаменной болезни
 Современные руководства дают четкие рекомендации по диагностике и лечению осложненных форм желчнокаменной болезни, однако в условиях недостаточной оснащенности хирургических стационаров, редкости данных осложнений по-прежнему отмечаются трудности в оказании ургентной хирургической помощи таким пациентам. В данной работе представлены случаи успешного хирургического лечения больных с различными редкими формами осложненной желчнокаменной болезни.
Современные руководства дают четкие рекомендации по диагностике и лечению осложненных форм желчнокаменной болезни, однако в условиях недостаточной оснащенности хирургических стационаров, редкости данных осложнений по-прежнему отмечаются трудности в оказании ургентной хирургической помощи таким пациентам. В данной работе представлены случаи успешного хирургического лечения больных с различными редкими формами осложненной желчнокаменной болезни.
Ключевые слова: желчнокаменная болезнь, желчный конкремент, холецистопанкреатит энтеролитотомия, Синдром Бувере.
Желчнокаменная болезнь (ЖКБ) является наиболее часто встречающейся хирургической патологией во всем мире, на которую приходится большая часть госпитализаций и хирургических вмешательств. В развитых странах частота встречаемости данной патологии составляет 15-25%, при этом в последние десятилетия отмечается неуклонный рост количества заболевших. Также ЖКБ является основной причиной заболеваемости как в развитых, так и в развивающихся странах. Необходимо отметить, что, несмотря на то что от данной патологии страдают в основном женщины, доля пациентов мужского пола также составляет значительную часть заболевших в общей популяции. Осложнения ЖКБ варьируют от острого холецистита до перфорации желчного пузыря, формирования внутренних свищей, а также панкреатита. Наиболее интересными с точки зрения диагностики и лечения являются редкие осложнения, к которым можно отнести синдром Мириззи (наблюдается в 1% случаев) и холецистодигестивные свищи (встречаются в 0,15-4% наблюдений). Еще более редкими являются комбинированные холецистобилиарно-дигестивные фистулы.
Клиническое наблюдение № 1
Пациентка, 86 лет, доставлена в клинику Института в ургентном порядке с диагнозом «острая кишечная непроходимость» через 7 сут от начала заболевания. При сборе анамнеза пациентка сообщила, что в течение многих лет она отмечала боли в правом подреберье, однако не обследовалась, самостоятельно принимала спазмолитические препараты. Также пациентка не отмечала хирургических вмешательств на органах брюшной полости. Начало заболевания было постепенным, однако в последние несколько суток пациентка постоянно отмечала приступы рвоты, которые приобрели каловый характер.
При поступлении состояние тяжелое, с признаками обезвоживания и дисэлектролитных нарушений. Диурез значительно снижен. Живот вздут, ассиметричен, умеренно болезнен. Перистальтика слабая. Шум «плеска». При рентгенологическом исследовании определяются признаки тонкокишечной непроходимости (спаечной?) в виде значительного расширения петель тонкой кишки, множественных чаш Клойбера.
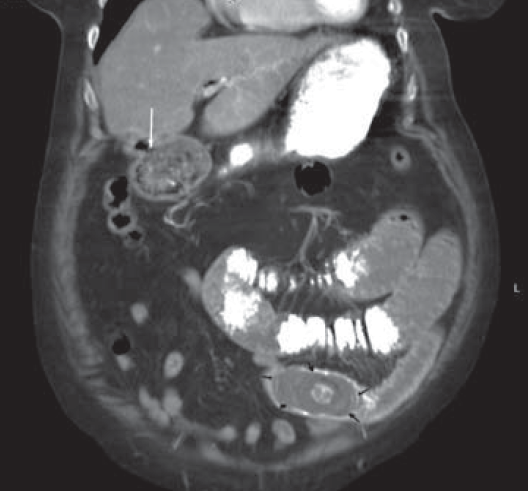
В связи с тяжестью состояния, наличием признаков тяжелой дегидратации и дисэлектролитных расстройств пациентке начата предоперационная подготовка, а также назначена терапия, стимулирующая кишечную перистальтику. Больной дан барий. При контрольной рентгенографии через 4 ч пассаж бария замедлен, 2/3 его в желудке, барием выполнены начальные отделы тонкой кишки. Для уточнения диагноза больной выполнена компьютерная томография (КТ), по данным которой определяется холецистодуоденальный свищ размером до 0,5 см в диаметре, в терминальном отделе тонкой кишки выявлен конкремент 3×4 см, полностью обтурирующий просвет тонкой кишки, являющийся причиной острой тонкокишечной непроходимости (рис. 1, 2).
Рис. 1. Компьютерная томограмма, фронтальная проекция: определяется холецистодуоденальный свищ (белая стрелка), конкремент в подвздошной кишке, обтурирующий ее просвет (черные стрелки), расширение петель тонкой кишки, которые содержат бариевую взвесь, 2/3 которой находятся в желудке
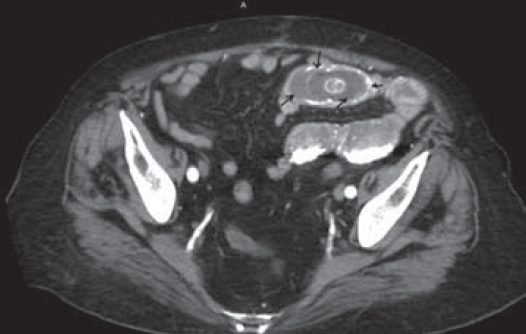
Рис. 2. Компьютерная томограмма, аксиальная проекция: билиарный конкремент (черные стрелки), обтурирующий просвет подвздошной кишки
Больной установлен диагноз: «Желчнокаменная болезнь III ст., хронический рецидивирующий холецистопанкреатит. Холецистодуоденальный свищ. Билиарный илеус (синдром Бувере)».
Пациентке назначено оперативное лечение по жизненным показаниям. Через 8 ч после поступления больной в ургентном порядке выполнена операция, которая включала: лапаротомию, энтеролитотомию, интубацию тонкой кишки через аппендикоцекостому (рис. 3, 4).
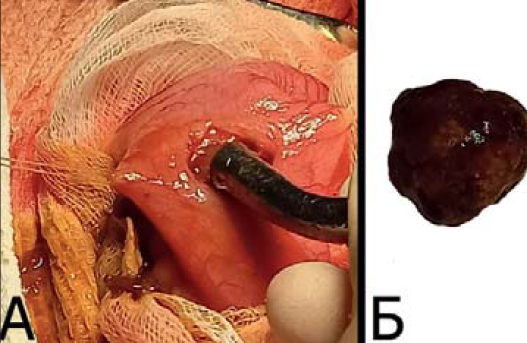
Рис. 3. Этап операции: в просвете тонкой кишки идентифицировано инородное тело, полностью обтурирующее просвет кишки
Рис. 4. Этап операции: выполнена энтеролитотомия (А), извлечено инородное тело – желчный конкремент (Б)
Течение послеоперационного периода в целом без осложнений. Однократно выполнялась плевральная пункция в связи с явлениями правостороннего гидроторакса. Кишечный зонд удален на 5-й день после операции. Больная выписана в удовлетворительном состоянии под наблюдение хирурга по месту жительства на 13-е сутки после оперативного вмешательства.
Еще две пациентки старшей возрастной группы оперированы в условиях центральной районной больницы. Окончательный диагноз был установлен во время лапаротомии, которая, по сути, явилась окончательным методом диагностики причины кишечной непроходимости. В обоих наблюдениях выявлена обструкция желчным конкрементом терминальных отделов тонкой кишки вследствие формирования холецистодуоденального свища. Объем операции также был одинаковым: энтеролитотомия, трансназальная интубация тонкой кишки. Исход лечения в обоих наблюдениях был положительным. Необходимо отметить, что ни в одном из наблюдений не выполнялось устранение существующего холецистодуоденального свища в связи с тяжелой сопутствующей патологией.
Клиническое наблюдение № 2
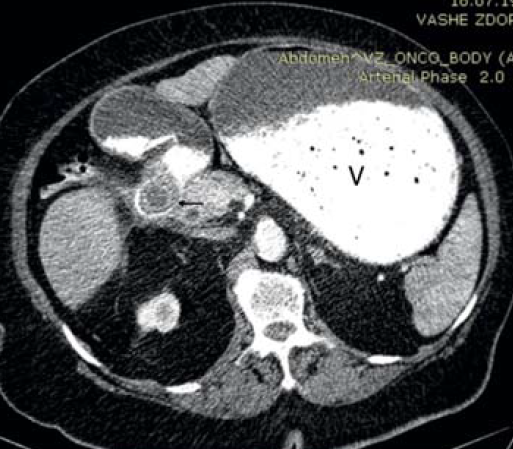
Пациентка, 76 лет, поступила в клинику с жалобами на рвоту съеденной накануне пищей, тяжесть, вздутие в верхних отделах живота, потерю веса, слабость. Из анамнеза – болеет около 3 недель, ранее неоднократно отмечала приступы боли в правом подреберье. При поступлении отмечались вздутие верхних отделов живота, наличие шума «плеска», признаки обезвоживания – сухость и дряблость кожных покровов, явления олигурии. Больная обследована. По данным КТ области брюшной полости в нисходящей ветви двенадцатиперстной кишки определяется слоистый конкремент размерами до 31×25 мм. Стенки нисходящего отдела двенадцатиперстной кишки утолщены, наружный контур нечеткий. Окружающая жировая клетчатка инфильтрирована, в т.ч. между головкой поджелудочной железы и кишкой. Желудок значительно растянут содержимым (рис. 5, 6). Лабораторно обращали на себя внимание явления гиперкоагуляции наряду с повышением уровня эритроцитов и гемоглобина (178×1012/л и 5,86 г/л соответственно), дисэлектролитными расстройствами.
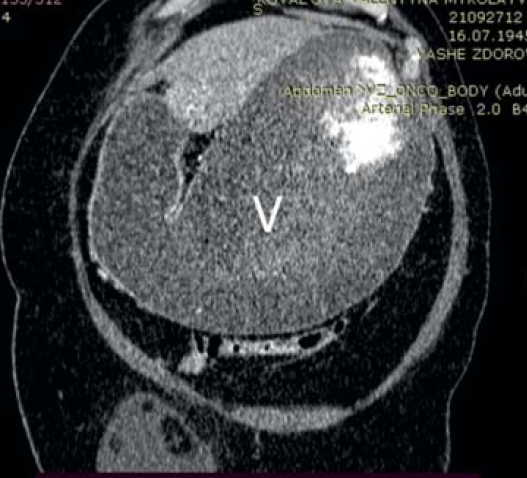
Рис. 5. Компьютерная томограмма, аксиальная проекция: билиарный конкремент (стрелка), обтурирующий просвет двенадцатиперстной кишки в нисходящей части; аэробилия; желудок, растянутый содержимым (V)
Рис. 6. Компьютерная томограмма, фронтальная проекция: выраженное расширение желудка (V) на фоне обтурации двенадцатиперстной кишки конкрементом
По данным эндоскопического исследования у больной определяется вклиненный конкремент в нисходящем отделе двенадцатиперстной кишки, признаки дуоденальной непроходимости. Визуализировать свищевое отверстие, низвести конкремент не представляется возможным.
Больной установлен диагноз: «ЖКБ III ст. Хронический рецидивирующий холецистопанкреатит. Внутренний комбинированный холецистохоледохо(?)-гастральный свищ. Инородное тело (билиарный конкремент) в нисходящей части двенадцатиперстной кишки. Дуоденальная непроходимость».
На фоне консервативного лечения больная подготовлена к плановому оперативному вмешательству. Через 4 сут после поступления оперирована. Выполнена лапаротомия. При ревизии: желудок значительно увеличен в размерах, в его пилорической части определяется плотный конкремент до 4 см в диаметре. В подпеченочном пространстве – грубый рубцовый процесс, в который вовлечены толстая и двенадцатиперстная кишки, пилорический отдел желудка и печеночно-двенадцатиперстная связка. В ходе мобилизации был разъединен комбинированный холецистохоледохо-гастральный свищ с удалением билиарного конкремента. Выполнена холецистэктомия по Прибраму. Дефект холедоха в его супрадуоденальной части до 2/3 окружности. Выполнена гастропластика с заведением зонда в двенадцатиперстную кишку. Сформирован гепатикоеюноанастомоз по Ру. Операция завершена дренированием брюшной полости из двух точек.
Послеоперационный период осложнился желчеистечением до 200 мл/сут. На фоне общего и местного лечения желчеистечение прекратилось на 7-е сутки после операции. Зонд удален на 5-й день после оперативного вмешательства. Также отмечалось нагноение послеоперационной раны, что потребовало дополнительного ее дренирования. Больная выписана на 16-й день после операции под наблюдение хирурга по месту жительства.
Осмотрена через 1 месяц. Жалоб не предъявляет. По результатам ультразвукового исследования – признаки аэробилии. Данных в пользу билиарной гипертензии, холангита нет. По результатам эндоскопического исследования – выявленные изменения соответствуют объему перенесенного вмешательства.
Обсуждение
Синдром Бувере впервые был описан М. Beaussier в 1770 году, а первое сообщение в медицинской литературе об обструкции выходного отдела желудка желчным конкрементом, вклиненным в двенадцатиперстную кишку или желудок, принадлежит именно Л. Бувере, который в 1896 году описал два подобных случая. В дальнейшем все случаи желчнокаменного илеуса получили название синдрома Бувере.
Кишечная непроходимость, обусловленная билиарным конкрементом, является редким и жизнеугрожающим осложнением ЖКБ, встречающимся в 0,15-4,2% клинических случаев. При этом вероятность развития данного осложнения повышается с возрастом и длительностью основного заболевания. Средний возраст пациентов с энтеробилиарными фистулами, по данным литературы, составляет 74,1 года. Большинство пациентов (65%) –женщины с наличием сопутствующих заболеваний. Необходимо отметить, что именно ЖКБ вызывает развитие спонтанных внутренних билиарных фистул в 91-94% наблюдений. Анатомически наиболее часто встречаются холецистодуоденальные фистулы (77-90%), реже – холецистотолстокишечные свищи (8-26%), наиболее редко – патологические холецистогастральные соустья (2%). Кроме того, необходимо отметить, что частота развития внутренних холецистобилиарных свищей (синдрома Мириззи 2 типа) является также достаточно редким осложнением ЖКБ, наблюдающимся в 1% случаев, а комбинация синдрома Мириззи с билио-кишечным сообщением является чрезвычайно редкой.
Обструкция желудочно-кишечного тракта желчным конкрементом в 70% наблюдений возникает в терминальном отделе тонкой кишки или в области илеоцекального клапана, реже наблюдается обструкция в проксимальных отделах тощей или подвздошной кишки (20-40%), а также желудка (14,1%).
Несмотря на развитие методов диагностики как ЖКБ, так и ее осложнений, диагностика билиарного илеуса остается сложной, и в более чем 80% наблюдений причина кишечной непроходимости в таких ситуациях выявляется по данным интраоперационной ревизии.
Современные литературные данные рекомендуют использовать мини-инвазивные методы для лечения синдрома Бувере, включая применение эндоскопических и чрескожных процедур до выполнения открытого хирургического вмешательства. Это связано с тем, что от данной патологии в основном страдают пациенты пожилой и старческой возрастных групп. При этом множественная коморбидность у них делает открытые вмешательства чрезвычайно рискованными. Среди таких методов можно выделить механическую, лазерную, интракорпоральную электрогидравлическую литотрипсию, а также экстракорпоральную ударно-волновую литотрипсию.
Несмотря на определенные успехи, достигнутые при лечении данной патологии с помощью мини-инвазивных вмешательств, 91% больных приходится оперировать в традиционном либо лапароскопическом варианте. Это связано с целым рядом факторов. Во-первых, при размере конкрементов >2,5 см их эндоскопическое извлечение затрудняется и может приводить к эзофагеальной обструкции. Во-вторых, фрагментация крупных конкрементов может приводить к возникновению обструкции терминальных отделов тонкой кишки. В-третьих, выполнение литотрипсии потенциально опасно повреждением кишечной стенки с развитием кишечного кровотечения и/или ее перфорацией. Таким образом, хирургическое вмешательство остается на данный момент основным методом лечения синдрома Бувере.
Хирургическая тактика при данной патологии во многом определяется наличием сопутствующей патологии, соматическим статусом пациента, а также особенностями течения основного заболевания.
Так, гастро- или энтеролитотомия являются основными хирургическими опциями для лечения синдрома Бувере. Вопрос холецистэктомии решается индивидуально: она рекомендована при наличии конкрементов в желчном пузыре для предупреждения рецидивов заболевания и связанных с ними осложнений. Вместе с тем наличие тяжелой сопутствующей патологии, общего тяжелого состояния больного, острого воспалительного процесса в желчном пузыре (при отсутствии деструкции) в ряде случаев приводит к отказу от холецистэктомии в пользу холецистолитотомии с формированием холецистостомы, что значительно снижает риск развития послеоперационных осложнений и летальность.
Наличие энтеробилиарной фистулы приводит к высокой вероятности развития холангита, что особенно важно учитывать у более молодых пациентов, у которых ликвидация патологического соустья является важным моментом хирургического лечения. При этом в случае хорошего соматического статуса больного, отсутствия активного воспалительного процесса в желчном пузыре и гепатодуоденальной связке возможна одновременная ликвидация холецистодигестивного свища с выполнением холецистэктомии и гастро(энтеро)литотомии. При высоком операционном риске требуется двухэтапный подход: на первом этапе ликвидируют причину, вызвавшую кишечную обструкцию, а на втором – разъединяют патологическое билиодигестивное соустье.
При вовлечении в процесс желчных протоков и формировании сложных внутренних билиодигестивных свищей решают вопрос о формировании гепатикоеюноанастомоза на изолированной петле тонкой кишки. Необходимо отметить, что применение подобного дифференцированного подхода позволило снизить летальность при синдроме Бувере с 30 до 12%.
Выводы
Формирование патологических билиодигестивных фистул является редким и потенциально жизнеугрожающим осложнением ЖКБ, в большинстве случаев возникающим у пациентов старшей возрастной группы. Несмотря на развитие эндоскопических и чрескожных технологий лечения, хирургический метод в стандартном или лапароскопическом варианте остается основным в лечении синдрома Бувере.
При выборе тактики хирургического вмешательства необходимо учитывать операционный риск, вероятность развития послеоперационных осложнений, а также тяжесть сопутствующей патологии, на основании которых дифференцированно использовать одно- или двухэтапный подход лечения. Как можно более ранняя диагностика ЖКБ и ее хирургическое лечение позволяют значительно снизить частоту развития осложнений данного заболевания, и в частности – синдрома Бувере.
Литература
- Ferhatoğlu M.F., Kartal A. Bouveret’s Syndrome: A Case-Based Review, Clinical Presentation, Diagnostics and Treatment Approaches. Med Bull Sisli Etfal Hosp 2020;54(1):1-7. DOI: 10.14744/SEMB.2018.03779.
- AL-Habbal Y., Ng M., Bird D., McQuillan T., AL-Khaffaf H. Uncommon presentation of a common disease – Bouveret’s syndrome: A case report and systematic literature review World J Gastrointest Surg 2017 January 27; 9(1): 25-36. DOI: 10.4240/wjgs.v9.i1.25.
- Rodriguez J.E.R. et al. Gallstone ileus associated with cholecystogastric fistula: Case report, diagnosis and surgical treatment International Journal of Surgery Case Reports 2021; 86: 106328. https://doi.org/10.1016/j.ijscr.2021.106328
- Boland M.R., Bass G.A., Robertson I., Walsh T.N. Cholecystogastric fistula: a brief report and review of the literature JSCR2013; 4 (3 pages). doi:10.1093/jscr/rjt028.
- Chatzoulis G., Kaltsas A., Danilidis L., Dimitriou J., Pachiadakis I. Mirizzi syndrome type IV associated with cholecystocolic fistula: a very rare condition-report of a case. BMC Surgery 2007, 7:6 doi:10.1186/1471-2482-7-6.
- Ahmed M.J., Mahmood R., Rana R.S., Pirzada M.T., Haider J., Siddiqui S.S., Alam S.N. Metabolic Syndrome: An Indicator of Complicated Gall Stone Disease? Cureus 10 (11): e3659. DOI 10.7759/cureus.3659.
- Ali M.F., Friedela D., Levin G. Two anomalies in One: A Rare Case of an Intrahepatic Gallbladder with a Cholecystogastric Fistula. Case Rep Gastroenterol 2017;11:148-154. DOI: 10.1159/000462964.
- Purandare S.N., Patil B., Chakane V., Jadhav S.E. Gallstone Bezoar Following Cholecystogastric Fistula: a Rare Sequelae of Cholelithiasis. Indian J Surg (Dec 2015) 77 (Suppl 3): S1403-S1404. DOI 10.1007/s12262-014-1114-6.
- Jaguś D., Karthik A., Tan Z.Y., Mlosek R.K., Białek E: Gallbladder-duodenal fistula detected by ultrasound – a case report. J Ultrason 2020; 20: e214-e217. doi: 10.15557/JoU.2020.0036.
- Nickel F., Müller-Eschner M.M., Chu J., von Tengg-Kobligk H., Müller-Stich B.P. Bouveret’s syndrome: presentation of two cases with review of the literature and development of a surgical treatment strategy. BMC Surgery 2013, 13:33. http://www.biomedcentral.com/1471-2482/13/33 (Электронный ресурс).
- Aamery A., Pujji O., Mirza M. Operative management of cholecystogastric fistula: case report and literature review Journal of Surgical Case Reports, 2019;11:1-2. doi: 10.1093/jscr/rjz345.
- Malenie R., Leone L., Gilliland M.G.F. Sigmoid gallstone ileus: a challenging diagnosis. Autopsy Case Rep [Internet]. 2019 9(2): e2019102. https://doi.org/10.4322/acr.2019.102.
- Fujimoto G. Laparoscopic and endoscopic cooperative surgery for cholecystogastric fistula: A case report. International Journal of Surgery Case Reports. 2020; 71: 116-119. https://doi.org/10.1016/j.ijscr.2020.04.100.