13 грудня, 2021
Можливості та перспективи лікування лімфоми Ходжкіна
.jpg) У міжнародних клінічних настановах щодо лікування онкологічної та онкогематологічної патології стійко закріпилися позиції імунотерапевтичних агентів. Пембролізумаб – гуманізоване моноклональне антитіло з великим переліком показань до застосування, який поступово розширюється. На сьогодні пембролізумаб є терапевтичною опцією для лікування дорослих і дітей з лімфомою Ходжкіна (ЛХ).
У міжнародних клінічних настановах щодо лікування онкологічної та онкогематологічної патології стійко закріпилися позиції імунотерапевтичних агентів. Пембролізумаб – гуманізоване моноклональне антитіло з великим переліком показань до застосування, який поступово розширюється. На сьогодні пембролізумаб є терапевтичною опцією для лікування дорослих і дітей з лімфомою Ходжкіна (ЛХ).
У рамках ХІІІ науково-практичної конференції з міжнародною участю «Сучасні підходи до діагностики та лікування лімфопроліферативних захворювань» про нові можливості та перспективи імунотерапії ЛХ розповіла завідувачка науково-дослідного відділення хіміотерапії гемобластозів та ад’ювантних методів лікування Національного інституту раку (м. Київ), доктор медичних наук, професор Ірина Анатоліївна Крячок.
– У більшості пацієнтів з ЛХ досягається повна відповідь на 1-шу лінію терапії, зокрема за схемами ABVD (доксорубіцин + блеоміцин + вінбластин + дакарбазин), BEACOPP (блеоміцин + етопозид + доксорубіцин + циклофосфамід + вінкристин + прокарбазин + преднізолон) з ескалацією доз, брентуксимабу ведотин + AVD (доксорубіцин + вінбластин + дакарбазин). Ефективність 2-ї лінії терапії при ЛХ також є високою: близько 70-80% пацієнтів на сальвадж-терапії з подальшою трансплантацією гемопоетичних стовбурових клітин (ТГСК) досягають стійкої ремісії. Результати 3-ї лінії терапії (після 2-го рецидиву хвороби, рефрактерності до 2-ї лінії) значно погіршуються, що зумовлює потребу у розробленні нових підходів до лікування. Серед нових підходів до лікування В-клітинних лімфом – застосування ДНК-вакцин, дендритноклітинних вакцин, CAR-T клітинна терапія, імунотерапія.
Створення імунотерапевтичних препаратів стало великим проривом в онкології. За дуже короткий час відбулося стрімке збільшення кількості клінічних досліджень інгібіторів контрольних точок, зокрема для пембролізумабу зареєстровано близько 1000 клінічних досліджень, а лікарський засіб застосовується для лікування раку понад 10 локалізацій.
Імунна система організму може визначити та знищити пухлинні клітини завдяки активації Т-клітинної ланки імунітету та інших механізмів. У сучасних дослідженнях визначено рецептори програмованої смерті (PD-1), які є основним шляхом імунних контрольних точок. Пухлинні клітини здатні пригнічувати Т-клітинну відповідь за рахунок використання шляху PD-1 через експресію PD-1 лігандів – PD-L1 та PD-L2. Зв’язування PD-L1 та PD-L2 з PD-1 на Т-клітинах супроводжується деактивацією останніх, таким чином пухлина ухиляється від імунної відповіді. Дія імунотерапевтичних агентів (пембролізумабу) спрямована на активацію протипухлинного імунітету шляхом блокади взаємодії між PD-1 та PD-L1 і PD-L2.
Клітини ЛХ мають генетичну схильність до блокади сигнального шляху PD-1: у них часто спостерігається ампліфікація ділянки хромосоми 9р24.1, що запускає сигнальний шлях JAK2/STAT, який активує підвищену експресію PD-L1 та PD-L2. Таким чином, клітини ЛХ також є мішенню для моноклонального антитіла пембролізумабу.
Міжнародні клінічні настанови
Згідно з останніми оновленнями клінічних настанов Національної онкологічної мережі США (NCCN) щодо ведення пацієнтів з ЛХ (версія 4, 2021), пембролізумаб є терапевтичною опцією для 2-ї та подальших ліній терапії при ЛХ. Згідно з клінічними настановами NCCN щодо інгібіторів контрольних точок і затвердженими Управлінням з контролю якості харчових продуктів і лікарських препаратів США (FDA) показаннями, ніволумаб застосовується для лікування дорослих із класичною ЛХ, у яких виник рецидив або прогресування хвороби після проведення аутологічної ТГСК (аутоТГСК) чи використання брентуксимабу ведотину, після більше ніж 3 ліній системної терапії, яка включає аутоТГСК. Пембролізумаб застосовується для лікування дітей і дорослих із рефрактерною класичною ЛХ, а також тих, хто мав рецидив після більше ніж 3 попередніх ліній терапії.
За основу рекомендацій із застосування пембролізумабу при ЛХ взяті результати клінічних досліджень Keynote-013 (I фаза), Keynote-087 (II фаза) та Keynote-204 (III фаза).
Дослідження Keynote-013
У дослідженні Keynote-013 вивчали ефективність і безпеку пембролізумабу у 31 пацієнта зі злоякісними онкогематологічними захворюваннями. У дослідження були включені особи, які мали рецидивуючу/рефрактерну ЛХ, прогресування хвороби під час або після лікування брентуксимабу ведотином. Пацієнти отримували пембролізумаб у дозі 10 мг/кг маси тіла через кожні 2 тижні. Відповідь на терапію оцінювали через 12 тижнів, далі – через кожні 8 тижнів. За результатами дослідження частота об’єктивної відповіді (ЧОВ) склала 58%, повна відповідь (ПВ) була досягнута у 19% хворих. Підгруповий аналіз показав зіставну ефективність пембролізумабу у пацієнтів з первинно рефрактерним і непервинно рефрактерним захворюванням. Медіана виживаності без прогресування (ВБП) склала 11,4 міс, (95% довірчий інтервал – ДІ – 4,9-27,8), а 12-місячна ВБП – 48%. Медіана загальної виживаності не була досягнута, 12-місячна загальна виживаність – 87%. Найчастішими побічними явищами (ПЯ) усіх ступенів тяжкості були гіпотиреоїдизм, діарея, пневмоніт, нудота, втома, задишка (P. Armand et al., 2020).
Дослідження Keynote-087
У клінічне дослідження II фази Keynote-087 було включено 3 групи пацієнтів з рефрактерною/рецидивною класичною ЛХ, у яких відбулося прогресування хвороби: після аутоТГСК і наступної терапії брентуксимабу ведотином (група 1); при неефективності резервної поліхіміотерапії, терапії брентуксимабу ведотином у разі неможливості виконання аутоТГСК (група 2); після аутоТГСК без подальшого застосування брентуксимабу ведотину (група 3). Більшість пацієнтів отримували ≥3 попередніх лінії терапії.
Хворим було призначено пембролізумаб у дозі 200 мг через кожні 3 тижні. Ефективність терапії оцінювали через кожні 12 тижнів.
За результатами дослідження ЧОВ склала 69,0% (95% ДІ 62,3-75,2), частота ПВ – 22,4% (95% ДІ 16,9-28,6). Середній час до відповіді на терапію становив 2,7 (95% ДІ 2,1-8,3) міс. У пацієнтів, у яких отримано відповідь на терапію, медіана тривалості відповіді склала 11,1 міс (R. Chen et al., 2017). При 3-річному періоді спостереження медіана загальної тривалості відповіді дорівнювала 16,6 міс, медіана тривалості відповіді у групі 1 – 25,0 міс, у групі 2 – 11,1 міс, групі 3 – 16,8 міс. Медіана ВБП у всіх групах пацієнтів становила 13,6 міс (95% ДІ 11,1-16,7); у групі 1 – 16,4 міс, 2 – 11,1 міс, 3 – 19,4 міс. Найчастішими ПЯ будь-якого ступеня тяжкості, що виникали у ≥5% пацієнтів, були гіпотиреоїдизм, лихоманка, втома, висип на шкірі, діарея, головний біль, нудота, кашель (P.L. Zinzani et al., 2019).
Дослідження Keynote-204
Метою відкритого рандомізованого дослідження III фази Keynote-204 було порівняти ефективність пембролізумабу та брентуксимабу ведотину у пацієнтів з рефрактерною/рецидивною класичною ЛХ. У клінічне дослідження було включено пацієнтів ≥18 років, яким виконано аутоТГСК, а також хворих, які не є кандидатами для аутоТГСК, з вимірюваною хворобою та статусом за ECOG 0 або 1. Пацієнти були рандомізовані у співвідношенні 1:1 у групу пембролізумабу (200 мг через кожні 3 тижні) та брентуксимабу ведотину (1,8 мг через кожні 3 тижні).
Результати проміжного аналізу показали перевагу пембролізумабу над брентуксимабу ведотином. Медіана ВБП у групі пембролізумабу становила 13,2 міс, у групі брентуксимабу ведотину – 8,3 міс (відношення ризиків – ВР – 0,65; 95% ДІ 0,48-0,88; p=0,00271), 12-місячна ВБП – 53,9 та 35,6% відповідно (рис. 1).
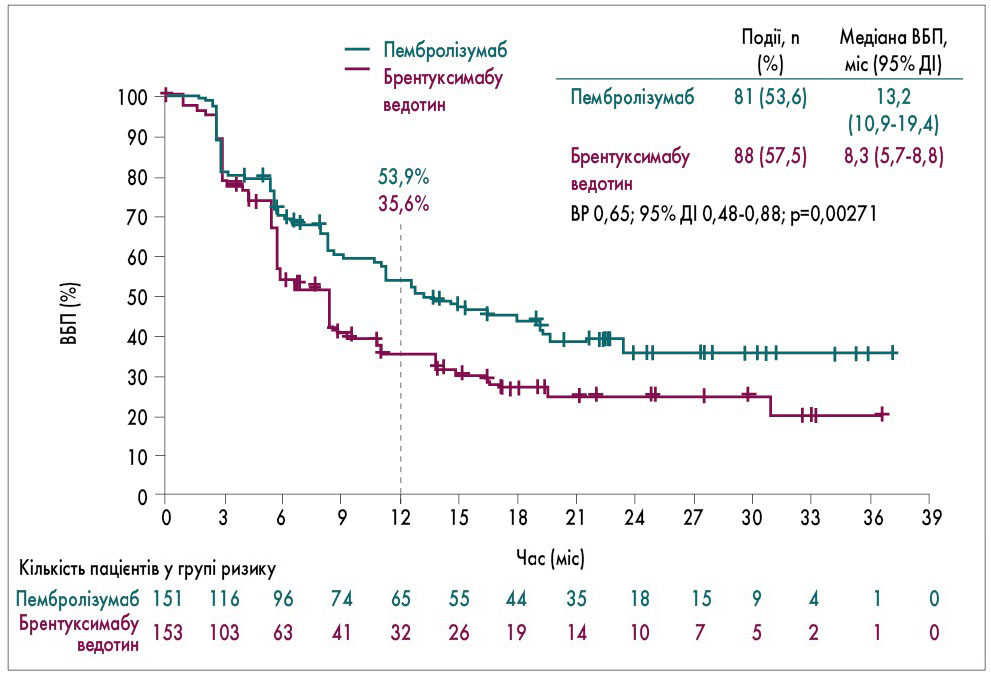 Рис. 1. ВБП у дослідженні Keynote-204
Рис. 1. ВБП у дослідженні Keynote-204
Перевага пембролізумабу спостерігалася в усіх підгрупах пацієнтів: яким не проводили аутоТГСК, з первинною рефрактерністю хвороби, а також у пацієнтів, які отримували/не отримували попереднє лікування брентуксимабу ведотином. ЧОВ у групі пембролізумабу склала 65,6% (95% ДІ 57,4-73,1%), у групі брентуксимабу ведотину – 54,2% (95% ДІ 46,0-62,3), частота ПВ у групах була приблизно на однаковому рівні (24,5 та 24,2% відповідно).
В обох групах спостерігалася зіставна частота ПЯ, однак за клінічними проявами вона була різною. У групі пембролізумабу частіше виникали гіпотиреоїдизм, лихоманка, свербіж, втома, нудота, у групі брентуксимабу ведотину – периферична нейропатія, периферична сенсорна нейропатія, а також нудота, втома. ПЯ при застосуванні пембролізумабу є імунно-опосередкованими, тому важливо їх розпізнати та провести корекцію (рис. 2; J. Kuruvilla et al., 2020).
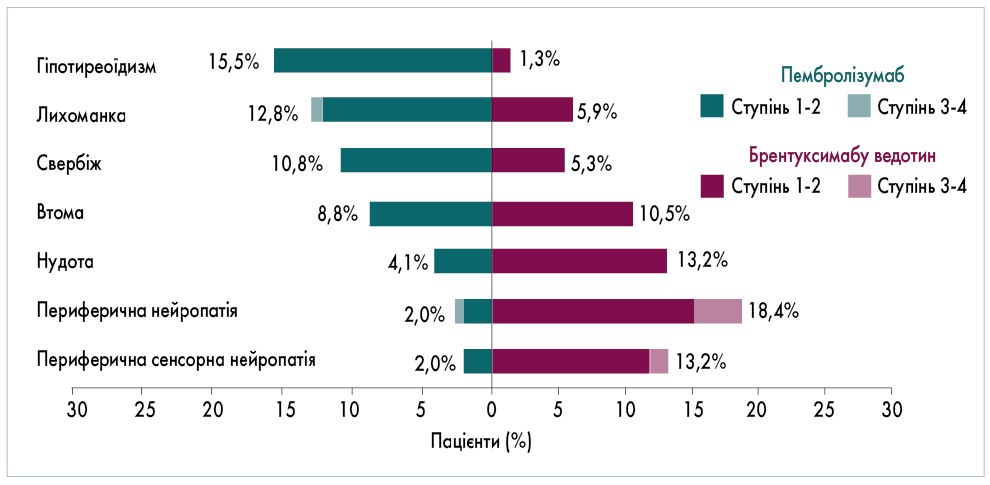 Рис. 2. Порівняння ПЯ при лікуванні пембролізумабом і брентуксимабу ведотином (Keynote-204)
Рис. 2. Порівняння ПЯ при лікуванні пембролізумабом і брентуксимабу ведотином (Keynote-204)
За результатами підгрупового аналізу дослідження Keynote-204 залежно від кількості попередніх ліній терапії (1 або ≥2 ліній терапії) відзначено перевагу пембролізумабу над брентуксимабу ведотином в обох підгрупах за показниками ВБП, ЧОВ, тривалістю відповіді (J. Kuruvilla et al., 2020).
Таким чином, за результатами досліджень у пацієнтів з рефрактерною/рецидивною ЛХ, у яких виник рецидив після ТГСК або які не є кандидатами на проведення ТГСК, лікування пембролізумабом значно збільшує ВБП порівняно з брентуксимабу ведотином. На тлі лікування пембролізумабом вдається досягти більш стійкої відповіді. Пембролізумаб рекомендований для терапії дорослих і дітей із рефрактерною ЛХ та рецидивом хвороби.
Підготувала Ілона Цюпа
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 5 (72) 2021 р.



