31 грудня, 2021
Порівняння МРТ-керованої цільової та стандартної біопсії при скринінгу раку передміхурової залози
Високі показники гіпердіагностики є основною перепоною для організованого скринінгу раку передміхурової залози (РПЗ). Цю проблему можна вирішити застосуванням магнітно-резонансної томографії (МРТ) із цільовою біопсією, однак досі не з’ясовано, чи придатний такий метод для організованого скринінгу РПЗ.
Автори провели популяційне дослідження, у якому вивчали, чи не поступається експериментальна методика скринінгу РПЗ за ефективністю стандартній. До участі у скринінгу були запрошені чоловіки віком від 50 до 74 років із загальної популяції; учасники з рівнями простат-специфічного антигена (ПСА) ≥3 нг/мл були рандомно розподілені по групах у співвідношенні 2:3 для проходження стандартної біопсії (група стандартної біопсії) та МРТ-керованої цільової та стандартної біопсії, якщо за результатами МРТ у них діагностували ознаки, характерні для РПЗ (група експериментальної біопсії).
За даними цього популяційного дослідження з особистим запрошенням учасників встановлено, що МРТ із цільовою та стандартною біопсією у чоловіків із МРТ-ознаками раку простати не поступається стандартній біопсії за ефективністю виявлення клінічно значущого РПЗ. Випадків діагностики клінічно незначущого раку було менше, ніж в умовах звичайного скринінгу.
Ключові слова: рак передміхурової залози, скринінг, стандартна біопсія, МРТ-керована цільова та стандартна біопсія.
Організований скринінг раку передміхурової залози (РПЗ), під час якого визначають рівень простат-специфічного антигена (ПСА), а згодом у чоловіків із підвищеним рівнем ПСА проводять систематичну трансректальну біопсію простати під ультразвуковим контролем, знижує рівень смертності від РПЗ [1, 2]. Однак скринінг із визначенням рівня ПСА також призводить до високих показників гіпердіагностики та лікування клінічно незначущого РПЗ і частого виконання біопсії в осіб, яким вона не показана [3, 4]. З огляду на це у жодній країні, крім Литви, немає загальнообов’язкових скринінгових програм для діагностики РПЗ [5].
Для вдосконалення діагностики РПЗ вчені почали активно застосовувати метод МРТ [6], за допомогою якого можна виявити ділянки простати з імовірним раковим ураженням і провести цільову біопсію залози, зменшивши кількість біопсій, які виконують у пацієнтів без видимих уражень [7, 8]. Проведено низку досліджень за участю чоловіків, яким призначено біопсію через клінічну підозру на наявність РПЗ. Виконання цільової біопсії в осіб із позитивними результатами МРТ (тобто ознаками, характерними для РПЗ) призводило до меншого виявлення клінічно незначущих видів раку, ніж під час стандартної біопсії, однак мало подібну або кращу здатність до виявлення клінічно значущих видів раку [9-12].
Мета дослідження – оцінити ефективність МРТ-керованої цільової біопсії під час популяційного скринінгу РПЗ.
У ході дослідження STHLM3-MRI автори порівняли кілька різних методик скринінгу із застосуванням комбінації прогнозування ризику, МРТ-керованої цільової та стандартної біопсії у популяційному організованому скринінгу із запрошенням учасників [13, 14]. У цій статті автори порівняли результати застосування МРТ-керованої цільової біопсії, поєднаної зі стандартною біопсією, у чоловіків із позитивними результатами МРТ та стандартної методики скринінгу в учасників із підвищеним рівнем ПСА (≥3 нг/мл).
Дизайн та огляд дослідження
Дослідження STHLM3-MRI – проспективне рандомізоване популяційне дослідження серед чоловіків віком 50-74 років, у межах якого автори оцінили різні методики скринінгу для виявлення РПЗ. У цій статті автори навели результати аналізів, проведених до збору даних, за допомогою яких вони встановили, що застосування у чоловіків із МРТ-ознаками РПЗ цільової і стандартної біопсії (група експериментальної біопсії) є не менш ефективним для виявлення клінічно значущого РПЗ при скринінгу раку, ніж стандартна біопсія (група стандартної біопсії).
Для проведення дослідження STHLM3-MRI вчені використали дизайн, у якому поєднано етап парного позитивного скринінгу (всі учасники підлягали двом скринінговим дослідженням) і рандомізований розподіл між групою експериментальної або стандартної біопсії всіх учасників, які отримали позитивні результати за даними будь-якого зі скринінгових досліджень [16-18]. На етапі парного скринінгу автори застосували визначення рівня ПСА та модель «Стокгольм-3», за допомогою яких оцінили ризик РПЗ серед залучених до скринінгу учасників.
Дослідження «Стокгольм-3» – це модель прогнозування ризику, заснована на клінічних змінних (вік, наявність РПЗ серед родичів першого ступеня споріднення та дані попередньої біопсії), біомаркерах крові (рівні загального та вільного ПСА, співвідношення рівнів вільного та загального ПСА, людський калікреїн 2, макрофаг-інгібуючий цитокін 1 і β-мікросемінопротеїн), а також на оцінюванні полігенного ризику для прогнозування ризику РПЗ за шкалою Глісона (≥7 балів) [19, 20]. Учасники із підвищеним рівнем ПСА (≥3 нг/мл) або відповідними оцінками за даними моделі «Стокгольм-3» (≥11%) були рандомно розподілені у співвідношенні 2:3 до групи стандартної чи експериментальної біопсії (рандомізовані за допомогою генерованих комп’ютером блоків із п’яти груп і стратифіковані за шістьома класами ризику раку, визначеними відповідно до розподілу ризиків у моделі «Стокгольм-3»). Дизайн дослідження забезпечив аналітичну основу, за допомогою якої можна було порівняти кілька різних процесів (або методик) скринінгу, враховуючи поєднання показань для призначення біопсії (тобто наявності лише підвищеного рівня ПСА, лише позитивної оцінки за моделлю «Стокгольм-3», або наявності підвищеного рівня ПСА і відповідної оцінки за моделлю «Стокгольм-3»), та методи біопсії (стандартну, МРТ-керовану цільову або МРТ-керовану цільову та стандартну [біопсію в експериментальній групі виконували лише у чоловіків із ознаками раку за даними МРТ]).
У наведених далі аналізах вчені дослідили безпечність та ефективність стандартної біопсії, порівнявши її з методикою скринінгу, для якої застосовували МРТ-керовану цільову біопсію. Єдиним показанням до призначення МРТ або стандартної біопсії був рівень ПСА ≥3 нг/мл (узгоджено з показаннями, що застосовували у Європейському рандомізованому дослідженні скринінгу на РПЗ – ERSPC). Дослідники, які проводили ERSPC, навели докази 1-го рівня про те, що серед чоловіків, які підлягали організованому скринінгу рівня ПСА, рівень смертності від РПЗ був нижчим, ніж серед осіб, які такому скринінгу не підлягали [1, 2]. Якщо точніше: хоча показанням до рандомізованого розподілу та подальшої біопсії був підвищений рівень ПСА (≥3 нг/мл) або позитивна оцінка за моделлю «Стокгольм-3», до наведеного тут аналізу було залучено виключно учасників, які пройшли рандомізацію і мали рівень ПСА ≥3 нг/мл, незалежно від їхньої оцінки за моделлю «Стокгольм-3».
Результати
Первинним результатом дослідження була ймовірність виявлення клінічно значущого РПЗ, яку визначали як відсоток учасників у кожній групі, котрим встановлено діагноз раку на підставі оцінки за шкалою Глісона 3+4 або вище (ступінь диференціації ≥2 за рекомендаціями Міжнародного товариства урологічної патології). Шкала Глісона передбачає оцінювання первинного ступеня диференціації (переважаюча оцінка пухлини) та вторинного (найвища з непереважаючих оцінок): загальну суму отримують, складаючи значення первинного і вторинного ступенів диференціації. Загальна оцінка за шкалою Глісона становить від 6 до 10 балів; при цьому вищі бали свідчать про більш агресивну форму РПЗ. Вторинними результатами дослідження були: виявлення ймовірності (тобто пропорції) біопсій із доброякісними результатами, діагностування клінічно незначущого раку (яким вважався рак, оцінений за шкалою Глісона як 3+3, або рак 1 ступеня за даними Міжнародного товариства урологічної патології), виявлення раку з оцінкою за шкалою Глісона 4+3 або вище (ступінь диференціації ≥3 за даними Міжнародного товариства урологічної патології) і настання тяжких побічних явищ (інфекцій, що потребували антибіотикотерапії, госпіталізації або призводили до смерті впродовж 30 днів після біопсії) у кожній групі.
За всіма учасниками стежили щонайменше протягом 200 днів після отримання результатів дослідження рівня ПСА. За чоловіками, які пройшли біопсію, спостерігали протягом щонайменше 30 днів після біопсії, щоб виявити можливі негативні наслідки. За учасниками, яким було виконано радикальну простатектомію до 22 жовтня 2020 р., спостерігали до отримання результатів патологоанатомічного дослідження видаленої простати.
Досліджувана популяція
Усього з лютого 2018 р. по березень 2020 р. до участі в дослідженні було запрошено 49 118 чоловіків, з яких 12 750 осіб погодилися на скринінг і надали зразки крові для дослідження; 2293 особи мали рівень ПСА ≥3 нг/мл або оцінку у дослідженні «Стокгольм-3» ≥11% і пройшли рандомізацію. У представлених у цій статті аналізах були використані дані учасників із рівнем ПСА ≥3 нг/мл, незалежно від оцінки за моделлю «Стокгольм-3» (1532 учасники); 929 осіб були випадково розподілені до групи експериментальної біопсії, а 603 – до групи стандартної біопсії. Характеристики пацієнтів на початку лікування були зіставними в обох групах. У групі експериментальної біопсії 338 (36%) учасникам виконано біопсію: 297 – на підставі отриманої оцінки ≥3 бали за системою PI-RADS (система оцінювання зображень МРТ і обробки отриманих даних), 34 – на підставі отриманого за моделлю «Стокгольм-3» ризику ≥25%, незважаючи на негативні результати МРТ, та 7 – на підставі рішення лікаря-дослідника скасувати протокол дослідження з отриманою медіанною кількістю 15 біоптатів. У групі стандартної біопсії 438 (73%) учасників пройшли біопсію (із медіанною кількістю 12 отриманих біоптатів). У всій популяції, що підлягала втручанню, абсолютна різниця між відсотковим значенням кількості чоловіків, які перенесли біопсію, становила 36 відсоткових пунктів (95% довірчий інтервал [ДІ]: від -41 до -32); за даними аналізу зі зважуванням зворотної ймовірності, абсолютна різниця між групами становила -55 відсоткових пунктів (95% ДІ: від -58 до -51).
Результати біопсії
За результатами аналізу, проведеного в усій популяції, що підлягала втручанню, діагноз клінічно значущого раку встановили у 192 із 929 учасників (21%) із групи експериментальної біопсії, натомість як у групі стандартної біопсії цей діагноз отримали 106 із 603 учасників (18%), різниця між групами становила 3 відсоткові пункти (95% ДІ: від -1 до 7) (рис. 1). Оскільки нижня межа двостороннього 95% ДІ охоплювала показник -4 відсоткових пункти, дослідники зробили висновок, що експериментальна методика не поступається стандартній за ефективністю виявлення клінічно значущого раку (p<0,001). За результатами аналізу показників пацієнтів, які виконали всі вимоги протоколу дослідження, клінічно значущий рак було виявлено у 183 із 790 учасників (23%) в експериментальній групі біопсії, а у групі стандартної біопсії – у 105 із 436 учасників (24%). Результати множинного відновлення даних із застосуванням моделювання були зіставними з результатами, отриманими в усій популяції, що підлягала втручанню, і відповідали дослідницькій презумпції про випадкову втрату даних. Результати аналізу зі зважуванням зворотної ймовірності були також зіставними з результатами, отриманими в усій популяції, що підлягала втручанню.
 Рис. 1. Застосування аналізу в усій популяції, що підлягала втручанню, аналізу з відновленням даних та аналізу зі зважуванням зворотної ймовірності для обробки первинних результатів дослідження: визначення ймовірності виявлення клінічно значущого раку
Рис. 1. Застосування аналізу в усій популяції, що підлягала втручанню, аналізу з відновленням даних та аналізу зі зважуванням зворотної ймовірності для обробки первинних результатів дослідження: визначення ймовірності виявлення клінічно значущого раку
Чорні ромби позначають абсолютну різницю між групами стандартної та експериментальної біопсії у ймовірності виявлення клінічно значущого РПЗ (оцінка за шкалою Глісона ≥7). До аналізу всієї популяції, що підлягала втручанню, залучено всіх учасників із рівнем ПСА ≥3 нг/мл, які пройшли рандомізацію. Дослідники виконали множинне відновлення даних із застосуванням моделювання, визначеного до збору даних, під час якого результати біопсії для учасників, які пройшли рандомізацію, але не підлягали біопсії, були підставлені автоматично, відповідно до моделі оцінки ризику «Стокгольм-3» у групі стандартної біопсії та відповідно до моделі оцінки ризику «Стокгольм-3 у поєднанні з оцінкою за системою PI-RADS у групі експериментальної біопсії. Крім того, дослідники провели аналіз зі зважуванням зворотної ймовірності, щоб врахувати випадки неповного дотримання протоколу дослідження. Якщо нижня межа двостороннього 95% ДІ для міжгрупової різниці у ймовірності виявлення раку (група експериментальної біопсії мінус група стандартної біопсії) охоплювала показник -4 відсоткових пункти (пунктирна вертикальна лінія), виконання МРТ-керованої цільової та стандартної біопсії у чоловіків із МРТ-ознаками РПЗ (оцінка за системою PI-RADS ≥3) вважалося не менш ефективним, ніж стандартна методика. Якщо нижня межа знаходилась вище нуля (суцільна вертикальна лінія), МРТ-керована цільова біопсія зі стандартною біопсією вважалась більш ефективною, ніж стандартна методика. Представлені p-значення підтверджують не меншу ефективність експериментальної методики біопсії порівняно зі стандартною.
За даними аналізу, проведеного в усій популяції, що підлягала втручанню, клінічно незначущий рак діагностували в меншої кількості учасників із групи експериментальної біопсії порівняно з групою стандартної біопсії (41 [4%] проти 73 [12%]); міжгрупова різниця становила -8 відсоткових пунктів (95% ДІ: від -11 до -5). Крім того, в експериментальній групі, на відміну від групи стандартної біопсії, було менше учасників із доброякісними результатами біопсії (105 [11%] проти 259 [43%]); міжгрупова різниця становила -32 відсоткові пункти (95% ДІ: від -36 до -27). Ці відмінності були більш помітними за даними аналізу зі зважуванням зворотної ймовірності, у якому різниця ефективності діагностики клінічно незначущого раку між групою експериментальної та стандартної біопсії становила -11 відсоткових пунктів (95% ДІ: від -15 до -7). За даними цього ж аналізу, міжгрупова різниця за кількістю біопсій із доброякісними результатами становила -46 відсоткових пунктів (95% ДІ: від -52 до -41). На рис. 2 узагальнено відповідну відносну кількість втручань та кількість клінічно значущих і незначущих форм раку, виявлених за допомогою кожної діагностичної методики, розрахованих на 10 000 обстежених чоловіків.
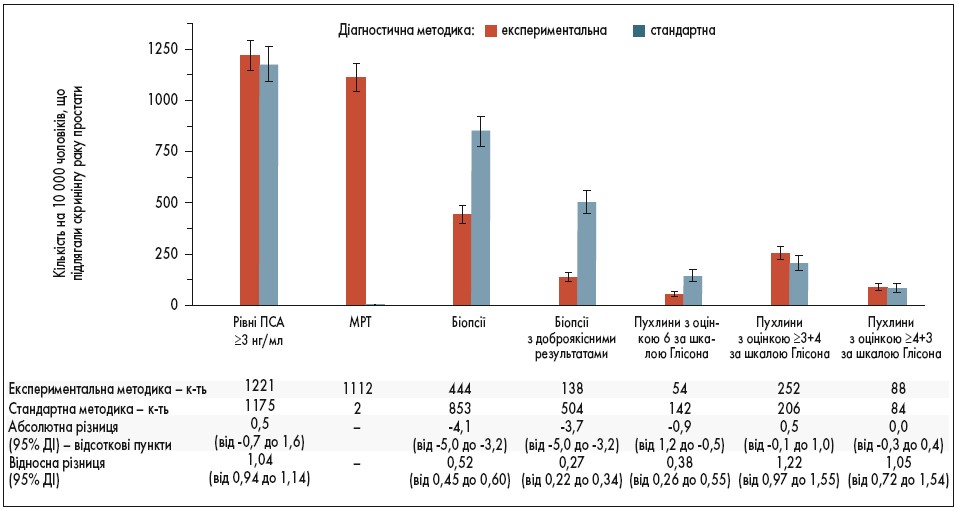 Рис. 2. Пацієнти з підвищеним рівнем ПСА, виконаними втручаннями і виявленим раком
Рис. 2. Пацієнти з підвищеним рівнем ПСА, виконаними втручаннями і виявленим раком
Стовпчики позначають відносні показники, отримані в дослідженні STHLM3-МРТ, розраховані на 10 000 чоловіків віком 50-74 років, які підлягали скринінгу РПЖ. Червоні стовпчики представляють результати застосування скринінгової методики з використанням МРТ, що виконували у групі експериментальної біопсії (визначення рівня ПСА з подальшим МРТ для учасників із рівнем ПСА ≥3 нг/мл та комбінована біопсія у чоловіків із МРТ-ознаками раку). Сині стовпчики представляють результати застосування скринінгової методики, що виконували у групі стандартної біопсії (визначення рівня ПСА із подальшою стандартною біопсією у чоловіків із рівнем ПСА ≥3 нг/мл). Оцінка за шкалою Глісона складається з оцінки первинного ступеня диференціації (переважаюча оцінка пухлини) та вторинного (найвища з непереважаючих оцінок); щоб отримати загальний бал за шкалою, оцінки первинного і вторинного ступенів складають. Загальний бал за шкалою Глісона становив від 6 до 10, при цьому вищі бали свідчили про більш агресивну форму РПЗ. Враховуючи розшифрування оцінки за шкалою Глісона, можна припустити, що оцінка за шкалою Глісона 4+3 бали зазвичай означає більш несприятливий прогноз, ніж 3+4 бали, хоча сума обох показників становить 7. Блоки «І» позначають 95% ДІ.
За даними аналізу підгруп встановлено, що в межах всієї популяції, яка підлягала втручанню, відмінності експериментальної та стандартної методик біопсії у ймовірності виявлення значущого та незначущого раку були зіставними у підгрупах, виділених за віком і рівнем ПСА, у підгрупі чоловіків, які підлягали попередній біопсії й отримали негативний результат, та підгрупі, яка не підлягала попередній біопсії.
Неврахування результатів біопсії серед учасників, які отримали негативні результати за даними МРТ, але мали високий ризик виникнення раку (оцінка за моделлю «Стокгольм-3» ≥25%), призвело до того, що у групі експериментальної біопсії було виявлено на 6 випадків менше клінічно значущого раку та на 5 випадків менше клінічно незначущого раку, ніж у групі стандартної біопсії. Навіть незважаючи на це в межах популяції, що підлягала втручанню, експериментальна методика вважалася не менш ефективною, ніж стандартна.
Виключивши стандартну біопсію, дослідники виявили, що застосування лише МРТ-керованої цільової біопсії у групі експериментальної біопсії зменшило ймовірність виявлення клінічно значущого раку у всій популяції, що підлягала втручанню, до 17% (162 із 929 учасників), й експериментальна методика більше не відповідала критерію не меншої ефективності на 2,5% альфа-рівні (різниця: -0,1 відсоткового пункту; 95% ДІ: від -4 до 4).
Побічні явища
Серед усієї популяції, яка підлягала втручанню, 20 учасників (2%) із групи експериментальної біопсії та 23 особи (4%) із групи стандартної біопсії мали після проведення біопсії інфекції, які лікували антибіотиками (різниця: -2 відсоткові пункти; 95% ДІ: від -4 до 0,1). Частота госпіталізації становила 13 (1%) учасників у групі експериментальної біопсії та 17 (3%) – у групі стандартної біопсії (різниця: -1 відсотковий пункт; 95% ДІ: від -3 до 0,1). В обох групах протягом усього періоду дослідження не було зареєстровано жодного летального випадку.
Обговорення
Високі показники гіпердіагностики раку та значна кількість біопсій простати, проведених за відсутності належних показань, є основними причинами, за якими програми скринінгу РПЗ не проводять на державному рівні [3-5]. За результатами цього популяційного дослідження з особистим запрошенням учасників, ймовірність виявлення клінічно незначущих пухлин й отримання доброякісних результатів біопсії у чоловіків із підвищеним рівнем ПСА (≥3 нг/ мл) була нижчою (на 64 та 74% відповідно) при проведенні біопсії тільки у чоловіків із позитивними результатами МРТ, ніж при виконанні стандартної методики біопсії. Ці результати не вплинули на частоту діагностики клінічно значущих форм раку. Крім того, у групі експериментальної біопсії було виявлено менше інфекцій, ніж у групі стандартної біопсії (хоча ця різниця не є статистично значущою для рівня значущості: 5%). Це зумовлено тим, що в експериментальній групі біопсії підлягала менша кількість учасників, ніж у групі стандартної біопсії.
Висновки
За даними цього популяційного дослідження з особистим запрошенням учасників виявлено, що серед чоловіків із підвищеним рівнем ПСА проведення комбінованої біопсії лише на підставі позитивних результатів МРТ є не менш ефективним для виявлення клінічно значущого РПЗ, ніж стандартна біопсія. Застосування цієї методики зменшує кількість біопсій, виконаних без належних показань, та випадків виявлення клінічно незначущих форм раку. Отже, застосування даної методики може вирішити проблеми, що перешкоджають державній імплементації популяційного скринінгу РПЗ. Порівнюючи показники, розраховані на 10 000 чоловіків віком 50-74 років із підвищеним рівнем ПСА (≥3 нг/мл), направлених на біопсію, у групі, де застосовували комбіновану методику біопсії у чоловіків із позитивними результатами МРТ, виконано на 409 менше біопсій, була на 366 меншою кількість біопсій із доброякісними результатами та виявлено на 88 менше клінічно незначущих онкологічних захворювань, ніж у стандартній групі. У відносних показниках – це відповідно на 48, 73 і 62% менше, ніж у стандартній групі (рис. 2).
Менша кількість біопсій та скорочення пов’язаних із ними медичних витрат дозволить заощадити кошти у сфері охорони здоров’я.
Підготувала Анна Сакалош
За матеріалами: Eklund M., Jaderling F., Discacciati A. et al. MRI-Targeted or Standard Biopsy in Prostate Cancer Screening. NEJM; Published online 9 July 2021.
Тематичний номер «Урологія. Нефрологія. Андрологія» № 4 (25), 2021 р.



