24 січня, 2022
Платиночутливий рецидивуючий рак яєчника: нові можливості лікування
Одним із найпоширеніших злоякісних новоутворень жіночої репродуктивної системи, яке посідає перше місце у структурі смертності від онкогінекологічної патології, є рак яєчника (РЯ). Висока смертність жінок унаслідок РЯ зумовлена відсутністю скринінгу та малосимптомним перебігом захворювання, що в результаті призводить до пізньої діагностики та низької ефективності лікування.
За ініціативи Національної асоціації онкологів України 4 вересня пройшла національна науково-практична конференція з міжнародною участю «Досягнення в клінічній онкології в 2021 році: прорив в терапії раку яєчників», наукова програма якої була представлена на високому рівні кращими фахівцями онкологічної галузі.
 Завідувачка хіміотерапевтичного відділення № 2 КНП «Харківський обласний центр онкології» Наталія Миколаївна Отченаш виступила з доповіддю «Платиночутливий рецидивуючий РЯ з мутаціями в генах BRCA1/2: як довго можна контролювати хворобу».
Завідувачка хіміотерапевтичного відділення № 2 КНП «Харківський обласний центр онкології» Наталія Миколаївна Отченаш виступила з доповіддю «Платиночутливий рецидивуючий РЯ з мутаціями в генах BRCA1/2: як довго можна контролювати хворобу».
– Відомо, що кожен гістологічний підтип РЯ характеризується різними генетичними особливостями. Серозний РЯ високого ступеня злоякісності розвивається у 70% випадків і характеризується наявністю генетичних мутацій (зокрема, в генах BRCA1 чи BRCA2) та геномних аберацій, які призводять до дефіциту гомологічної рекомбінації ДНК пухлинної клітини (J. Prat et al., 2012; S. Banerjee et al., 2013).
Одним із лікарських засобів, який селективно викликає загибель BRCA-позитивних пухлин, не впливаючи на здорові клітини, є PARP-інгібітор олапариб (Лінпарза). Він має важливе значення у підтримуючій терапії рецидивуючого платиночутливого РЯ. Головною метою лікування рецидивуючого РЯ є подовження ремісії у 1-й та 2-й лініях терапії шляхом призначення підтримуючого лікування після початкової хіміотерапії, оскільки з кожною наступною лінією відбувається скорочення періоду ремісії і розвивається резистентність до препаратів (M. Markman et al., 2000; L.C. Hanker et al., 2012). Підтримуюча терапія проводиться з метою запобігання розвитку рецидиву та впливу на мінімальну резидуальну пухлину та пухлинну ДНК, яка не ідентифікується після первинного лікування. Крім того, застосування підтримуючої терапії сприяє сповільненню росту пухлини при поширеному процесі та частковій відповіді (ЧВ) на первинне лікування, що дає змогу відтермінувати прогресування захворювання і збільшити загальну виживаність (ЗВ). Застосування олапарибу як підтримуючої терапії при платиночутливому серозному РЯ після позитивної відповіді на терапію препаратами платини дає змогу подовжити виживаність без прогресування (ВБП) та відстрочити рецидив (L. Mei et al., 2013; M. Markman et al., 2000; J.A. Ledermann et al., 2019).
У рекомендаціях Національної онкологічної мережі США зазначено, що тестуванню на наявність мутацій BRCA підлягають пацієнтки з епітеліальним РЯ (в тому числі з раком маткових труб і первинним перитонеальним раком) будь-якого віку. У настановах Європейського товариства медичної онкології (ESMO) вказано, що тестування на наявність мутацій BRCA1/2 рекомендоване всім пацієнткам з немуцинозним РЯ, а також що PARP-інгібітори є найбільш ефективними у хворих із мутаціями BRCA1/2 (N. Colombo et al., 2019).
SOLO-2 – перше клінічне дослідження III фази, в якому використано нову лікарську форму олапарибу (таблетки) при рецидивуючому РЯ з мутацією BRCA (BRCAm). У цьому дослідженні брали участь пацієнтки з рецидивуючим серозним чи ендометріоїдним РЯ високого ступеня злоякісності, чутливим до препаратів платини, з підтвердженими гермінальними чи соматичними мутаціями BRCA1/2, частковою чи повною відповіддю (ПВ) на останній цикл хіміотерапії на основі препаратів платини (мінімум 4 цикли) та загальним функціональним статусом за ECOG 0-1. Учасниць дослідження було рандомізовано у співвідношенні 2:1 у дві групи: в 1-й (n=196) хворі отримували олапариб, у 2-й (n=99) – плацебо (E. Pujade-Lauraine et al., 2017). Пацієнтки приймали 300 мг олапарибу у формі таблеток (2 таблетки по 150 мг 2 рази на добу), це забезпечувало ідентичну ефективність щодо зменшення розмірів пухлини та прийнятний профіль безпеки порівняно з такими олапарибу у формі капсул у дозі 400 мг 2 рази на добу (J. Mateo et al., 2016). У дослідження були включені хворі, які отримали дві та більше ліній платиновмісної хіміотерапії. У 40% пацієнток безплатиновий інтервал становив від 6 до 12 міс, а ЧВ на терапію препаратами платини отримана у >50% учасниць (E. Pujade-Lauraine et al., 2017).
За оцінкою дослідників медіана ВБП у групі олапарибу склала 19,1 проти 5,5 міс в групі плацебо (відношення ризиків – ВР – 0,30; 95% довірчий інтервал – ДІ – 0,22-0,41; p<0,0001), що свідчить про значне подовження ВБП на тлі підтримуючої терапії олапарибом (рис. 1А). Крім того, ризик прогресування чи смерті в групі олапарибу під час дослідження був знижений на 70%. При аналізі ВБП незалежною групою експертів (BICR) було встановлено, що медіана ВБП у групі олапарибу складала 30,2 проти 5,5 міс у групі плацебо (ВР – 0,25; 95% ДІ 0,18-0,35; p<0,0001; рис. 1Б), а ризик прогресування чи смерті під час дослідження був знижений на 75% у групі олапарибу, що співвідноситься з результатами оцінки цього показника дослідниками (E. Pujade-Lauraine et al., 2017).
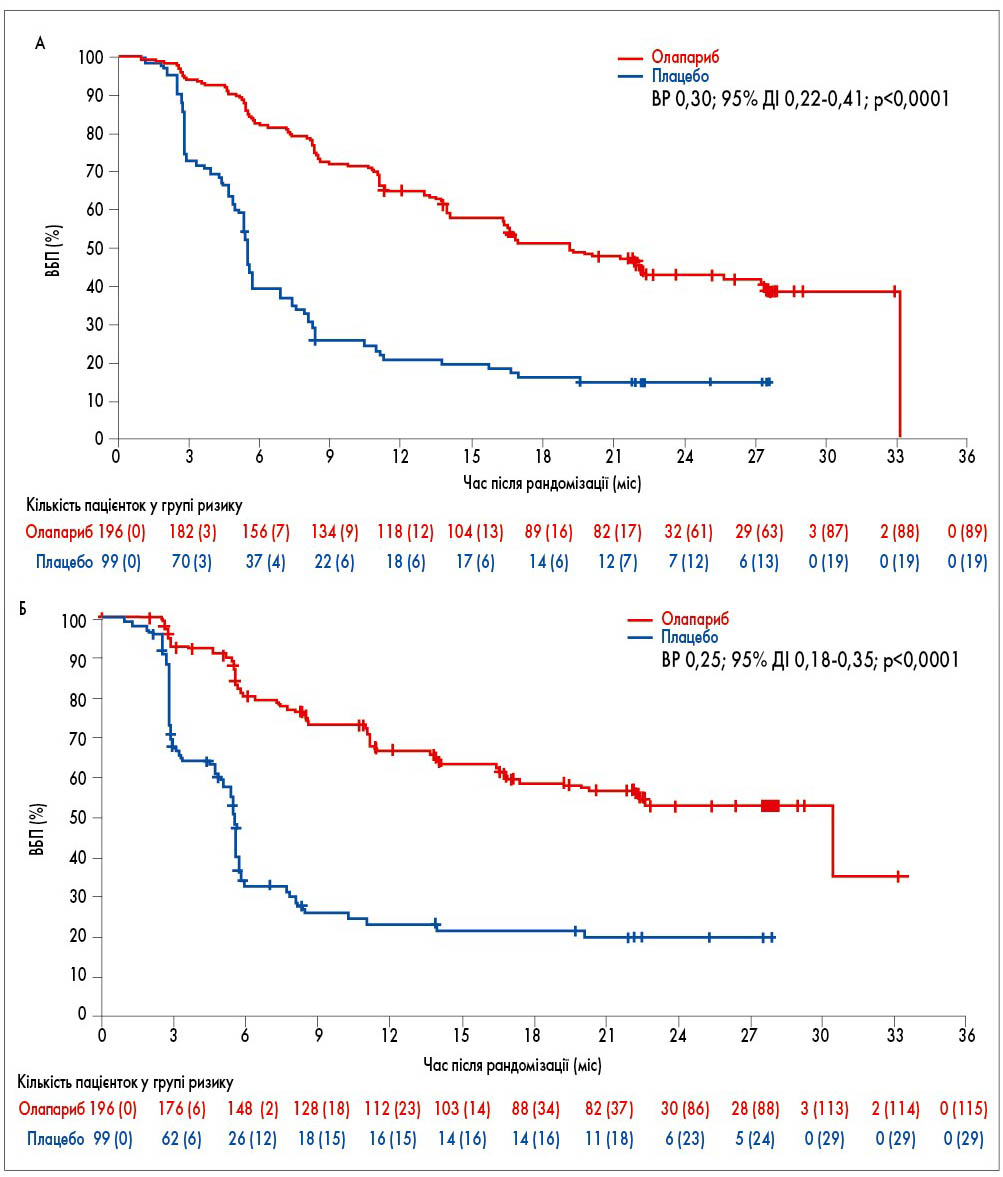 Рис. 1. Медіана ВБП у групах олапарибу та плацебо у дослідженні SOLO-2: А – за оцінкою дослідників; Б – за оцінкою BICR
Рис. 1. Медіана ВБП у групах олапарибу та плацебо у дослідженні SOLO-2: А – за оцінкою дослідників; Б – за оцінкою BICR
Прогресування захворювання через 18 міс не відмічалося у 51% пацієнток, які приймали олапариб, порівняно з 16% учасниць, які отримували плацебо (E. Pujade-Lauraine et al., 2017).
Збільшення ВБП при використанні олапарибу порівняно з плацебо спостерігалося незалежно від відповіді пухлини на платиновмісну терапію. Медіана ВБП у пацієнток із ПВ на момент включення у дослідження не була досягнута у групі олапарибу та складала 5,6 міс у групі плацебо (ВР 0,26; 95% ДІ 0,16-0,42), а у хворих із ЧВ – 13,8 та 5,5 міс відповідно (ВР 0,37; 95% ДІ 0,25-0,54). Тобто спостерігалося кількісне зростання ефективності олапарибу у пацієнток із ПВ на попередню терапію (A.M. Oza et al., 2017).
Використання олапарибу також сприяло збільшенню ВБП у пацієнток із рецидивуючим РЯ, чутливим до препаратів платини, та BRCAm незалежно від кількості отриманих попередніх ліній хіміотерапії. Після 2 попередніх ліній хіміотерапії медіана ВБП складала 22,1 міс у групі олапарибу проти 5,7 міс у групі плацебо (ВР 0,38; ВР 0,26; 95% ДІ 0,26-0,57), після 3 – 16,9 проти 5,1 міс (ВР 0,24; 95% ДІ 0,13-0,42), а після 4 – 17,0 проти 5,4 міс відповідно (ВР 0,26; 95% ДІ 0,13-0,51; R. Penson et al., 2017).
Застосування олапарибу у пацієнток із платиночутливими рецидивами РЯ дозволяло пізніше переходити на наступну лінію терапії. Це супроводжувалося подовженням медіани часу до першої подальшої терапії (ЧППТ), яка у групі олапарибу складала 27,4 міс, а в групі плацебо – 7,2 міс (ВР 0,37; 95% ДІ 0,28-0,48; p<0,0001; A. Poveda et al., 2020).
Проміжний аналіз показника ВБП2, який відображає час до прогресування при застосуванні наступної лінії терапії, показав істотну перевагу олапарибу над плацебо: медіана ВБП2 у групі олапарибу не досягнута, у групі плацебо – 18,4 міс (ВР 0,5; 95% ДІ 0,34-0,72; p=0,0002; E. Pujade-Lauraine et al., 2017).
Крім того, незважаючи на відміну олапарибу після першого прогресування, ефект від проведеного лікування поширювався на наступні лінії терапії, що супроводжувалося подовженням часу до другої подальшої лінії терапії (ЧДПТ). Медіана ЧДПТ у групі олапарибу склала 35,8 проти 18,9 міс у групі плацебо (ВР 0,51; 95%ДІ 0,39-0,68; p<0,0001; A. Poveda et al., 2020).
Підтримуюча терапія олапарибом забезпечувала клінічно значуще збільшення ЗВ на 13 міс порівняно з плацебо (медіана ЗВ у групі олапарибу 51,7 міс, плацебо – 38,8 міс; ВР 0,74; 95% ДІ 0,54-1,0; p=0,0537; A. Poveda et al., 2020; S. Aghajanian et al., 2015; J.A. Ledermann et al., 2017).
Після виключення з аналізу даних 38% пацієнток з групи плацебо і 10% з групи олапарибу, які отримували інгібітор PARP як подальшу терапію, відмічалося зростання медіани ЗВ на 16,3 міс при прийомі олапарибу порівняно з плацебо. Медіана ЗВ у пацієнток, які приймали олапариб, становила 51,7 міс, плацебо – 35,4 міс (ВР 0,56; 95% ДІ 0,35-0,97; рис. 2; A. Poveda et al., 2020).
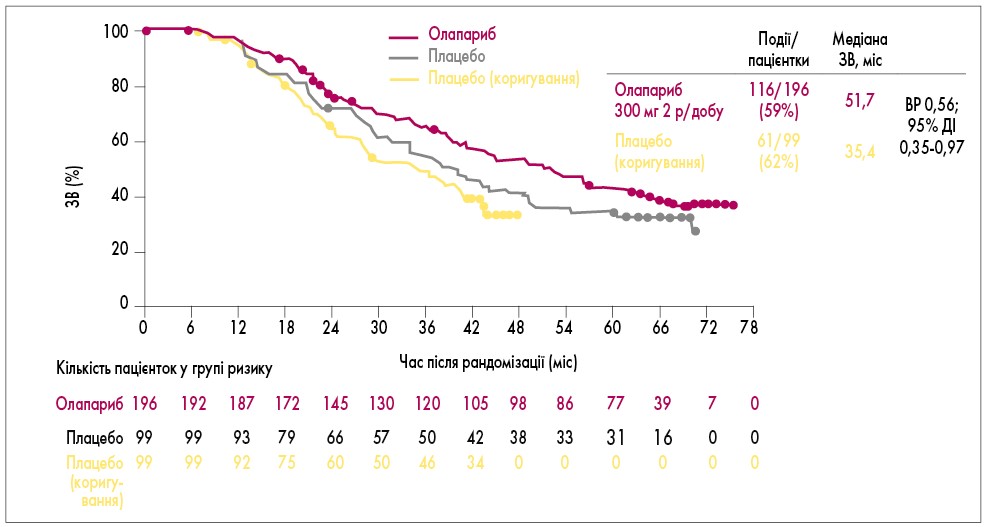 Рис. 2. Медіана ЗВ у групах олапарибу та плацебо (після коригування) у дослідженні SOLO-2
Рис. 2. Медіана ЗВ у групах олапарибу та плацебо (після коригування) у дослідженні SOLO-2
Таким чином, при оцінюванні вторинних кінцевих точок у дослідженні SOLO-2 було продемонстровано подовження ЧППТ, ВБП2, ЧДПТ, ЗВ після прогресування у групі олапарибу порівняно з плацебо (E. Pujade-Lauraine et al., 2017; A. Poveda et al., 2020).
Профіль безпеки олапарибу у дослідженні SOLO-2 відповідав раніше отриманим даним, при цьому більшість побічних явищ (ПЯ) були легкого та середнього ступеня тяжкості. Найбільш частими ПЯ, про які повідомлялося у пацієнток, котрі приймали олапариб, були нудота, втомлюваність і анемія. Тільки 11% пацієнток передчасно припинили терапію через ПЯ, які були пов’язані з лікуванням (E. Pujade-Lauraine et al., 2017).
Клінічний випадок
Пацієнтка, 1958 р.н.
У березні 2015 р. хворій було проведено оперативне втручання (аднексектомія, резекція великого чепця) з приводу РЯ, T3cN0M0. Патогістологічний висновок: серозна низькодиференційована аденокарцинома з метастазами у чепці. Хворій було проведено 6 циклів поліхіміотерапії (карбоплатин + паклітаксел + бевацизумаб) з подальшим призначенням у підтримуючому режимі бевацизумабу у дозі 15 мг/кг маси тіла протягом 1-го року та у дозі 10 мг/кг протягом 2-го року до листопада 2017 р. Було отримано ПВ на хіміотерапію з подальшою ремісією, яка тривала 2 роки 11 міс. Після лікування було проведено дослідження з визначення BRCAm методом полімеразної ланцюгової реакції (4 мутації), результат негативний.
У жовтні 2018 р. у хворої стався рецидив з метастазуванням у печінку, заочеревинні лімфатичні вузли.
13 листопада 2018 р. пацієнтці було проведено вторинну циторедукцію у вигляді комбінованої ретроперитонеальної пангістеректомії з тазовою перитонектомією, екстирпації культі чепця, видалення метастазів печінки, атипової резекції S4, 5, 7 печінки, холецистектомії, низької передньої резекції прямої кишки, санації та дренування черевної порожнини. Патогістологічно у підслизовому шарі кишечнику і в 7 із 12 лімфатичних вузлів виявлено клітини низькодиференційованого залозистого папілярного раку, а у черевній порожнині – розростання низькодиференційованого залозистого папілярного раку з великими некрозами та 1 метастазом у печінці.
Хворій було проведено 6 циклів 2-ї лінії поліхіміотерапії (карбоплатин + гемцитабін). Після закінчення терапії ознак прогресування захворювання за даними комп’ютерної томографії (КТ) не виявлено, рівень онкомаркера CA-125 був у межах норми. Повторно виконано тестування на BRCAm методом полімеразної ланцюгової реакції (8 мутацій) та отримано позитивний результат. З травня 2019 р. пацієнтка приймає препарат Лінпарза у стандартній дозі у підтримуючому режимі. У хворої не відмічається прогресування захворювання протягом 2 років і 4 міс.
Таким чином, SOLO-2 – дослідження, в якому було продемонстровано клінічно та статистично значущі результати щодо первинних і вторинних кінцевих точок у пацієнток з рецидивуючим платиночутливим BRCA-позитивним РЯ. Дані, отримані в цьому клінічному дослідженні, підтверджують результати дослідження Study-19.
 Завідувачка відділення хіміотерапії Центру міжнародних клінічних досліджень (м. Дніпро), кандидат медичних наук Наталія Григорівна Уржумова розповіла про тактику лікування платиночутливого рецидивуючого РЯ.
Завідувачка відділення хіміотерапії Центру міжнародних клінічних досліджень (м. Дніпро), кандидат медичних наук Наталія Григорівна Уржумова розповіла про тактику лікування платиночутливого рецидивуючого РЯ.
– Порушення гомологічної рекомбінації та розвиток її дефіциту (HRD) характерний для близько 50% пацієнток із серозними пухлинами яєчників високого ступеня злоякісності. При цьому найвідоміші мутації, які призводять до HRD, – гермінальні та соматичні мутації в генах BRCA1/2, що складають близько 30% усіх мутацій при серозному РЯ високого ступеня злоякісності (P.A. Konstantinopoulos et al., 2015). HRD призводить до накопичення додаткових мутацій, нестабільності хромосом, підвищеного ризику злоякісного переродження та зниження здатності пухлинної клітини відновлюватися після пошкодження цитостатичними препаратами (C.J. Lord et al., 2012; A.M. Manrquard et al., 2015; M.J. O’Connor et al., 2015).
При прийомі препаратів платини через наявність HRD відновлення пошкоджень ДНК не відбувається, що супроводжується збільшенням кількості двониткових розривів у клітинах серозної епітеліальної пухлини високого ступеня злоякісності, які діляться. Механізм дії олапарибу полягає у блокаді здатності клітини відновлювати однониткові розриви, тим самим сприяючи збільшенню кількості двониткових розривів, що спричиняє загибель клітини (M.J. O’Connor et al., 2015; H. Farmer et al., 2005; H.E. Bryant et al., 2005).
Виділяють декілька біомаркерів, які дозволяють визначити чутливість до PARP-інгібіторів, а саме: лабораторні (наявність BRCAm, HRD) та клінічні (високозлоякісний серозний гістотип, кількість попередніх ліній терапії, тривалість безплатинового періоду, відповідь на терапію препаратами платини; S. Benafif et al., 2015; P.A. Konstantinopoulos et al., 2015; L.C. Hanker et al., 2012). За даними J. Ledermannn та співавт. (2016), чим вищий рівень HRD, тим більша чутливість пухлини до PARP-інгібіторів. Сьогодні активно дискутується питання про доцільність впровадження визначення HRD у клінічну практику, однак клінічні біомаркери при рецидивуючому РЯ поки залишаються основними предикторами для подальшого прийому PARP-інгібіторів.
Ефективність і безпеку PARP-інгібітору олапарибу вивчали у рандомізованому дослідженні Study-19 у пацієнток із платиночутливим рецидивом РЯ після ≥2 попередніх платиновмісних режимів незалежно від статусу BRCA. Хворих було рандомізовано у 2 групи: у 1-й призначали олапариб у дозі 400 мг (капсули) 2 р/добу, у 2-й – плацебо. У дослідження включали пацієнток із ПВ чи ЧВ на платиновмісну терапію, при цьому більше 51% учасниць в обох групах отримали 3 і більше попередніх ліній хіміотерапії.
Було встановлено достовірне зростання медіани ВБП, яка у групі олапарибу складала 8,4 міс, а в групі плацебо – 4,8 міс (ВР 0,35; 95% ДІ 0,25-0,49; p<0,0001; J. Ledermannn et al., 2014). Підтримуюча терапія олапарибом подовжувала ВБП незалежно від статусу BRCAm, однак найбільша користь від терапії відмічалася у пацієнток з BRCAm. Так, медіана ВБП у пацієнток з BRCAm у групі олапарибу склала 11,2 проти 4,3 міс у групі плацебо (ВР 0,18; 95% ДІ 0,10-0,31; p<0,0001), а в учасниць без BRCAm – 7,4 проти 5,5 міс відповідно (ВР 0,54; 95% ДІ 0,34-0,85; p=0,0075; J. Ledermannn et al., 2016).
Застосування олапарибу у підтримуючому режимі також збільшує ЧППТ та ЧДПТ незалежно від статусу BRCA, однак найбільш значущі результати відмічалися у групі хворих з BRCAm. Медіана ЧППТ у пацієнток із BRCAm у групі олапарибу складала 15,6 міс (95% ДІ 15,6-28,2) проти 6,2 міс (95% ДІ 5,3-9,2) у групі плацебо (ВР 0,32; 95% ДІ 0,22-0,48; p<0,0001). За відсутності BRCAm медіана ЧППТ у групі олапарибу становила 12,9 міс (95% ДІ 7,8-15,3) проти 6,9 міс (95% ДІ 5,7-9,3) у групі плацебо (ВР 0,45; 95% ДІ 0,3-0,66; p<0,0001). Медіана ЧДПТ у хворих з BRCAm, які приймали олапариб, становила 22,0 міс (95% ДІ 17,7-34,9) проти 15,3 міс (95% ДІ 14,0-18,7) у пацієнток, які приймали плацебо (ВР 0,41; 95% ДІ 0,28-0,62; p<0,0001), а при відсутності BRCAm – 17,0 (95% ДІ 15,2-19,8) проти 14,7 міс (95% ДІ 12,8-18,3) відповідно (ВР 0,63; 95% ДІ 0,43-0,94; p=0,023; J. Lederman et al., 2016).
При фінальному аналізі ЗВ з медіаною тривалості спостереження 6,5 року було виявлено також переваги щодо ЗВ у загальній популяції групи олапарибу, незважаючи на кросовер (23% учасниць у групі плацебо згодом отримували PARP-інгібітори). Медіана ЗВ у групі олапарибу склала 29,8 проти 27,8 міс у групі плацебо (ВР 0,73; 95% ДІ 0,55-0,95; p=0,02138; J. Lederman et al., 2016). Отримані результати також показують, що існують пацієнтки, які відповідають на терапію олапарибом протягом 6 років незалежно від статусу BRCA (11% хворих мали відповідь на терапію препаратом Лінпарза упродовж 6 років і більше порівняно з 1% у групі плацебо). Крім того, аналіз біомаркерних характеристик у 15 пацієнток, які отримували олапариб понад 6 років, показав, що у 9 з них наявні BRCAm (C. Gourley et al., 2017).
Таким чином, у дослідженні Study-19 з найдовшим періодом спостереження серед всіх PARP-інгібіторів було показано ефективність олапарибу при платиночутливому високозлоякісному РЯ. При цьому 20% пацієнток отримували терапію 3 роки і довше, а 10% хворих продовжили лікування після 6 років (J. Lederman et al., 2016).
OPINION – непорівняльне відкрите багатоцентрове клінічне дослідження IIIb фази, проведене з метою підтвердження ефективності підтримуючої терапії олапарибом при чутливому до препаратів платини рецидивуючому РЯ з негермінальною мутацією гена BRCA за наявності ПВ чи ЧВ на хіміотерапію препаратами платини. У цьому дослідженні хворі отримували олапариб у дозі 300 мг перорально. На початковому етапі дослідження у 65,9% пацієнток відмічалася ЧВ на їх останню терапію препаратами платини, при цьому 40,9% хворих отримували олапариб у підтримуючому режимі у 3-й та подальших лініях терапії. Крім того, 43% учасниць мали позитивний статус HRD, незважаючи на те що пацієнтки з гермінальними BRCAm були виключені з дослідження (A. Poveda et al., 2021).
Медіана ВБП склала 9,2 міс (95% ДІ 7,6-10,9) у загальній популяції пацієнток з РЯ, а ознаки прогресування захворювання були відсутні у 65,6% пацієнток через 6 міс та у 37,0% – через 12 міс (рис. 3; A. Poveda et al., 2020).
 Рис. 3. Медіана ВБП у загальній популяції пацієнток з РЯ та негермінальною мутацією гена BRCA
Рис. 3. Медіана ВБП у загальній популяції пацієнток з РЯ та негермінальною мутацією гена BRCA
Активність олапарибу відмічалася незалежно від статусу HRD чи BRCAm. Профіль ПЯ у дослідженні OPINION відповідав такому у попередніх дослідженнях. При прийомі олапарибу ПЯ переважно були легкого чи помірного ступеня тяжкості, керувалися шляхом тимчасового припинення лікування чи корекції дози. 7,5% пацієнток припинили терапію через ПЯ, пов’язані з застосуванням олапарибу.
Отже, результати дослідження OPINION підтверджують ефективність підтримуючої терапії олапарибом при чутливому до препаратів платини рецидивуючому РЯ.
Сьогодні показаннями до призначення олапарибу є наявність серозного високозлоякісного рецидивуючого платиночутливого РЯ маткових труб або первинного перитонеального раку, ПВ чи ЧВ (>30% зменшення пухлини) на хіміотерапію препаратами платини незалежно від статусу BRCA.
 Клінічний онколог, хіміотерапевт онкологічної клініки «Інновація» (м. Київ) Оксана Миколаївна Лаціннікова представила цікавий клінічний випадок.
Клінічний онколог, хіміотерапевт онкологічної клініки «Інновація» (м. Київ) Оксана Миколаївна Лаціннікова представила цікавий клінічний випадок.
Клінічний випадок
Пацієнтка, 1969 р.н.
У січні 2017 р. хворій вперше було встановлено діагноз серозна аденокарцинома обох яєчників cT3c, G3. На 17.01.2017 рівень базового онкомаркера CA-125 становив 376 ОД/мл. Пацієнтці було проведено первинне лікування: лапароскопічна тотальна гістеректомія з оментектомією (06.02.2017) з подальшим призначенням одного циклу карбоплатину у поєднанні з паклітакселом та 5 циклів карбоплатину у комбінації з паклітаселом і бевацизумабом. Курс лікування хвора завершила 07.06.2017, після чого їй було проведено КТ (23.06.17), на якій ознак захворювання не виявлено. Рівень CA-125 складав 3,6 ОД/мл (23.06.2017). Як підтримуючу терапію хворій було призначено 18 циклів бевацизумабу у дозі 15 мг/кг, курс лікування яким хвора завершила 09.03.2018.
Перший рецидив у пацієнтки виявлено у червні 2018 р. Він характеризувався біохімічним і рентгенологічним прогресуванням і зростанням рівня CA-125 до 132 ОД/мл. На КТ (20.06.2018) відмічалися збільшення наддіафрагмальних лімфатичних вузлів до 11 мм та асцит. Крім того, було виявлено гермінальну мутацію гена BRCA1 (5382insC). Пацієнтці було призначено 6 циклів паклітакселу та карбоплатину, після завершення лікування (10.03.2018) було отримано ПВ. На КТ (жовтень 2018) спостерігалося зменшення розмірів наддіафрагмальних лімфатичних вузлів до 3-5 мм, вільної рідини у черевній порожнині не зафіксовано. Пацієнтці було призначено олапариб у підтримуючому режимі з жовтня 2018 по серпень 2020 р., що дозволило досягти ремісії тривалістю 21 міс.
Другий рецидив у хворої настав 04.09.2020. Він супроводжувався біохімічним і рентгенологічним прогресуванням, підвищенням рівня CA-125 до 97,5 ОД/мл. На КТ відмічалася негативна динаміка з появою ознак карциноматозу очеревини та розвитком асциту. Призначено 3 цикли карбоплатину у поєднанні з паклітакселом, після чого на КТ відмічалися ознаки стабілізації захворювання. Потім пацієнтці було проведено ще 3 цикли карбоплатину у поєднанні з паклітакселом, після чого рівень CA-125 знизився до 23,7 ОД/мл. На КТ відмічалася негативна динаміка у вигляді мінімальних ознак карциноматозу очеревини з ростом раніше виявлених вогнищ від 5 до 11 мм, збільшенням лімфатичних вузлів внутрішньої пахвової групи справа та появи поодиноких збільшених лімфатичних вузлів шлунково-дванадцятипалої зв’язки.
За рішенням консиліуму лікування з приводу третього рецидиву включало 3 цикли ліпосомального доксорубіцину, після чого на КТ у хворої відмічалися ознаки стабілізації, а рівень CA-125 дещо підвищився та складав 67 ОД/мл. Згодом хворій було призначено 2 цикли ліпосомального доксорубіцину у поєднанні з карбоплатином. Однак при проведенні КТ (28.07.2021) зафіксовано прогресування захворювання у вигляді мінімальних ознак карциноматозу очеревини, наявності метастазів у лімфатичних вузлах внутрішньої пахвової групи справа, поодиноких збільшених вузлів гепатодуоденальної зв’язки, появи поодиноких вогнищ у печінці, збільшення в розмірах вогнищ в очеревині та випоту у порожнині малого таза. Рівень CA-125 складав 219 ОД/мл.
Лікування з приводу четвертого рецидиву пацієнтка розпочала у вересні 2021 р. з прийому гемцитабіну та бевацизумабу з можливим подальшим продовженням застосування бевацизумабу у підтримуючому режимі. На початку вересня 2021 р. ЗВ цієї пацієнтки складала 49 міс. Хвора продовжує терапію.
При порівнянні даних дослідження SOLO-1 (призначення олапарибу як підтримуючої терапії після 1-ї лінії хіміотерапії) та SOLO-2 (застосування олапарибу після 2-ї лінії хіміотерапії) ВБП складала 56,0 та 22,1 міс відповідно. Отримані дані свідчать про те, що підтримуюча терапія олапарибом у 1-й лінії дозволяє досягти тривалішого безрецидивного періоду порівняно з іншими лініями терапії (R. Penson et al., 2017; R.A. Burger et al., 2011; S. Banerjee et al., 2020).
Таким чином, послідовність лікування у цьому клінічному випадку відповідала стандартам того часу. Однак якби на момент встановлення діагнозу були доступні результати дослідження SOLO-1, то послідовність прийому препаратів підтримуючої терапії могла б бути іншою, враховуючи ефективність олапарибу після 1-ї лінії хіміотерапії у пацієнток з BRCA-асоційованим РЯ.
 Завідувач хіміотерапевтичного відділення КНП ЛОР «Львівський онкологічний регіональний лікувально-діагностичний центр», кандидат медичних наук Ярослав Васильович Шпарик виступив з доповіддю «Чи змінюють результати Study-19 і OPINION сучасні підходи і практики в діагностиці та лікуванні пацієнток з рецидивуючим РЯ незалежно від BRCA мутації?».
Завідувач хіміотерапевтичного відділення КНП ЛОР «Львівський онкологічний регіональний лікувально-діагностичний центр», кандидат медичних наук Ярослав Васильович Шпарик виступив з доповіддю «Чи змінюють результати Study-19 і OPINION сучасні підходи і практики в діагностиці та лікуванні пацієнток з рецидивуючим РЯ незалежно від BRCA мутації?».
– Ефективність бевацизумабу у складі комбінованої хіміотерапії та у підтримуючому режимі у пацієнток із рецидивуючим РЯ вивчали у клінічних дослідженнях OCEANS, GOG-0213 та AURELIA (C. Aghajanian et al., 2012; R.L. Coleman et al., 2017; E. Pujade-Lauraine et al., 2014). У рандомізованому подвійному сліпому плацебо-контрольованому клінічному дослідженні III фази OCEANS було показано, що додавання бевацизумабу до хіміотерапії (гемцитабін + карбоплатин) з продовженням прийому бевацизумабу в підтримуючому режимі у пацієнток із платиночутливим рецидивуючим РЯ сприяло статистично значущому зростанню ВБП на 3,7 міс без збільшення ЗВ порівняно з такими у групі хворих, які отримували тільки комбінацію хіміотерапевтичних препаратів (C. Aghajanian et al., 2015).
У іншому клінічному дослідженні GOG-0213 було показано, що додавання бевацизумабу до хіміотерапії (паклітаксел + карбоплатин) із подальшою підтримуючою терапією бевацизумабом у пацієнток із платиночутливим рецидивуючим епітеліальним РЯ сприяло зростанню медіани ВБП на 3,4 міс та номінальному збільшенню медіани ЗВ на 4,9 міс (не була статистично значущою) порівняно з ХТ (R.L. Coleman et al., 2017). У рандомізованому дослідженні III фази AURELIA при поєднанні бевацизумабу з хіміотерапією у пацієнток із рецидивуючим РЯ, резистентним до препаратів платини, подовження ЗВ також не відмічалося (E. Pujade-Lauraine et al., 2014).
Ключовими дослідженнями з вивчення ефективності олапарибу у пацієнток із платиночутливим рецидивом РЯ незалежно від статусу BRCAm є Study-19 та OPINION, а у хворих із платиночутливим рецидивом РЯ та BRCAm – SOLO-2 (J.A. Ledermann et al., 2014; A. Poveda et al., 2021; E. Pujade-Lauraine et al., 2017).
При розгляді даних ключових досліджень із вивчення олапарибу та бевацизумабу можна зауважити, що 54% пацієнток у дослідженні Study-19 мали гермінальну або соматичну BRCAm, а 10% в OPINION – соматичну BRCAm, при цьому у дослідженнях OCEANS та GOG-0213 BRCAm не визначали. При використанні олапарибу в підтримуючому режимі у дослідженнях Study-19 та OPINION відмічалося подовження ВБП на 8,4 та 9,2 міс відповідно. У дослідженнях OCEANS та GOG-213 медіана ВБП при застосуванні бевацизумабу складала 12,4 та 13,8 міс відповідно. Однак при розгляді наявних даних слід враховувати, що у дослідженнях Study-19 та OPINION підрахунок медіани ВБП проводився від початку підтримуючої терапії, а у дослідженнях OCEANS та GOG-0213 – з моменту рандомізації та початку хіміотерапії, тривалість якої в середньому може складати від 4,2 до 5 міс (J.A. Ledermann et al., 2014; A. Poveda et al., 2021; C. Aghajanian et al., 2012; R.L. Coleman et al., 2017).
Оцінка користі терапії з використанням шкал ASCO-NHB та ESMO-MCBS проводилася J.R. Foote та співавт. (2019). За шкалою ASCO-NHB у дослідженнях OCEANS та GOG-213 кількість балів склала 35 та 26 відповідно при порівнянні з когортою пацієнтів з BRCAm у дослідженнях Study-19 та OPINION, у яких кількість балів становила 47 та 62 відповідно. За шкалою ESMO-MCBS у дослідженнях з бевацизумабом було отримано 2 бали при порівнянні з когортою хворих з BRCAm, котрі приймали олапариб (Study-19 та OPINION), у якій цей показник складав 4 бали. У пацієнтів без BRCAm у дослідженні Study-19 кількість балів за шкалами ASCO-NHB та ESMO-MCBS складала 32 та 2 відповідно.
Згідно з настановами ESMO, вибір лікування при рецидиві РЯ залежить від чутливості до платиновмісної хіміотерапії. При отриманні відповіді на платиновмісну хіміотерапію можна рекомендувати PARP-інгібітори у підтримуючому режимі. За відсутності раннього симптомного рецидиву при використанні попередньої лінії платиновмісної хіміотерапії можна призначати хворим платиновмісну хіміотерапію з додаванням бевацизумабу або підтримуючу терапію PARP-інгібіторами (за наявності показань). Можна рекомендувати застосування PARP-інгібіторів (олапарибу, нірапарибу* і рукапарибу*) в підтримуючому режимі при РЯ після відповіді на 2-гу або наступні лінії лікування на основі препаратів платини, однак найбільшу користь від терапії отримають пацієнтки із BRCAm. Тому пацієнткам, у яких немає потреби у терміновому симптоматичному лікуванні або яким бевацизумаб протипоказаний (наприклад, при тромбозі, фістулі), слід призначати PARP-інгібітори за отримання відповіді на лікування препаратами платини незалежно від наявності BRCAm. Пацієнткам із сильно вираженими симптомами, у яких немає протипоказань до застосування бевацизумабу, можна призначати комбінацію препаратів платини з бевацизумабом. Хворим із доведеною або прогнозованою/очікуваною платинорезистентністю може бути запропонована послідовна безплатинова хіміотерапія з додаванням бевацизумабу, якщо є показання (N. Colombo et al., 2019).
Таким чином, при платиночутливому рецидиві за відсутності потреби у терміновій сипмтоматичній терапії та наявності відповіді на лікування препаратами платини можна рекомендувати олапариб у підтримуючому режимі незалежно від BRCA-статусу.
 Головний лікар Лікарні ізраїльської онкології LISOD (м. Київ), доктор медичних наук, професор Алла Борисівна Вінницька представила цікавий клінічний випадок.
Головний лікар Лікарні ізраїльської онкології LISOD (м. Київ), доктор медичних наук, професор Алла Борисівна Вінницька представила цікавий клінічний випадок.
Клінічний випадок
Пацієнтка, зріст 165 см, маса тіла 127 кг, індекс маси тіла 46,6 кг/м2.
Госпіталізована 26.05.2012 у клініку з діагнозом асцит нез’ясованого генезу при радіологічних ознаках карциноматозу чепця і з невідомою знахідкою в ділянці яєчників (рівень CA-125 – 92,8 ОД/мл). Мала супутні захворювання: артеріальна гіпертензія 3 ступеня, кризовий перебіг; ішемічна хвороба серця; серцева недостатність 1 ступеня зі збереженою систолічною функцією.
Пацієнтці було проведено діагностичну лапароскопію з біопсією і виявлено інтраперитонеальний карциноматоз та асцит. При взятті біопсії встановлено наявність серозно-папілярної помірно диференційованої аденокарциноми яєчника/очеревини.
Хворій було розпочато неоад’ювантну хіміотерапію за протоколом паклітаксел + карбоплатин (3 цикли). Оцінка відповіді на терапію була утруднена через відсутність радіологічних знахідок, що можна виміряти, і наявність непереконливого збільшення рівня CA-125. Однак після 4-го циклу вміст CA-125 нормалізувався.
У жовтні 2012 р. у хворої виникло гостре порушення мозкового кровообігу, яке фахівці іншої клініки розцінювали як наявність метастазів у головному мозку. Проте у нашій клініці було підтверджено ішемічний інсульт, при якому хірургічне лікування не було показане. Тому пацієнтці було рекомендовано продовжити курс хіміотерапії до 6 циклів. Після закінчення хіміотерапії хвора перебувала у стабільному стані до лютого 2015 р. (моменту прогресування). Прогресування захворювання почалося через 30 міс після встановлення діагнозу і 25 міс після закінчення хіміотерапії. Було розпочато 8 циклів хіміотерапії за протоколом паклітаксел + карбоплатин + бевацизумаб з редукцією дози паклітакселу на 25% через розвиток полінейропатії. Прийом бевацизумабу у підтримуючому режимі продовжили ще на 4 цикли (до 12 циклів). Хвора закінчила лікування 16.10.2015.
Через 5,5 міс після закінчення останнього циклу хіміотерапії (05.04.2016) на КТ відмічалося незначне збільшення розмірів лімфатичних вузлів лівої надключичної групи і деяких заочеревинних лімфатичних вузлів. Рівень CA-125 складав 27,81 ОД/мл. Хворій було рекомендовано спостереження до появи клінічних проявів.
У січні 2017 р. у хворої відмічалося значне збільшення асциту. Було розпочато курс хіміотерапії паклітаксел (1 раз на тиждень) + карбоплатин (1 раз на 21 день); позитивна динаміка відмічалася після 3, а стабілізація – після 6 циклів. Крім того, у хворої було підтверджено наявність BRCAm.
07.01.2018 пацієнтці було призначено олапариб (400 мг 2 р/день перорально) в підтримуючому режимі. Причиною вибору олапарибу є висока платиночутливість у цієї пацієнтки (тривалість безплатинового періоду близько 2 років), хороша відповідь на останню платиновмісну хіміотерапію (наявність рентгенологічної відповіді, зменшення асциту і зникнення симптомів), артеріальна гіпертензія 3 ступеня й тромбоемболія легеневої артерії в анамнезі (протипоказання до прийому бевацизумабу), задовільний профіль безпеки й переносимості препарату та переконливі дані щодо його клінічної ефективності незалежно від статусу BRCA.
01.12.2020 хворій було виконано КТ органів грудної клітки й черевної порожнини, за даними якої було зроблено висновок про стабілізацію процесу з тенденцією до прогресування. При біопсії надключичного лімфатичного вузла гістологічно було виявлено метастаз серозної карциноми яєчника G2, ER та PR: 95%. Рівень CA-125 становив 291 ОД/мл. Пацієнтка продовжила прийом олапарибу.
06.06.2021 стан пацієнтки погіршився, з приводу чого було розпочато 3 цикли хіміотерапії паклітаксел + карбоплатин + бевацизумаб, після чого відмічалася позитивна динаміка. Хворій було рекомендовано продовжити хіміотерапію до 6 циклів з подальшим прийомом бевацизумабу.
Отже, слід переглянути ведення пацієнток з РЯ, особливо щодо виконання оперативного втручання у цих хворих, що може позитивно відобразитися на тривалості та якості їх життя.
Таким чином, представлені у рамках науково-практичного заходу результати клінічних досліджень, присвячених олапарибу, та досвід ведення хворих на РЯ сьогодні відкривають нові можливості підвищення ефективності лікування пацієнток із платиночутливим рецидивуючим РЯ незалежно від наявності BRCAm.
Підготувала Ірина Неміш
*В Україні не зареєстровані.
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 6 (73) 2021 р.



