26 січня, 2022
Сучасна стратегія ведення пацієнтів із рецидивною і рефрактерною множинною мієломою
Хворі на множинну мієлому (ММ) є гетерогенною групою пацієнтів. Протягом останніх років накопичено багато даних, що стали основою формування різних стратегій лікування пацієнтів з ММ залежно від клінічної ситуації. Для обговорення важливих питань діагностики ММ та лікування 2-ї лінії був проведений майстер-клас за участю провідних експертів галузі.
.jpg) У своїй доповіді керівник Центру гематології, хіміотерапії гемобластозів та трансплантації кісткового мозку Клінічної лікарні «Феофанія» Державного управління справами, завідувач кафедри клінічної лабораторної діагностики Національного університету охорони здоров’я України імені П.Л. Шупика (м. Київ), доктор медичних наук, професор Сергій Вікторович Клименко зосередив увагу слухачів на значенні з’ясування групи цитогенетичного ризику у пацієнтів з ММ, особливо в контексті рецидивної та рефрактерної форми хвороби.
У своїй доповіді керівник Центру гематології, хіміотерапії гемобластозів та трансплантації кісткового мозку Клінічної лікарні «Феофанія» Державного управління справами, завідувач кафедри клінічної лабораторної діагностики Національного університету охорони здоров’я України імені П.Л. Шупика (м. Київ), доктор медичних наук, професор Сергій Вікторович Клименко зосередив увагу слухачів на значенні з’ясування групи цитогенетичного ризику у пацієнтів з ММ, особливо в контексті рецидивної та рефрактерної форми хвороби.
– Порівнюючи моделі ризику при ММ та дифузній В-великоклітинній лімфомі (ДВКЛ) за кривою загальної виживаності (ЗВ) пацієнтів, можна відмітити істотну різницю між нозологіями. У разі ДВКЛ на графіку ЗВ спостерігається поступове зниження кривої із наступним переходом на рівень стійкого плато. Це відповідає двом групам ризику: високого, зі спадом ЗВ протягом перших років лікування, та низького – з хорошою відповіддю на терапію та тривалою ЗВ (остання група хворих численніша). При ММ у кривій ЗВ відсутнє плато і відмічається безперервна тенденція до зменшення кількості пацієнтів, що вижили, по усій її протяжності. Тобто група пацієнтів з ММ є неоднорідною і включає більшу кількість субпопуляцій із різним ступенем ризику, відповідно категоризація хворих і стратифікація тактики лікування при ММ складніша, ніж при ДВКЛ.
Сьогодні при визначенні групи ризику у пацієнта з ММ враховують два типи параметрів: молекулярні (цитогенетичні) та клінічні. Цитогенетичні аномалії при ММ можна розділити на дві групи: перебудова гена важких ланцюгів імуноглобуліну (t [4; 14], t [14; 16], t[14; 20], t [11; 14], t [6; 14]) та решта генетичних аномалій (гіпердиплоїдія, негіпердиплоїдний набір, порушення 1-ї хромосоми, моносомія 13, Del17p). Незважаючи на те що до сьогодні Міжнародна система стадіювання (ISS; за рівнем β-мікроглобуліну й альбуміну сироватки) залишається надійним інструментом для встановлення ступеня ризику, визначення цитогенетичних аномалій стало частинної рутинної клінічної практики.
У процесі еволюції ММ постійно набуває нових цитогенетичних аномалій, що зумовлює мінливість молекулярних характеристик пухлини у конкретного пацієнта від рецидиву до рецидиву. Поява вторинних цитогенетичних аномалій залежить від низки факторів, зокрема від маси пухлини: чим вона більша, тим вищим є ризик появи нових цитогенетичних аномалій.
З метою оптимізації цитогенетичного тестування у клінічній практиці доцільним є з’ясування генетичних подій, які визначають несприятливий прогноз для пацієнта. До них належать первинні генетичні події: транслокації t(4; 14) – ген FGFR3/MMSET, t(14; 16) – ген MAF, t(14; 20) – ген MAFB, а також вторинні генетичні події (делеції 17р – ген TP53 та 1q – гени CKS1B, ANP32E).
У 2015 р. була переглянута ISS і створена система R-ISS, яка включила деякі цитогенетичні параметри ММ (наявність делеції 17р та/або транслокації t(4; 14) та/або транслокації t(14; 16)). У R-ISS також враховується рівень лактатдегідрогенази (ЛДГ) сироватки крові. Відповідно до нової моделі стратифікації ризику ММ, ІІІ стадія (високий ризик) встановлюється при ІІІ стадії за ISS (β2-мікроглобулін ≥5,5 мг/л) та/або виявленні цитогенетичної аномалії високого ризику за FISH та високому рівні ЛДГ.
Під високим ризиком при ММ розуміють імовірність раннього прогресування захворювання та смерті від нього. Так, при тривалому спостереженні медіана ЗВ при ММ І стадії за R-ISS не досягнута, а при ІІІ стадії становить 43 міс (A. Palumbo et al., 2015).
Сьогодні R-ISS значно полегшує стратифікацію пацієнтів з ММ, проте з накопиченням нових даних система постійно удосконалюється.
У встановленні ризику при ММ велике значення має приріст на довгому плечі 1-ї хромосоми. V. Shah та співавт. (2018) виявили, що разом з t(4;14) та делецією 17р приріст 1q асоційований із коротшою виживаністю без прогресування (ВБП) і ЗВ. Включення цієї цитогенетичної аномалії у систему визначення ризику активно обговорюється у науковій спільноті, і найближчим часом слід очікувати впровадження параметра у рутинну клінічну практику. Іншим параметром, на який звертають увагу науковці, є наявність двох і більше несприятливих генетичних подій (double hit), що асоційовано з дуже поганим прогнозом (V. Shah et al., 2018).
На конгресі Американського товариства гематологів (ASH) у 2020 р. була запропонована нова система визначення ризику для пацієнтів з ММ – R2-ISS, яка включає параметри ISS: ІІ стадія – 1 бал, ІІІ стадія – 1,5 бала, високий рівень ЛДГ – 1 бал, Del(17p) – 1 бал, транслокація t(4; 14) – 1 бал, приріст 1q – 0,5 бала. За R2-ISS виділяють 4 групи ризику: низького (0 балів), низького проміжного (0,5-1,0 бал), високого проміжного (1,5-2,5 бала) та високого (3-5 бали).
Для перегляду моделі стратифікації використовували дані Європейської мережі мієломи, що включає понад 7000 хворих на ММ. Для порівняння ЗВ і ВБП пацієнтів, стратифікованих за різними моделями (R-ISS та R2-ISS), були використані дані 2227 хворих. Найчастішою причиною виключення решти пацієнтів було те, що у деяких дослідженнях опущено дані про наявність зміни 1q. При розподілі 2227 пацієнтів на 4 групи ризику за R2-ISS була відмічена істотна різниця за ВБП і ЗВ. За новою моделлю стратифікації R-ISS пацієнти з II стадією (n=1372) були краще розподілені на групи низького проміжного (n=517), середнього проміжного (n=811) та високого ризику (n=44). Це підтверджує, що ця численна група включала гетерогенних пацієнтів із різним ризиком прогресування та/або смерті (рис.; M. D’Agostino et al., 2020).
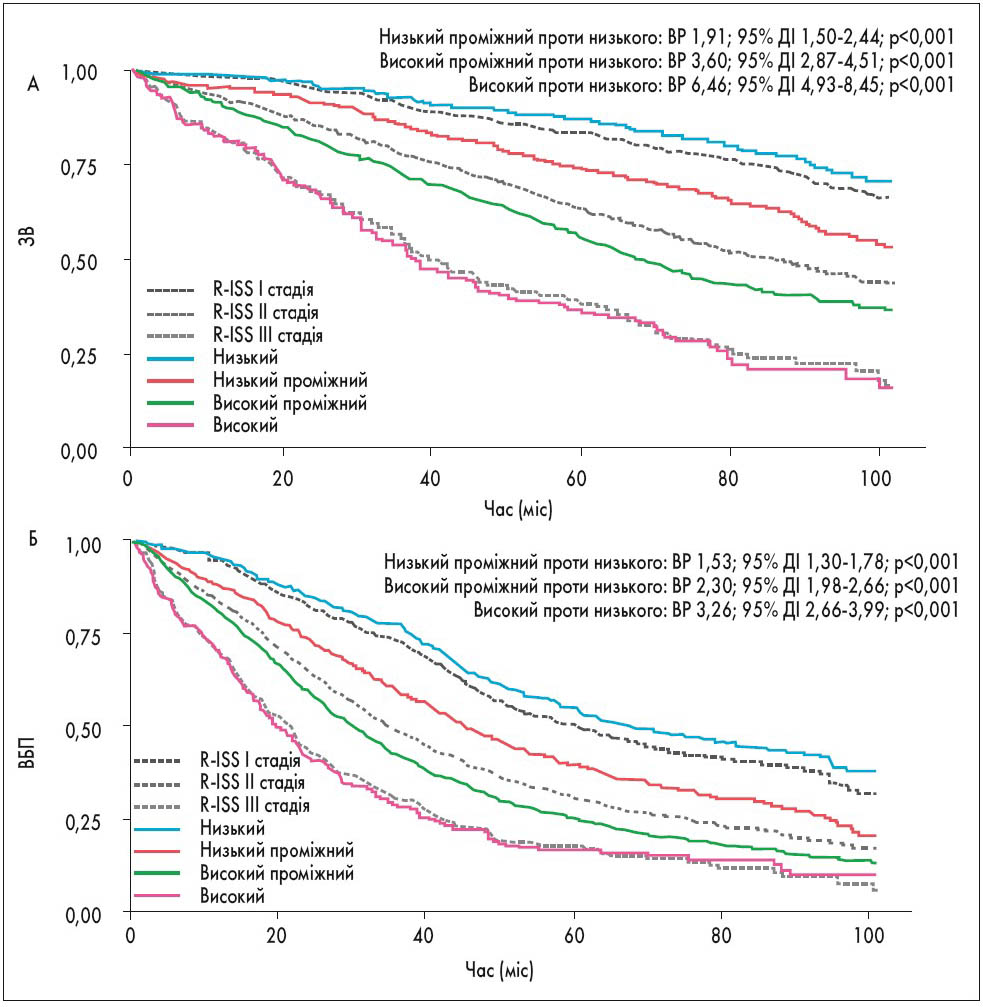 Рис. ЗВ (А) та ВБП (Б) при розподілі пацієнтів за новою моделлю стратифікації ризику R2-ISS. Пунктирна лінія – ЗВ і ВБП тих самих пацієнтів, розподілених на групи ризику за R-ISS
Рис. ЗВ (А) та ВБП (Б) при розподілі пацієнтів за новою моделлю стратифікації ризику R2-ISS. Пунктирна лінія – ЗВ і ВБП тих самих пацієнтів, розподілених на групи ризику за R-ISS
ВР – відношення ризиків; ДІ – довірчий інтервал.
Під час еволюції ММ може набувати нові генетичні аномалії: наприклад, при первинній діагностиці Del(17p) має місце у 10% випадків, а згодом цей показник може зростати до 50%. Таким чином, визначення ризику на основі цитогенетичного ризику має відбуватися не лише на етапі первинної діагностики пухлини, а й у динаміці. J. Croft та співавт. (2020) показали, що частота значущих цитогенетичних аномалій при рецидиві хвороби є вищою, ніж при первинній діагностиці. Найчастішими хромосомними змінами, пов’язаними з рецидивом ММ, були приріст або ампліфікація 1q (19%), del(13q) (10%), приріст або ампліфікація 11q (9%) і del(17p)/TP53 (8%). При аналізі ЗВ було виявлено, що у разі приросту 1q на етапі встановлення діагнозу та повторного аналізу при рецидиві хвороби прогноз був однаково гіршим, ніж за відсутності цієї аномалії. Таким чином, повторне оцінювання молекулярного ризику може надати важливу інформацію при плануванні стратегії лікування.
Ефективною терапевтичною опцією у пацієнтів з ММ, які мають цитогенетичні аномалії (транслокації t(4;14), t(14;16), del(17p)), асоційовані з високим ризиком, є даратумумаб. У 2020 р. були опубліковані результати метааналізу ключових рандомізованих клінічних досліджень з вивчення впливу включення даратумумабу у стандартні схеми лікування вперше діагностованої ММ або рецидивної/рефрактерної ММ (ррММ). Результати комбінованого аналізу засвідчили збільшення ВБП при застосуванні даратумумабу у пацієнтів із вперше діагностованою ММ групи високого ризику з коефіцієнтом відношення ризиків (ВР) 0,67, у пацієнтів з ррММ групи високого ризику – покращення ВБП з ВР 0,45 (S. Giri et al., 2020).
Отже, визначення молекулярних маркерів ризику має стати частиною рутинної клінічної практики. Доцільним є виявлення цитогенетичних аномалій не лише при первинній діагностиці хвороби, а й при кожному рецидиві. Пацієнти з ММ високого цитогенетичного ризику отримують користь від додавання даратумумабу до стандартних схем лікування.
 Завідувачка відділення онкогематології Національного інституту раку (м. Київ) Тетяна Вікторівна Каднікова розповіла про стандарти 2-ї лінії терапії хворих на ММ.
Завідувачка відділення онкогематології Національного інституту раку (м. Київ) Тетяна Вікторівна Каднікова розповіла про стандарти 2-ї лінії терапії хворих на ММ.
– До критеріїв прогресування ММ, вимірюваного за вмістом М-протеїну, належать: збільшення рівня М-протеїну ≥25% від мінімально досягнутого; кількість плазматичних клітин у кістковому мозку ≥10%; поява нових вогнищ у кістках або збільшення розмірів тих, що визначалися раніше; поява вогнищ у м’яких тканинах або збільшення їх розмірів; рівень кальцію сироватки крові ≥11,5 мг/дл (або 2,65 ммоль/л). Для ММ, яка визначається лише за вільними легкими ланцюгами (ВЛЛ), критерієм прогресування хвороби є зміна співвідношення ВЛЛ в бік збільшення різниці залучених і незалучених ВЛЛ на 100 мг/л.
Прийнято виділяти клінічний рецидив ММ, при якому необхідно проводити терапію, та біохімічний рецидив, коли можна застосовувати тактику активного спостереження (за відсутності симптомів). Біохімічний рецидив встановлюється на основі результатів двох послідовних аналізів крові або сечі з інтервалом не більше 2 міс. Про клінічний рецидив свідчить наявність 1 та більше з таких ознак: поява нової плазмоцитоми в м’яких тканинах або кісткових уражень; збільшення розмірів раніше виявленої плазмоцитоми або кісткових уражень на 50%; гіперкальціємія, зниження рівня гемоглобіну, порушення функції нирок, підвищення в’язкості крові, що потребує терапевтичного втручання.
Протирецидивну терапію також призначають у разі біохімічного рецидиву, при якому виявляють подвоєння рівня М-протеїну під час повторних обстежень з інтервалом не більше 2 міс та наявність у 2 послідовних дослідженнях щонайменше однієї з таких ознак: збільшення вмісту М-протеїну на >10 г/л, або екскреції білка Бенс-Джонса із сечею на 500 мг/добу, або ВЛЛ на ≥200 мг/л (при аномальному співвідношенні ВЛЛ), або збільшення залучених ВЛЛ на >25%.
Лікування першого рецидиву ММ залежить від того, якою була 1-ша лінія терапії, а також від тривалості та глибини відповіді. При виборі терапії враховують доступність лікарських препаратів, характеристики пухлини (ризик, цитогенетичні аберації, екстрамедулярне захворювання, швидке зниження пухлинного навантаження) та пацієнта (вік, коморбідність, побажання пацієнта щодо лікування). За результатами клінічних досліджень триплетні схеми терапії мають перевагу над дуплетними за ВБП, рівнем загальної відповіді, а в деяких дослідженнях – і за ЗВ. Однак дуплетні схеми можуть розглядатися для лікування ослаблених пацієнтів.
Викликом у лікуванні пацієнтів з ММ є подвійна рефрактерність (хоча б до одного інгібітору протеасом та одного імуномодулюючого засобу). Найчастіше спостерігається подвійна рефрактерність до бортезомібу та леналідоміду. Сьогодні немає стандарту терапії для пацієнтів з рефрактерною ММ. При повторному призначенні інгібіторів протеасом, імуномодуляторів (леналідоміду, талідоміду) спостерігається значне зниження загальної відповіді. Враховуючи низьку виживаність таких пацієнтів, проблема подвійної рефрактерності при ММ стоїть дуже гостро.
Згідно з оновленими рекомендаціями Європейського товариства медичної онкології (ESMO, 2021) щодо ведення пацієнтів із рецидивом ММ, у 2-й лінії терапії після схеми VRd (бортезоміб + леналідомід + дексаметазон) у пацієнтів, чутливих до леналідоміду, слід розглянути трикомпонентну схему з моноклональним антитілом (наприклад, D-Rd – даратумумаб + леналідомід + дексаметазон). При рефрактерності до леналідоміду спектр терапевтичних опцій істотно звужується, і рекомендоване застосування схем на основі бортезомібу/карфілзомібу + дексаметазон + моноклональне антитіло. Чутливим до бортезомібу пацієнтам можна призначати комбінації на основі бортезомібу/леналідоміду/карфілзомібу + дексаметазон + моноклональне антитіло (наприклад, схеми D-Rd, D-Vd – даратумумаб + бортезоміб + дексаметазон). Найменше терапевтичних опцій запропоновано для лікування пацієнтів із подвійною рефрактерністю до леналідоміду та бортезомібу: ESMO рекомендує дві терапевтичні схеми з карфілзомібом, який не зареєстрований в Україні.
В оновлених клінічних настановах Національної онкологічної мережі США (NCCN, версія 7, 2021) для лікування пацієнтів з ррММ запропоновано низку схем, серед яких в Україні доступними є VRd, D-Vd, D-Rd (схеми, яким слід віддавати перевагу). Велика частина схем, рекомендованих ESMO та NCCN для лікування ррММ, включає не зареєстровані в Україні препарати.
Перевага схеми з даратумумабом у пацієнтів з ррММ була продемонстрована у рандомізованому клінічному дослідження III фази POLLUX. Згідно з отриманими результатами, рівень відповіді у групі пацієнтів, які отримували D-Rd, був значно вищим, ніж у групі Rd (92,9 та 76,4%; p<0,001). Зокрема, повна відповідь і глибока повна відповідь були досягнуті у 43,1% пацієнтів групи D-Rd та 19,2% – Rd (p<0,001). Протягом періоду спостереження 44,3 міс виявлено, що у групі пацієнтів, які отримували даратумумаб, медіана ВБП була значно більшою, ніж у групі Rd: 44,5 та 17,5 міс відповідно (ВР 0,44; 95% ДІ 0,35-0,55; p<0,0001). Застосування схеми з даратумумабом дозволило подовжити середній час до призначення наступної лінії терапії (50,6 проти 23,1 міс; ВР 0,39; 95% ДІ 0,31-0,50; p<0,0001). При цьому медіана ВБП на тлі наступної лінії терапії у групі D-Rd не була досягнута, а в групі Rd склала 31,7 міс. Схема з даратумумабом значно подовжує виживаність пацієнтів порівняно зі схемою без даратумумабу, незалежно від кількості попередніх ліній терапії, а також у пацієнтів із порушенням функції нирок (N.J. Bahlis et al., 2020).
Користь призначення даратумумабу разом з бортезомібом і дексаметазоном (D-Vd) була продемонстрована у рандомізованому клінічному дослідженні III фази CASTOR. За результатами первинного аналізу (медіана спостереження 7,4 міс) застосування D-Vd знижувало ризик прогресування хвороби або смерті на 61% порівняно з Vd (A. Palumbo et al., 2016). При медіані спостереження 40 міс у групі D-Vd порівняно з Vd були вищі показники ВБП (медіана 16,7 та 7,1 міс відповідно) та загальної відповіді (85 та 63% відповідно). Найбільшу користь від додавання даратумумабу мали пацієнти з однією попередньою лінією терапії (M.-V. Mateos et al., 2020).
Досягнення MRD-негативного статусу асоційоване із тривалішою ВБП. При медіані спостереження 54,8 міс у дослідженні POLLUX частота MRD-негативного статусу склала 32,5% у групі D-Rd та 6,7% у групі Rd. При медіані спостереження 50,2 міс у дослідженні CASTOR MRD-негативний статус досягнуто у 15,1% пацієнтів групи D-Vd та 1,6% групи Vd (H. Avet-Loiseau et al., 2021).
Найскладнішою ситуацією у лікуванні ММ є розвиток потрійної резистентності до імуномодулюючих агентів, інгібіторів протеасом та анти-CD38 моноклональних антитіл. У такому випадку слід віддавати перевагу участі пацієнта у клінічних дослідженнях, однак це не завжди можливо.
Таким чином, із появою нових препаратів значно зросла виживаність пацієнтів із ММ. Застосування моноклональних антитіл є однією з найбільш ефективних терапевтичних стратегій при ррММ.
 Продовжила тему лікування ММ і значення даратумумабу у сучасних схемах терапії завідувачка відділення гематології Івано-Франківської обласної клінічної лікарні, кандидат медичних наук Наталія Любомирівна Глушко.
Продовжила тему лікування ММ і значення даратумумабу у сучасних схемах терапії завідувачка відділення гематології Івано-Франківської обласної клінічної лікарні, кандидат медичних наук Наталія Любомирівна Глушко.
– CD38 є однією з ключових молекул у патогенезі ММ. CD38 більшою мірою експресуються на малігнізованих клітинах, ніж на здорових плазматичних клітинах, зокрема, цю молекулу експресують 100% мієломних клітин. Даратумумаб (Дарзалекс®) – людське моноклональне антитіло класу IgG1 каппа, що зв’язується з CD38. Протипухлинний ефект даратумумабу зумовлений прямою та імуномодулюючою дією. Пряма дія включає комплементозалежну цитотоксичність, антитілозалежну клітинну цитотоксичність, антитілозалежний клітинний фагоцитоз, апоптоз шляхом перехресного зв’язування. Імуномодулююча дія зумовлена впливом на мікрооточення пухлини, збільшенням кількості цитотоксичних лімфоцитів і Т-хелперів та зменшенням кількості імуносупресивних клітин. Пряма дія даратумумабу забезпечує швидкий ефект, натомість імуномодулююча дія спрямована на глибоку та тривалу відповідь.
Протипухлинний потенціал даратумумабу у лікуванні пацієнтів з ррММ був підтверджений у дослідженнях III фази POLLUX (порівняння схем D-Rd та Rd) і CASTOR (порівняння схем D-Vd та Vd). Так, у дослідженні POLLUX при медіані спостереження 44,3 міс застосування схеми D-Rd знижувало ризик прогресування хвороби на 56% у загальній популяції пацієнтів та на 63% у пацієнтів із нирковою недостатністю (швидкість клубочкової фільтрації 30-60 мл/хв). Використання схеми D-Rd також сприяло кращій відповіді на терапію та довшій ВБП незалежно від цитогенетичного ризику. Частота досягнення MRD-негативного статусу у групі D-Rd була в 6 разів вищою, ніж у групі Rd: 30,4 та 5,3% відповідно (N.J. Bahlis et al., 2020).
У дослідженні CASTOR схема D-Vd мала перевагу над Vd. При медіані спостереження 40,0 міс D-Vd знижувала ризик прогресування хвороби або смерті на 76%, у групі високого цитогенетичного ризику – на 60%. Застосування схеми D-Vd порівняно з Vd подовжує ВБП незалежно від кількості попередніх ліній терапії, однак найвища ВБП (27,0 проти 7,9 міс) та загальна відповідь (92 проти 74%) були у пацієнтів, які отримували одну попередню лінію терапії. У рефрактерних до леналідоміду пацієнтів у групах D-Vd і Vd медіана ВБП склала 7,8 та 4,9 міс відповідно (M.-V. Mateos et al., 2020). Оновлені дані досліджень свідчать на користь концепції раннього призначення схеми D-Vd пацієнтам з ррММ при першому рецидиві хвороби, незалежно від попередньої лінії терапії на основі леналідоміду чи бортезомібу.
З метою оцінювання впливу монотерапії даратумумабом у пацієнтів з ррММ, які отримали кілька ліній лікування, був проведений комбінований аналіз досліджень GEN501 (за участю хворих, які отримали ≥2 ліній терапії з інгібіторами протеасом та імуномодулюючими агентами) та SIRIUS (за участю пацієнтів, які отримали ≥3 ліній терапії з інгібіторами протеасом та імуномодулюючими агентами, а також хворих із подвійною рефрактерністю). Медіана спостереження становила 36,6 міс, загальна кількість пацієнтів – 148. За результатами аналізу медіана ЗВ склала 20,5 міс з 3-річною виживаністю хворих 36,5%, рівень загальної відповіді – 30,4%. Таким чином, монотерапія даратумумабом супроводжувалася глибокою та тривалою відповіддю навіть у раніше лікованих пацієнтів із високим ступенем рефрактерності при збереженні прийнятного профілю безпеки (S.Z. Usmani et al., 2020).
Отже, даратумумаб у складі комбінованих схем і в монорежимі значно подовжує виживаність пацієнтів з ррММ, навіть якщо вони отримували >2 ліній терапії. Однак, як показують дані досліджень, призначення даратумумабу після першого рецидиву дозволяє досягти кращих результатів лікування.
Підготувала Ілона Цюпа
CP-282819
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 6 (73) 2021 р.



