18 лютого, 2022
Роль сучасних пробіотиків у лікуванні гострої діареї
Щороку в світі реєструються близько 1,5 млрд випадків гострої діареї, яка є причиною загибелі >2 млн людей, причому в структурі летальності від діареї переважають діти перших 5 років життя. Високий рівень захворюваності та смертності, надзвичайне різноманіття етіологічних збудників гострої діареї значно ускладнюють обрання тактики дії та підбір адекватного лікування в умовах первинної медичної практики.
Згідно із чинними міжнародними рекомендаціями, для дітей віком від 0 до 5 років (ESPGHAN, 2014) та більш дорослих дітей і дорослих (ВГО «Гостра діарея в дорослих і дітей», 2012) базисом лікування гострої інфекційної діареї є розчини для пероральної регідратації (РПР). Утім, таке лікування, спрямоване насамперед на нормалізацію водно-електролітного балансу, не має істотного впливу на тяжкість та тривалість діареї. Саме тому як допоміжна терапія широко обговорюється необхідність застосування пробіотиків. Було проведено низку досліджень з вивчення ефективності пробіотиків у лікуванні гострої діареї (у т. ч. антибіотик-асоційованої діареї) з різним умістом пробіотичних культур (Allen S. J. et al., 2011; Basu S. et al., 2007; Domingo J. J., 2017; Floch M. H. et al., 2011; Szajewska H. et al., 2006).
Однак наразі відсутні чіткі настанови щодо використання конкретних штамів мікроорганізмів у складі пробіотика, а також тривалості його призначення для лікування гострої діареї. Результати низки попередніх досліджень продемонстрували певний позитивний ефект (зменшення тяжкості та тривалості діареї) під час застосування пробіотиків, що містять Lactobacillus rhamnosus, Lactobacillus GG, Lactobacillus plantarum, штами біфідобактерій, Enterococcus faecium, Saccharomyces boulardii, Bacillus coagulans, Bacillus clausii чи поєднання зазначених штамів (Bastola R. et al., 2017; Davidson G. P., 2000; Isolauri Е., 2003; Saavedra J. M. et al., 1994; Szajewska H. et al., 2006; Tankanow R. M. et al., 1990). Втім, отримані результати мали суттєві розбіжності. Це можна пояснити різною стабільністю досліджуваних пробіотичних препаратів, відмінними властивостями пробіотичних мікроорганізмів та їхніх комбінацій.
Наразі одними з найперспективніших пробіотиків, здатних впливати на перебіг гострої діареї, вважаються представники роду Бацил – паличкоподібних, аеробних або факультативно-анаеробних, спороутворювальних грампозитивних бактерій.
Спори B. clausii мають високу резистентність до хімічних і фізичних чинників, тому вони легко проходять крізь бар’єр шлункового соку, потрапляючи неушкодженими до кишечного тракту, де перетворюються в метаболічно активні вегетативні клітини. B. clausii має високий ступінь гетерологічної резистентності до антибіотиків, що дає змогу застосовувати його як для профілактики зміни мікрофлори кишечнику, спричиненої селективною дією антибіотиків (особливо антибіотиків широкого спектра дії), так і для відновлення вже порушеного балансу мікрофлори кишечнику.
Пробіотики, створені на основі спор бацил, характеризуються відмінною стабільністю (Ahire J. J. et al., 2011), безпекою (Elshaghabee F. M. et al., 2017) та ефективністю (Hatanaka M. K. et al., 2018).
Сьогодні увага науковців прикута до штаму B. clausii UBBC‑07 (MTCC5472), який за допомогою дослідження R. M. Sudha та співавт. (2013) уже продемонстрував клінічну ефективність у зменшенні симптомів діареї серед пацієнтів дорослого віку, не спричиняючи жодних побічних ефектів. В описаному нижче дослідженні ті ж самі науковці вивчали безпеку та ефективність суспензії спор B. clausii UBBC‑07 лікування індійських дітей з гострою діареєю.
Матеріали та методи
В рандомізованому подвійному сліпому плацебо-контрольованому багатоцентровому дослідженні в паралельних групах взяли участь 120 дітей віком від 6 міс до 5 років, котрі звернулися по медичну допомогу щодо гострої діареї. Зі 119 пацієнтів, які завершили дослідження, 59 хворих отримували суспензію B. clausii UBBC‑07 (2×109 спор/5 мл і РПР), інші 60 пацієнтів – суспензію плацебо та РПР. До складу плацебо входила винятково очищена вода. Середній вік пацієнтів склав 37,20 (±14,31) міс (від 7 до 60 міс). 72 (60,50%) пацієнти були чоловічої статі та 47 (39,50%) – жіночої.
Критерії включення – вік від 6 міс до 5 років, клінічний діагноз – гостра діарея, >3 випадки кашеподібних випорожнень за останні 24 год, відсутність будь-яких інших серйозних захворювань.
Критерії виключення – тяжке недоїдання, прийом антибіотиків у період дослідження, наявність тяжкої діареї, яка, на думку дослідників, потребувала додаткового лікування, відмінного від досліджуваного препарату та РПР, наявність видимої крові у випорожненнях, використання пробіотиків протягом останніх 3 тиж до початку дослідження, використання антибіотиків / будь-яких протидіарейних препаратів протягом останніх 3 тиж до початку дослідження, участь у будь-якому клінічному випробуванні або використання будь-якого досліджуваного препарату протягом останніх 90 днів, відома чи очікувана підвищена чутливість до будь-якої з активних речовин або допоміжних речовин, попереднє використання (протягом 48 год) каоліну, пектину, вісмуту субсаліцілату, рацекадотрилу, лопераміду, атропіну й інших антихолінергічних засобів.
Подальші візити та лікування в рамках дослідження
Тривалість лікування становила 5 днів із подальшим спостереженням до 10-го дня. Суспензію спор B. clausii UBBC‑07 чи суспензію плацебо призначали перорально 2 р/день протягом 5 днів. Оскільки це амбулаторне дослідження, 3 візити були обов’язковими й реєструвалися. Візит 1: скринінг і початок лікування (день 1); візит 2: спостереження після закінчення лікування (день 6±1); візит 3: день 10±1 (завершення дослідження).
Критерії оцінки ефективності та безпеки
Оцінювали такі показники, як зниження частоти діареї (кількість випорожнень на день), зниження тривалості діареї та поліпшення консистенції випорожнень. Ці дані реєструвалися батьками в щоденнику пацієнта як первинні показники ефективності. Консистенція випорожнень оцінювалася за Бристольською шкалою випорожнень, яка класифікує випорожнення на 7 типів (від твердих до кашеподібних): 1 і 2 – тверді випорожнення, 3 і 4 – ідеальні випорожнення (особливо останні), 5-7 – кашеподібні та водянисті випорожнення.
Результати
Тривалість епізодів діареї
Тривалість діареї (час у годинах від перших до останніх ненормальних (кашеподібних або рідких) випорожнень, що передують нормальним) була значно меншою в пацієнтів, котрі отримували суспензію B. clausii (75,25±12,96 год), ніж у хворих, які отримували плацебо (81,60±15,43 год) (р=0,02).
З 2-го дня кількість пацієнтів, що одужали, в групі лікування суспензією B. clausii була більшою порівняно із групою плацебо (рис. 1).
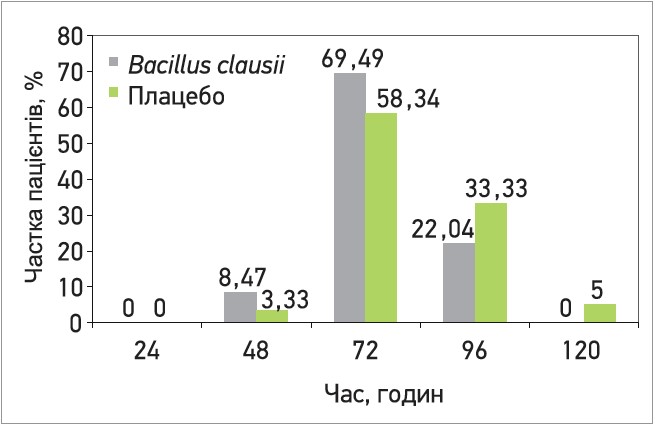
Рис. 1. Кількість пацієнтів, що одужали, в групі лікування суспензією B. clausii
Через 48 год на тлі лікування суспензією B. clausii в 5 (8,47%) дітей припинилася діарея порівняно із 2 (3,33%) дітьми, які отримували плацебо. Через 72 год у групах кількість випадків відновлення склала 41 (69,49%) та 35 (58,34%), через 96 год – 13 (22,04%), 20 (33,33%) у групах лікування суспензією B. clausii та плацебо відповідно.
Кількість і частота епізодів діареї
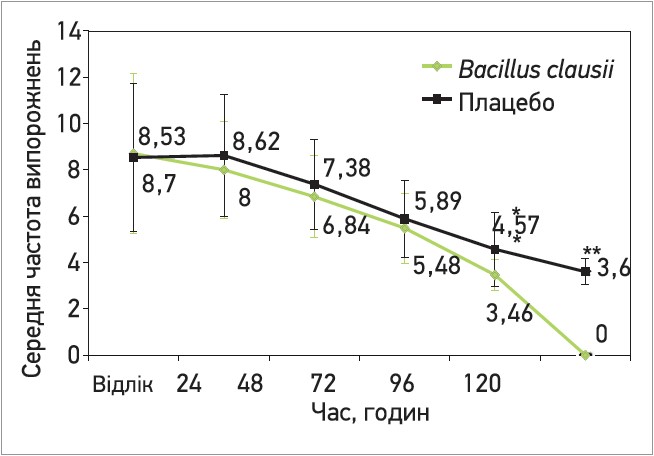
До початку лікування частота випорожнень склала 8,70±3,44 на день у групі пробіотика та 8,53±3,19 на день у групі плацебо (рис. 2).
Рис. 2. Частота випорожнень у групі пробіотика та в групі плацебо
З 1-го по 5-й день лікування в обох групах спостерігалося зниження середньої частоти випорожнень. На 4-й день було відзначено значне зниження середньої частоти випорожнень у групі лікування суспензією B. clausii (3,46±0,66) порівняно із групою контролю (4,57±1,59) (р<0,01).
Консистенція випорожнень
До початку лікування консистенція випорожнень в обох групах була >5 балів (кашеподібні, рідкі випорожнення). На тлі застосування суспензії B. clausii через 72 год у 78% (46/59) пацієнтів спостерігалася нормалізація консистенції випорожнень. У групі контролю нормалізація випорожнень відзначалася в 62% (37/60) дітей. До 4-го дня (96 год) у всіх пацієнтів групи лікування були нормальні випорожнення, тоді як у групі контролю зазначених результатів вдалося досягти лише на 5-й день.
Обговорення та висновки
Отже, на тлі застосування суспензії B. clausii UBBC‑07 тривалість діареї була значно коротшою порівняно із групою контролю. Отримані дані узгоджуються з результатами попереднього клінічного дослідження B. clausii UBBC‑07, проведеного тим самим колективом авторів на популяції дорослих пацієнтів із гострою діареєю (Sudha M. R., 2013), а також із низкою інших досліджень.
G. Ianiro та співавт. (2018) провели систематичний огляд і метааналіз рандомізованих контрольованих випробувань з використанням B. clausii для лікування гострої діареї у дітей. Для метааналізу відібрали 6 рандомізованих контрольованих випробувань (1298 пацієнтів). Дані, отримані в результаті аналізу об’єднаного масиву даних, продемонстрували, що застосування B. clausii значно скорочує тривалість діареї та тривалість госпіталізації порівняно з контрольною групою.
Механізм лікувальної дії B. clausii в пацієнтів із діареєю пов’язують із синтезом антимікробних речовин, а також ефектами імуномодуляції (Maugo, 2012). Водночас B. clausii може пригнічувати ріст патогенів у шлунково-кишковому тракті за рахунок колонізації вільних екологічних ніш, роблячи їх недоступними для розвитку інших мікроорганізмів, а також за рахунок конкурентної адгезії епітеліальних клітин. Відомо, що штами B. clausii здатні до синтезу пептидних антибіотиків, а також низки ферментів, які виявляють літичну активність щодо Pseudomonas aeruginosa. M. C. Urdaci та співавт. (2004) продемонстрували, що штами B. clausii виділяють у середовище антимікробні речовини, активні проти грампозитивних бактерій, зокрема проти Staphylococcus aureus, Enterococcus faecium, Clostridium difficile.
На вітчизняному фармацевтичному ринку суспензія штаму B. clausii UBBC07 представлена у вигляді дієтичної добавки Лактіалє® Жерміна. Флакон ємністю 5 мл містить 2×109 спор цього штаму.
Лактіалє® Жерміна може бути рекомендована лікарем до раціону харчування для підтримки нормального балансу шлунково-кишкової мікрофлори при кишкових інфекціях, інтоксикаціях, порушенні травлення, незбалансованій дієті та прийомі антибіотиків; вона полегшує перебіг діареї, біль у животі, зменшує газоутворення.
Крім того, завдяки здатності B. clausii синтезувати різні вітаміни (особливо групи В) ця дієтична добавка сприяє корекції дисвітамінозу, спричиненого застосуванням антибіотиків або хіміотерапевтичних препаратів. Завдяки метаболічній активності B. clausii застосування дієтичної добавки дає змогу досягти неспецифічного антигенного й антитоксичного ефекту (табл.).
Рекомендується споживати натще. Якщо продукт призначають одночасно з антибіотиками, його слід споживати між двома прийомами антибіотика.
Підготував В’ячеслав Килимчук