25 жовтня, 2022
Кашель у дитини: просто про складне
 У рамках науково-практичного онлайн-семінару «Якість життя та інновації у практиці сімейного і дитячого лікаря», що відбувся 23 липня 2022 р., провідні українські експерти в галузі педіатрії та суміжних спеціальностей обговорювали найбільш нагальні питання щодо ведення педіатричних пацієнтів в умовах бойових дій.
У рамках науково-практичного онлайн-семінару «Якість життя та інновації у практиці сімейного і дитячого лікаря», що відбувся 23 липня 2022 р., провідні українські експерти в галузі педіатрії та суміжних спеціальностей обговорювали найбільш нагальні питання щодо ведення педіатричних пацієнтів в умовах бойових дій.
Науковий керівник відділення дитячої пульмонології та алергології ДУ «Національний інститут фтизіатрії та пульмонології ім. Ф.Г. Яновського НАМН України» (м. Київ), доктор медичних наук Олена Олександрівна Речкіна у своїй доповіді висвітила проблему менеджменту дітей із кашлем.
Перед клініцистом завжди постає важливе питання: «Дитина, що кашляє, – це просто чи складно?». Так, якщо говорити про кашель у дитини при гострій респіраторній вірусній інфекції (ГРВІ), – просто, однак у випадку наявності у дитини хронічного кашлю – складно, оскільки такий кашель іноді є медичною «загадкою», ребусом, і клініцисту необхідна певна кількість часу для диференційної діагностики. Визначення саме тривалості кашлю допомагає встановити перелік захворювань, що можуть бути включені в диференційно-діагностичний ряд, і почати своєчасну діагностику та лікування, щоб запобігти розвитку незворотніх змін.
Сьогодні у сучасних гайдлайнах для дітей у віці до 14 років пропонується визначати хронічний кашель як наявність щоденного кашлю тривалістю більше 4 тижнів. І це основна відмінність від кашлю у дорослих, в яких хронічним вважається кашель, що триває більше 8 тижнів.
Сьогодні наявна значна кількість клінічних рекомендацій провідних медичних товариств, у тому числі Європейського респіраторного товариства, NICE та CHEST, щодо менеджменту дорослих та дітей із хронічним кашлем [1, 2]. Крім того, широко застосовуються спеціальні педіатричні рекомендації та алгоритми лікування хронічного кашлю [3-5]. Усі рекомендації мають певні відмінності щодо ведення педіатричних пацієнтів, проте ключова теза, яка їх всіх об’єднує: проведення поглибленої клінічної оцінки кашлю є наріжним каменем процесу діагностики кашлю [6].
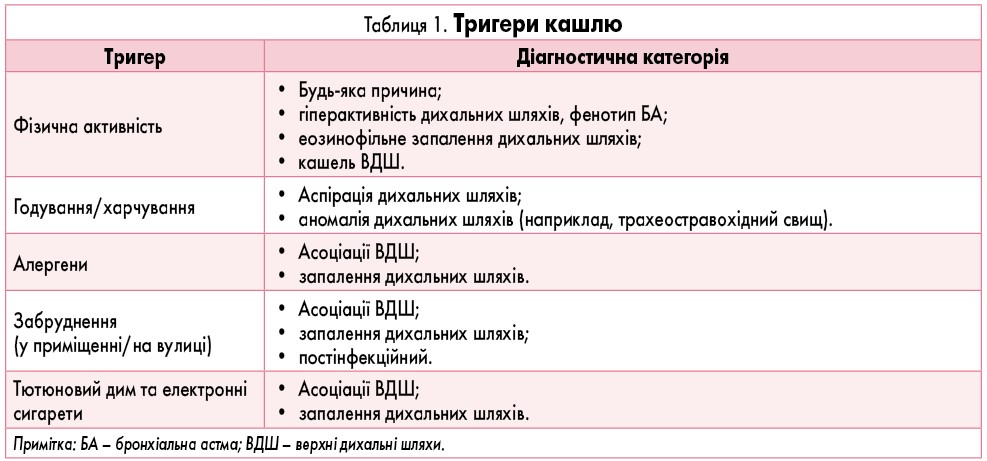
Сучасні рекомендації визначають основні питання для ретельного вивчення та оцінки хронічного кашлю, які необхідно поставити пацієнту/членам його родини при зборі анамнезу. Вони включають: вік пацієнта, коли кашель розпочався, характер кашлю, тригери та його траєкторія (табл. 1), супутні симптоми, відповідь на попереднє лікування тощо (рис. 1). Відповіді на ці питання є важливими, оскільки вони допоможуть клініцисту диференціювати захворювання. Так, наприклад, якщо у дитини наявний хронічний кашель від народження, клініцист одразу запідозрить у неї вади бронхолегеневої системи, муковісцидоз або гастроезофагеальний рефлюкс (ГЕР). При цьому чим старша дитина, тим більше буде змінюватися перелік захворювань, для яких характерним симптомом є хронічний кашель, тому вік дитини, коли почався кашель, є важливим для оцінки.
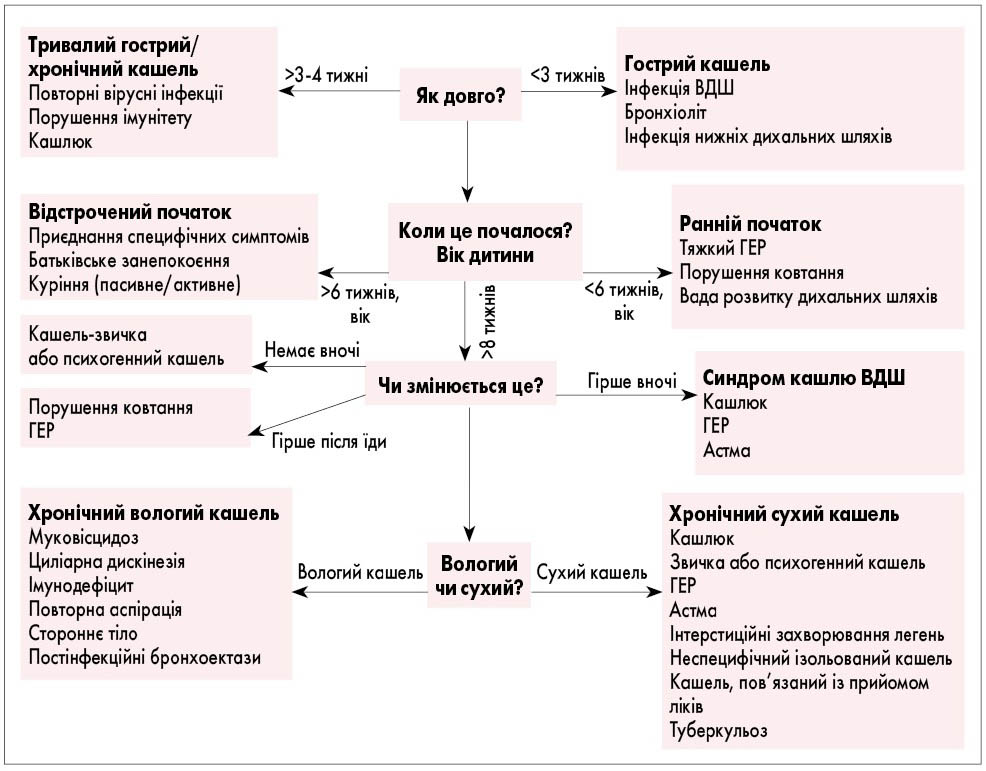 Рис. 1. Збір анамнезу при хронічному кашлі
Рис. 1. Збір анамнезу при хронічному кашлі
Супутні симптоми є також важливими для оцінки та диференціації захворювання. Наявність у дитини чхання та атопії допоможе запідозрити в неї алергічну етіологію кашлю. Якщо кашель посилюється або з’являється, коли дитина їсть/п’є, клініцист подумає про наявність у дитини ГЕР або синдрому аспірації. Поява кашлю під час фізичного навантаження може вказувати на БА або бути проявом бронхоектатичної хвороби/затяжного бактеріального бронхіту. Важливим для подальшої стратегії ведення дитини з кашлем є також визначення, чи впливало попереднє лікування на прояви кашлю, тобто чи зникав кашель при призначенні β2-агоністів короткої дії або застосуванні антибактеріальних препаратів.
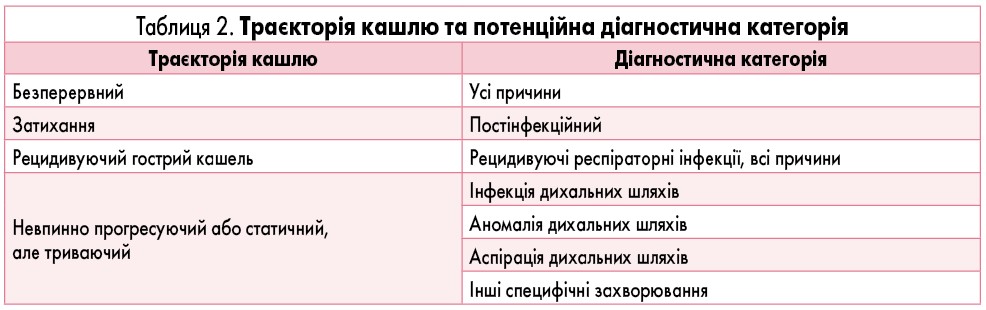
При диференційній діагностиці захворювань важливо також оцінювати траєкторію кашлю, що буде корисно для визначення потенційної діагностичної категорії (табл. 2).
Характер кашлю є надважливою характеристикою, яка допомагає диференціювати ряд захворювань (рис. 1). Отримання інформації про характер кашлю (сухий чи вологий) у дитини є ключовим компонентом анамнезу при встановленні діагнозу, тому клініцист не повинен покладатися виключно на оцінку батьками того, чи дійсно кашель є сухим або вологим. За даними літератури, кожний 3-4-й з батьків надає невірну характеристику, саме тому лікар повинен сам почути та/або «побачити» кашель. В останньому факторі лікарю на допомогу можуть прийти сучасні технології, наприклад, батьки можуть зробити запис на відео нападу кашлю у дитини та відправити лікарю.
Після підтвердження діагнозу наступним важливим кроком є вибір ефективної та безпечної стратегії лікування. Відповідно до сучасних даних, актуальною є проблема невідповідного лікування, що включає: поліфармацію, практику призначення препаратів off-label, призначення одночасно препаратів із протикашльовим та муколітичним механізмами дії, ранню необґрунтовану антибіотикотерапію та нераціональне використання небулайзерної терапії, застосування компресів, гірчичників, розтирань із ароматичними бальзамами, парових інгаляцій. Усе зазначене є помилковим та повинно бути викорінено із сучасної практики.
Проблема вибору препарату для лікування кашлю в педіатрії спирається на правильний вибір та обґрунтування муколітичної терапії, що засновані на глибокому розумінні механізмів дії муколітичних препаратів, і це є обов’язково прерогативою лікаря. Важливо розуміти, що ефективні ліки проти одного захворювання можуть бути неефективні або навіть шкідливі при лікуванні іншого. Тому терапія кашлю в педіатрії повинна бути діагноз-орієнтована, тобто спочатку встановлюється діагноз захворювання і лише після цього призначається терапія. При цьому перевагу в лікуванні кашлю у дітей необхідно надавати препаратам з універсальною дією, доведеним високим профілем ефективності та безпеки.
Сьогодні як провідна молекула серед муколітичних препаратів із високою ефективністю та безпекою при гострому та хронічному кашлі розглядається ердостеїн, відомий під брендовою назвою Ермуцин [8-10]. Ердостеїн є неактивними проліками, які швидко трансформуються до біологічно активних метаболітів. Завдяки відсутності вільних тіолових груп ердостеїн (на відміну від ацетилцистеїну та його комбінацій) не подразнює слизову оболонку шлунка, також відсутній ризик інактивації антибіотика. Саме тому, на відміну від зазначених вище препаратів, не треба робити перерву 2 години між прийомом препарату Ермуцин й антибіотиків.
Муколітичний ефект препарату Ермуцин реалізується за рахунок руйнування дисульфідних зв’язків, що пов’язують між собою волокна мокротиння. Завдяки такому механізму дії Ермуцин зменшує в’язкість мокротиння без збільшення його кількості; це дозволяє уникнути синдрому затоплення, що дуже важливо в педіатричній практиці.
Друга важлива перевага препарату – його протизапальна дія, яка реалізується за рахунок пригнічення синтезу ІЛ-6 та ІЛ-8, які є ключовими цитокінами, що беруть безпосередню участь у формуванні нейтрофільного запального процесу в бронхіальному дереві та легеневій паренхімі [12-14].
Останнім часом було доведено, що ердостеїн впливає не лише на нейтрофільне, але й на алергічне запалення. В експериментальній моделі доведено, що 10-денне застосування ердостеїну призвело до розширення бронхів та збільшення частоти циліарних ударів при алергічному запаленні не лише за рахунок блокади прозапальних цитокінів, але і завдяки збільшенню концентрації протизапального цитокіну ІЛ-10. Саме тому ми можемо з високою ефективністю призначати Ермуцин дітям, у яких спостерігається кашель при алергічних захворюваннях.
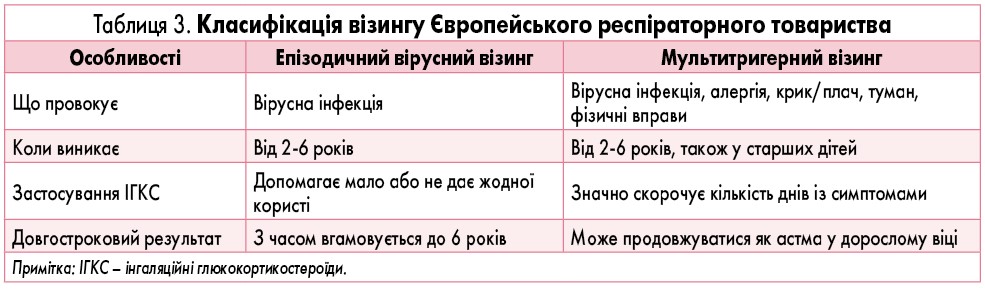
У зв’язку з цим доцільно згадати про бронхообструктивний синдром (візинг), який часто виникає у дітей на тлі вірусних інфекцій та алергічних реакцій внаслідок вираженого набряку слизової та продукції в’язкого мокротиння. У дітей дошкільного віку основним тригером є вірусна інфекція. А у школярів, окрім вірусів, до появи бронхоспазму можуть призвести також і алергічні реакції та інші чинники.
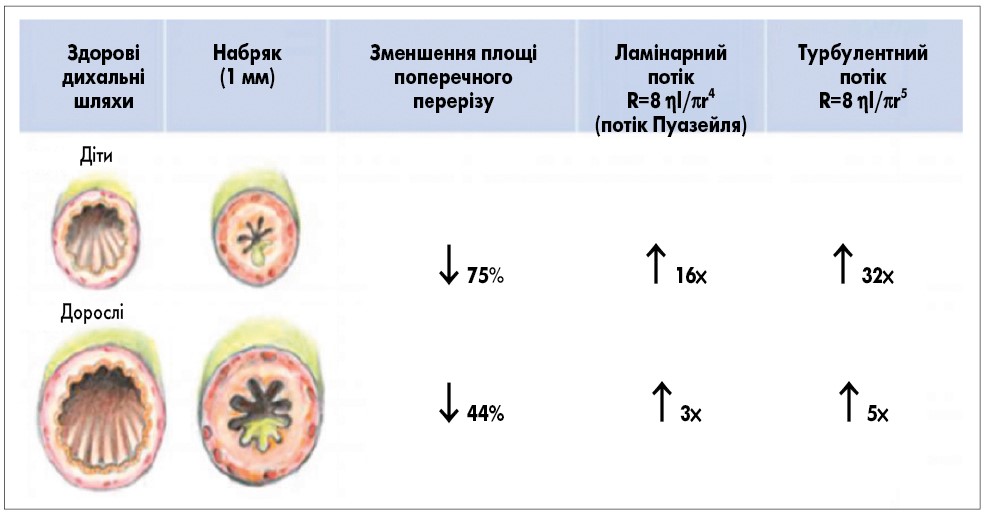
Чому діти схильні до розвитку бронхоспазму? Тому що мають певні анатомо-функціональні особливості, наприклад, просвіт бронхів у дітей відносно менший, ніж у дорослих. Саме тому при вірусних інфекціях або алергічних реакціях діти більш схильні до бронхообструкції через набряк слизових і продукцію в’язкого мокротиння (рис. 2).
Рис. 2. Вплив набряку слизової на зменшення просвіту бронхів у дітей та дорослих
При лікуванні візингу у дітей треба спочатку зняти гіперактивність бронхів: призначити β2-агоністи короткої дії, після цього – Ермуцин, який краще, ніж інші муколітики, впливає на механізми бронхообструкції саме за рахунок комбінації муколітичного ефекту (без збільшення кількості мокротиння) і протизапального ефекту за рахунок блокади цитокінів запалення та активації протизапальних цитокінів.
Сучасні дані також свідчать, що ердостеїн впливає на потенціювання дії антибіотиків, зокрема, значно збільшує їх концентрацію в мокротинні, а включення його до схеми антибактеріальної терапії прискорює досягнення терапевтичного ефекту [16]. Наявні дані підтверджують, що метаболіти ердостеїну значно зменшують адгезію бактерій, зокрема S. aureus, до епітеліальних клітин і виникнення бактеріальних ускладнень [11].
У порівнянні з іншими муколітиками (амброксолом, ацетилцистеїном, карбоцистеїном) Ермуцин має доведені переваги щодо зменшення частоти й тривалості кашлю (метааналіз 15 рандомізованих клінічних досліджень, що включав 1046 пацієнтів).
У педіатричній практиці особливого значення набувають якість та безпека препарату. Ермуцин – це оригінальний ердостеїн італійської компанії Edmomd Pharma, який має патентовану технологію виробництва за допомогою безперервного потокового процесу. Це дозволяє виробляти лікарську речовину такої якості, що за потреби на її основі можна виготовляти навіть ін’єкційні форми.
Таким чином, наявні дані свідчать, що Ермуцин є сучасним муколітиком, який чинить не лише муколітичний, а й протизапальний ефекти при бактеріальному та алергійному запаленні, має високу якість діючої речовини, що дозволяє застосовувати його при лікуванні кашлю різного генезу у дітей.
Список літератури знаходиться в редакції.
Підготувала Анна Хиць
Ермуцин порошок для оральної суспензії
5 мл суспенії містить ердостеїну 175 мг
Дітям дозу визначають відповідно до маси тіла і віку:
- 15-20 кг (3-6 років) – 2,5 мл 2 р/добу;
- 21-30 кг (7-12 років) – 5 мл 2 р/добу;
- >30 кг (>12 років) – 5 мл 3 р/добу.
Дорослим призначають 10 мл препарату 2 р/добу або капсули 300 мг 2 р/добу.
Тематичний номер «Педіатрія»№ 3 (64)-4 (65) 2022 р.