22 листопада, 2022
Оновлені рекомендації EASL із застосування неінвазивних тестів для оцінки тяжкості захворювань печінки різної етіології
 Кількість пацієнтів із хронічними захворюваннями печінки (ХЗП) неухильно зростає. Також зростає і кількість їхніх ускладнень – фіброзу та цирозу печінки, розвиток та тяжкість яких корелює з подальшим прогнозом перебігу захворювання та життя пацієнта. Золотим стандартом діагностики цирозу та фіброзу печінки залишається біопсія, але це обстеження має обмеження та недоліки: вплив людського фактору на проведення процедури та оцінку результатів, інвазивність та, як наслідок, можливі ускладнення, висока вартість. Тому розробка та використання неінвазивних, дешевших та більш простих методів діагностики фіброзу та цирозу печінки дуже важливі. Водночас ці дослідження повинні бути максимально точними та легко відтворюваними, адже фіброз – це динамічний процес, який із часом може як регресувати, так і посилюватися. Неінвазивні тести (НІТ) також повинні забезпечувати прогностичну інформацію про стадію фіброзу та його ускладнення, подальший перебіг захворювання та смертність.
Кількість пацієнтів із хронічними захворюваннями печінки (ХЗП) неухильно зростає. Також зростає і кількість їхніх ускладнень – фіброзу та цирозу печінки, розвиток та тяжкість яких корелює з подальшим прогнозом перебігу захворювання та життя пацієнта. Золотим стандартом діагностики цирозу та фіброзу печінки залишається біопсія, але це обстеження має обмеження та недоліки: вплив людського фактору на проведення процедури та оцінку результатів, інвазивність та, як наслідок, можливі ускладнення, висока вартість. Тому розробка та використання неінвазивних, дешевших та більш простих методів діагностики фіброзу та цирозу печінки дуже важливі. Водночас ці дослідження повинні бути максимально точними та легко відтворюваними, адже фіброз – це динамічний процес, який із часом може як регресувати, так і посилюватися. Неінвазивні тести (НІТ) також повинні забезпечувати прогностичну інформацію про стадію фіброзу та його ускладнення, подальший перебіг захворювання та смертність.
Можливості використання НІТ для різних клінічних ситуацій у контексті ХЗП були представлені в рекомендаціях Європейської асоціації з вивчення печінки (European Association for the Study of the Liver – EASL) «Оновлені рекомендації із застосування НІТ для оцінки гостроти та прогнозу захворювань печінки» (EASL Clinical Practice Guidelines on non-invasive tests for evaluation of liver diseases severity and prognisis – 2021 update).
EASL – це одна з провідних медичних організацій в Європі, яка займається вивченням патології печінки. Її робота перш за все присвячена удосконаленню та розробці досліджень, створенню та оновленню рекомендацій щодо діагностики та лікування захворювань печінки. Також важливим є освітній напрямок роботи для всіх, хто цікавиться темою гепатології.
До НІТ, які використовуються при ХЗП, належать:
- аналізи крові (запатентовані та незапатентовані сироваткові маркери фіброзу, лабораторні показники);
- оцінка фізичних властивостей тканини печінки за допомогою ультразвукового дослідження (УЗД) та еластографії. Найбільш широко в цих цілях застосовується транзієнтна еластографія (ТЕ);
- методи візуалізації, які допомагають оцінити анатомію печінки та інших абдомінальних органів, – УЗД, комп’ютерна томографія (КТ), магнітно-резонансна томографія (МРТ).
Ці дослідження можуть застосовуватися при різних захворюваннях печінки. Водночас усі результати НІТ, біопсії чи інших діагностичних методів повинні бути інтегровані між собою для встановлення коректного діагнозу та стратифікації ризиків.
Важливими аспектами використання НІТ є доступність, вартість та можливість застосування на різних рівнях медичної допомоги. Сироваткові тести широко використовуються, однак їхні результати можуть бути спотворені захворюваннями інших органів чи певними функціональними станами. На результати ТЕ можуть впливати наявність запальних процесів у гепатобіліарній зоні, обструктивний холелітіаз, венозний тромбоз, вживання їжі та заняття спортом напередодні обстеження. Тому рекомендовано утриматися від прийому їжі та тренувань мінімум за 2-3 години до його проведення.
Використання НІТ також має певні системні обмеження. Зокрема, ефективність більшості НІТ для використання на первинній ланці надання медичної допомоги, а також в якості скринінгу в загальній популяції не перевірялася. НІТ мають низьку діагностичну цінність для виявлення фіброзу легкого та середнього ступеня і для визначення ступеня фіброзу загалом. Наразі бракує доказів ефективності НІТ для діагностики субклінічних запальних процесів печінки та ступеня портальної гіпертензії при компенсованому тяжкому ХЗП (КТХЗП; compensated advanced chronic liver disease, cACLD).
Варто зазначити, що термін КТХЗП був запропонований як альтернатива для пацієнтів із ХЗП із ризиком розвитку клінічно значущої портальної гіпертензії (КЗПГ), щоб краще відобразити ступінь тяжкого фіброзу і цирозу печінки у безсимптомних пацієнтів. Відповідно до критеріїв, розроблених консенсусною конференцією Baveno VI, показники жорсткості печінки (Liver stiffness measurement, LSM) зі значенням ≥10 кПа можуть свідчити про розвиток КТХЗП, при LSM ≥15 кПа є висока ймовірність КТХЗП.
Структура рекомендацій базується на етіологічному підході до патології печінки, оскільки це дозволяє порівнювати інформацію щодо гомогенних груп пацієнтів, а також бракує доказів щодо доцільності використання НІТ при мультифакторіальних захворюваннях, що супроводжуються ураженням печінки.
Основні теми, які були розглянуті в цих рекомендаціях: ідентифікація випадків тяжкого фіброзу в загальній популяції та з огляду на низьку поширеність цієї патології серед населення, оцінка тяжкості та прогнозу захворювання у пацієнтів, що зловживають алкоголем, із хронічним вірусним гепатитом С (HCV) після досягнення стійкої вірусологічної відповіді (sustained virological response, SVR), неалкогольною жировою хворобою печінки (НАЖХП), неалкогольним стеатогепатитом (НАСГ), холестатичними та аутоімунними захворюваннями печінки (первинний біліарний холангіт, ПБХ; первинний склерозуючий холангіт, ПСХ; аутоімунний гепатит, АІГ), із КТХЗП та портальною гіпертензією.
Використання НІТ у загальній популяції
- НІТ повинні використовуватися більше з метою виключення фіброзу печінки, ніж для його діагностики при низькій поширеності серед населення (рівень доказовості – РД – 1, сильна рекомендація);
- НІТ повинні застосовуватися в осіб із групи ризикуу розвитку поширеного фіброзу печінки, наприклад, у пацієнтів із метаболічними факторами ризику та/або у тих, хто зловживає алкоголем (РД 2, сильна рекомендація);
- визначення рівнів аланінамінотрансферази (АЛТ), аспартатамінотрансферази (АСТ) та рівня тромбоцитів повинне проводитися на первинній ланці медичної допомоги в усіх пацієнтів, в яких підозрюється захворювання печінки (РД 2, сильна рекомендація);
- у пацієнтів, які мають ризики запущеного фіброзу печінки, а також метаболічні фактори ризику та/або у тих, хто зловживає алкоголем, на первинній ланці рекомендується систематичне проведення тесту fibrosis-4 (FIB-4) для того, щоб провести стратифікацію ризиків та визначити подальшу терапевтичну тактику (РД 1, сильна рекомендація);
FIB-4 – це онлайн-калькулятор, який враховує вік пацієнта, рівні АЛТ, АСТ та тромбоцитів. Проте слід пам’ятати, що цей показник містить непрямі маркери пошкодження печінки. Якщо є підозра, що у пацієнта наявний фіброз печінки, а НІТ при цьому демонструють нормальні показники, слід більш ретельно обстежити пацієнта за допомогою інших методів;
- особам із ризиком запущеного фіброзу печінки через метаболічні фактори та/чи зловживання алкоголем повинні проводити стратифікацію ризиків за допомогою НІТ (РД 1, сильна рекомендація);
- вибір методики НІТ та розробка маршруту пацієнта мають відбуватися у тісній співпраці з фахівцями, які спеціалізуються на захворюваннях печінки (РД 3, сильна рекомендація).
Алгоритм використання НІТ у загальній популяції з метою відбору пацієнтів для подальшого дообстеження та діагностики й визначення ступеня фіброзу представлений на рис. 1.
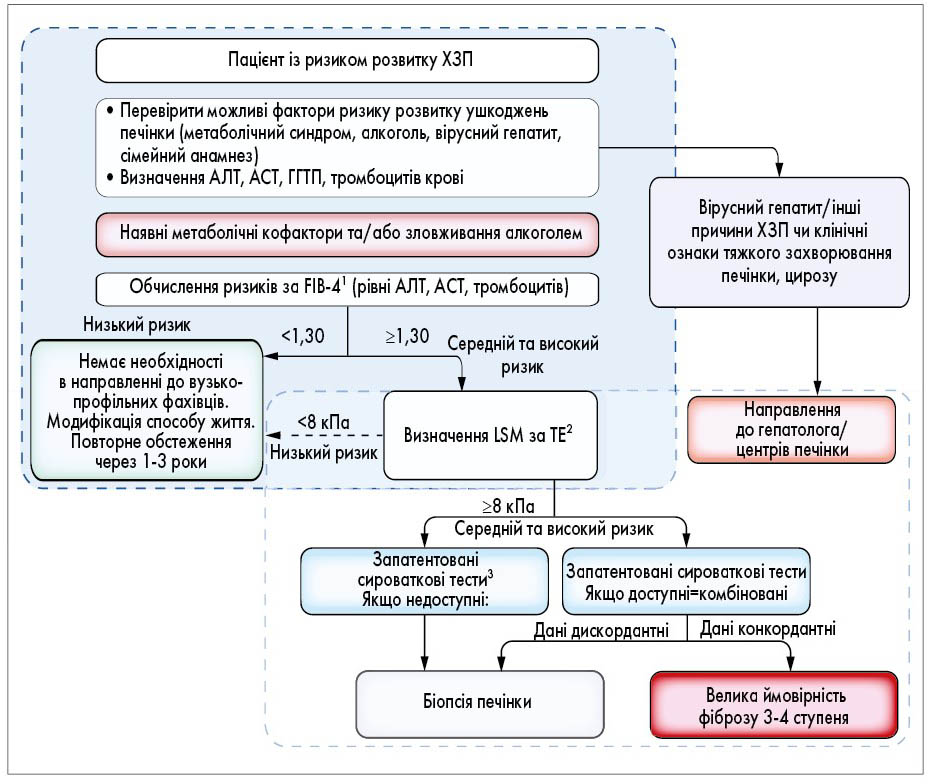 Рис. 1. Алгоритм використання НІТ на первинному рівні надання медичної допомоги. А) Обчислення FIB-4 при метаболічних кофакторах чи зловживанні алкоголем може використовуватися для відбору пацієнтів, які потребують направлення до гепатолога чи в центри печінки. Б) Визначення LSM за TЕ та FIB-4 може проводитися як до, так і після направлення пацієнтів до вузькопрофільних фахівців (залежно від локальних протоколів). В) Запатентовані сироваткові тести: ELFTM (enhanced liver fibrosis); FibroMeter, Fibrotest
Рис. 1. Алгоритм використання НІТ на первинному рівні надання медичної допомоги. А) Обчислення FIB-4 при метаболічних кофакторах чи зловживанні алкоголем може використовуватися для відбору пацієнтів, які потребують направлення до гепатолога чи в центри печінки. Б) Визначення LSM за TЕ та FIB-4 може проводитися як до, так і після направлення пацієнтів до вузькопрофільних фахівців (залежно від локальних протоколів). В) Запатентовані сироваткові тести: ELFTM (enhanced liver fibrosis); FibroMeter, Fibrotest
Алкогольна хвороба печінки
- У пацієнтів із алкогольною хворобою печінки (АХП) та показниками LSM за ТЕ <8 кПa рекомендовано виключити наявність запущеного фіброзу, з повторними проведеннями ТЕ під час подальшого спостереження. Якщо це неможливо, можна використовувати інші НІТ. Зокрема, запатентовані тести ELFТМ (<9,8), FibroMeterТМ (<0,45), FibroTest® (<0,48), незапатентований – FIB-4 (<1,3). У дужках перераховані порогові нормальні показники тестів. Якщо отримані дані нижче за ці показники, то з великою ймовірністю можна виключити можливість розвитку тяжкого фіброзу (РД 3, сильна рекомендація).
- У пацієнтів із АХП та показниками LSM за ТЕ >12-15 кПa можна підтвердити наявність запущеного фіброзу печінки після детального розгляду всіх причин можливого хибнопозитивного результату (РД 2, сильна рекомендація).
- У пацієнтів із підвищеними показниками жорсткості печінки та біохімічними показниками, що свідчать про запальний процес у гепатобіліарній ділянці (збільшення рівнів АСТ чи гамаглютамілтранспептидази – ГГТП), рекомендовано повторити LSM за ТЕ через тиждень після початку утримання від вживання алкоголю або хоча б зменшення його дози (РД 3, сильна рекомендація).
HCV після SVR/антивірусної терапії
- НІТ, LSM за ТЕ та інші методики еластографії неефективні для визначення регресу фіброзу після SVR у пацієнтів із HCV та попередньою антивірусною терапією. Тому їх рутинне використання не рекомендоване (РД 3, сильна рекомендація).
- LSM за ТЕ, що використовувалися для пацієнтів із нелікованим HCV, не повинні використовуватися для визначення ступеня фіброзу печінки після SVR (РД 3, сильна рекомендація).
- У пацієнтів із передньою антивірусною терапією проти HCV та КТХЗП LSM після SVR може бути корисним для оцінки залишкових ризиків, пов’язаних із ураженням печінки (РД 4, сильна рекомендація).
- Пацієнтам із КТХЗП та попередньою антивірусною терапією необхідно продовжити моніторинг для вчасного виявлення гепатоцелюлярної карциноми та портальної гіпертензії незалежно від результатів НІТ (РД 3, сильна рекомендація).
Неалкогольна жирова хвороба печінки та неалкогольний стеатогепатит
- Вимірювання сонографічного згасання ехо-хвилі (controled attenuarion parametr, CAP), яке вже імплементоване в пристрій FibroScan, є перспективною методикою для швидкого та стандартизованого визначення стеатозу. Але її обмежена доступність, а також брак наукових праць, порівняно з дослідженнями ультразвуку, поки не дозволяють рекомендувати CAP як метод діагностики першої лінії (РД 2).
- Також відсутні узгоджені порогові нормальні значення для методики САР, проте показники, більші за 275 дБ/м, можуть свідчити про наявність стеатозу, оскільки продемонстрували понад 90% чутливості до виявлення цієї патології (РД 2).
- НІТ не рекомендовані для діагностики стеатозу печінки в клінічній практиці (РД 2, сильна рекомендація).
- УЗД діагностика рекомендована як засіб першої лінії для виявлення стеатозу, незважаючи на її добре вивчені обмеження (РД 1, сильна рекомендація).
- Кількісна МРТ із вимірюванням протонної щільності жирової фракції печінки (ПЩЖФ, proton density fat-fraction) є найбільш точним неінвазивним методом для діагностики стеатозу. Але він не рекомендований як діагностичний інструмент першої лінії через високу вартість та обмежену доступність (РД 2, сильна рекомендація).
- Біопсія печінки є «золотим стандартом» для діагностики НАСГ, оскільки жоден із наявних НІТ не має достатньої точності для його верифікації (РД 2).
- У пацієнтів із НАЖХП для виключення запущеного фіброзу рекомендовані наступні НІТ при зазначених нормальних порогових значеннях: LSM за TE <8 кПа, ELFТМ <9,8, FibroMeterТМ <0,45, FibroTest® <0,48, FIB-4 <1,3, незапатентований тест NFS (шкала фіброзу при НАЖХП) <1,455 (РД 1, сильна рекомендація).
- Якщо результати НІТ перевищують допустимі порогові значення, то підтвердити чи спростувати запущений фіброз необхідно за допомогою ТЕ (РД 2, сильна рекомендація).
- МРТ є найбільш точним неінвазивним методом для визначення ступеня фіброзу печінки. Але його застосування все ж має незначні переваги перед іншими НІТ і низку обмежень водночас. Тому МРТ не рекомендована як метод діагностики першої лінії (РД 2, сильна рекомендація).
- Для стратифікації ризиків наслідків ураження печінки у пацієнтів із НАЖХП необхідно використовувати індекс відношення АСТ до рівня тромбоцитів (APRI), FIB-4, NFS, ELFTМ, а також LSM за TE (РД 3, сильна рекомендація).
- Повторні НІТ можуть проводитися для уточнення ризиків ускладнень, пов’язаних із ураженням печінки у пацієнтів із НАЖХП/НАСГ. Наразі недостатньо доказів із даними про те, як часто необхідно проводити ці дослідження. Проте в деяких наукових працях вказується на необхідність виконання LSM кожних 3 роки у пацієнтів на ранній стадії захворювання та щорічно – на пізній (РД 3, сильна рекомендація).
- Біопсія печінки залишається найкращим методом для перевірки ефективності медикаментозного лікування на ІІb та ІІІ фазі клінічних досліджень, тому для цих цілей необхідно використовувати саме її (РД 1, сильна рекомендація).
- МРТ ПЩЖФ може застосовуватися для оцінки впливу лікування на розвиток стеатозу. Але мінімальне його зменшення на МРТ ПЩЖФ, яке може мати клінічні прояви, або реакція на призначене лікування все ж мають бути оцінені за допомогою більш точних методів (РД 2, слабка рекомендація).
- Біопсія печінки залишається «золотим стандартом» для оцінки зменшення проявів НАСГ та фіброзу печінки (РД 2, сильна рекомендація).
Холестатичні та аутоімунні захворювання печінки
У пацієнтів із ПБХ визначення сироваткових маркерів фіброзу та виконання інших НІТ не рекомендовані для визначення ступеня уражень у клінічній практиці (РД 3, сильна рекомендація).
- У пацієнтів із ПБХ LSM за ТЕ може використовуватися для діагностики тяжкого фіброзу чи наявності КТХЗП при результатах більших за 10 кПа (РД 3, сильна рекомендація).
- У пацієнтів із ПСХ значення LSM за ТЕ більше ніж 9,5 кПа може слугувати підтвердженням діагнозу запущеного фіброзу у компенсованих пацієнтів із нормальними показниками білірубіну та без стенозу високого ступеня (РД 3, слабка рекомендація).
- У пацієнтів із ПБХ неінвазивне виявлення раннього чи тяжкого фіброзу може бути засноване на біохімічних показниках (рівні альбуміну та білірубіну), а також при результатах LSM за ТЕ більшими за 10кПа (РД 3, сильна рекомендація).
- Протягом лікування стратифікація ризиків має бути заснована на оцінці відповідей на терапію за допомогою шкал GLOBE (Global primary biliary cholangitis Study Group – PBS) та UK-PBC та/або якісних критеріїв (Paris II, Toronto, Rotterdam, Barcelona, Paris I) відповіді. Також для цього може застосовуватися LSM за ТЕ (РД 3, сильна рекомендація).
- У пацієнтів із ПСХ є кореляція між результатами ELFTM, LSM за ТЕ і наслідками захворювання, тому обидва дослідження необхідно використовувати для стратифікації ризиків на початку лікування та в подальшому (РД 3, сильна рекомендація).
- LSM за ТЕ може застосовуватися у пацієнтів, які отримують лікування з приводу АІГ для моніторингу перебігу захворювання разом із визначенням рівнів трансамінази та імуноглобуліну G (Ig G), а також для визначення ступеня фіброзу щонайменше через 6 місяців після імуносупресивної терапії (РД 3, слабка рекомендація).
КТХЗП та портальна гіпертензія
- Запатентовані сироваткові тести та еластографія мають використовуватися для діагностики КТХЗП як методи другої лінії в спеціалізованих закладах (РД 2, сильна рекомендація).
- Fibrotest®, FibroMeterТМ чи ELFТМ можуть застосовуватися для виключення фіброзу, якщо вони доступні (РД 3, сильна рекомендація).
- Значення <8-10 кПа LSM за ТЕ може використовуватися для виключення діагнозу КТХЗП, а >12-15 кПа – для підтвердження. Показники 10-12 кПа потребують додаткових обстежень (РД 3, сильна рекомендація).
- Точкова еластографія зсувної хвилі (point-shear wave elastography – pSWE) та двовимірна еластографія зсувної хвилі (bidimensional shear wave elastography – 2D-SWE) можуть бути застосовані для виключення діагнозу КТХЗП (РД 2, сильна рекомендація).
- Не рекомендовано порівнювати між собою результати різних видів еластографії (РД 3, сильна рекомендація).
Клінічно значуща портальна гіпертензія
- Якщо значення LSM за ТЕ становить >20-25 кПа, то можна діагностувати клінічно значущу портальну гіпертензію (КЗПГ) у пацієнтів із КТХЗП (РД 1, сильна рекомендація).
- Рівень тромбоцитів, розмір селезінки, а також щільність тканини селезінки мають слугувати додатковими маркерами для стратифікації ризиків при КЗПГ (РД 3, сильна рекомендація).
- Наявність портосистемних колатералей на УЗД, КТ чи МРТ є ознакою КЗПГ у пацієнтів із КТХЗП (РД 2, сильна рекомендація).
- Для точної оцінки гостроти портальної гіпертензії та гемодинамічної відповіді у пацієнтів із КТХЗП найбільш точним методом є вимірювання градієнту печінкового венозного тиску (ГПВТ; РД 1, сильна рекомендація).
- У пацієнтів із КТХЗП та нелікованим вірусним гепатитом, коінфекцією вірусом імунодефіциту людини та HCV, зловживанням алкоголем, НАЖХП, ПБС та ПСХ при LSM за ТЕ <20 кПa та рівнем тромбоцитів >150 г/л (критерій Baveno VI) еластографія дозволяє виключити наявність варикозно розширених вен стравоходу та уникнути ендоскопічного обстеження. Цей критерій має застосовуватися там, де є можливість виконати ТЕ (РД 1, сильна рекомендація).
- Показники щільності тканини селезінки можна використовувати як додатковий інструмент для уточнення ризику розвитку варикозно розширених вен стравоходу у пацієнтів із КТХЗП (РД 2, сильна рекомендація).
- Не рекомендовано застосовувати КТ для первинного скринінгу варикозно розширених вен шлунка чи стравоходу, але якщо вона виконується з іншою метою, то варто звернути увагу на можливу локалізацію розширених вен у черевній порожнині (РД 3, сильна рекомендація).
- У пацієнтів із КТХЗП показники LSM мають використовуватися як доповнення до функціональних печінкових проб для стратифікації ризиків клінічної декомпенсації та смертності (РД 1, сильна рекомендація).
- Повторні LSM можуть проводитися для уточнення стратифікації ризиків у пацієнтів із КТХЗП (РД 5, слабка рекомендація).
- LSM може використовуватися додатково до клінічних даних та різноманітних шкал для стратифікації ризиків гепатоцелюлярної карциноми у пацієнтів із КТХЗП, викликаним вірусним гепатитом В (HBV; РД 3, слабка рекомендація).
На рис. 2 представлені НІТ, які можна використовувати для стратифікації ризиків у пацієнтів із КТХЗП.
 Рис. 2. Алгоритм застосування НІТ для діагностики та стратифікації ризиків при різних клінічних ситуаціях у пацієнтів із КТХЗП
Рис. 2. Алгоритм застосування НІТ для діагностики та стратифікації ризиків при різних клінічних ситуаціях у пацієнтів із КТХЗП
Фіброз – одне з найчастіших ускладнень ХЗП незалежно від їх етіології. Його розвиток потребує своєчасної діагностики, прогнозування та розробки подальшої стратегії лікування пацієнта. І хоча найбільш точним методом для визначення тяжкості ураження паренхіми печінки є біопсія, НІТ поступово замінюють цю процедуру на різних рівнях надання медичної допомоги. Проте чимало тестів потребують вивчення їхньої ефективності у тій чи іншій клінічній ситуації. До того ж необхідно знати, який саме НІТ необхідно застосовувати при різних етіологіях та стадіях захворювання. Для того щоб лікарі могли більш детально розібратися у різних аспектах застосування НІТ, спеціалісти EASL з різних країн світу видали оновлені рекомендації. Вони стануть у нагоді як фахівцям первинної ланки надання медичної допомоги, так і працівникам спеціалізованих закладів.
EASL Clinical Practice Guidelines on non-invasive tests for evaluation of liver disease severity and prognosis – 2021 update. J of Hepatology, 2021. https://doi.org/10.1016/j.jhep.2021.05.025
Підготувала Роксоляна Денисюк
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 1(63)-2(64) 2022 р.




