14 січня, 2023
Аналіз результатів 5-річного спостереження після застосування пембролізумабу в ад’ювантній терапії при меланомі III стадії
Опорні рандомізовані контрольовані дослідження у пацієнтів з меланомою шкіри та високим ризиком рецидиву, в яких вивчали інгібітори імунних контрольних точок іпілімумаб, ніволумаб і пембролізумаб та комбінацію інгібітора кінази сімейства Raf типу B (BRAF)/інгібітора мітогенактивованої протеїнкінази дабрафенібу й інгібітора мітогенактивованої протеїнкінази (MEK) траметинібу, що застосовувалися як ад’ювантна терапія, показали обнадійливі результати і стали підставою для схвалення усіх цих лікарських засобів Управлінням з контролю якості харчових продуктів і лікарських препаратів США (FDA) для використання за цим показанням [1-11].
Дослідження, в яких оцінювали іпілімумаб [1-3], пембролізумаб [6-8] і дабрафеніб + траметиніб [9-11], проводили у пацієнтів з меланомою III стадії. Дослідження CheckMate 238, в якому вивчали використання ніволумабу (порівняно з іпілімумабом), включило пацієнтів з меланомою IIIB-C стадії і резекованою меланомою IV стадії [4, 5]. Дослідження SWOG1404, в якому оцінювали пембролізумаб (порівняно з високими дозами інтерферону-2b або іпілімумабом), що застосовувався як ад’ювантна терапія, включило пацієнтів з меланомою IIIA (N2a), IIIB-C стадії і резекованою меланомою IV стадії [12]. Нещодавно подібні позитивні результати були отримані при використанні пембролізумабу як ад’ювантної терапії у пацієнтів з меланомою IIB-C стадії у дослідженні KN-716, які також сприяли схваленню такого лікування FDA [13].
Проведено подвійне сліпе дослідження III фази Європейської організації з вивчення і лікування онкологічних захворювань (EORTC) 1325/KEYNOTE-054 з метою порівняти застосування пембролізумабу як ад’ювантної терапії та плацебо у пацієнтів з резекованою меланомою III стадії високого ризику.
Методи
До дослідження EORTC 1325/KEYNOTE-054 було включено 1019 пацієнтів (вік ≥18), які мали гістологічно підтверджену меланому шкіри з метастазами в регіонарних лімфатичних вузлах. Пацієнтів було рандомізовано на дві групи у співвідношенні 1:1: перша група приймала пембролізумаб у дозі 200 мг (n=514), друга група – контрольна (n=505). Препарати вводилися шляхом внутрішньовенної інфузії через кожні 3 тижні у загальній кількості 18 доз (протягом приблизно 1 року; 1-ша частина дослідження) або до розвитку рецидиву, побічних явищ, значного відхилення від протоколу або відкликання згоди пацієнта на участь у дослідженні.
Пацієнти мали пройти повну регіонарну лімфаденектомію у межах 13 тижнів до лікування. У пацієнтів мала бути або меланома IIIA стадії (хворі з N1a чи N2a повинні були мати принаймні один мікрометастаз розміром >1 мм у найбільшому діаметрі), або IIIB чи IIIC стадії без транзиторних метастазів за класифікацією Американського об’єднаного комітету з раку (AJCC, 2009 року, 7-ме видання) [14]. Функціональний статус пацієнтів мав бути на рівні 0 або 1 бала за шкалою Східної кооперативної онкологічної групи. Критеріями виключення були аутоімунне захворювання, неконтрольовані інфекції, застосування системних кортикостероїдів, попередня системна терапія з приводу меланоми.
Первинною кінцевою точкою була безрецидивна виживаність у загальній популяції і в підгрупі пацієнтів з PD-L1-позитивними пухлинами. Вторинними кінцевими точками були виживаність без віддалених метастазів, загальна виживаність, безпека і пов’язана зі здоров’ям якість життя. Результати оцінки за останніми двома кінцевими точками вже були раніше опубліковані [6-8, 15, 16].
Результати
З серпня 2015 по листопад 2016 року було рандомізовано 1019 пацієнтів у 123 дослідницьких центрах із 23 країн: 514 пацієнтів були розподілені в групу прийому пембролізумабу і 505 – у групу плацебо.
Останній пацієнт отримав пембролізумаб або плацебо у листопаді 2017 року. Однорічне лікування згідно з протоколом пройшли 297 пацієнтів у групі пембролізумабу і 300 пацієнтів у групі плацебо. Медіана тривалості спостереження, визначена в цьому дослідженні, становила 4,9 року в кожній групі лікування.
Безрецидивна виживаність
Загалом 532 пацієнти мали рецидив захворювання або померли: 228 (44,4%) із 514 пацієнтів у групі пембролізумабу і 304 (60,2%) із 505 пацієнтів у групі плацебо. Безрецидивна виживаність через 5 років у групі пембролізумабу й у групі плацебо становила 55,4% (95% ДІ 50,8-59,8) і 38,3% (95% ДІ 33,9-42,7) відповідно; відношення ризиків виникнення рецидиву або смерті становило 0,61 (95% ДІ 0,51-0,72; рис. A). Позитивний ефект лікування спостерігався як щодо локорегіонарних рецидивів, так і щодо віддалених метастазів (рис. А).
У 853 пацієнтів з PD-L1-позитивними пухлинами безрецидивна виживаність через 5 років становила 56,2% (95% ДІ 51,1-61,0) і 40,0% (95% ДІ 35,2-44,8) у групах пембролізумабу і плацебо відповідно; відношення ризиків зі стратифікацією за стадією захворювання дорівнювало 0,62 (99% ДІ 0,48-0,79). Зіставні результати були отримані і для пацієнтів з PD-L1-негативними пухлинами.
Безрецидивна виживаність через 5 років становила 73,2% (95% ДІ 60,8-82,2) і 56,8% (95% ДІ 43,7-67,9) при IIIA стадії, 58,3% (95% ДІ 51,5-64,5) і 39,3% (95% ДІ 32,8-45,9) при IIIB стадії та 45,1% (95% ДІ 37,8-52,2) і 30,0% (95% ДІ 23,7-36,5) при IIIC стадії у групах пембролізумабу і плацебо відповідно. Відношення ризиків дорівнювало 0,61 (99% ДІ 0,30-1,26), 0,59 (99% ДІ 0,42-0,83) і 0,62 (99% ДІ 0,45-0,87) у пацієнтів з меланомою IIIA, IIIB і IIIC стадій відповідно. У пацієнтів із захворюванням IIIB або IIIC стадії за класифікацією AJCC-7 5-річна безрецидивна виживаність становила 52,3% (95% ДІ 47,4-57,1) у групі пембролізумабу і 35,0% (95% ДІ 30,4-39,7) у групі плацебо. Такі ж результати були отримані для стадій за класифікацією AJCC-8 і залежно від статусу за наявністю мутації BRAF. Частка пацієнтів з мутацією BRAF V600, які залишалися живими і без рецидивів через 5 років, дорівнювала 54,3% (95% ДІ 47,0-61,1) у групі пембролізумабу і 35,2% (95% ДІ 29,0-41,4) у групі плацебо (відношення ризиків 0,58; 99% ДІ 0,41-0,81).
Виживаність без віддалених метастазів
Загалом 470 пацієнтів мали віддалені метастази або померли: 201 (39,1%) із 514 пацієнтів у групі пембролізумабу і 269 (53,3%) із 505 пацієнтів у групі плацебо. Виживаність без віддалених метастазів через 5 років становила 60,6% (95% ДІ 56,0-64,9) і 44,5% (95% ДІ 39,9-48,9) у групах пембролізумабу і плацебо відповідно. Відношення ризиків розвитку віддалених метастазів або смерті для цих груп дорівнювало 0,62 (95% ДІ 0,52-0,75; рис. Б). Величина цього ефекту залишалася стабільною в підгрупах, виділених за початковими характеристиками (наприклад, за статусом щодо PD-L1, за стадією відповідно до класифікації AJCC-7 або AJCC-8 чи за статусом щодо наявності мутації BRAF). У підгрупі пацієнтів із меланомою IIIA стадії за класифікацією AJCC-7 (152 пацієнти) виживаність без віддалених метастазів через 5 років становила 78,3% (95% ДІ 67,0-86,1) і 61,4% (95% ДІ 48,0-72,4) у групах пембролізумабу і плацебо відповідно, тоді як у підгрупі пацієнтів із IIIA стадією за класифікацією AJCC-8 (82 пацієнти) – 77,7% (95% ДІ 61,5-87,7) і 66,4% (95% ДІ 49,2-78,9) у групах пембролізумабу і плацебо відповідно.
Виживаність без прогресування/безрецидивна виживаність-2
Загалом 162 (31,5%) із 514 пацієнтів у групі пембролізумабу і 220 (43,6%) із 505 пацієнтів у групі плацебо мали прогресування захворювання чи другий рецидив або померли: 5-річна виживаність без прогресування/безрецидивна виживаність-2 становила 68,2% (95% ДІ 63,9-72,1) у групі пембролізумабу порівняно з 55,5% (95% ДІ 51,0-59,8) у групі плацебо. Відношення ризиків прогресування захворювання чи другого рецидиву або смерті становило 0,65 (95% ДІ 0,53-0,80; рис. В). У підгрупі пацієнтів із захворюванням IIIA стадії за класифікацією AJCC-7 (152 пацієнти) виживаність без прогресування/безрецидивна виживаність-2 через 5 років становила 81,1% (95% ДІ 70,2-88,3) і 73,7% (95% ДІ 61,8-82,4) у групах пембролізумабу і плацебо відповідно, у підгрупі пацієнтів із захворюванням IIIA стадії за класифікацією AJCC-8 – 82,6% (95% ДІ 66,9-91,3) і 77,0% (95% ДІ 60,4-87,3) у групах пембролізумабу і плацебо відповідно.
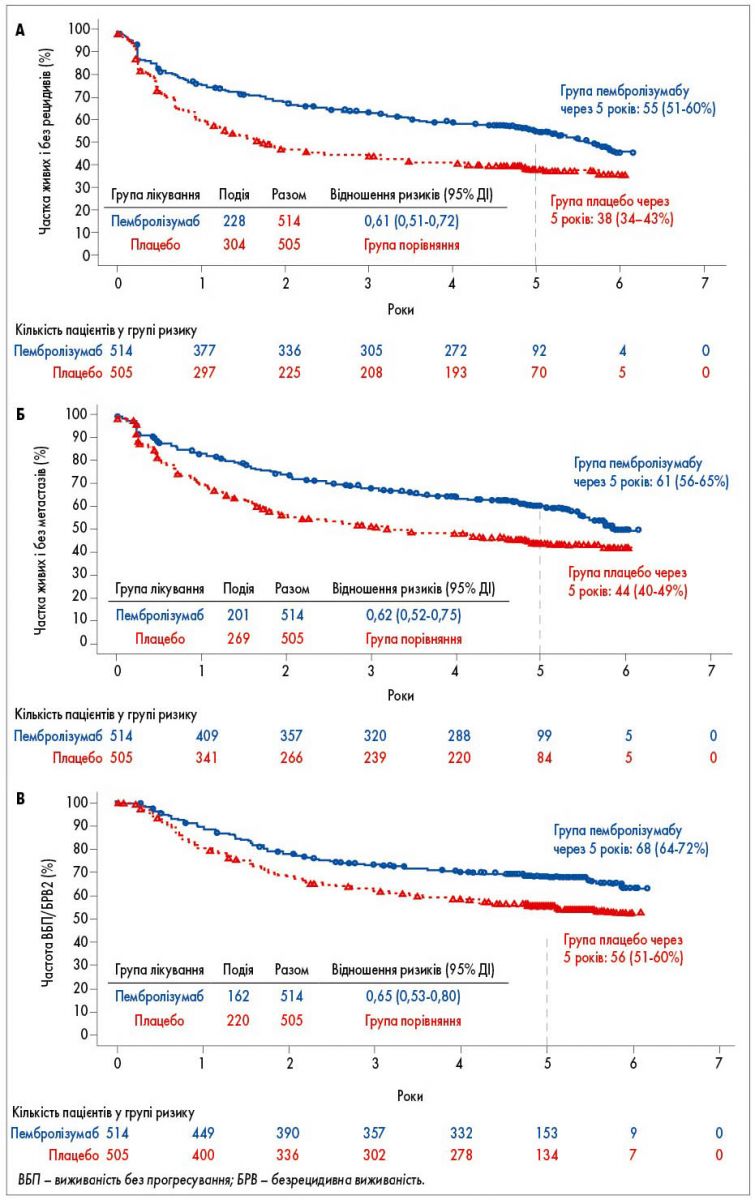 Рис. Показники ефективності, оцінені методом Каплана – Меєра: А – безрецидивної виживаності; Б – виживаності без віддалених метастазів; В – безрецидивної виживаності-2
Рис. Показники ефективності, оцінені методом Каплана – Меєра: А – безрецидивної виживаності; Б – виживаності без віддалених метастазів; В – безрецидивної виживаності-2
Через 4 роки після першого рецидиву частка пацієнтів, які залишалися живими і без прогресування захворювання та другого рецидиву, дорівнювала 21,8% (95% ДІ 15,6-28,6) і 24,3% (95% ДІ 19,4-29,6) у групах пембролізумабу і плацебо відповідно. Медіана тривалості становила 9 місяців в обох групах.
Безпека
Протягом періоду спостереження серйозні побічні явища, пов’язані з лікуванням, зареєстровані у 9 пацієнтів групи пембролізумабу і в 1 пацієнта групи плацебо.
Висновки
Результати аналізу дослідження EORTC1325/KEYNOTE-054 продемонстрували, що порівняно з плацебо ад’ювантна терапія пембролізумабом протягом 12 місяців забезпечувала тривалу стійку користь як за первинною кінцевою точкою (безрецидивною виживаністю), так і за вторинною кінцевою точкою (виживаністю без віддалених метастазів) у пацієнтів із резекованою меланомою III стадії високого ризику. Препарати характеризувалися хорошим профілем безпеки, тяжких побічних ефектів не спостерігалося. Отже, отримані дані свідчать про користь застосування пембролізумабу у пацієнтів із резекованою меланомою III стадії високого ризику.
Реферативний огляд статті Eggermont A.M.M., Kicinski M., Blank C.U. et al. Five-Year Analysis of Adjuvant Pembrolizumab or Placebo in Stage III Melanoma. NEJM Evid. 2022. 1 (11). Doi: https://doi.org/10.1056/EVIDoa2200214.
Підготувала Анна Хиць
Повну версію статті дивіться на сайті: https://evidence.nejm.org/
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 5 (78) 2022 р.



