30 березня, 2025
Рупатадин у лікуванні алергічного риніту: ретроспективний аналіз ефективності в пацієнтів з інтермітуючим і персистуючим перебігом
 Алергічний риніт (АР) – одне з найпоширеніших хронічних захворювань, яке уражає значну частину населення, знижує якість життя, порушує сон, працездатність і концентрацію уваги. За даними епідеміологічних досліджень, поширеність АР у дорослих досягає 20-30% і має тенденцію до зростання.
Алергічний риніт (АР) – одне з найпоширеніших хронічних захворювань, яке уражає значну частину населення, знижує якість життя, порушує сон, працездатність і концентрацію уваги. За даними епідеміологічних досліджень, поширеність АР у дорослих досягає 20-30% і має тенденцію до зростання.
Патофізіологія АР включає як ранню фазу запалення, зумовлену вивільненням гістаміну з опасистих клітин, так і пізню фазу, в якій ключову роль відіграють інші медіатори, зокрема фактор активації тромбоцитів (PAF), цитокіни та хемокіни. Ця складна запальна каскадність пояснює випадки недостатнього контролю симптомів при застосуванні традиційних антигістамінних препаратів ІІ покоління, які блокують лише гістамінові H1-рецептори.
Рупатадин – сучасний селективний антагоніст гістамінових H1-рецепторів, який одночасно блокує PAF‑рецептори. Завдяки цьому комбінованому механізму дії він впливає як на ранню, так і на пізню фазу алергічного запалення, забезпечуючи виражену протинабрякову, протизапальну та симптоматичну дію при АР.
У клінічній практиці на особливу увагу заслуговують пацієнти, у яких традиційна терапія АР виявилася малоефективною. Саме в таких випадках доцільним видається використання рупатадину як препарату з розширеним спектром дії.
Матеріали та методи
Проведено ретроспективне одноцентрове дослідження, спрямоване на оцінку клінічної ефективності рупатадину в пацієнтів із різними клінічними формами АР, які перебували на амбулаторному лікуванні в ЛОР‑відділенні міської клінічної лікарні № 11 м. Одеси. Через ретроспективний характер дослідження отримання інформованої згоди не вимагалося. Дані були знеособлені та оброблялися з дотриманням етичних принципів Належної клінічної практики (GCP).
До аналізу включено 200 пацієнтів віком від 18 до 65 років (122 жінки, 78 чоловіків), які звернулися по медичну допомогу з приводу симптомів АР, що недостатньо контролювалися на фоні попереднього лікування, зокрема за допомогою інших антигістамінних препаратів ІІ покоління.
Пацієнтів було розподілено на дві групи:
- група 1 (n=120): інтермітуючий АР;
- група 2 (n=80): персистуючий АР.
Діагноз встановлювали на підставі клінічної картини, даних анамнезу, огляду та результатів алергологічного обстеження.
Критеріями включення були вік від 18 до 65 років; наявність симптомів АР (закладеність носа, ринорея, чхання, свербіж); попереднє лікування антигістамінними препаратами, яке не забезпечило належного контролю симптомів; повнота медичної документації щодо динаміки симптомів у процесі лікування рупатадином.
Критерії виключення: ознаки гострого бактеріального синуситу (за результатами клінічного та рентгенологічного обстеження); супутні тяжкі соматичні або психічні захворювання; наявність в анамнезі гіперчутливості до рупатадину; вагітність або лактація.
Усім пацієнтам призначався рупатадин (Рупафін, Zentiva) у дозі 10 мг 1 раз на добу впродовж 7-10 днів без інших супутніх антигістамінних чи системних протизапальних препаратів.
Оцінка динаміки симптомів здійснювалася шляхом порівняння значень на 1-й день лікування та на 7-10-й день терапії. Використовували такі інструменти:
- шкала Total Nasal Symptom Score (TNSS): оцінювалася інтенсивність 4 основних назальних симптомів (ринорея, закладеність, свербіж у носі, чхання). Кожен симптом оцінювався за 4-бальною шкалою (0-3), максимальний бал – 12;
- шкала Total Ocular Symptom Score (TOSS): у пацієнтів із супутніми очними симптомами (свербіж, почервоніння, сльозотеча) застосовувалася аналогічна шкала з максимальною оцінкою 9 балів;
- Mini Rhinoconjunctivitis Quality of Life Questionnaire (MiniRQLQ): містить 14 питань, що охоплюють симптоми, емоційний стан, повсякденну активність, сон і соціальні взаємодії. Кожне питання оцінюється пацієнтом за 7-бальною шкалою, де 0 – «не турбує зовсім», 6 – «турбує максимально». Результати розраховували як середнє арифметичне балів за всіма пунктами.
На завершальному етапі лікування усім пацієнтам було запропоновано відповісти на питання Patient Global Impression of Change (PGIC) – стандартизованої шкали для суб’єктивної оцінки динаміки стану. Формулювання запитання: «Як Ви оцінюєте зміни у своєму загальному стані після початку лікування?». Можливі варіанти відповідей: «значно покращився», «покращився», «не змінився», «погіршився», «значно погіршився». PGIC дозволяє кількісно оцінити загальне відчуття ефективності терапії з боку пацієнта та використовується як додатковий параметр реальної клінічної ефективності.
Аналіз даних проводився за допомогою стандартних методів описової статистики. Для кількісних показників розраховували середні значення (M) та стандартне відхилення (SD). Для порівняння показників до та після лікування використовували парний t-тест або тест Вілкоксона залежно від типу розподілу. Рівень статистичної значущості встановлювався на рівні p<0,05.
Результати
Усі 200 пацієнтів завершили повний курс терапії рупатадином. Препарат добре переносився, випадків відміни через побічні реакції не зафіксовано, що свідчить про сприятливий профіль безпеки в амбулаторних умовах. У жодного з пацієнтів не відзначено побічних ефектів, які потребували б медичного втручання чи корекції дози рупатадину.
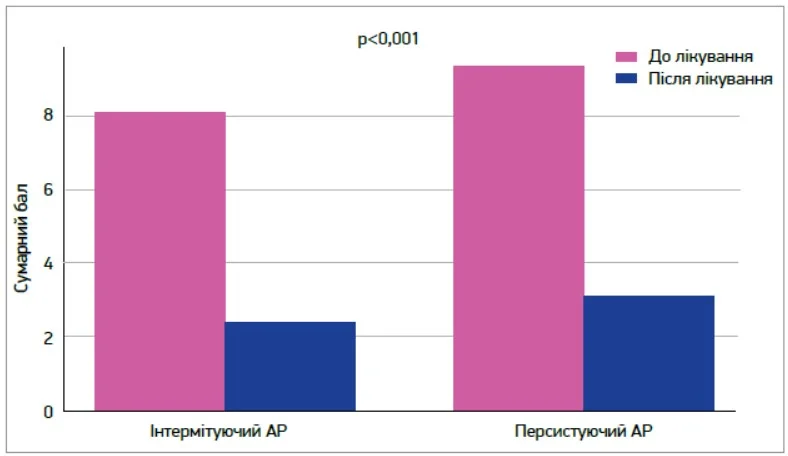
У динаміці лікування спостерігалося достовірне зниження вираженості основних назальних симптомів. За шкалою TNSS середній бал у пацієнтів з інтермітуючим АР зменшився з 8,1±1,6 до 2,3±1,4 бала (p<0,001), а в пацієнтів із персистуючим перебігом – з 9,4±1,3 до 3,1±1,7 бала (p<0,001) (рис. 1). Покращення спостерігалося вже протягом перших 2-3 днів прийому препарату.
Рис. 1. Зміна вираженості назальних симптомів (TNSS)
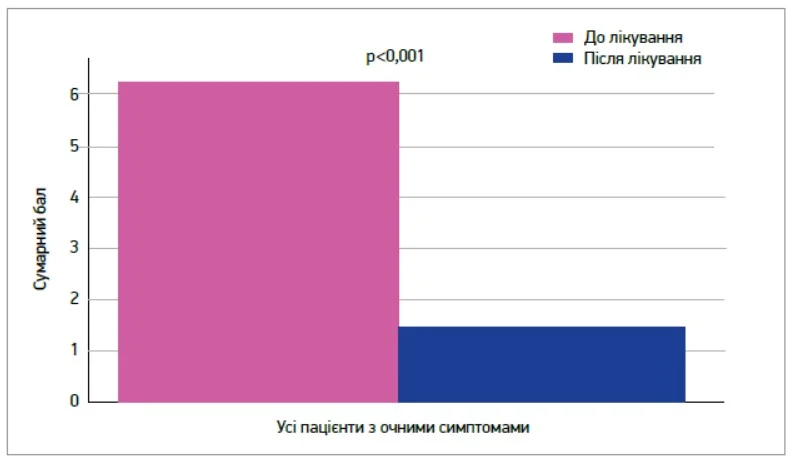
У пацієнтів із наявними очними симптомами (52% випадків) оцінка за шкалою TOSS також демонструвала значуще зниження – з 6,2±1,1 до 1,4±0,8 бала (p<0,001) (рис. 2), що підтверджує системну дію препарату на весь спектр симптомів АР.
Рис. 2. Зміна вираженості очних симптомів (TOSS)
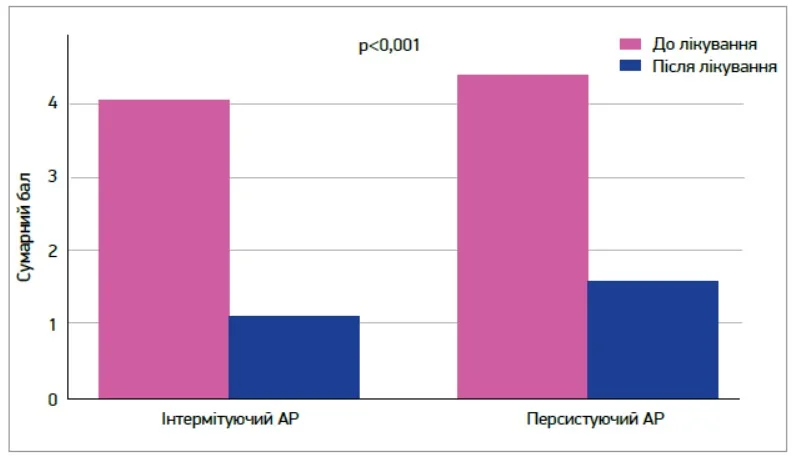
Покращення якості життя було зафіксовано за результатами MiniRQLQ. Середній бал у пацієнтів з інтермітуючим АР знизився з 3,9±0,7 до 1,1±0,5, а в пацієнтів із персистуючим перебігом – з 4,3±0,8 до 1,6±0,6 (p<0,001 в обох групах) (рис. 3). Найбільше покращення зафіксовано у сферах сну та повсякденної активності, що особливо важливо для оцінки впливу лікування на функціональне самопочуття пацієнтів.
Рис. 3. Зміна якості життя (MiniRQLQ)
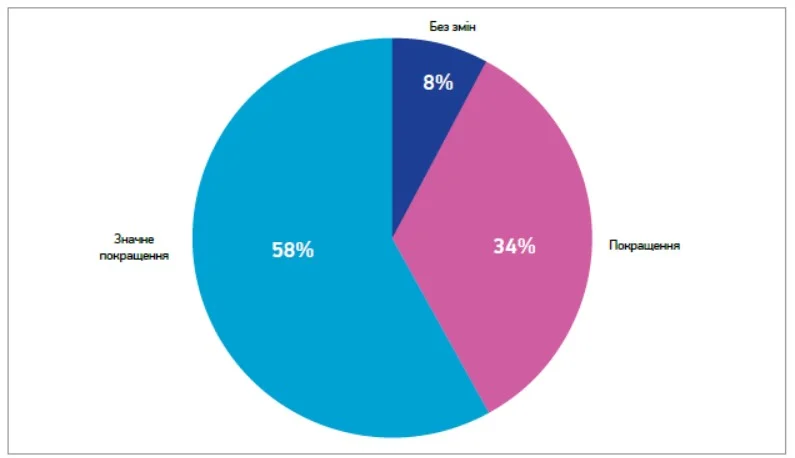
За результатами оцінки PGIC, 58% пацієнтів відзначили «значне покращення» свого стану, 34% – «покращення», тоді як жоден пацієнт не повідомив про погіршення симптомів (рис. 4). Отже, загальна ефективність лікування рупатадином у реальній клінічній практиці була високою, з вираженим зменшенням як суб’єктивних, так і об’єктивно оцінених проявів АР.
Рис. 4. Зміна стану за суб’єктивною оцінкою пацієнтів (PGIC)
Обговорення
Алергічний риніт належить до найпоширеніших хронічних захворювань у дорослого населення, маючи не лише значну епідеміологічну, а й соціально-економічну вагу. На перший погляд «легкий» нежить насправді може суттєво знижувати якість життя, порушуючи сон, концентрацію уваги, працездатність і навіть психоемоційний стан. У багатьох пацієнтів перебіг АР є тривалим або має рецидивуючий характер, формуючи потребу в регулярному або повторному медикаментозному втручанні. За оцінками ARIA (Allergic Rhinitis and its Impact on Asthma), в основі успішного контролю симптомів АР лежить індивідуалізований підхід до лікування з урахуванням частоти, тривалості, тяжкості симптомів і впливу на повсякденне життя пацієнта.
Серед препаратів першої лінії в сучасних рекомендаціях чільне місце посідають неседативні антигістамінні препарати ІІ покоління. Вони рекомендовані як для початкової терапії, так і для тривалого застосування в пацієнтів з інтермітуючим або легким персистуючим перебігом АР. Проте клінічний досвід і результати досліджень свідчать, що не всі пацієнти досягають бажаного контролю симптомів лише на фоні стандартного блокування гістамінових H1-рецепторів. У реальній практиці доволі часто трапляються ситуації, коли, незважаючи на дотримання схеми прийому препаратів ІІ покоління, в пацієнтів зберігаються закладеність носа, ринорея або свербіж. Це може бути пов’язано з індивідуальними особливостями метаболізму, коморбідністю (наприклад, алергічний кон’юнктивіт), або з тим, що в розвитку симптомів бере участь не лише гістамін, а й інші медіатори, зокрема фактор активації тромбоцитів (PAF), цитокіни, хемокіни.
У цьому контексті особливого значення набувають антигістамінні препарати з додатковими механізмами дії, як-от рупатадин. Завдяки здатності блокувати як H1-рецептори, так і рецептори до PAF рупатадин впливає на обидві фази алергічного запалення – ранню та пізню. Це забезпечує більш комплексну протизапальну дію та потенційно кращий контроль симптомів у «важчих» пацієнтів – тих, хто не відповідає на стандартну антигістамінну терапію.
Одним із ключових компонентів пізньої фази алергічного запалення є фактор активації тромбоцитів (PAF, platelet-activating factor) – потужний медіатор, який відіграє важливу роль у розвитку набряку, посиленні судинної проникності, міграції еозинофілів і пролонгації запалення. PAF синтезується різними клітинами, включаючи опасисті клітини, еозинофіли, базофіли, макрофаги, ендотеліальні клітини, у відповідь на стимуляцію алергенами або запальними сигналами.
Особливість PAF полягає в його сильному судинорозширювальному ефекті, здатності індукувати дегрануляцію опасистих клітин і посилювати відповідь гістамінзалежного запалення, що клінічно проявляється стійкою закладеністю носа, ринореєю, іноді – гіперреактивністю нижніх дихальних шляхів. У пацієнтів із персистуючим або тяжким перебігом АР підвищена активність PAF корелює з тривалістю симптомів та їх резистентністю до стандартної терапії.
Рупатадин є єдиним серед антигістамінних ІІ покоління, який одночасно блокує гістамінові H1-рецептори та рецептори до PAF, тим самим перериваючи як гістамінзалежні, так і PAF‑опосередковані ланки запалення. Цей подвійний механізм дії дозволяє ефективніше знижувати не лише гострі симптоми алергії (наприклад, чхання, свербіж), а й стійкі прояви, зумовлені хронічною запальною відповіддю, зокрема закладеність носа та постійне слизове виділення, які найчастіше залишаються неконтрольованими при використанні звичайних H1-блокаторів.
У нашому дослідженні було продемонстровано, що рупатадин забезпечує достовірне покращення симптомів АР вже протягом першого тижня лікування у пацієнтів як з інтермітуючим, так і з персистуючим перебігом. Зменшення сумарного бала TNSS свідчить про значне полегшення основних симптомів риніту, а зниження TOSS підтверджує ефективність препарату при супутньому алергічному кон’юнктивіті. На особливу увагу заслуговує динаміка показників MiniRQLQ: зниження балів за всіма доменами, включно зі сном, емоційним станом та соціальною активністю, свідчить не лише про зменшення симптомів, а й про покращення повсякденного функціонування пацієнтів. Високий відсоток пацієнтів, які оцінили свій стан як «значно покращений», узгоджується з об’єктивними показниками ефективності й доводить важливість врахування суб’єктивного досвіду пацієнта при оцінці результатів терапії.
Ще одним важливим аспектом, що підтверджується нашим аналізом, є сприятливий профіль безпеки рупатадину. Жоден пацієнт не відзначив небажаних ефектів, що збігається з результатами багатоцентрових клінічних випробувань і дає підстави рекомендувати препарат для широкого застосування в амбулаторній практиці.
Наше дослідження має певні обмеження, зумовлені його ретроспективним характером, проте саме такий підхід дозволяє відобразити реальні умови клінічного застосування препарату з типовими пацієнтськими запитами, анамнезом і лікувальними рішеннями. Результати підтверджують ефективність рупатадину не лише як препарату для стартової терапії АР, а й як раціонального варіанта заміни у випадках недостатньої відповіді на інші антигістамінні засоби ІІ покоління.
Висновки
Результати ретроспективного аналізу клінічного застосування рупатадину в пацієнтів з АР свідчать про його високу ефективність як при інтермітуючому, так і при персистуючому перебігу захворювання. Застосування препарату асоціювалося з достовірним зменшенням вираженості назальних та очних симптомів, покращенням якості життя, сну і повсякденної активності.
Рупатадин продемонстрував добру переносимість і сприятливий профіль безпеки, що є особливо важливим у контексті амбулаторного лікування. Подвійний механізм дії – блокада H1-рецепторів та антагонізм до PAF – забезпечує переваги в контролі симптомів у пацієнтів, у яких терапія іншими антигістамінними засобами виявилася недостатньо ефективною.
Отримані результати дозволяють розглядати рупатадин як раціональний вибір у лікуванні пацієнтів з АР, особливо за наявності стійких проявів або супутнього алергічного кон’юнктивіту, а також як альтернативу в разі недостатньої відповіді на стандартні препарати ІІ покоління.
Медична газета «Здоров’я України 21 сторіччя» № 5 (591), 2025 р