27 березня, 2015
Безопасность применения сердечно-сосудистых лекарственных средств
 В последние годы для лечения целого ряда сердечно-сосудистых заболеваний (ССЗ) – хронической сердечной недостаточности (СН), артериальной гипертензии (АГ) острого инфаркта миокарда, стенокардии, аритмий – используется множество лекарственных средств (ЛС), эффективных с позиций доказательной медицины: ингибиторы ангиотензинпревращаюшего фермента (ИАПФ), b-адреноблокаторы (БАБ), антагонисты кальция (АК), гиполипидемические и антиагрегантные препараты. Для многих ЛС этих групп подтвержден высокий уровень доказательности, то есть высокая достоверность данных, полученных в ходе крупных рандомизированных клинических исследований.
В последние годы для лечения целого ряда сердечно-сосудистых заболеваний (ССЗ) – хронической сердечной недостаточности (СН), артериальной гипертензии (АГ) острого инфаркта миокарда, стенокардии, аритмий – используется множество лекарственных средств (ЛС), эффективных с позиций доказательной медицины: ингибиторы ангиотензинпревращаюшего фермента (ИАПФ), b-адреноблокаторы (БАБ), антагонисты кальция (АК), гиполипидемические и антиагрегантные препараты. Для многих ЛС этих групп подтвержден высокий уровень доказательности, то есть высокая достоверность данных, полученных в ходе крупных рандомизированных клинических исследований.
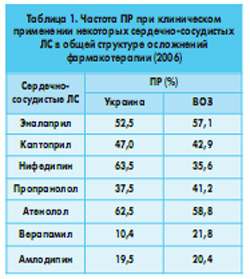
Сердечно-сосудистые ЛС являются причиной осложнений фармакотерапии (ФТ) у 2-8% больных (ВОЗ, 2004). В структуре побочных реакций (ПР), зарегистрированных Государственным фармакологическим центром (ГФЦ) МЗ Украины по состоянию на 01.03.2007, эффекты от применения сердечно-сосудистых ЛС составляли 18%. По итогам 2006 г. в топ-20 препаратов по частоте регистрации ПР ЛС в Украине доля сердечно-сосудистых ЛС составляла 25% (эналаприл – 6-я позиция, пентоксифиллин – 7-я, каптоприл – 10-я, лидокаин – 11-я, нифедипин – 14-я). В таблице 1 приведены сравнительные данные по частоте ПР, не связанных с качеством применяемых препаратов, при использовании ряда распространенных сердечно-сосудистых ЛС в Украине и в мире (ВОЗ, 2006).
По данным ВОЗ, при авиакатастрофах погибают 1:3 млн пассажиров, а при проведении фармакотерапии – 1:300 пролеченных больных. Часть из них (4-17%) связана с врачебными ошибками. И дело не только в этом. При появлении на рынке новейших, высокоэффективных ЛС сама по себе не может исчезнуть обеспокоенность в отношении потенциальных известных и не описанных ранее ПР, связанных с их применением.
Вместе с тем, какими бы ни были успехи в области рациональной ФТ ССЗ, современный эффективный контроль за безопасностью – значимой составляющей лечения указанных выше патологических состояний – является важнейшим направлением в здравоохранении и кардиологии в частности.
 В начале 1980-х годов экспертами ВОЗ были разработаны основные требования к ЛС: эффективность, безопасность, доступность и приемлемость для пациента, а также определен главный фармакотерапевтический критерий – соотношение польза/риск. Все эти требования вскоре стали неотъемлемой частью одного из основных направлений современной медицины, рациональной ФТ. Под рациональной ФТ понимают принципы назначения ЛС, отвечающие условиям конкретной клинической ситуации, в дозах, комплементарных индивидуальным требованиям больного на адекватный период времени и с наименьшими затратами для пациента и общества.
В начале 1980-х годов экспертами ВОЗ были разработаны основные требования к ЛС: эффективность, безопасность, доступность и приемлемость для пациента, а также определен главный фармакотерапевтический критерий – соотношение польза/риск. Все эти требования вскоре стали неотъемлемой частью одного из основных направлений современной медицины, рациональной ФТ. Под рациональной ФТ понимают принципы назначения ЛС, отвечающие условиям конкретной клинической ситуации, в дозах, комплементарных индивидуальным требованиям больного на адекватный период времени и с наименьшими затратами для пациента и общества.
В своем развитии клиническая фармакология прошла во второй половине XX ст. несколько принципиальных этапов, которые стали основой дальнейшего развития ее научных направлений:
– 1960-1970 гг. – начало проведения клинических испытаний, введение мониторинга нежелательных ПР, развитие фармакокинетики;
– 1970-1980 гг. – изучение взаимодействия ЛС, фармакогенетики, введение терапевтического мониторинга, усовершенствование методов оценки эффективности и методологии клинических исследований ЛС;
– 1980-1990 гг. – введение фармакоэпидемиологических исследований, создание международной (ВОЗ) базы данных ПР, переход к индивидуальному дозированию ЛС, введение международной (ВОЗ) и национальной систем информации про ЛС, применение методов контроля медикаментозной терапии в клинике;
– 1990-2000 гг. – практическое освоение методик молекулярной фармакогенетики, оценки режима дозирования ЛС, фармакокинетических принципов оптимизации эффектов ЛС, доказательной фармакотерапии и фармакоэкономики.
При выборе того или иного ЛС врачу необходимо проанализировать как можно больше различных факторов, потенциально влияющих на успех лечения, в том числе клинико-фармакологических параметров ЛС, минимизируя при этом вероятность развития нежелательных ПР. Подобный подход вполне справедлив и в отношении одной из самых обширных групп современных ЛС как по номенклатуре, так и по разнообразию механизмов действия – сердечно-сосудистых препаратов.
Согласно ВОЗ все современные сердечно-сосудистые ЛС, рекомендуемые для применения в клинической практике, подразделяются на основные и неосновные классы. Например, в соответствии с рекомендациями ВОЗ шесть классов ЛС относятся к числу основных препаратов для лечения АГ: тиазидные диуретики, БАБ, ИАПФ, блокаторы медленных кальциевых каналов (АК), блокаторы рецепторов ангиотензина (БРА), a-адреноблокаторы (Ю.П. Беленков, В.Ю. Мареев, 2003). Прочие ЛС, а именно производные раувольфии, клонидин, дибазол, папазол, комбинированные препараты, содержащие апрессин (Адельфан, Трирезид К), Но-шпа и др., не рекомендованы в качестве основных для лечения АГ. Для лечения хронической СН используют пять основных классов ЛС: ИАПФ, БАБ, диуретики, сердечные гликозиды (СГ) и антагонисты альдостерона. Не рекомендованы, но пользуются большой популярностью у практикующих врачей нитраты.
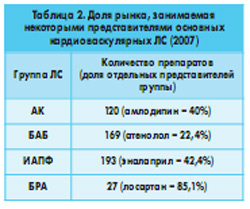 В Украине в настоящее время разрешено для медицинского применения свыше 700 представителей вышеупомянутых ЛС. Например, только общее количество препаратов АК (по состоянию на 01.06.2007) превысило 120 наименований, a-адреноблокаторов – 50, а диуретиков – 95. В первой группе соответственно доминировали дигидропиридиновые производные (74,2%), во второй – доксазозин (70,2%), в третьей – тиазидные производные. Выбор препарата в соответствии с принципами доказательной медицины и рациональной ФТ среди такого разнообразия ЛС требует от врача-кардиолога глубоких знаний в области клинической фармакологии. Препараты, при медицинском применении которых по данным ГФЦ МЗ Украины чаще всего возникают ПР, занимают значительный удельный вес в общем объеме выпуска ЛС своей фармакологической группы (табл. 2).
В Украине в настоящее время разрешено для медицинского применения свыше 700 представителей вышеупомянутых ЛС. Например, только общее количество препаратов АК (по состоянию на 01.06.2007) превысило 120 наименований, a-адреноблокаторов – 50, а диуретиков – 95. В первой группе соответственно доминировали дигидропиридиновые производные (74,2%), во второй – доксазозин (70,2%), в третьей – тиазидные производные. Выбор препарата в соответствии с принципами доказательной медицины и рациональной ФТ среди такого разнообразия ЛС требует от врача-кардиолога глубоких знаний в области клинической фармакологии. Препараты, при медицинском применении которых по данным ГФЦ МЗ Украины чаще всего возникают ПР, занимают значительный удельный вес в общем объеме выпуска ЛС своей фармакологической группы (табл. 2).
В нашей стране системный анализ подобных данных не производился, однако, судя по номенклатуре фармацевтического рынка, соотношение отдельных представителей фармакологических групп принципиально не отличается от приведенных выше. Об этом свидетельствуют зарегистрированные в Украине за 1996-2006 гг. ПР при клиническом применении отдельных ЛС. Так, по данным отдела фармакологического надзора ГФЦ МЗ Украины, при назначении некоторых ЛС, например каптоприла, ПР регистрировались по отношению к другим ИАПФ в 47% случаев (по данным ВОЗ – 42,9%, а в Великобритании – 12,7%); при назначении нифедипина по отношению к другим АК – в 63,55% (по данным ВОЗ – 35,6%); при использовании атенолола по отношению к другим БАБ – в 62,5% (по данным ВОЗ – 58,2%, а в Великобритании – 7,27%).
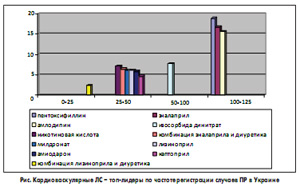
В 2007 г. перечень топ-лидеров среди ЛС в Украине по частоте регистрации случаев ПР подвергся некоторым изменениям за счет появления новых наименований ЛС, давно известных своей способностью вызывать ПР (кислоты никотиновой, амлодипина, лизиноприла, пентоксифиллина). По данным ГФЦ МЗ Украины на 2008 г., этот своего рода рейтинг можно проиллюстрировать следующим образом (рис.).
 Среди системных нарушений, зарегистрированных при использовании различных групп сердечно-сосудистых ЛС, наблюдались разнообразные отклонения (табл. 3).
Среди системных нарушений, зарегистрированных при использовании различных групп сердечно-сосудистых ЛС, наблюдались разнообразные отклонения (табл. 3).
Таким образом, для ИАПФ были характерны нарушения функции дыхания и аллергические реакции, для АК – сердечно-сосудистые и аллергические, для БАБ – сердечно-сосудистые реакции и осложнения со стороны центральной нервной системы, для дигиталиса – сердечно-сосудистые осложнения, реакции со стороны центральной нервной системы и пищеварительного тракта, аллергические реакции.
ПР в результате применения сердечно-сосудистых ЛС можно разделить на кардиальные и экстракардиальные. Кардиальные ПР проявляются в виде тахи- или брадикардии, других нарушений сердечного ритма и проводимости, снижения или повышения артериального давления, нарушения сократимости миокарда. Риск их возникновения может возрастать при комбинации с другими ЛС. Так, тиазидные диуретики и резерпин способствуют развитию интоксикации СГ. Симпатомиметики даже в невысоких дозах оказывают аритмогенное действие при их назначении в сочетании с некоторыми анестезирующими средствами. Антиаритмические ЛС способны оказывать негативное влияние на нормальный ритм сердца, приводить к развитию блокад или аритмий. Ишемию миокарда могут спровоцировать трициклические антидепрессанты, дигоксин, прокаинамид. Дипиридамол, вводимый внутривенно, вызывает синдром коронарного обкрадывания, проявляющийся ухудшением кровоснабжения ишемизированных участков миокарда.
Различным фармакологическим группам сердечно-сосудистых ЛС присущи свои особенности проявления ПР. По данным В.Т. Кукеса (1993), лечение СГ может обусловливать интоксикацию в 26-29% случаев. ПР развиваются при использовании строфантина, изоланида, дигоксина. При этом прогрессирование СН ведет к увеличению частоты интоксикации СГ с 12 до 46%. Клинически это явление проявляется сердечно-сосудистыми (92%), диспепсическими (37%) и нервно-психическими (8,4%) нарушениями. Среди кардиоваскулярных расстройств чаще всего отмечается суправентрикулярная (12%) и желудочковая (73%) экстрасистолия. У 11,6% больных развивается пароксизмальная суправентрикулярная тахикардия, у 15,5% – нарушение кардиальной проводимости. Характерным для интоксикации СГ является снижение суточного диуреза.
Обладая высоким раздражающим эффектом, СГ вызывают нарушение функции пищеварительной системы. Появляются анорексия, тошнота, рвота, диарея, боль в животе. По данным R. Fowler et al. (1970), при назначении СГ детям в 93% случаев возникает рвота. СГ вызывают нарушение сна у 81% больных, а при длительном применении препаратов наперстянки возможно развитие психических расстройств вплоть до психозов. Иногда эти препараты вызывают расстройство цветного зрения, а в тяжелых случаях – ретробульбарный паралич, поражение зрительного нерва, нарушение слуха, невралгии тройничного, седалищного, локтевого нервов, люмбалгию. СГ оказывают токсическое действие на функцию почек, поэтому возможно развитие почечной недостаточности.
Наиболее частые нарушения при передозировке СГ развиваются со стороны сердечно-сосудистой системы. Так, препараты наперстянки у 10% пациентов вызывают чувство давящей боли в области сердца. Прием СГ приводит к изменениям в электролитном обмене, к которым чувствителен прежде всего миокард. При этом развитие гипокалиемии и гиперкальциемии считается ключевым моментом в возникновении аритмий. Последние проявляются в виде брадикардии, экстрасистолии, тахикардии (синусовой, предсердной либо желудочковой). Грозным осложнением дигиталисной терапии является фибрилляция желудочков, приводящая к летальному исходу. При лечении СГ у 3/4 пациентов развивается брадикардия, более чем у половины – атриовентрикулярная блокада. Очень часто у детей регистрируется выпадение пульса (87%).
При приеме антиаритмических ЛС отмечаются нарушения нервно-психической функции. Появляются головная боль, головокружение, психомоторное возбуждение, бессонница, галлюцинации, депрессивные расстройства, сумеречные состояния сознания, бред. Одновременно могут обнаруживаться нарушения зрения и слуха, вплоть до полной их потери. Аллергические поражения характеризуются появлением сыпи, зуда, повышением температуры тела, развитием ангионевротического отека или крапивницы, а также системной красной волчанки. При длительном или повторном применении антиаритмических ЛС может наблюдаться развитие пурпуры вследствие приема хинидина. Осложнения, возникающие в ответ на введение коронаролитиков, чаще всего имеют аллергический, реже – токсический характер. Кожные поражения проявляются в виде зуда, сыпи, покраснения или бледности кожи, крапивницы, отека слизистых оболочек. Возможны одышка, приступы удушья, бронхоспазм, отек Квинке.
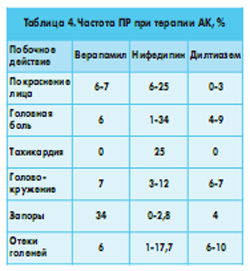 Большой практический интерес имеют также ПР, вызываемые приемом АК (табл. 4). При медицинском применении b-адреноблокаторов наблюдаются кардиальные (брадикардия, АГ, атриовентрикулярные блокады) и экстракардиальные (головокружение, депрессия, ночные кошмары, бессонница, ухудшение памяти, утомляемость, гипергликемия, гиперлипидемия, мышечная слабость, эректильная дисфункция) ПР. К прямым ПР вследствие применения БАБ относятся: усиление СН, тяжелые брадикардия и гипотония, абдоминальные болевые кризы, а также тошнота и диарея. Замедление сердцебиения и уменьшение ударного объема ведут к декомпенсации сердечной деятельности. У больных с синусовым ритмом под влиянием БАБ могут развиться тяжелая брадикардия и атриовентрикулярная блокада. Усиление бронхоконстрикции у больных бронхитом, особенно у пациентов с бронхиальной астмой, может повлечь за собой приступ удушья.
Большой практический интерес имеют также ПР, вызываемые приемом АК (табл. 4). При медицинском применении b-адреноблокаторов наблюдаются кардиальные (брадикардия, АГ, атриовентрикулярные блокады) и экстракардиальные (головокружение, депрессия, ночные кошмары, бессонница, ухудшение памяти, утомляемость, гипергликемия, гиперлипидемия, мышечная слабость, эректильная дисфункция) ПР. К прямым ПР вследствие применения БАБ относятся: усиление СН, тяжелые брадикардия и гипотония, абдоминальные болевые кризы, а также тошнота и диарея. Замедление сердцебиения и уменьшение ударного объема ведут к декомпенсации сердечной деятельности. У больных с синусовым ритмом под влиянием БАБ могут развиться тяжелая брадикардия и атриовентрикулярная блокада. Усиление бронхоконстрикции у больных бронхитом, особенно у пациентов с бронхиальной астмой, может повлечь за собой приступ удушья.
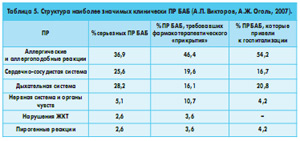 В Украине общая структура наиболее клинически значимых серьезных ПР БАБ, которые требовали медикаментозной коррекции, госпитализации или ее продления, представлены в таблице 5. Во всех этих случаях превалировали аллергические и алергоподобные реакции, преимущественно отек Квинке и анафилактический шок. Практически равными по количеству были поражения дыхательной (бронхоспазм с приступами удушья) и сердечно-сосудистой систем (чаще всего – брадиаритмии и блокады сердца, коллаптоидные состояния).
В Украине общая структура наиболее клинически значимых серьезных ПР БАБ, которые требовали медикаментозной коррекции, госпитализации или ее продления, представлены в таблице 5. Во всех этих случаях превалировали аллергические и алергоподобные реакции, преимущественно отек Квинке и анафилактический шок. Практически равными по количеству были поражения дыхательной (бронхоспазм с приступами удушья) и сердечно-сосудистой систем (чаще всего – брадиаритмии и блокады сердца, коллаптоидные состояния).
Степень достоверности сообщений про ПР БАБ была достаточно высокой: причинно-следственная связь расценивалась как вероятная в 65% случаев, как установленная в 26% и как возможная в 10% случаев. В 99,1% случаев проявления ПР были вполне предсказуемыми (в т. ч. 13% – серьезные). Только в 0,3% отмечались непредвиденные серьезные ПР. В 0,6% случаев поступили сообщения об отсутствии эффекта препарата.
В большинстве случаев способом коррекции была отмена препарата (93%). В остальных – снижение дозы (5%). Только в 2% в режим терапии изменений не вносили. В то же время у 99% проявления ПР проходили бесследно и только менее чем у 1% пациентов наблюдались остаточные явления. Летальных случаев, связанных с применением БАБ, не было зафиксировано.
Медикаментозную терапию ПР применяли в 19% случаев – в среднем по два дополнительных препарата на одного пациента. Преобладали антигистаминные средства и глюкокортикостероидные препараты у 63 и 46% соответственно. У 14% больных был применен атропин наряду с энтеросорбентами, у 9% – эуфиллин и у 7% – симпатомиметики с различным способом введения и механизмом действия. При этом 8% пациентов нуждались в госпитализации или ее продлении из-за развития ПР.
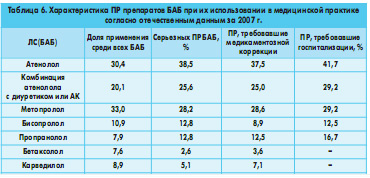
В трети всех случаев ПР возникали на фоне назначения препарата отечественного производства. Только в 11% фигурировали «брендовые» препараты, в остальных 89% – генерические. Среди подозреваемых ЛС преобладали метопролол (33%) и атенолол в комбинации с диуретиком и/или АК (30%). Доли бисопролола (11%), карведилола (9%), бетаксолола (8%) и пропранолола (8%) не отличались существенно.
В структуре системных поражений ожидаемо превалировали ПР со стороны сердечно-сосудистой системы на фоне небольшого числа «парадоксальных» проявлений, причем сообщения о «синдроме отмены» составили только 0,3%, что может быть следствием недооценки риска возникновения данного состояния. Вторую по количеству зарегистрированных случаев позицию заняли аллергические и аллергоподобные реакции. Это отвечает отечественной тенденции подачи информации о наиболее очевидных ПР с недостаточным вниманием к более специфическим, редкостным и отсроченным нежелательным проявлениям, однако процент их был гораздо меньшим по сравнению с таковым в структуре ПР ЛС всех групп. Некоторые из них, по-видимому, были дозозависимыми (псевдоаллергическими), часть из них могла быть вызвана компонентами наполнителей или сопутствующих компонентов таблетки. При этом следует учитывать значительное число генерических (89%) и комбинированных (20%) ЛС среди тех, которые вызывают подозрение в отношении безопасности. Третье по значимости место принадлежит нарушениям центральной и периферической нервной системы и органов чувств. Они составляют 17,5% и развиваются при использовании БАБ, способных проникать через гематоэнцефалический барьер. Такие ПР могут быть следствием ухудшения периферического артериального кровотока. Только четвертое место занимают негативные реакции со стороны органов дыхания (10,9% прежде всего бронхообструкция). Такую их позицию можно объяснить применением b1-селективных препаратов.
Известно, что БАБ и ИАПФ относятся к числу ЛС с бронхоконстрикторным действием, поэтому они противопоказаны больным астмой. В клинической практике описаны случаи успешного продолжительного лечения пациентов с ишемической болезнью сердца ЛС указанных групп, однако часто после перенесенного вирусного заболевания их прием провоцирует бронхоспазм. Кроме того, ИАПФ в достаточно большом проценте случаев (свыше 30%) вызывают кашель и более чем в 4% – обострение бронхиальной астмы.
Токсические ПР в большинстве своем развиваются в результате применения СГ или антиаритмических ЛС, токсическое действие которых проявляется при передозировке или их кумуляции в организме больного. Токсичность препаратов проявляется даже при терапевтических дозах в случае предшествующего поражения почек и гепатобилиарной системы.
Огромное значение для терапевтической практики за последние десятилетия приобрели гиполипидемические ЛС. Одновременно с их внедрением возник целый ряд проблем, связанных с безопасностью их применения. Так, в Украине, по данным ГФЦ МЗ Украины, в 2008 г. среди препаратов данного класса ПР чаще всего регистрировались вследствие при назначении ловастатина (46,8%), аторвастатина (23,4%), симвастатина (21,2%), реже на фоне назначения флувастатина (2,1%). Среди системных ПР доминировали аллергические реакции, в том числе анафилактический шок (34,0%), осложнения со стороны печени и желчевыводящих путей (10,6%), кардиальные, экстракардиальные (8,5%) и гемостатические (2,1%) нарушения.
 Широко применяются в медицинской практике диуретические ЛС, многие из которых наряду с четко выраженным терапевтическим эффектом вызывают и ПР, в том числе опасные для жизни. Острая потеря натрия чаще всего развивающаяся у больных с сохраненной функцией почек и отеками на фоне терапии диуретиками сопровождается быстрым уменьшением отечности, снижением массы тела, тахикардией, гипотонией, адинамией, сонливостью. Для хронической потери натрия характерны астения, мышечные подергивания, тошнота и такие психические расстройства, как дезориентация и сомноленция. У больных с декомпенсированной СН и циррозом печени назначение диуретиков может повлечь за собой развитие так называемой гипонатриемии разведения. Этот вид гипонатриемии носит в основном субклинический характер и лишь в тяжелых случаях проявляется судорогами, мышечными подергиваниями и потерей сознания. Довольно опасным для жизни осложнением терапии диуретиками является гиперкалиемия. Хотя клинически гиперкалиемия ярко не выражена, однако в силу способности к быстрому прогрессированию и трудности коррекции она приводит к остановке сердца в результате брадикардии с последующей фибрилляцией желудочков.
Широко применяются в медицинской практике диуретические ЛС, многие из которых наряду с четко выраженным терапевтическим эффектом вызывают и ПР, в том числе опасные для жизни. Острая потеря натрия чаще всего развивающаяся у больных с сохраненной функцией почек и отеками на фоне терапии диуретиками сопровождается быстрым уменьшением отечности, снижением массы тела, тахикардией, гипотонией, адинамией, сонливостью. Для хронической потери натрия характерны астения, мышечные подергивания, тошнота и такие психические расстройства, как дезориентация и сомноленция. У больных с декомпенсированной СН и циррозом печени назначение диуретиков может повлечь за собой развитие так называемой гипонатриемии разведения. Этот вид гипонатриемии носит в основном субклинический характер и лишь в тяжелых случаях проявляется судорогами, мышечными подергиваниями и потерей сознания. Довольно опасным для жизни осложнением терапии диуретиками является гиперкалиемия. Хотя клинически гиперкалиемия ярко не выражена, однако в силу способности к быстрому прогрессированию и трудности коррекции она приводит к остановке сердца в результате брадикардии с последующей фибрилляцией желудочков.
Метаболические расстройства развиваются при терапии всеми видами диуретиков и проявляются гиперурикемией. Возникновению этого осложнения способствуют различные нарушения метаболизма, почечная недостаточность, ожирение в сочетании с гипокалорийной диетой, гипертоническая болезнь и сахарный диабет. К метаболическим осложнениям лечения диуретиками следует отнести развитие гипергликемии, особенно у лиц, страдающих диабетом.
Токсические ПР при терапии диуретиками включают реакции со стороны системы кроветворения, органов пищеварения, кожи, половой системы. Характер токсического действия во многом определяется видом диуретика. Так, тиазидные диуретики чаще вызывают тромбоцитопению; сульфонамидные – агранулоцитоз; салуретики – некротический панкреатит; фуросемид, этакриновая кислота и триамтерен – гепатит. У пациентов с заболеваниями почек ототоксический эффект вызывает этакриновая кислота, при длительном приеме альдактона возникают гинекомастия у мужчин и нарушение менструального цикла у женщин.
Представляется целесообразным применение ЛС, увеличивающих вариабельность ритма сердца, для улучшения прогноза течения сердечно-сосудистых заболеваний с целью коррекции вегетативной регуляции сердечного ритма. В первую очередь это касается БАБ и ИАПФ.
Большое значение для возникновения ПР сердечно-сосудистых средств и других лекарственных препаратов имеет приверженность терапии или так называемая комплайентность пациентов.
Среди причин отказа больных от начала или продолжения фармакотерапии указывают на следующие (Ю.С. Рудык, 2008):
· асимптомное течение сердечно-сосудистых заболеваний – часто становится мотивацией для пациента не покупать необходимых лекарственных препаратов или несвоевременно прекращать их дальнейший прием. Особенность ментальности населения состоит в том, что значительная часть его нацелена на быстрое и полное выздоровление, исцеление, чего практически вообще не происходит при хронических заболеваниях;
· исчезновение симптоматики сердечно-сосудистого заболевания вследствие приема соответствующих ЛС часто становится импульсом прекращения дальнейшего приема препаратов для пациента;
· низкая эффективность ЛС (недостаточная эффективность), которая может быть связана с временным этапом подбора фармакотерапии, нежеланием повторного обращения к доктору, продолжением лечения согласно собственным представлениям, советам друзей, знакомых;
· иррациональное использование ЛС, их безосновательные назначения.
Под приверженностью терапии понимают соответствие поведения пациента рекомендациям врача, включая прием препаратов, диету и/или изменение образа жизни (доклад ВОЗ). Приверженность лечению включает такие понятия, как упорство и комплайентность (Е. Зоткин, А. Григорьева, 2007). Упорство определяется длительностью периода получения медикаментозной терапии и оценивается количеством дней, в течение которых пациент получал терапию, или процентом больных, продолжающих лечение на протяжении определенного периода. Комплайентность – показатель приверженности медикаментозной терапии (соблюдение дозы, кратности и режима приема). Комплайентность оценивается индексом использования препарата, представляющим собой частное от деления количества дней приема полной дозы препарата (или его количества, выданного больному) на длительность (в днях) всего периода исследования (наблюдения).
 Идеальной целью представляется достижение стопроцентной приверженности, однако при любом хроническом заболевании получение подобного результата затруднительно. Если индекс использования препарата достигает 80% и более, комплайентность считается приемлемой. Другие авторы выделяют следующие степени приверженности проводимому лечению: полная (пропуск менее 25% назначений), частичная (пропуск 25-65% назначений) и ее отсутствие (пропуск более 65% назначений) (М. Еременко, 2008).
Идеальной целью представляется достижение стопроцентной приверженности, однако при любом хроническом заболевании получение подобного результата затруднительно. Если индекс использования препарата достигает 80% и более, комплайентность считается приемлемой. Другие авторы выделяют следующие степени приверженности проводимому лечению: полная (пропуск менее 25% назначений), частичная (пропуск 25-65% назначений) и ее отсутствие (пропуск более 65% назначений) (М. Еременко, 2008).
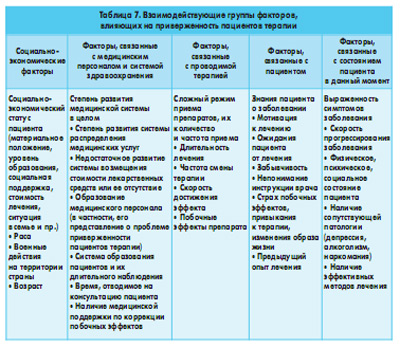
В настоящее время идентифицировано порядка 250 факторов, так или иначе обусловливающих отношение больных к соблюдению режима терапии. Часть из них представлена в таблице 7. В целом приверженность отражает сложное взаимодействие этих факторов, конфигурация сочетаний которых меняется в динамике заболевания и на отдаленных этапах может существенно отличаться от начальной (Н.Г. Незнанов, В.Д. Вид, 2004).
Проблема недостаточной приверженности больных лечению особенно актуальна при хронических заболеваниях. Так, до 50% пациентов с АГ, бронхиальной астмой, атеросклерозом с гиперлипидемией, сахарным диабетом, эпилепсией и другими заболеваниями самостоятельно прерывают лечение, назначенное врачом (R.Bi. Haynes, 2001: World Health Organization, 2003). Считается, что низкая приверженность является главной причиной уменьшения выраженности терапевтического эффекта, существенно повышает вероятность развития осложнений основного заболевания, ведет к снижению качества жизни больных и увеличению затрат на лечение.
Приведенные данные свидетельствуют о том, что использование в практической кардиологии огромного арсенала ЛС различных фармакологических групп в разных клинических ситуациях требует должного внимания к вопросам безопасности при медицинском применении препаратов – как включенных в общепринятые современные стандарты лечения, так и редко применяемых, однако потенциально не менее опасных в отношении возникновения ПР.


