27 березня, 2015
Гиперурикемия как фактор риска сердечно-сосудистой заболеваемости и смертности
 Исторически представление о гиперурикемии было связано с ее клиническими проявлениями, то есть подагрой и нефролитиазом. Взаимосвязь подагры с кардиоваскулярными заболеваниями и нефропатией многократно подтверждалась, однако не привлекала значительного внимания ввиду относительно небольшой распространенности подагры в популяции. Вместе с тем попытки применения мочевой кислоты (МК) как суррогатного маркера развития нефропатии оказались несостоятельными.
Исторически представление о гиперурикемии было связано с ее клиническими проявлениями, то есть подагрой и нефролитиазом. Взаимосвязь подагры с кардиоваскулярными заболеваниями и нефропатией многократно подтверждалась, однако не привлекала значительного внимания ввиду относительно небольшой распространенности подагры в популяции. Вместе с тем попытки применения мочевой кислоты (МК) как суррогатного маркера развития нефропатии оказались несостоятельными.
align="justify">
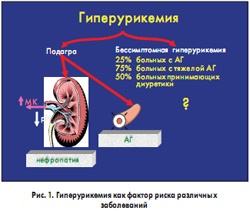 Новая волна интереса к МК связана с пониманием роли (рис. 1) бессимптомной гиперурикемии (определяемой чаще всего как повышение уровня МК в плазме >6,5 мг/дл для мужчин и >6,0 мг/дл для женщин) как мощного, независимого и модифицируемого фактора риска сердечно-сосудистой (СС) заболеваемости и смертности, основанное на данных многочисленных эпидемиологических и проспективных исследований (рис. 2).
Новая волна интереса к МК связана с пониманием роли (рис. 1) бессимптомной гиперурикемии (определяемой чаще всего как повышение уровня МК в плазме >6,5 мг/дл для мужчин и >6,0 мг/дл для женщин) как мощного, независимого и модифицируемого фактора риска сердечно-сосудистой (СС) заболеваемости и смертности, основанное на данных многочисленных эпидемиологических и проспективных исследований (рис. 2).
Роль МК как предиктора СС заболеваемости и смертности изучалась практически во всех крупных популяционных исследованиях, причем были получены различные результаты.
 Сопоставление двух наиболее крупных исследований NHANES и Framingham Heart Study позволило выявить очень важную закономерность, подтвердившуюся и в других исследованиях. Оказалось, что в целом в популяциях с более высоким кардиоваскулярным риском возрастает роль МК как независимого фактора риска СС заболеваемости и смертности (кардиоваскулярная смертность была почти в 2 раза выше у лиц, включенных в исследование NHANES, в сравнении с Framingham Heart Study).
Сопоставление двух наиболее крупных исследований NHANES и Framingham Heart Study позволило выявить очень важную закономерность, подтвердившуюся и в других исследованиях. Оказалось, что в целом в популяциях с более высоким кардиоваскулярным риском возрастает роль МК как независимого фактора риска СС заболеваемости и смертности (кардиоваскулярная смертность была почти в 2 раза выше у лиц, включенных в исследование NHANES, в сравнении с Framingham Heart Study).
Данное положение было подтверждено в исследовании на основе базы данных PreCIS. В исследование были включены 3 098 больных с высоким кардиоваскулярным риском. Период наблюдения составил 14 262 человеко-лет. По результатам данного исследования, повышение исходного уровня МК на 1 мг/дл ассоциировалось с увеличением на 39% риска смерти независимо от других известных факторов риска.
В настоящее время доказана роль гиперурикемии как независимого предиктора кардиоваскулярной заболеваемости и смертности у больных ишемической болезнью сердца (ИБС), хронической и острой сердечной недостаточностью, артериальной гипертензией (АГ) и предгипертензией и метаболическим синдромом (МС).
Ишемическая болезнь сердца
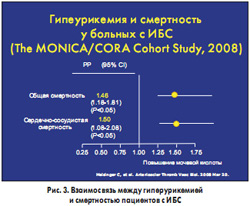 Особенно значительна роль гиперурикемии как независимого фактора риска СС смертности у больных с ИБС и хронической сердечной недостаточностью (ХСН). Опубликованные в начале 2008 г. данные когортного исследования MONICA/KORA показали, что у больных с документированной ИБС повышение уровня МК независимо от других известных факторов риска ассоциировалось с достоверным и значительным увеличением как сердечно-сосудистой, так и общей смертности (рис. 3). У больных с инфарктом миокарда с элевацией сегмента ST повышение уровня МК – мощный и независимый предиктор неблагоприятных исходов.
Особенно значительна роль гиперурикемии как независимого фактора риска СС смертности у больных с ИБС и хронической сердечной недостаточностью (ХСН). Опубликованные в начале 2008 г. данные когортного исследования MONICA/KORA показали, что у больных с документированной ИБС повышение уровня МК независимо от других известных факторов риска ассоциировалось с достоверным и значительным увеличением как сердечно-сосудистой, так и общей смертности (рис. 3). У больных с инфарктом миокарда с элевацией сегмента ST повышение уровня МК – мощный и независимый предиктор неблагоприятных исходов.
Хроническая и острая сердечная недостаточность
Впечатляющие данные получены у больных с ХСН. Несколько небольших по количеству наблюдений исследований показали, что бессимптомная гиперурикемия является независимым предиктором смертности и потребности в трансплантации сердца у больных с ХСН. При повышении уровня МК более 9,50 мг/дл риск смерти в течение года у этих больных возрастал в 7 (!) раз. Гиперурикемия согласно этим исследованиям оказалась более значимым предиктором смертности, чем фракция выброса левого желудочка, несмотря на то что уровень МК имел с ней сильную отрицательную корреляцию и положительную с давлением в легочной артерии. Повышение уровня МК увеличивает риск смерти и у больных с острой сердечной недостаточностью. Гиперурикемия – не только предиктор неблагоприятных исходов у больных с ХСН, но и независимый фактор риска развития сердечной недостаточности у лиц старше 60 лет.
Наиболее изучена роль МК как предиктора кардиоваскулярных событий у больных АГ, сахарным диабетом и МС.
Артериальная гипертензия
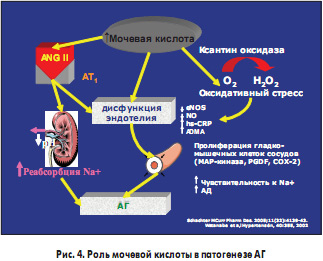 Повышение уровня МК связано с риском развития АГ у нормотензивных лиц. Экспериментальные исследования показали, что повышение уровня МК приводит к развитию АГ за счет прямого влияния на гладкие мышцы и эндотелий сосудов (рис. 4). Кроме того, у подростков с впервые возникшей АГ распространенность повышения уровня МК составляет более 90%. В данной популяции препараты, снижающие уровень МК, приводят к снижению артериального давления (АД).
Повышение уровня МК связано с риском развития АГ у нормотензивных лиц. Экспериментальные исследования показали, что повышение уровня МК приводит к развитию АГ за счет прямого влияния на гладкие мышцы и эндотелий сосудов (рис. 4). Кроме того, у подростков с впервые возникшей АГ распространенность повышения уровня МК составляет более 90%. В данной популяции препараты, снижающие уровень МК, приводят к снижению артериального давления (АД).
Бессимптомная гиперурикемия встречается у 25% больных АГ, у 75% – тяжелой АГ и у половины больных, принимающих тиазидные и тиазидоподобные диуретики, и является, как правило, следствием нарушенного клиренса уратов почками.
Повышение уровня МК стимулирует активацию ренин-ангиотензиновой системы и усугубляет дисфункцию эндотелия. Кроме того, в условиях ишемии происходит превращение фермента ксантиноксиредуктазы в ксантиноксидазу, что приводит к изменению метаболизма ксантинов, превращению МК из антиоксиданта в прооксидант и стимулированию оксидативного стресса. Таким образом, МК является не маркером, а активным компонентом в развитии АГ.
 Однако более важной представляется роль МК как фактора риска кардиоваскулярных событий у больных с АГ, что подтверждается данными проспективных исследований. Вначале были опубликованы данные исследования The Worksite Treatment Program, в котором у 8690 пациентов в течение года был достигнут контроль АД и поддерживался в течение 18 лет. У тех больных, у которых уровень МК в ходе терапии повысился (в среднем на 1 мг/дл), наблюдалось на 32% больше кардиоваскулярных событий, несмотря на одинаковый контроль АД. Кардиоваскулярный риск, ассоциированный с повышением уровня МК, сопоставим, по данным авторов исследования, с повышением на 46 мг/дл уровня общего холестерина или на 10 мм рт. ст. систолического АД.
Однако более важной представляется роль МК как фактора риска кардиоваскулярных событий у больных с АГ, что подтверждается данными проспективных исследований. Вначале были опубликованы данные исследования The Worksite Treatment Program, в котором у 8690 пациентов в течение года был достигнут контроль АД и поддерживался в течение 18 лет. У тех больных, у которых уровень МК в ходе терапии повысился (в среднем на 1 мг/дл), наблюдалось на 32% больше кардиоваскулярных событий, несмотря на одинаковый контроль АД. Кардиоваскулярный риск, ассоциированный с повышением уровня МК, сопоставим, по данным авторов исследования, с повышением на 46 мг/дл уровня общего холестерина или на 10 мм рт. ст. систолического АД.
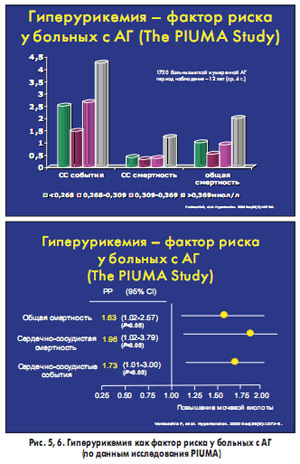
Краеугольным камнем в понимании роли МК как независимого предиктора кардиоваскулярной заболеваемости и смертности у больных АГ стало исследование PIUMA, в которое были включены 1720 больных АГ, наблюдавшихся в течение 12 лет.
У больных АГ с исходным уровнем МК более 0,396 ммоль/л риск кардиоваскуляных событий, фатальных СС событий и общей смертности был достоверно выше, чем у больных с исходным уровнем МК от 0,268 до 0,309 ммоль/л. У больных АГ с низким исходным уровнем МК (менее 0,268 ммоль/л) было достоверно больше СС событий и выше общая смертность (рис. 5, 6).
Следующим важным шагом в доказательстве роли МК как независимого предиктора СС событий и смертности у больных АГ стало исследование Systolic Hypertension in the Elderly Trial (SHEP), включавшее 4327 больных старше 60 лет с изолированной систолической АГ, которые принимали в течение 5 лет тиазидные диуретики или плацебо с добавлением атенолола или резерпина при необходимости. Прежде всего подтвердилась линейная зависимость у больных с АГ количества кардиоваскулярных событий, за исключением инсультов, от исходного уровня МК (рис. 7). Наряду с этим терапия тиазидным диуретиком в обычных терапевтических дозах у половины больных в течение года привела к повышению уровня МК.
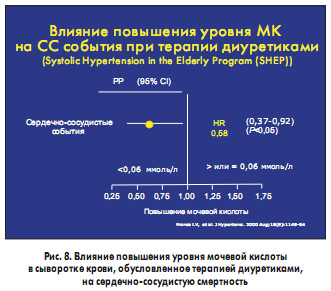
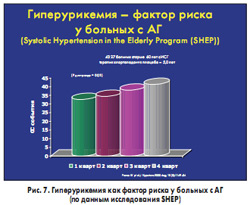 Наряду с этим в обычных терапевтических дозах у половины больных в течение года привела к повышению уровня Наиболее интересно то, что в группе больных, у которых применение тиазидного диуретика привело к повышению уровня МК, количество СС событий было почти на 50% выше, чем в группе больных, у которых не было отмечено повышение МК (рис. 8). Таким образом, исследование SHEP дало нам два очень важных вывода для клинической практики. Применение тиазидных диуретиков в обычных терапевтических дозах у половины больных в течение года приводит к бессимптомному повышению уровня МК, с которым ассоциируется значительное увеличение количества кардиоваскулярных событий. Следовательно, у таких больных необходимо мониторирование уровня МК и предотвращение его повышения.
Наряду с этим в обычных терапевтических дозах у половины больных в течение года привела к повышению уровня Наиболее интересно то, что в группе больных, у которых применение тиазидного диуретика привело к повышению уровня МК, количество СС событий было почти на 50% выше, чем в группе больных, у которых не было отмечено повышение МК (рис. 8). Таким образом, исследование SHEP дало нам два очень важных вывода для клинической практики. Применение тиазидных диуретиков в обычных терапевтических дозах у половины больных в течение года приводит к бессимптомному повышению уровня МК, с которым ассоциируется значительное увеличение количества кардиоваскулярных событий. Следовательно, у таких больных необходимо мониторирование уровня МК и предотвращение его повышения.
 Доказана роль МК и в развитии гипертрофии миокарда левого желудочка (ГЛЖ) у больных АГ. В экспериментальных исследованиях было показано, что аллопуринол обладает способностью предотвращать развитие ГЛЖ при отсутствии снижения АД. Полагают, что МК обладает способностью стимулировать рост кардиомиоцитов. Роль гиперурикемии в развитии ГЛЖ у больных АГ была подтверждена в крупном японском исследовании, в котором участвовали 3305 мужчин в возрасте 35-66 лет. ГЛЖ диагностировалась на основании ЭКГ критериев Соколова-Лайона и/или Корнельского индекса. Повышение уровня МК в пределах 0,39-0,65 ммоль/л или 6,6-11,0 мг/дл значительно и достоверно увеличивало количество больных с ГЛЖ независимо от индекса массы тела, уровня креатинина наличия диабета и дислипидемии (дополнительный риск 1,58, р<0,001). Аналогичные результаты были получены у лиц с нормальным АД. Эти данные объясняют высокую эффективность лосартана, обладающего урикозурическим эффектом в уменьшении ГЛЖ.
Доказана роль МК и в развитии гипертрофии миокарда левого желудочка (ГЛЖ) у больных АГ. В экспериментальных исследованиях было показано, что аллопуринол обладает способностью предотвращать развитие ГЛЖ при отсутствии снижения АД. Полагают, что МК обладает способностью стимулировать рост кардиомиоцитов. Роль гиперурикемии в развитии ГЛЖ у больных АГ была подтверждена в крупном японском исследовании, в котором участвовали 3305 мужчин в возрасте 35-66 лет. ГЛЖ диагностировалась на основании ЭКГ критериев Соколова-Лайона и/или Корнельского индекса. Повышение уровня МК в пределах 0,39-0,65 ммоль/л или 6,6-11,0 мг/дл значительно и достоверно увеличивало количество больных с ГЛЖ независимо от индекса массы тела, уровня креатинина наличия диабета и дислипидемии (дополнительный риск 1,58, р<0,001). Аналогичные результаты были получены у лиц с нормальным АД. Эти данные объясняют высокую эффективность лосартана, обладающего урикозурическим эффектом в уменьшении ГЛЖ.
Метаболический синдром
Хорошо изучена роль МК как фактора риска кардиоваскулярной заболеваемости и смертности у больных с МС. Данные нескольких популяционных исследований, опубликованных в 2008 г., наиболее крупным из которых было Сингапурское когортное исследование (рис. 9), показали, что МС повышает риск общей и кардио-васкулярной смертности как у мужчин, так и у женщин независимо от известных факторов риска, явлющихся его компонентами (таких как АГ, сахарный диабет и др.).
Ключевым моментом в развитии МС в сегодняшнем понимании является абдоминальное ожирение, которое запускает активацию синтеза адипокинов и цитокинов. Повышение синтеза адипокинов наряду с другими факторами приводит к развитию основных компонентов МС: резистентности периферических тканей к инсулину, дислипидемии и дисфункции эндотелия. Дальнейшее прогрессирование процесса приводит к повышению АД, развитию сахарного диабета 2 типа, ускоренному прогрессированию атеросклероза и соответствующим клиническим проявлениям.
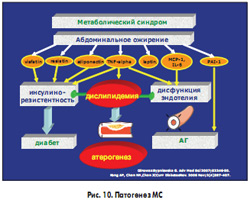 Гиперурикемия рассматривается как важный компонент МС также авторами современного определения МС – G.M. Reaven и I. Zavaroni et al. Более того, первые определения МС включали гиперурикемию как основной компонент наряду с гипертензией и гипергликемией. Опубликованные в начале 2008 г. многочисленные исследования позволили четко определить роль МК в патогенезе МС (рис. 10).
Гиперурикемия рассматривается как важный компонент МС также авторами современного определения МС – G.M. Reaven и I. Zavaroni et al. Более того, первые определения МС включали гиперурикемию как основной компонент наряду с гипертензией и гипергликемией. Опубликованные в начале 2008 г. многочисленные исследования позволили четко определить роль МК в патогенезе МС (рис. 10).
Гиперинсулинемия вследствие резистентности периферических тканей к инсулину приводит к снижению экскреции почками МК и гиперурикемии, связанной со снижением ее экскреции. Абдоминальное ожирение приводит к повышению синтеза МК, путем увеличения поступления в печень жирных кислот. Таким образом, гиперурикемия у бльных с МС носит смешанный характер.
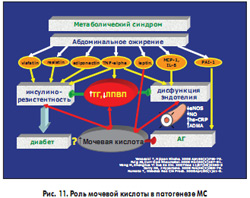 В свою очередь, гиперурикемия, связанная с повышением уровня HbA1с и уровня МК у больных с МС, – сильный предиктор развития сахарного диабета 2 типа. Известно также, что уровень МК тесно коррелирует с уровнем лептина у больных МС, а ксантин-оксидоредуктаза является одним из ключевых факторов дифференциации адипоцитов. Кроме того, у больных с МС гиперурикемия тесно коррелирует с уровнем триглицеридов, однако механизм этой взаимосвязи до настоящего момента не понятен. Если при этом учесть хорошо изученное влияние МК на функцию эндотелия и регуляцию АД, то становится очевидной ключевая роль МК в развитии МС (рис. 11).
В свою очередь, гиперурикемия, связанная с повышением уровня HbA1с и уровня МК у больных с МС, – сильный предиктор развития сахарного диабета 2 типа. Известно также, что уровень МК тесно коррелирует с уровнем лептина у больных МС, а ксантин-оксидоредуктаза является одним из ключевых факторов дифференциации адипоцитов. Кроме того, у больных с МС гиперурикемия тесно коррелирует с уровнем триглицеридов, однако механизм этой взаимосвязи до настоящего момента не понятен. Если при этом учесть хорошо изученное влияние МК на функцию эндотелия и регуляцию АД, то становится очевидной ключевая роль МК в развитии МС (рис. 11).
Не стоит забывать и хорошо известную роль бессимптомной гиперурикемии в развитии нефролитиаза у больных МС.
Таким образом, гиперурикемия – сильный, независимый и, главное, модифицируемый предиктор СС и общей смертности у больных с высоким и очень высоким сердечно-сосудистым риском (АГ, ИБС, ХСН, МС/сахарный диабет).
Роль бессимптомной гиперурикемии как независимого предиктора кардиоваскулярной заболеваемости и смертности у больных с высоким общим кардиоваскулярным риском не вызывает сомнений и необходима разработка методов коррекции и доказательство их эффективности в рандомизированных проспективных исследованиях.
В настоящее время известны следующие группы препаратов, снижающих уровень МК и устраняющих гиперурикемию:
· ингибиторы ксантин-оксидазы (аллопуринол)
· препараты с урикозурическим эффектом (пробенецид, сульфинпиразон, бензбромарон, бензиодарон, фенофибрат, аторвастатин, лосартан).
Целесообразность использования ингибиторов ксантиноксидазы у больных кардиоваскулярными заболеваниями и бессимптомной гиперурикемией требуют доказательства в рандомизированных исследованиях.
Более интересным с точки зрения клинической практики является использование препаратов с доказанной высокой эффективностью у больных с сердечно-сосудистыми заболеваниями и обладающих урикозурическим эффектом, таких как аторвастатин, фенофибрат и лосартан.
Наиболее хорошо изучено влияние на гиперурикемию лосартана в большом количестве рандомизированных и нерандомизированных исследований. В начале 2008 г. опубликованы данные наиболее крупного исследования J-HEALTH, проведенного в Японии и включавшего 30 тыс. больных АГ. Период наблюдения составил в среднем 2,9 года. Все больные получали лосартан в средней дозе 47 мг/день (монотерапия – 59%).
В ходе терапии лосартаном 26 516 (88%) больных достигли целевого уровня АД, 1081 (3,6%) больной имел побочные эффекты, что сопоставимо с плацебо.
 Кроме высокой эффективности и безопасности лосартана, было доказано его влияние на уровень МК у больных с гиперурикемией. Исходно все больные были разделены в зависимости от уровня МК и наличия гиперурикемии (> или = 7 мг/дл) или ее отсутствия (<7 мг/дл). Терапия лосартаном привела к достоверному снижению уровня МК при исходной гиперурикемии, причем снижение уровня МК не зависело от одновременного назначения ингибиторов ксантиноксидазы (рис. 12).
Кроме высокой эффективности и безопасности лосартана, было доказано его влияние на уровень МК у больных с гиперурикемией. Исходно все больные были разделены в зависимости от уровня МК и наличия гиперурикемии (> или = 7 мг/дл) или ее отсутствия (<7 мг/дл). Терапия лосартаном привела к достоверному снижению уровня МК при исходной гиперурикемии, причем снижение уровня МК не зависело от одновременного назначения ингибиторов ксантиноксидазы (рис. 12).
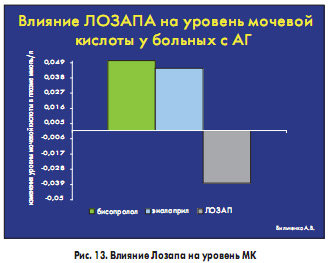
Проведенные нами исследования с препаратом Лозап (Zentiva) показали, что применение лосартана в отличие от эналаприла и бисопролола приводит к снижению уровня МК у больных АГ (рис. 13). Это влияние Лозапа на уровень МК не коррелировало с изменениями АД и гемодинамики, показателями липидного обмена и вариабельностью сердечного ритма.
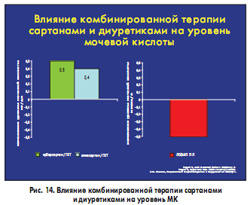
 Лосартан также обладает способностью устранять гиперурикемию, связанную с применением тиазидных и тиазидоподобных диуретиков. Исследования с применением препарата Лозап плюс, содержащим фиксированную комбинацию лосартана и гидрохлортиазида, показало не только метаболическую нейтральность данного препарата по отношению к углеводному и липидному обмену, но и снижение уровня МК у больных АГ через 12 недель терапии (рис. 14). Проведенные многочисленные исследования с различными комбинациями сартанов и тиазидных диуретиков продемонстрировали уникальность данного свойства молекулы лосартана. Ни один из сартанов, кроме лосартана, не обладал способностью снижать уровень МК при комбинации с тиазидными и тиазидоподобными диуретиками.
Лосартан также обладает способностью устранять гиперурикемию, связанную с применением тиазидных и тиазидоподобных диуретиков. Исследования с применением препарата Лозап плюс, содержащим фиксированную комбинацию лосартана и гидрохлортиазида, показало не только метаболическую нейтральность данного препарата по отношению к углеводному и липидному обмену, но и снижение уровня МК у больных АГ через 12 недель терапии (рис. 14). Проведенные многочисленные исследования с различными комбинациями сартанов и тиазидных диуретиков продемонстрировали уникальность данного свойства молекулы лосартана. Ни один из сартанов, кроме лосартана, не обладал способностью снижать уровень МК при комбинации с тиазидными и тиазидоподобными диуретиками.
 Более важно в данном случае, насколько снижение уровня МК при терапии лосартаном оказывает влияние на риск кардиоваскулярной заболеваемости и смертности у больных АГ. Частично ответ на этот вопрос дал анализ исследования LIFE.
Более важно в данном случае, насколько снижение уровня МК при терапии лосартаном оказывает влияние на риск кардиоваскулярной заболеваемости и смертности у больных АГ. Частично ответ на этот вопрос дал анализ исследования LIFE.
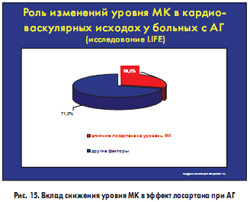
Сопоставление вклада различных факторов показало, что снижение кардиоваскулярного риска у больных, получавших лосартан, на 29% было обусловлено снижением уровня МК (рис. 15). Эти данные позволяют рассматривать лосартан как препарат выбора у больных АГ с бессимптомной гиперурикемией, в том числе вызванной применением тиазидных и тиазидоподобных диуретиков.
 Вторая клиническая ситуация, в которой лосартан (Лозап) должен быть препаратом выбора, – это лечение больных МС. Помимо известных эффектов, таких как повышение чувствительности тканей к инсулину, снижение уровня инсулина и глюкозы в плазме, устранение дисфункции эндотелия, замедление развития атеросклероза и уменьшение образования адипокинов, лосартан единственный из гипотензивных препаратов обладает способностью у больных МС повышать выведение МК и снижать ее уровень в плазме.
Вторая клиническая ситуация, в которой лосартан (Лозап) должен быть препаратом выбора, – это лечение больных МС. Помимо известных эффектов, таких как повышение чувствительности тканей к инсулину, снижение уровня инсулина и глюкозы в плазме, устранение дисфункции эндотелия, замедление развития атеросклероза и уменьшение образования адипокинов, лосартан единственный из гипотензивных препаратов обладает способностью у больных МС повышать выведение МК и снижать ее уровень в плазме.
Выводы
· У больных АГ повышение уровня МК повышает риск СС событий, фатальных СС событий и общей смертности.
· При лечении больных АГ тиазидными и тиазидоподобными диуретиками повышение уровня МК – независимый предиктор увеличения СС смертности.
· У больных с ИБС повышение уровня МК на 1 мг/дл приводит к увеличению смертности на 26%. Увеличение СС риска сопоставимо с повышением на 10-12-мм рт. ст. систолического АД.
· У больных с ХСН повышение уровня МК ассоциируется с достоверным и значительным увеличением смертности.
· Повышение уровня МК у больных МС – независимый предиктор кардиоваскулярной смертности, развития сахарного диабета, АГ и нефролитиаза.
· При гиперурикемии у больных с АГ, МС, ХСН препаратом выбора является Лозап (лосартан), снижающий уровень МК за счет урикозурического эффекта.
· У больных с АГ и гиперурикемией вследствие применения тиазидных или тиазидоподобных диуретиков необходимо комбинировать их с лосартаном или же использовать фиксированные комбинации, такие как Лозап плюс.
Список литературы находится в редакции.


