6 листопада, 2016
Эффективность и переносимость комбинации нуклеотидов ЦМФ и УТФ у пациентов с диабетической нейропатией

Диабетическая нейропатия (ДН) является ранним и наиболее частым осложнением сахарного диабета (СД; обнаруживается примерно у 50% пациентов с СД 1 и 2 типа). По данным ВОЗ, в 2008 г. в мире насчитывалось 347 больных СД (Hartmann et al., 2012). ДН развивается вследствие повреждения нервов, вызванного диабетом, и присутствует примерно у 50% пациентов с СД (Muller, 2002). Эта патология может возникать у пациентов с СД 1 и 2 типа как в молодом, так и в более старшем возрасте (Muller, 2002). В 40-50% случаев ДН прогрессирует в болевую нейропатию (Veves et al., 2008). Тяжесть этого осложнения обусловлена его клиническими последствиями (трофические расстройства, нейропатическая боль, глубокие нарушения автономной функции) (Boulton et al., 2005).
Неотъемлемой составляющей ведения ДПН является лечение хронической нейропатической боли. Для этого используются различные препараты (антидепрессанты, антипсихотики и др.), однако все они ассоциируются с выраженными побочными эффектами (Boulton et al., 2005; Hartmann et al., 2012; Javed et al., 2015; Mibielli et al., 2010; Saeed et al., 2014). В лечении нейропатий различного генеза широко применяется препарат нуклеотидов, представляющий собой комбинацию динатрия цитидина 5’-монофосфата (ЦМФ) и динатрия уридина 5’-трифосфата (УТФ). В многочисленных доклинических исследованиях была продемонстрирована способность этого препарата восстанавливать нервные клетки путем стимуляции синтеза фосфолипидов и сфинголипидов – основных компонентов мембран и миелиновой оболочки нервов (Durany, 2005; Martianez et al., 2012). В клинических исследованиях у пациентов с полинейропатиями комбинация ЦМФ/УТФ эффективно уменьшала боль и улучшала скорость проведения импульса по сенсорным нервам (Gallai et al., 1992; Muller, 2002). Целью настоящего исследования было изучить эффективность и безопасность комбинации ЦМФ/УТФ у пациентов с ДПН.
Методы
В исследование включали больных СД 1 или 2 типа с клинически диагностированной ДПН и патологическими данными электромиографии (ЭМГ). Все пациенты предоставили письменное информированное согласие на участие. Критерии исключения: возраст <18 лет; беременность или кормление грудью; неврологическое или системное заболевание либо другие факторы, потенциально связанные с нейропатией; аллергия или непереносимость нуклеотидов; лечение нейропротекторными препаратами.
Нейропатию оценивали клинически во время полного неврологического обследования с помощью визуальной аналоговой шкалы (ВАШ), шкалы симптомов нейропатии (NSS) и шкалы дисфунции при нейропатии (NDS). При оценке ВАШ ≤4 балла боль считали легкой, 5-7 баллов – умеренной и >7 баллов – тяжелой. Все пациенты были обследованы три раза: до начала лечения, на 45-й день терапии и в конце лечения (на 90-й день). Образцы крови и мочи для исследований получали до и после лечения для оценки потенциальных биологических и биохимических отклонений со стороны печени, почек и форменных элементов крови. Помимо общего анализа крови с формулой, определяли активность аланин- (АЛТ) и аспартатаминотрансферазы (АСТ), креатинин сыворотки, гликозилированный гемоглобин (HbA1c) и глюкозу крови натощак. С помощью ЭМГ до и после лечения оценивали скорость сенсорного проведения по правому и левому икроножным нервам, а также скорость моторного проведения по правому и левому латеральным подколенным нервам, правому и левому внутренним подколенно-седалищным нервам, правому срединному нерву и левому локтевому нервам.
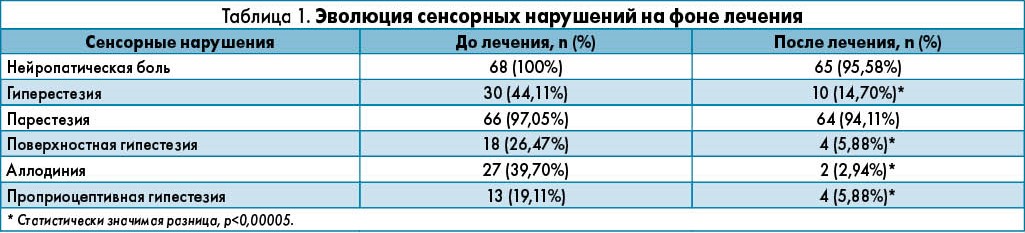
Автономную эфферентную функцию оценивали по симпатическому кожному рефлексу. Все пациенты получали ЦМФ/УТФ в суточной дозе 15 мг (3 капсулы в сутки: в 8:00, 14:00 и 20:00) в течение 90 дней. На протяжении этого периода оценивали комплайенс и потенциальные побочные реакции с указанием даты их развития, тяжести и вероятности связи с исследуемым препаратом. Ввод и обработку данных осуществляли с помощью программного обеспечения SPSS для Windows вер. 18.0. Частоту, средние показатели и стандартные отклонения рассчитывали путем одномерного анализа. С помощью двухмерного анализа и t-теста сравнивали средние показатели до и после лечения; результаты рассчитывали с 99% доверительным интервалом. Результаты Изначально в исследование включили 75 пациентов; впоследствии 7 из них были исключены по причинам, не связанным с получаемым лечением. Средний возраст больных составил 56 лет (от 21 года до 76 лет), женщин было 72%. У большинства пациентов (95,6%) был диагностирован СД 2 типа. Нейропатическая боль наблюдалась у 100% пациентов, парестезии – у 97,05%, гиперестезия – у 44,4% и аллодиния – у 39,7% (табл. 1). Боль пациенты оценивали как интенсивную (35,3%) или умеренную (58,8%). Средняя оценка по шкале NDS до лечения составила 5,82 балла.
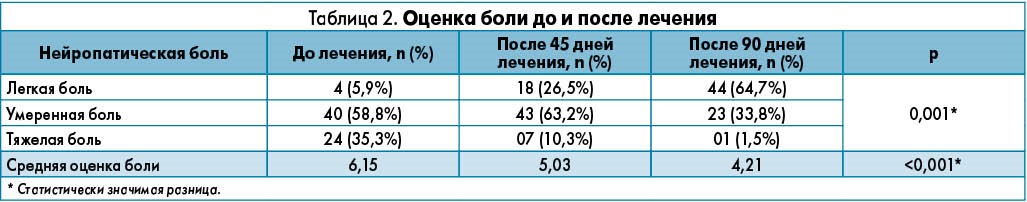
Результаты биохимического исследования до лечения: гликемия натощак – 208±0,92 мг/дл, HbA1c – 9,06±2,88%, креатинин сыворотки – 9,6±3,2 мг/дл, АСТ – 26,74±3,14 МЕ/л, АЛТ – 24,03±2,86 МЕ/л. После лечения наблюдалось уменьшение сенсорных нарушений (табл. 1), интенсивности и тяжести нейропатической боли (табл. 2), улучшение проведения по сенсорным нервам. Оценка NDS снизилась с 5,82 до 4,52 балла (р<0,0001), частота автономной дисфункции – с 35,3 до 17,6% (р<0,01). На протяжении лечения и по его окончании нейропсихиатрические, кожные, гастроинтестинальные и кардиоваскулярные побочные реакции не регистрировались. Показатели почечной и печеночной функции на фоне терапии не изменялись.
Обсуждение
Из 75 первоначально включенных пациентов полностью завершили исследование 68 больных, или 90,66%; как правило, приемлемым считается показатель >80% (Bouvenot et al., 2002). Средний возраст участников (56 лет) примерно соответствует таковому в других исследованиях по ДН (Abougalambou & Abougalambou, 2012; Adonkounou et al., 2008; Hussein, 2013). Такой относительно большой средний возраст частично объясняется преобладанием пациентов с СД 2 типа, который обычно развивается во взрослом возрасте, а также тем, что развитие нейропатии непосредственно связано с длительностью диабета (Hartmann et al., 2012). Соотношение женщин и мужчин в проведенном исследовании равнялось 2,6. Преобладание женщин среди пациентов с ДН отмечали и другие авторы (Muller, 2002; Abougalambou & Abougalambou, 2012), несмотря на то что СД развивается одинаково часто у мужчин и женщин. У подавляющего большинства участников настоящего исследования (96,6%) был диагностирован СД 2 типа, что также соответствует данным литературы (Hartmann et al., 2012; Pirart, 1978). Среди наблюдавшихся сенсорных нарушений (нейропатическая боль, гиперестезия, парестезия, поверхностная гипестезия, проприоцептивная аллодиния и глубокая гипестезия) после лечения отмечена значительная регрессия гиперчувствительности (с 44,11 до 14,70%), поверхностной гипестезии (с 26,47 до 5,88%), аллодинии (с 39,70 до 2,94%) и глубокой гипестезии (с 19,11 до 5,88%). Комбинация ЦМФ/УТФ обеспечила статистически значимое (р<0,01) уменьшение интенсивности нейропатической боли, что отражалось в достоверном снижении оценки по ВАШ. Полученные результаты практически идентичны таковым в более раннем исследовании, проведенном в Германии, в котором оценка по ВАШ снизилась с исходных 6,02 до 4,04 в конце терапии (Muller, 2002). До начала лечения большинство пациентов (58,8%) предъявляли жалобы на умеренную нейропатическую боль, а у 35,3% боль имела интенсивный характер. После 45 дней терапии умеренная боль все еще преобладала (63,2%), однако распространенность интенсивной боли значительно снизилась до 10,3%. По окончании 90-дневного курса лечения у большинства пациентов боль была легкой, а интенсивная боль наблюдалась только у 1,5%. Для объективной оценки симптомов использовали шкалу NDS.
На фоне лечения оценка по этой шкале достоверно снизилась. В вышеупомянутом германском исследовании снижение оценки NDS не достигло статистической значимости (Muller, 2002). ЭМГ-исследование показало достоверное (р<0,001) улучшение проводимости по сенсорным нервам. В частности, скорость проведения импульса по левому седалищному нерву увеличилась с 37,39 до 40,10 м/с.
Сопоставимые результаты были получены и в работе Muller (2002). По завершении лечения распространенность автономных нарушений по данным ЭМГ снизилась с 35,3 до 17,6%, что коррелировало с клинически наблюдаемой регрессией тахикардии и автономной дисфункции кишечника. Комбинация ЦМФ/УТФ хорошо переносилась пациентами, каких-либо побочных реакций не отмечено. Функции печени и почек, которые оценивались по динамике АЛТ/АСТ и креатинина соответственно, на протяжении исследования оставались в нормальном диапазоне.
Выводы
У пациентов с ДН комбинация ЦМФ/УТФ продемонстрировала эффективность в уменьшении боли и сенсорных нарушений, а также улучшении проводимости по сенсорным нервам. Препарат хорошо переносился, не вызывал побочных реакций и не влиял на основные биохимические показатели. Полученные результаты позволяют рекомендовать исследованную комбинацию нуклеотидов для широкого применения в лечении ДН.
Список литературы находится в редакции.
Статья печатается в сокращении.
Seck L. B., Basse A., Cisse E. H. et al. Efficacy and tolerance of combination of Cytidine 5'monophosphate (CMP) and Uridine-5 ' Triphosphate Trisodium (UTP) in patients with diabetic neuropathy. International Journal of Medicine and Medical Sciences. 2015; 5 (8): 284-287.
Перевел с англ. Александр Гладкий
UA/CNS/0916/0053
Медична газета «Здоров’я України 21 сторіччя» № 18 (391), вересень 2016