4 травня, 2016
Антидіабетичні властивості комбінованого препарату Кратал
Цукровий діабет (ЦД) залишається глобальною медико-соціальною проблемою ХХІ ст., що зумовлено пандемічним характером захворювання і високим ризиком інвалідизації та смерті. Так, за останні 30 років кількість хворих на ЦД у світі збільшилася вдвічі, очікується подальше її зростання (за прогнозами, до 592 млн осіб у 2035 р.).
ЦД 2 типу істотно впливає на тривалість життя хворих, знижуючи її в середньому на 10 років у разі встановлення діагнозу до 50-річного віку. У хворих на ЦД 2 типу атеросклероз є основною причиною інвалідизації та смерті, зумовленої макросудинною патологією. Ранній прояв і більш швидке прогресування атерогенних процесів за умов ЦД 2 типу тісно корелюють з високою частотою інфаркту міокарда, захворювань периферичних судин та інсульту. Оскільки основною метою терапії ЦД 2 типу є збільшення тривалості та збереження якості життя пацієнтів, фармакологічне втручання має бути спрямоване не тільки на зниження гіперглікемії, а й на більш ефективний захист серцево-судинної системи. Сформульована в останні роки мультигенна концепція розвитку ЦД дозволила відійти від так званої глюкоцентричної теорії, яка панувала в лікуванні захворювання протягом багатьох років, й обґрунтувати нові підходи до ведення таких хворих. Згідно з останніми даними, пріоритет належить антидіабетичним препаратам, ефекти яких не обмежуються усуненням симптомів ЦД, а забезпечують блокування основних патогенетичних ланок захворювання, впливаючи на внутрішньоклітинні метаболічні процеси. Слід зазначити, що особлива увага приділяється застосуванню препаратів на основі природних компонентів, які містять комплекси біологічно активних речовин, структурно подібних метаболітам організму, і мають меншу токсичність, ніж синтетичні лікарські засоби. Одним із таких препаратів є Кратал (ПАТ НВЦ «Борщагівський хіміко-фармацевтичний завод», м. Київ), який містить природну амінокислоту таурин, екстракти плодів глоду та кропиви собачої. Протягом багатьох років препарат Кратал, який виявляє кардіотонічну дію, антиангінальний, антиаритмічний, антиагрегантний та седативний ефекти, успішно застосовується при нейроциркуляторній дистонії, хронічній ішемічній хворобі серця та пострадіаційному синдромі. Поєднання в одному препараті декількох біологічно активних сполук зумовлює синергізм їх терапевтичної дії та розширює можливості клінічного застосування. Останнім часом з’явилися повідомлення про те, що основні складові Краталу мають також антидіабетичні властивості. Це стало підґрунтям для проведення експериментальних і клінічних досліджень щодо визначення ефективності зазначеного препарату як потенційного засобу для профілактики і лікування ЦД та його судинних ускладнень.
Таурин
Важливим компонентом Краталу є таурин (2-аміноетансульфонова кислота) – вільна амінокислота, яка не входить до складу білків та наявна в цитозолі клітин майже всіх органів ссавців. Основна кількість таурину надходить в організм людини з їжею тваринного походження, а також у невеликій кількості синтезується в печінці з цистеїну за участю декарбоксилази цистеїнсульфонової кислоти. Завдяки унікальній хімічній структурі таурин залучений до таких фундаментальних клітинних процесів, як осмотична регуляція, іонний гомеостаз, посттранскрипційна регуляція активності ферментів і модуляція внутрішньоклітинного сигналінгу. Він бере участь у широкому спектрі біологічних процесів, включно з кон’югацією жовчних кислот, стабілізацією фоторецепторних клітин сітківки; має антиоксидантні та протизапальні властивості, виявляє антиаритмічну, іонотропну та хронотропну дію, є нейромодулятором центральної нервової системи. Згідно з експериментальними та клінічними даними, концентрація таурину в плазмі та всередині клітин (тромбоцитів) у разі ЦД як 1, так і 2 типу знижується в 1,5-2 рази порівняно з відповідним показником в осіб без ЦД. Оскільки дефіцит таурину асоційований з дисфункцією в різних тканинах, він також може впливати на патогенез діабетичних судинних ускладнень. В останні роки з’явилися дані щодо ефективності застосування таурину не тільки як гепато-, нейро- і кардіопротектора, а й як засобу для профілактики і лікування ЦД та його судинних ускладнень. В експериментальних дослідженнях установлено, що таурин покращує чутливість периферичних тканин до інсуліну та гальмує розвиток абдомінального ожиріння в щурів зі спонтанним ЦД 2 типу, знижує гіпертригліцеридемію в щурів зі стрептозотоциновим діабетом, підвищує рівень відновленого глутатіону в ізольованих гепатоцитах. Клінічні дослідження показали, що таурин запобігає розвитку інсулінорезистентності та дисфункції панкреатичних β-клітин, що індуковані підвищеним рівнем вільних жирних кислот у чоловіків із надмірною масою тіла. На сьогодні накопичено велику кількість експериментальних даних про позитивні результати застосування таурину для запобігання розвитку діабетичних ускладнень, спричинених тривалою некомпенсованою гіперглікемією, зокрема діабетичної нефропатії. Установлено, що використання високих доз таурину запобігає появі функціональних і структурних порушень нирок у тварин зі стрептозотоциновим діабетом. Показано, що таурин знижує ступінь протеїнурії, попереджає гіпертрофію клубочків і розвиток гломерулосклерозу, знижує рівень продуктів ліпопероксидації та трансформуючого фактора росту‑1β у нирках. Завдяки своїм антиоксидантним властивостям таурин зменшує апоптоз ендотеліальних клітин, індукований вільними радикалами, може відновлювати проникність мембран і запобігати клітинним ушкодженням, пов’язаним зі збільшенням внутрішньоклітинного току Са2+. Антидіабетичні властивості таурину можуть реалізовуватися за рахунок 4 основних механізмів дії: антиоксидантної активності, протизапальних ефектів, осморегуляторної активності, впливу на глюкозний гомеостаз (табл. 1).
Результати низки досліджень указують на участь таурину в регулюванні гомеостазу глюкози, проте точні механізми його дії дотепер не відомі. Припускають, що таурин може впливати на глюкозний гомеостаз двома шляхами: підсилюючи експресію генів, що відповідають за глюкозстимульовану секрецію інсуліну, а також підвищуючи чутливість периферичних тканин до дії гормону. Показано, що таурин може сприяти взаємодії інсуліну з його рецептором, а також посилювати інсуліновий сигналінг, що призводить до підвищення синтезу глікогену, посилення гліколізу і захоплення глюкози в печінці та серці. Знижуючи підвищену активність роз’єднувального білка (UCP2) на внутрішній мембрані мітохондрій, таурин сприяє відновленню порушеної при ЦД 2 типу глюкозіндукованої секреції інсуліну. Численні експериментальні дослідження (як in vivo, так і in vitro) дозволили встановити декілька додаткових молекулярних механізмів протекторної дії таурину щодо діабетичних мікро- та макросудинних ускладнень (табл. 2).
Експериментальні докази широкого спектра антидіабетичних властивостей таурину свідчать про доцільність його вивчення в рамках подальших широкомасштабних клінічних випробувань як додаткового засобу комплексної фармакотерапії ЦД та його ускладнень.
Екстракт плодів глоду (Crataegus oxyacantha L.)
Протягом багатьох століть глід використовується в традиційній та народній медицині різних країн для лікування серцево-судинних захворювань, зокрема артеріальної гіпертензії, аритмій, хронічної серцевої недостатності, пароксизмальної тахікардії та ін. Біологічна активність екстракту плодів глоду зумовлена наявністю в них флавоноїдів, тритерпенових кислот, олігомерних проантоціанідів, органічних кислот та кардіоактивних амінів. Спектр найбільш досліджених фармакологічних властивостей глоду включає кардіотропну, гіполіпідемічну, антиоксидантну, протизапальну та седативну активність. Нещодавно було отримано експериментальні дані, які свідчать про наявність в екстракту глоду також антидіабетичних властивостей. Так, у дослідах на С57BL/6J мишах із ЦД, індукованим дієтою з високим умістом жиру, було виявлено, що застосування цього екстракту сприяє зниженню гіперглікемії, гіпертригліцеридемії та гіперхолестеринемії. Вважають, що механізм антигіперглікемічної дії глоду полягає в активації АМФ-залежної кінази (AMPK) шляхом посилення її фосфорилювання, у результаті чого знижується активність ключового ферменту глюконеогенезу – фосфоенолпіруваткарбоксикінази, що супроводжується зменшенням продукції глюкози печінкою. Окрім того, покращенню гомеостазу глюкози може сприяти підвищення синтезу та транслокації глюкозного транспортера GLUT 4, що посилює утилізацію глюкози в скелетних м’язах. З іншого боку, активація AMPK у печінці під впливом глоду зумовлює зниження рівня мРНК-синтази жирних кислот, посилення β-окислення за рахунок підвищення експресії генів ферментів окислення жирних кислот, зокрема PPARα, та зниження концентрації циркулюючих тригліцеридів і холестерину завдяки пригніченню експресії регуляторних протеїнів SREBP1c та SREBP2. Зниження синтезу тригліцеридів у печінці під впливом глоду також супроводжується зменшенням маси жирової тканини, переважно за рахунок зниження кількості адипоцитів великого розміру, які посилюють атерогенність у тварин з діабетом. Таким чином, активація AMPK у печінці під впливом глоду може пояснити його плейотропні антидіабетичні властивості. В інших дослідженнях показано, що застосування настоянки плодів Crataegus oxyacantha у щурів, які перебували на гіперліпідемічній дієті, попереджує підвищення концентрації ліпідів у плазмі крові та жирових депо в печінці та аорті. Окрім того, у щурів на атерогенній дієті екстракт глоду посилював зв’язування ЛПНЩ із плазматичною мембраною печінки in vitro та їх взаємодію з рецепторами, підвищував екскрецію жовчних кислот, знижував синтез холестерину. Відомо, що глід також може знижувати абсорбцію холестерину шляхом пригнічення активності кишкової ацетил-коензим А-холестеринацилтрансферази. Зазначені фармакологічні ефекти можуть досягатися завдяки синергічній дії флавоноїдів, тритерпенів, сапонінів і деяких амінів, що входять до складу настоянки з плодів глоду. Виявлені антигіперглікемічні та гіполіпідемічні властивості глоду обґрунтовують доцільність його використання у складі комплексної фармакотерапії ЦД 2 типу.
Екстракт кропиви собачої (Leonurus cardiaca L.)
Завдяки наявності таких фізіологічно активних речовин, як алкалоїди, флавоноїди, терпени, органічні кислоти та їхні деривати, антоціани, стероли, глікозиди та ін., кропива собача має широкий спектр фармакологічних властивостей та тривалу історію використання у фітотерапії різних захворювань. Відомо, що екстракт цієї рослини виявляє антибактеріальну, седативну, аналгетичну, протисудомну, антиангінальну, гіпотензивну, спазмолітичну, діуретичну та м’яку кардіотонічну активність. Крім того, показано, що кропива собача знижує рівень прозапальних цитокінів і фактора некрозу пухлин, індукує експресію оксиду азоту, має антиоксидантні властивості. У дослідах на мишах лінії C57BL/6, які отримували атерогенну дієту, застосування екстракту Leonurus забезпечувало зниження у плазмі рівня холестерину, тригліцеридів, підвищення вмісту холестерину ліпопротеїнів високої щільності та зменшення експресії рецепторів лептиноподібних окиснених ЛПНЩ, тим самим покращуючи ендотеліальну функцію. Літературні дані свідчать про перспективність застосування екстрактів кропиви собачої при ЦД 2 типу. Встановлено позитивний вплив цієї рослини на секрецію інсуліну, електрофізіологічні характеристики, проліферацію та внутрішньоклітинну концентрацію кальцію при застосуванні на культурах клітин інсуліноми INS‑1E. Припускають, що активні компоненти, які стимулюють секрецію інсуліну, є полярними та добре розчиняються у воді; ймовірно, серед них – кверцетин-О-гексозилгексозид та кверцетин-О-деоксигексозилгексозид. Вони інгібують мітохондріальний роз’єднуючий протеїн, що підвищує мембранний потенціал і рівень АТФ та пригнічує АТФ-чутливі калієві канали в панкреатичних β-клітинах. Одним із можливих пояснень дії екстрактів Leonurus на вивільнення інсуліну також можуть бути посилення електричної активності та підвищення концентрації кальцію в гормонпродукуючих клітинах. З’ясовано, що застосування протягом 3 тиж леонуріну; SCM‑198 – алкалоїду, що міститься в траві кропиви собачої, – у мишей призводить до зниження постпрандіальної гіперглікемії, рівня тригліцеридів у плазмі крові та підвищення концентрації інсуліну; це підтверджує антидіабетичні властивості цієї речовини. Гіпоглікемічний ефект SCM‑198, імовірно, зумовлений його здатністю регулювати транскрипцію генів метаболізму глюкози та знижувати її продукцію печінкою. Встановлено, що леонурін посилює експресію мРНК глюкокінази та знижує таку фосфоенолпіруваткарбоксикінази, впливаючи на Akt-шлях і посилюючи фосфорилювання FOXO1. Таким чином, аналіз літературних джерел свідчить про те, що кожен із компонентів препарату Кратал по-різному впливає на основні патогенетичні ланки ЦД та його судинних ускладнень, а поєднання активних сполук може забезпечити синергізм антидіабетичної дії.
Експериментальні дослідження антидіабетичних властивостей препарату Кратал
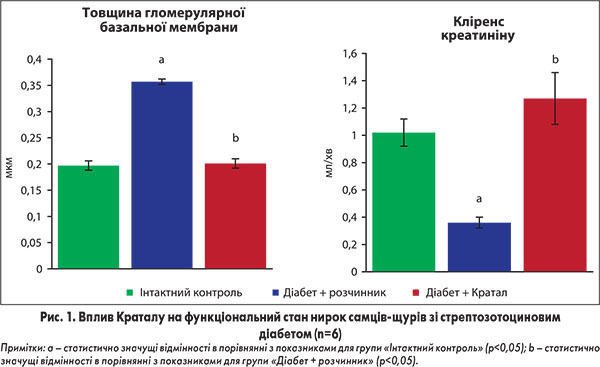
При експериментальному вивченні впливу препарату Кратал на розвиток метаболічного синдрому, індукованого високофруктозною дієтою, встановлено, що цей засіб сприяє покращенню толерантності до вуглеводів та чутливості до інсуліну, зниженню вираженості абдомінального ожиріння, гіпертригліцеридемії, гіперхолестеринемії та відновленню продукції оксиду азоту. Показано, що використання Краталу відновлює біоенергетичні процеси в серцевому м’язі за рахунок нормалізації швидкості АДФ-стимульованого дихання мітохондрій за наявності НАД-залежного субстрату, запобігає розвитку оксидативного стресу внаслідок зниження вмісту ТБК-активних продуктів і підвищенню глутатіону в мітохондріях кардіоміоцитів в умовах метаболічного синдрому (МС). Нормалізація метаболічних показників під впливом Краталу супроводжувалася покращенням функціонального стану серцево-судинної системи в щурів із МС за рахунок відновлення нормального серцевого ритму й атріовентрикулярної провідності, позитивного впливу на систолічну та діастолічну активність серця, гальмування розвитку синусової тахікардії та ішемічних процесів у міокарді. У результаті дослідження впливу Краталу на розвиток діабетичної нефропатії в щурів зі стрептозотоциновим діабетом було виявлено, що застосування препарату протягом 2 міс сприяє зниженню базальної гіперглікемії, глюкозурії, нормалізації кліренсу креатиніну та швидкості клубочкової фільтрації, ослабленню оксидативного і нітрозивного стресу в нирках, зменшенню вираженості мікроальбумінурії та морфоструктурних змін у нирках (рис. 1).
Клінічна оцінка ефективності та переносимості препарату Кратал у комплексній терапії хворих на ЦД 2 типу
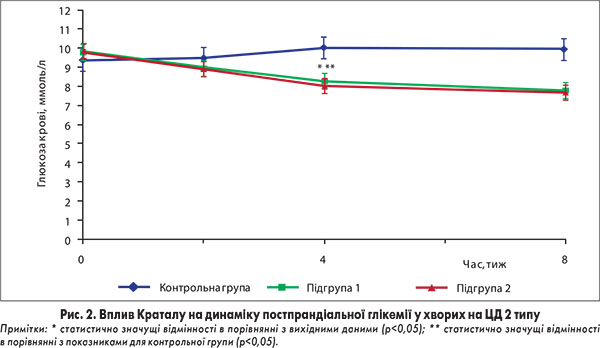
Дослідження було проведено на базі клініки ДУ «Інститут проблем ендокринної патології ім. В. Я. Данилевського НАМН України» (м. Харків). Обстежено 95 хворих на ЦД 2 типу з анамнезом захворювання від 1 до 5 років, рівнем глюкози від 7 до 10 ммоль/л протягом доби, які отримували пероральні цукрознижувальні засоби не менше 1 міс. Вік учасників варіював у межах від 30 до 65 років. Тривалість курсу лікування становила 8 тиж. До контрольної групи хворих, які отримували стандартну цукрознижувальну терапію, було включено 45 осіб; до першої підгрупи основної групи (препарат Кратал по 1 таблетці 3 р/добу на тлі стандартної цукрознижувальної терапії) – 25 пацієнтів, до другої підгрупи основної групи (препарат Кратал по 2 таблетки 3 р/добу на тлі стандартної базисної цукрознижувальної терапії) – також 25 учасників. Під впливом призначеного лікування у хворих на ЦД 2 типу першої та другої підгруп основної групи відмічали покращення глікемічного контролю, про що свідчило зниження рівня базальної та постпрандіальної глікемії, а також фруктозаміну (як відносно показників до початку лікування, так і порівняно з відповідними показниками контрольної групи; рис. 2).
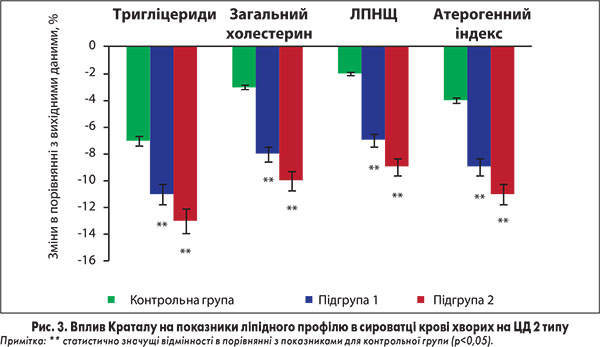
Оцінка ліпідного обміну у хворих на ЦД 2 типу в обох підгрупах основної групи підтвердила протекторний ефект Краталу щодо розвитку діабетичної дисліпідемії. Так, у цих пацієнтів спостерігалося значне зниження концентрації тригліцеридів та загального холестерину в сироватці крові (як у порівнянні з показниками до лікування, так і відносно таких в учасників контрольної групи). Окрім того, встановлено достовірне зниження рівня ЛПНЩ у сироватці крові хворих на ЦД 2 типу, які отримували Кратал, що сприяло суттєвому зменшенню атерогенного індексу (рис. 3).
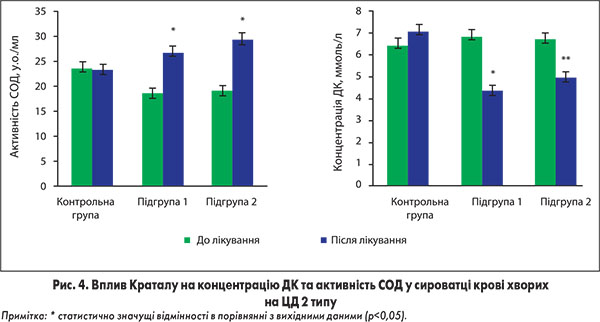
При визначенні впливу Краталу на інтенсивність процесів перекисного окислення ліпідів у хворих на ЦД основної групи встановлено майже двократне зменшення концентрації його первинних продуктів – дієнових кон’югатів (ДК) – та вторинних (малонового діальдегіду) в сироватці крові порівняно з відповідними показниками до лікування та в учасників контрольної групи. Разом із тим у хворих основної групи відмічалось істотне зростання активності ферменту супероксиддисмутази (СОД), який каталізує реакцію дисмутації супероксидного радикалу, порівняно з відповідним показником до лікування у пацієнтів контрольної групи, що свідчить про активацію під впливом препарату антирадикальної системи захисту (рис. 4).
При застосуванні препарату Кратал не виявлено будь-яких серйозних гастроентерологічних, дерматологічних, алергічних, гематологічних, ендокринних та інших побічних явищ. Було встановлено, що застосування препарату Кратал по 1 таблетці 3 р/добу протягом 8 тиж є достатнім для прояву антидіабетичної активності.
Висновки
Аналіз результатів експериментальних і клінічних досліджень дозволяє стверджувати, що застосування препарату Кратал у комплексній терапії ЦД 2 типу знижує кардіометаболічний ризик і гальмує розвиток діабетичних мікро- та макросудинних ускладнень. Це може сприяти підвищенню тривалості та якості життя хворих на ЦД.
Список літератури знаходиться в редакції.
Медична газета «Здоров’я України 21 сторіччя» №6 (379), березень 2016 р.