12 грудня, 2016
Флосін і Простамол Уно – комплексний підхід до лікування симптомів нижніх сечових шляхів у чоловіків
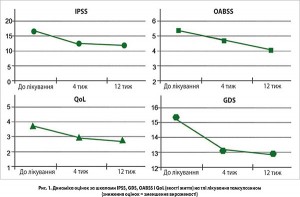 Покращення оцінки IPSS на 12-му тижні в порівнянні з вихідним показником було зіставним в обох групах (6,44±1,56 vs 6,0±1,37). Серед пацієнтів 2-ї групи найбільш виражене зменшення депресивних симптомів було зафіксовано у хворих з гіршими оцінками IPSS до лікування. Таким чином, у пацієнтів з ДГПЗ і коморбідною депресією лікування тамсулозином забезпечує значне зменшення СНСШ і депресії, а також покращення якості життя.
Сьогодні для лікування захворювань ПЗ широко використовується препарат Простамол Уно (оригінальний екстракт плодів пальми пилкоподібної – Serenoa repens), якому притаманний багатовекторний вплив на ПЗ. Екстракт Serenoa repens має антиандрогенний ефект, обумовлений гальмуванням активності 5α-редуктази, блокуванням зв’язування дигідротестостерону з рецептором. Крім того, ріст тканин ПЗ уповільнюється внаслідок гальмування зв’язування рецепторів пролактину і порушення процесів передачі сигналу, пригнічення проліферації епітелію ПЗ, блокади естрогенного каскаду. Перевагами Простамолу Уно є відсутність негативного впливу на сексуальну функцію пацієнтів, а також протинабрякова і протизапальна дія.
У численних дослідженнях доведено, що препарат Простамол Уно на основі плодів Serenoa repens інгібує ріст тканин ПЗ шляхом блокади 5α-редуктази й ароматази, виявляє пряму розслаблюючу дію на непосмуговану мускулатуру, має протизапальний ефект й усуває набряк за рахунок блокування циклооксигенази і 5-ліпоксигенази, впливає на простатичні фактори росту.
Існує низка клінічних досліджень, що вказують на хорошу ефективність екстракту Serenoa repens щодо СНСШ у чоловіків із ДГПЗ. В одному з досліджень оцінювали результати лікування 60 пацієнтів із ДГПЗ і СНСШ (Hizli, Uygur, 2007). Хворі були розподілені на 3 групи: 1-ша група (n=20) приймала екстракт Serenoa repens 320 мг/добу, 2-га (n=20) – тамсулозин 0,4 мг/добу і 3-тя (n=20) – комбінацію препаратів. Після закінчення лікування оцінювали загальний бал шкали IPSS і максимальну швидкість потоку сечі. У результаті лікування в усіх трьох групах було відзначено приблизно однакове достовірне покращення СНСШ і Qmax. Автори статті дійшли висновку, що екстракт Serenoa repens є ефективним і безпечним лікарським засобом у випадку СНСШ, зумовлених ДГПЗ.
Ще однією важливою роботою стало дослідження, дані якого було опубліковано у 2011 р. Sinescu і співавт. У дослідження були включені 120 пацієнтів з легкими і помірними СНСШ на тлі ДГПЗ. При цьому в усіх хворих Qmax не перевищувала 15 мл/с, а об’єм залишкової сечі становив не більше 150 мл. Хворі приймали екстракт Serenoa repens по 320 мг щодня протягом 12 міс. У підсумку було виявлено достовірне покращення середнього бала за IPSS – на 5,5, якості життя – на 1,8 бала, Qmax – на 5,6 мл/с. Міжнародний індекс еректильної функції (IIEF) збільшився на 6,4 бала. Також відзначено зменшення об’єму залишкової сечі і розмірів ПЗ. Автори роботи зазначили, що тривале лікування екстрактом Serenoa repens ефективне в разі легких і средньотяжких СНСШ при ДГПЗ. Крім цього, тривале використання препарату може бути сприятливим і щодо еректильної функції, що продемонстровано статистично значущим покращенням значення IIEF.
У міжнародному рандомізованому подвійному сліпому контрольованому дослідженні французькі вчені оцінювали протизапальні властивості екстракту Serenoa repens у 206 чоловіків з ДГПЗ і СНСШ (Latil A. et al., 2015). Протягом 3 міс пацієнти основної групи отримували екстракт Serenoa repens 320 мг/добу; хворим контрольної групи призначали тамсулозин 4 мг/добу. До початку лікування і на 90-й день після пальцевого ректального дослідження (ПРД) ПЗ отримували зразки сечі. З простатичних клітин, десквамованих після ПРД, екстрагували мРНК для подальшого аналізу 29 найбільш значущих запальних маркерів.
В обох групах прихильність пацієнтів до лікування була дуже високою (>95%). Оцінка за IPSS знизилася значно більше в групі Serenoa repens, що супроводжувалося покращенням якості життя.
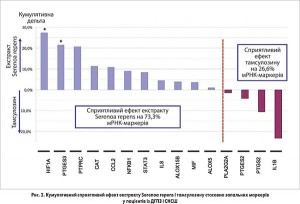
Після 3 міс експресія запальних маркерів знизилася на 65,4% в основній групі і на 46,2% – в контрольній. Для 15 найчастіше експресованих генів ця різниця була ще більш істотною (80 vs 33% відповідно). Кумулятивний сприятливий ефект Serenoa repens спостерігався відносно 73,3% запальних маркерів, тамсулозину – для 26,6% маркерів (рис. 2). Рівні трьох запальних білків (MCP‑1/CCL2, IP‑10/CXCL10 і MIF) зменшувалися лише в пацієнтів, які отримували екстракт Serenoa repens. В основній групі в учасників з вихідною підвищеною експресією MIF частота відповіді за шкалою IPSS була значно вищою порівняно з такою у хворих з нормальною експресією цього білка (6,4 vs 4,5 бала відповідно). У групі тамсулозину подібна залежність не простежувалася. Лікування досліджуваними препаратами добре переносилося, частота побічних ефектів була однаково низькою в обох групах. Таким чином, отримані результати продемонстрували виражену протизапальну активність і безпеку екстракту Serenoa repens у веденні симптомної ДГПЗ.
Покращення оцінки IPSS на 12-му тижні в порівнянні з вихідним показником було зіставним в обох групах (6,44±1,56 vs 6,0±1,37). Серед пацієнтів 2-ї групи найбільш виражене зменшення депресивних симптомів було зафіксовано у хворих з гіршими оцінками IPSS до лікування. Таким чином, у пацієнтів з ДГПЗ і коморбідною депресією лікування тамсулозином забезпечує значне зменшення СНСШ і депресії, а також покращення якості життя.
Сьогодні для лікування захворювань ПЗ широко використовується препарат Простамол Уно (оригінальний екстракт плодів пальми пилкоподібної – Serenoa repens), якому притаманний багатовекторний вплив на ПЗ. Екстракт Serenoa repens має антиандрогенний ефект, обумовлений гальмуванням активності 5α-редуктази, блокуванням зв’язування дигідротестостерону з рецептором. Крім того, ріст тканин ПЗ уповільнюється внаслідок гальмування зв’язування рецепторів пролактину і порушення процесів передачі сигналу, пригнічення проліферації епітелію ПЗ, блокади естрогенного каскаду. Перевагами Простамолу Уно є відсутність негативного впливу на сексуальну функцію пацієнтів, а також протинабрякова і протизапальна дія.
У численних дослідженнях доведено, що препарат Простамол Уно на основі плодів Serenoa repens інгібує ріст тканин ПЗ шляхом блокади 5α-редуктази й ароматази, виявляє пряму розслаблюючу дію на непосмуговану мускулатуру, має протизапальний ефект й усуває набряк за рахунок блокування циклооксигенази і 5-ліпоксигенази, впливає на простатичні фактори росту.
Існує низка клінічних досліджень, що вказують на хорошу ефективність екстракту Serenoa repens щодо СНСШ у чоловіків із ДГПЗ. В одному з досліджень оцінювали результати лікування 60 пацієнтів із ДГПЗ і СНСШ (Hizli, Uygur, 2007). Хворі були розподілені на 3 групи: 1-ша група (n=20) приймала екстракт Serenoa repens 320 мг/добу, 2-га (n=20) – тамсулозин 0,4 мг/добу і 3-тя (n=20) – комбінацію препаратів. Після закінчення лікування оцінювали загальний бал шкали IPSS і максимальну швидкість потоку сечі. У результаті лікування в усіх трьох групах було відзначено приблизно однакове достовірне покращення СНСШ і Qmax. Автори статті дійшли висновку, що екстракт Serenoa repens є ефективним і безпечним лікарським засобом у випадку СНСШ, зумовлених ДГПЗ.
Ще однією важливою роботою стало дослідження, дані якого було опубліковано у 2011 р. Sinescu і співавт. У дослідження були включені 120 пацієнтів з легкими і помірними СНСШ на тлі ДГПЗ. При цьому в усіх хворих Qmax не перевищувала 15 мл/с, а об’єм залишкової сечі становив не більше 150 мл. Хворі приймали екстракт Serenoa repens по 320 мг щодня протягом 12 міс. У підсумку було виявлено достовірне покращення середнього бала за IPSS – на 5,5, якості життя – на 1,8 бала, Qmax – на 5,6 мл/с. Міжнародний індекс еректильної функції (IIEF) збільшився на 6,4 бала. Також відзначено зменшення об’єму залишкової сечі і розмірів ПЗ. Автори роботи зазначили, що тривале лікування екстрактом Serenoa repens ефективне в разі легких і средньотяжких СНСШ при ДГПЗ. Крім цього, тривале використання препарату може бути сприятливим і щодо еректильної функції, що продемонстровано статистично значущим покращенням значення IIEF.
У міжнародному рандомізованому подвійному сліпому контрольованому дослідженні французькі вчені оцінювали протизапальні властивості екстракту Serenoa repens у 206 чоловіків з ДГПЗ і СНСШ (Latil A. et al., 2015). Протягом 3 міс пацієнти основної групи отримували екстракт Serenoa repens 320 мг/добу; хворим контрольної групи призначали тамсулозин 4 мг/добу. До початку лікування і на 90-й день після пальцевого ректального дослідження (ПРД) ПЗ отримували зразки сечі. З простатичних клітин, десквамованих після ПРД, екстрагували мРНК для подальшого аналізу 29 найбільш значущих запальних маркерів.
В обох групах прихильність пацієнтів до лікування була дуже високою (>95%). Оцінка за IPSS знизилася значно більше в групі Serenoa repens, що супроводжувалося покращенням якості життя.
Після 3 міс експресія запальних маркерів знизилася на 65,4% в основній групі і на 46,2% – в контрольній. Для 15 найчастіше експресованих генів ця різниця була ще більш істотною (80 vs 33% відповідно). Кумулятивний сприятливий ефект Serenoa repens спостерігався відносно 73,3% запальних маркерів, тамсулозину – для 26,6% маркерів (рис. 2). Рівні трьох запальних білків (MCP‑1/CCL2, IP‑10/CXCL10 і MIF) зменшувалися лише в пацієнтів, які отримували екстракт Serenoa repens. В основній групі в учасників з вихідною підвищеною експресією MIF частота відповіді за шкалою IPSS була значно вищою порівняно з такою у хворих з нормальною експресією цього білка (6,4 vs 4,5 бала відповідно). У групі тамсулозину подібна залежність не простежувалася. Лікування досліджуваними препаратами добре переносилося, частота побічних ефектів була однаково низькою в обох групах. Таким чином, отримані результати продемонстрували виражену протизапальну активність і безпеку екстракту Serenoa repens у веденні симптомної ДГПЗ.
 У дослідженні QUALIPROST оцінювали зміни симптомів і якості життя в пацієнтів із чили 1713 чоловіків віком ≥40 років з оцінкою за шкалою IPSS ≥8 балів. До лікування оцінка IPSS та індекс впливу ДГПЗ на якість життя (BII) становили 16,8±5,4 і 6,8±2,6 бала відповідно. Близько 9% обстежених не отримували лікування (група спостереження), 70% отримували монотерапію (α-блокатори, фітотерапію або інгібітори 5α-редуктази). В 95,2% фітотерапія проводилась екстрактом Serenoa repens. Комбіноване лікування (α-блокатор + інгібітор 5α-редуктази, α-блокатор + екстракт Serenoa repens) призначалося 21% пацієнтів.
Через 6 міс в усіх групах активної терапії було зафіксовано поліпщення якості життя і зменшення симптомів порівняно з вихідними показниками і групою спостереження. Екстракт Serenoa repens як в монотерапії, так і в комбінації з α-блокатором продемонстрував ефективність, порівняну з такою α-блокаторів та інгібіторів 5α-редуктази, але частота побічних ефектів була нижчою при застосуванні фітопрепарату (Alcaraz A. et al., 2016).
Крім ДГПЗ формування СНСШ нерідко буває спричинене таким станом, як хронічний простатит (ХП). За даними Di Silverio і співавт. (2003), у 43% пацієнтів з доброякісною простатичною обструкцією при проведенні біопсії ПЗ вдається виявити запальні зміни. Більш того, доведено існування достовірної кореляції між розміром ПЗ і хронічним запаленням. Певні дані свідчать про наявність високого ризику розвитку доброякісної простатичної обструкції в разі ХП і формування ускладнень у пацієнтів з обструктивними проявами СНСШ на тлі ДГПЗ і супутнім запаленням у ПЗ.
У комплексному лікуванні хворих на ХП з розладами сечовипускання Простамол Уно показав себе як високоефективний препарат з мінімальними побічними ефектами (Пасєчніков С. П., Нікітін О. Д., 2004). Включення Простамолу Уно до складу комплексної терапії пацієнтів із ДГПЗ і ХП, яка передбачає призначення α1-адреноблокаторів, прискорювало терміни лікування й покращувало показники якості життя. Використання препарату Простамол Уно в монотерапії ХП, особливо асептичного, дозволяло швидко й ефективно усувати обструктивні й іритативні СНСШ і покращувити якість життя хворих.
З огляду на різноспрямовані механізми дії раціональною є комбінована терапія ДГПЗ/СНСШ тамсулозином та екстрактом Serenoa repens.
Одним з останніх досліджень, у яких вивчався цей підхід, є робота Y. W. Ryu і співавт. (2014). Пацієнти із симптомною ДГПЗ (IPSS >10 балів) були рандомізовані для отримання тамсулозину 0,2 мг/добу в монотерапії (n=53) або в комбінації з екстрактом Serenoa repens 320 мг/добу (n=60) протягом 12 міс. Крім IPSS до початку лікування і після його закінчення визначали об’єм ПЗ та оцінювали якість життя, пов’язане із СНСШ. Через 12 міс загальна оцінка за шкалою IPSS знизилася на 5,5 балів у групі монотерапії і на 5,8 бала в групі комбінованого лікування. Симптоми накопичення зменшилися значно більше при одночасному застосуванні досліджуваних препаратів (1,7 vs 0,8 у групі тамсулозину; р=0,024), причому цей ефект тривав 12 міс. Переносимість лікування була хорошою, за частотою несприятливих подій групи не розрізнялися.
У дослідженні Литвинця і співавт. (2011) у чоловіків із синдромом незапального хронічного тазового болю комплексна терапія Флосіном (0,4 мг 1 р/добу вранці після їди) і Простамолом Уно (1 капсула увечері) забезпечила значне покращення оцінки IPSS, якості життя і загального стану при оцінці на 15-й і 30-й день лікування.
Дослідження ПРОСПЕКТ за участю 2240 пацієнтів із ДГПЗ з усіх регіонів України підтвердило ефективність і безпеку комбінованої терапії Флосіном і Простамолом Уно. Дані, отримані в різних урологічних центрах України, свідчили про повну відповідність результатам досліджень, проведених в інших європейських державах. Це стало доказом того, що оперативне лікування давно втратило статус золотого стандарту для ДГПЗ ІІ-ІІІ стадії, поступившись місцем консервативній терапії.
З урахуванням отримання настільки обнадійливих даних українських урологів порівняльне дослідження ПРОСПЕКТ II було продовжено на 12 міс. Результати засвідчили високу ефективність комплексної терапії Флосіном і Простамолом Уно, що становила 96,9%, з меншою частотою побічних ефектів (5,4%) в порівнянні з відповідним показником для терапії доксазозином і фінастеридом (43,3%).
Метою дослідження ПРОСПЕКТ III було визначити можливості довгострокової терапії комбінацією Флосін / Простамол Уно в аспекті оцінки якості життя, можливості покращення об’єктивних даних урологічного статусу і впливу на сексуальний статус у чоловіків з ДГПЗ ІІ стадії. У підсумку ефективність використання 3-річної комбінованої терапії із застосуванням препаратів Флосін і Простамол Уно дорівнювала 94,1%, у контрольній групі (доксазозин і фінастерид) – 89,3% (р<0,05).
Довгострокова комбінована терапія з використанням препаратів Флосін і Простамол Уно добре переносилася пацієнтами й асоціювалася з низькою частотою розвитку побічних ефектів (5,75% випадків). При комбінуванні препаратів доксазозину і фінастериду побічні явища спостерігалися в 33,1% пацієнтів (р<0,05).
Доведено, що довгострокова комбінована терапія із застосуванням Флосіну і Простамолу Уно є оптимальною для лікування пацієнтів із ДГПЗ II стадії, оскільки забезпечує синергізм ефективності.
Слід зазначити, що оптимальним співвідношенням ефективність/безпека характеризуються не всі лікарські комбінації, які застосовуються в лікуванні ДГПЗ/СНСШ. Зокрема, в дослідженні MTOPS (2003) поєднане призначення фінастериду (блокатор α1-адренорецепторів) і доксазозину (інгібітор 5α-редуктази) в порівнянні з монотерапією одним з них було більш ефективним у зменшенні симптомів, проте асоціювалося з більшою частотою побічних ефектів – периферичних набряків, задишки і ретроградної еякуляції. У дослідженні C. G. Roehrborn і співавт. (2008) на тлі комбінованого прийому тамсулозину і дутастериду була зафіксована підвищена частота розвитку еректильної дисфункції, порушень сім’явиверження, зменшення об’єму еякуляту та гінекомастії.
Таким чином, застосування комбінованої терапії СНСШ дозволяє забезпечити ефект синергізму дії декількох препаратів, що сприяє швидшому уповільненню прогресування хвороби. Комбінація оригінального екстракту Serenoa repens (Простамол Уно) і тамсулозину (Флосін) може розглядатися як оптимальна для лікування ДГПЗ/СНСШ, у тому числі на тлі ХП, оскільки вона добре переноситься, має високу ефективність в усуненні порушень сечовипускання і коморбідних проявів, а також дозволяє покращити якість життя пацієнтів.
Підготував Олексій Терещенко
У дослідженні QUALIPROST оцінювали зміни симптомів і якості життя в пацієнтів із чили 1713 чоловіків віком ≥40 років з оцінкою за шкалою IPSS ≥8 балів. До лікування оцінка IPSS та індекс впливу ДГПЗ на якість життя (BII) становили 16,8±5,4 і 6,8±2,6 бала відповідно. Близько 9% обстежених не отримували лікування (група спостереження), 70% отримували монотерапію (α-блокатори, фітотерапію або інгібітори 5α-редуктази). В 95,2% фітотерапія проводилась екстрактом Serenoa repens. Комбіноване лікування (α-блокатор + інгібітор 5α-редуктази, α-блокатор + екстракт Serenoa repens) призначалося 21% пацієнтів.
Через 6 міс в усіх групах активної терапії було зафіксовано поліпщення якості життя і зменшення симптомів порівняно з вихідними показниками і групою спостереження. Екстракт Serenoa repens як в монотерапії, так і в комбінації з α-блокатором продемонстрував ефективність, порівняну з такою α-блокаторів та інгібіторів 5α-редуктази, але частота побічних ефектів була нижчою при застосуванні фітопрепарату (Alcaraz A. et al., 2016).
Крім ДГПЗ формування СНСШ нерідко буває спричинене таким станом, як хронічний простатит (ХП). За даними Di Silverio і співавт. (2003), у 43% пацієнтів з доброякісною простатичною обструкцією при проведенні біопсії ПЗ вдається виявити запальні зміни. Більш того, доведено існування достовірної кореляції між розміром ПЗ і хронічним запаленням. Певні дані свідчать про наявність високого ризику розвитку доброякісної простатичної обструкції в разі ХП і формування ускладнень у пацієнтів з обструктивними проявами СНСШ на тлі ДГПЗ і супутнім запаленням у ПЗ.
У комплексному лікуванні хворих на ХП з розладами сечовипускання Простамол Уно показав себе як високоефективний препарат з мінімальними побічними ефектами (Пасєчніков С. П., Нікітін О. Д., 2004). Включення Простамолу Уно до складу комплексної терапії пацієнтів із ДГПЗ і ХП, яка передбачає призначення α1-адреноблокаторів, прискорювало терміни лікування й покращувало показники якості життя. Використання препарату Простамол Уно в монотерапії ХП, особливо асептичного, дозволяло швидко й ефективно усувати обструктивні й іритативні СНСШ і покращувити якість життя хворих.
З огляду на різноспрямовані механізми дії раціональною є комбінована терапія ДГПЗ/СНСШ тамсулозином та екстрактом Serenoa repens.
Одним з останніх досліджень, у яких вивчався цей підхід, є робота Y. W. Ryu і співавт. (2014). Пацієнти із симптомною ДГПЗ (IPSS >10 балів) були рандомізовані для отримання тамсулозину 0,2 мг/добу в монотерапії (n=53) або в комбінації з екстрактом Serenoa repens 320 мг/добу (n=60) протягом 12 міс. Крім IPSS до початку лікування і після його закінчення визначали об’єм ПЗ та оцінювали якість життя, пов’язане із СНСШ. Через 12 міс загальна оцінка за шкалою IPSS знизилася на 5,5 балів у групі монотерапії і на 5,8 бала в групі комбінованого лікування. Симптоми накопичення зменшилися значно більше при одночасному застосуванні досліджуваних препаратів (1,7 vs 0,8 у групі тамсулозину; р=0,024), причому цей ефект тривав 12 міс. Переносимість лікування була хорошою, за частотою несприятливих подій групи не розрізнялися.
У дослідженні Литвинця і співавт. (2011) у чоловіків із синдромом незапального хронічного тазового болю комплексна терапія Флосіном (0,4 мг 1 р/добу вранці після їди) і Простамолом Уно (1 капсула увечері) забезпечила значне покращення оцінки IPSS, якості життя і загального стану при оцінці на 15-й і 30-й день лікування.
Дослідження ПРОСПЕКТ за участю 2240 пацієнтів із ДГПЗ з усіх регіонів України підтвердило ефективність і безпеку комбінованої терапії Флосіном і Простамолом Уно. Дані, отримані в різних урологічних центрах України, свідчили про повну відповідність результатам досліджень, проведених в інших європейських державах. Це стало доказом того, що оперативне лікування давно втратило статус золотого стандарту для ДГПЗ ІІ-ІІІ стадії, поступившись місцем консервативній терапії.
З урахуванням отримання настільки обнадійливих даних українських урологів порівняльне дослідження ПРОСПЕКТ II було продовжено на 12 міс. Результати засвідчили високу ефективність комплексної терапії Флосіном і Простамолом Уно, що становила 96,9%, з меншою частотою побічних ефектів (5,4%) в порівнянні з відповідним показником для терапії доксазозином і фінастеридом (43,3%).
Метою дослідження ПРОСПЕКТ III було визначити можливості довгострокової терапії комбінацією Флосін / Простамол Уно в аспекті оцінки якості життя, можливості покращення об’єктивних даних урологічного статусу і впливу на сексуальний статус у чоловіків з ДГПЗ ІІ стадії. У підсумку ефективність використання 3-річної комбінованої терапії із застосуванням препаратів Флосін і Простамол Уно дорівнювала 94,1%, у контрольній групі (доксазозин і фінастерид) – 89,3% (р<0,05).
Довгострокова комбінована терапія з використанням препаратів Флосін і Простамол Уно добре переносилася пацієнтами й асоціювалася з низькою частотою розвитку побічних ефектів (5,75% випадків). При комбінуванні препаратів доксазозину і фінастериду побічні явища спостерігалися в 33,1% пацієнтів (р<0,05).
Доведено, що довгострокова комбінована терапія із застосуванням Флосіну і Простамолу Уно є оптимальною для лікування пацієнтів із ДГПЗ II стадії, оскільки забезпечує синергізм ефективності.
Слід зазначити, що оптимальним співвідношенням ефективність/безпека характеризуються не всі лікарські комбінації, які застосовуються в лікуванні ДГПЗ/СНСШ. Зокрема, в дослідженні MTOPS (2003) поєднане призначення фінастериду (блокатор α1-адренорецепторів) і доксазозину (інгібітор 5α-редуктази) в порівнянні з монотерапією одним з них було більш ефективним у зменшенні симптомів, проте асоціювалося з більшою частотою побічних ефектів – периферичних набряків, задишки і ретроградної еякуляції. У дослідженні C. G. Roehrborn і співавт. (2008) на тлі комбінованого прийому тамсулозину і дутастериду була зафіксована підвищена частота розвитку еректильної дисфункції, порушень сім’явиверження, зменшення об’єму еякуляту та гінекомастії.
Таким чином, застосування комбінованої терапії СНСШ дозволяє забезпечити ефект синергізму дії декількох препаратів, що сприяє швидшому уповільненню прогресування хвороби. Комбінація оригінального екстракту Serenoa repens (Простамол Уно) і тамсулозину (Флосін) може розглядатися як оптимальна для лікування ДГПЗ/СНСШ, у тому числі на тлі ХП, оскільки вона добре переноситься, має високу ефективність в усуненні порушень сечовипускання і коморбідних проявів, а також дозволяє покращити якість життя пацієнтів.
Підготував Олексій Терещенко


