17 травня, 2016
Мужское бесплодие
Руководство Европейской ассоциации урологов, 2015 г.
Рекомендации, представленные в настоящем документе, основаны на систематическом обзоре литературы, доступной в Medline, Cochrane Central Register of Controlled Trials и списках литературы, цитированной в научных статьях и обзорах. Использовался контролируемый словарь базы данных Medical Subject Headings (MeSH) по протоколу «свободный текст». Вводили фразу «мужское бесплодие» в сочетании с терминами «диагностика», «эпидемиология», «обследование», «лечение», «нарушение сперматогенеза», «генетические нарушения», «обструкция», «гипогонадизм», «варикоцеле», «крипторхизм», «рак яичка», «инфекции добавочных мужских желез», «идиопатический», «контрацепция», «нарушение эякуляции» и «криоконсервация». Группа экспертов изучила эти материалы и выбрала статьи с наиболее высоким уровнем доказательств в соответствии с адаптированной градацией Оксфордского центра медицинских исследований, основанной на доказательствах (табл. 1). Указывался уровень рекомендаций для обеспечения ясности между надлежащими доказательствами и указанными рекомендациями (табл. 2).
Под бесплодием понимается отсутствие в течение 1 года и более беременности у женщины в сексуально активной паре, не использующей противозачаточные средства (ВОЗ).
Приблизительно 15% сексуально активных пар не достигают беременности в течение 1 года и обращаются за помощью по этому поводу. В конечном счете 5% пар остаются бездетными, несмотря на попытки лечения. У половины (50%) бездетных пар бесплодие связано с «мужским фактором», проявляющимся отклонениями в параметрах эякулята. В ряде случаев женщина с хорошей способностью к зачатию может компенсировать субфертильность мужчины, поэтому обычно бесплодие проявляется при снижении фертильности у обоих партнеров.
Фертильность мужчин может снижаться в результате следующих факторов:
• врожденные или приобретенные аномалии мочеполовых органов;
• инфекции мочеполовой системы;
• повышение температуры в мошонке (например, вследствие варикоцеле);
• эндокринные нарушения;
• генетические отклонения;
• иммунологические факторы.
По меньшей мере в 30-40% причинный фактор мужского бесплодия не выявляется (идиопатическое бесплодие). У этих пациентов в анамнезе нет проблем с фертильностью, изменений при физикальном осмотре и в лабораторных данных гормональных исследований. При этом в анализе эякулята выявляется снижение числа сперматозоидов (олигозооспермия), снижение подвижности сперматозоидов (астенозооспермия) и большое число сперматозоидов с измененной формой (тератозооспермия). Эти изменения в спермограмме часто наблюдаются одновременно и обозначаются как олигоастенотератозооспермия (ОАТ-синдром). В таблице 3 суммированы основные факторы, ассоциированные с мужским бесплодием. Идиопатическое мужское бесплодие обычно связано с гормональными нарушениями, возникающими вследствие загрязнения окружающей среды, процессом накопления свободных радикалов кислорода, генетическими отклонениями.
Прогностические факторы мужского бесплодия:
• длительность бесплодия;
• первичное или вторичное бесплодие;
• данные спермограммы;
• возраст и фертильность партнерши.
В бесплодных парах с длительностью наблюдения 2 года и с олигозооспермией в качестве первичной причины бесплодия кумулятивный уровень беременностей составляет 27%. Во многих западных странах женщины откладывают первую беременность, мотивируя это необходимостью завершения образования, затем началом профессиональной карьеры. Возраст женщины – наиболее важный прогностический фактор, независимо влияющий на эффективность вспомогательных репродуктивных технологий. У женщин в возрасте 35, 38 и >40 лет по сравнению с 25-летними потенциал к зачатию снижается до 50, 25 и <5% соответственно.
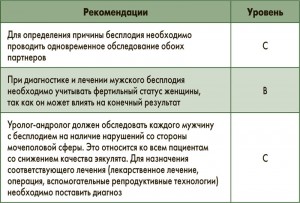
При наличии в анализе эякулята отклонений от нормы показано обследование у андролога (табл. 4).
Определение лечебной тактики напрямую зависит от результатов спермограммы при основном условии стандартизации работы лабораторий, занимающихся лабораторным исследованием. Показатели анализа эякулята стандартизируются ВОЗ и распространяются в публикациях ВОЗ по лабораторному исследованию эякулята человека, взаимодействию сперматозоидов и слизистой шейки матки. Достигнут консенсус о том, что современная сперматология должна следовать последним рекомендациям без каких-либо исключений.
Если в соответствии с критериями ВОЗ показатели эякулята находятся в пределах нормативных показателей, то достаточно выполнения 1 теста. Если имеются отклонения от нормы по крайней мере 2 показателей, то это является показанием к обследованию у андролога. Важно различать следующие понятия для описания отклонений от нормативных показателей эякулята:
• олигозооспермия: <15 млн сперматозоидов в 1 мл;
• астенозооспермия: <32% подвижных сперматозоидов;
• тератозооспермия: <4% сперматозоидов нормальной формы.
Довольно часто все 3 параметра встречаются вместе (ОАТ-синдром). В случаях выраженного ОАТ-синдрома (<1 млн сперматозоидов/мл), как при азооспермии, отмечается высокая встречаемость обструкции семенных путей (1-, 2-сторонней), а также генетических аномалий.
Тестикулярная недостаточность
(сперматогенные нарушения)
Тестикулярная недостаточность и, как следствие, сперматогенные нарушения вызываются любыми причинами, за исключением заболеваний гипоталамо-гипофизарной системы и обструкции мужских половых путей. Это наиболее частая форма снижения мужской фертильности. Тестикулярная недостаточность имеет различную этиологию, но проявляется клинически как тяжелая OAT или необструктивная азооспермия (НОА).
Причины тестикулярной недостаточности представлены в таблице 5.
К типичным находкам при сборе анамнеза и физикальном осмотре пациентов с тестикулярной недостаточностью относятся:
• крипторхизм;
• перекрут яичка;
• мочеполовые инфекции;
• травма яичка;
• действие токсинов окружающей среды;
• действие гонадотоксичных лекарственных препаратов;
• действие облучения или химических веществ;
• рак яичка;
• отсутствие яичек;
• нарушения вторичных половых признаков;
• гинекомастия;
• объем и консистенция яичек, отличающиеся от нормы;
• варикоцеле.
Стандартное обследование включает анализ эякулята и определение уровня гормонов. Другие исследования могут потребоваться в зависимости от конкретной ситуации.
Обычно у мужчин с тестикулярной недостаточностью присутствует гипергонадтропный гипогонадизм (высокий уровень фолликулостимулирующего (ФСГ) и лютеинизирующего (ЛГ) гормонов, иногда в сочетании с низким уровнем тестостерона). Уровень ФСГ коррелирует с числом сперматогоний:
• при отсутствии сперматогоний или при значительном снижении их числа уровень ФСГ обычно повышен;
• при нормальном числе сперматогоний, но при полной блокаде сперматоцитов или сперматид уровень ФСГ находится в пределах нормальных значений.
В определенных случаях по уровню ФСГ не точно прогнозируется состояние сперматогенеза. Последние данные показывают сильную корреляцию между низким уровнем ингибина В и поражением сперматогенной ткани.
Биопсия может быть частью лечебного плана ИКСИ (интрацитоплазматической инъекции сперматозоида) у больных с клиническими признаками НОА. Сперматогенез может быть фокальным. Примерно у 50-60% мужчин обнаруживаются сперматозоиды, которые могут быть использованы при ИКСИ.
Большинство авторов рекомендуют брать образцы из нескольких участков яичка. Отмечается хорошая корреляция между морфологическими находками при диагностической биопсии яичка и вероятностью обнаружения зрелых сперматозоидов во время исследования эякулята и ИКСИ.
Не обнаружено четкой взаимосвязи между успешным забором сперматозоидов и уровнями ФСГ, ингибина В или объемом яичка. В случае полной AZFa- и AZFb-микроделеции вероятность выделения сперматозоидов практически равна нулю. Аспирация сперматозоидов из яичка (TESA) – метод выбора, показывающий превосходную воспроизводимость. Микрохирургическое извлечение сперматозоидов может увеличить вероятность получения сперматозоидов, хотя сравнительные исследования на данный момент отсутствуют. После выделения яичка жидкость из канальца большого диаметра аспирируется под контролем операционного микроскопа. Частота осложнений в этом случае ниже, чем при классической TESE (выделение сперматозоидов из ткани яичка). О положительном результате применения microTESE сообщают даже при такой патологии, как синдром клеток Сертоли.
Результаты ИКСИ хуже при использовании сперматозоидов, полученных от мужчин с НОА, по сравнению со сперматозоидами, полученными из эякулята и от мужчин с обструктивной азооспермией (ОА):
• рождаемость ниже при НОА, чем при ОА (19 против 28%);
• уровень фертильности и имплантации значительно ниже;
• частота выкидышей выше при НОА, чем при ОА (11,5 против 2,5%).
При ОА нет статистически значимой разницы в результатах ИКСИ при использовании сперматозоидов из ткани яичка или его придатка. Также не получено достоверных различий в результатах ИКСИ при использовании свежего или размороженного после криоконсервации эякулята.
Генетические нарушения при бесплодии
Урологи, практикующие в сфере репродуктивной андрологии, должны владеть знаниями о генетических основах мужской инфертильности на уровне, достаточном для формирования обоснованных рекомендаций бесплодным парам, желающим иметь детей и обратившимся по этому поводу. Мужчинам со сниженным числом сперматозоидов должен быть предоставлен обоснованный шанс отцовства с помощью экстракорпорального оплодотворения (ЭКО), внутрицитоплазматической инъекции сперматозоида и получения сперматозоидов из придатка яичка или ткани яичка в случае азооспермии. У бесплодных мужчин в сперматозоидах чаще обнаруживаются анеуплоидия, другие генетические изменения и повреждение ДНК, что определяет возможность передачи генетических изменений потомству. Хотя сегодня существуют перспективы для скрининга сперматозоидов, обычная клиническая практика основана на скрининге образцов периферической крови.
Хромосомные аберрации
Хромосомные нарушения могут быть связаны как с нарушением числа (например, трисомия), так и структуры хромосом (например, инверсии или транслокации). В обзоре объединенных данных 11 публикаций результатов исследований, включивших 9766 бесплодных мужчин, частота хромосомных аномалий составила 5,8%. Изменения в Y-хромосоме встречались у 4,2%, а отклонения в аутосомных хромосомах – у 1,5% бесплодных мужчин. Для сравнения: уровень отклонений, по данным 3 крупных исследований, среди 94 465 новорожденных младенцев мужского пола составил 0,38%, из которых у 131 (0,14%) были изменения в половых хромосомах и у 232 – аберрации в аутосомных хромосомах (0,25%).
Чем тяжелее тестикулярная недостаточность, тем выше встречаемость хромосомных аберраций. У пациентов с концентрацией сперматозоидов <10×106/мл в 10 раз чаще (4%) по сравнению с общей популяцией встречаются нарушения аутосомных хромосом преимущественно структурного характера. Наибольший риск выявления хромосомных аберраций отмечается у мужчин с азооспермией. На основании частоты встречаемости хромосомных аберраций у пациентов с различной концентрацией сперматозоидов кариотипирование рекомендуется проводить мужчинам с азооспермией и с олигозооспермией при концентрации сперматозоидов <10×106/мл. При наличии в семейном анамнезе рецидивирующих абортов, задержки умственного развития рекомендовано проведение анализа кариотипа независимо от концентрации сперматозоидов.
Нарушения в половых хромосомах
(синдром Клайнфельтера и его варианты –
47, XXY; 46, XY/47, XXY мозаицизм)
Синдром Клайнфельтера – наиболее распространенная частая патология половых хромосом. У взрослых мужчин с синдромом Клайнфельтера при осмотре выявляются маленькие плотные яички, в которых отсутствуют герминогенные клетки. Фенотип может варьировать от мужчин с нормальной вирилизацией до наличия одного из проявлений андрогенного дефицита: оволосения по женскому типу, недостатка волос на теле, длинных рук и ног из-за позднего окостенения эпифизов трубчатых костей. Функция клеток Лейдига при синдроме Клайнфельтера также зачастую нарушена. Уровень тестостерона нормальный или низкий, уровень эстрадиола нормальный или повышен, уровень ФСГ повышен. Либидо часто нормальное, несмотря на сниженный уровень тестостерона, но с возрастом может понадобиться андрогензаместительная терапия. Наличие герминогенных клеток и продукция сперматозоидов у больных с мозаицизмом при синдроме Клайнфельтера варьирует – 46 XY/47 XXY. Описано 1 клиническое наблюдение мужчины с синдромом Клайнфельтера со сниженным сперматогенезом, которому была рекомендована хирургическая экстракция сперматозоидов. Клинические исследования на основании FISH-анализа сперматозоидов показали, что чем выше частота хромосомных нарушений и встречаемость анеуплоидии в аутосомных хромосомах (дисомия 13, 18 и 21 хромосом), тем более серьезной является проблема хромосомной патологии плода, зачатого с использованием ИКСИ. Образование сперматозоидов 24XY встречается у 0,9-7% мужчин с мозаицизмом при синдроме Клайнфельтера и у 1,36-25% мужчин с соматическим кариотипом 47XXY. К настоящему времени сообщается о рождении 49 здоровых детей и 1 ребенка с кариотипом 47XXY при использовании ИКСИ без предимплантационной генетической диагностики (ПГД, PGD). Однако исследования, основанные на ИКСИ в сочетании с ПГД у 113 эмбрионов, показали, что по сравнению с контролем имеется значительное снижение частоты получения нормальных эмбрионов от пар с синдромом Клайнфельтера (54 против 77,2%). Из-за серьезного учащения нарушений в половых и аутосомных хромосомах эмбрионов у пациентов с синдромом Клайнфельтера строго рекомендуется ПГД или амниоцентез для исследования кариотипа. Мужчины с синдромом Клайнфельтера требуют длительного наблюдения. При снижении уровня тестостерона до гипоандрогенного уровня, необходимо проведение андрогензаместительной терапии.
Все мужчины с синдромом Клайнфельтера, которым была выполнена биопсия яичка с целью выделения сперматозоидов, в последующем нуждаются в длительном наблюдении за эндокринным статусом.
Нарушения в аутосомных хромосомах
Консультация генетика должна быть предложена парам, обратившимся для лечения бесплодия (включая методы ЭКО), в случаях, когда известно, что у мужчины имеются генетические нарушения аутосомных хромосом, подтвержденные исследованием кариотипа.
Хромосомные аберрации сперматозоидов
Флуоресцентная гибридизация in situ (FISH – fluorescence in situ hybridization) с помощью нескольких красителей позволяет определить состояние хромосомного аппарата сперматозоидов. Анеуплоидия в сперматозоидах, особенно в половых хромосомах, ассоциирована с тяжелыми нарушениями сперматогенеза, также она наблюдается при наличии транслокаций. В основном FISH-анализ сперматозоидов относится к области научных исследований, его следует применять для оценки состояния сперматозоидов у мужчин с определенными андрологическими заболеваниями. Данные методы необходимы для отделения популяции сперматозоидов с генетическими отклонениями от нормальных сперматозоидов либо для безошибочного исследования и отбора отдельных сперматозоидов для выполнения ЭКО/ИКСИ.
Генетические дефекты
У мужчины есть только 1 Х-хромосома. При Х-сцепленном типе наследования мутация клинически проявляется у мужчин, но в дальнейшем передается только дочерям.
Синдром Каллмана – наиболее частая патология, ассоциируемая с мужским бесплодием и имеющая Х-сцепленный рецессивный тип наследования. У пациентов с синдромом Каллмана выявлена делеция гена KALIG‑1, который локализуется на хромосоме Хр22.3. Различные нововыявленные генные аутосомные мутации также могут привести к развитию синдрома Каллмана. Для пациентов с данным синдромом характерны гипогонадотропный гипогонадизм и аносмия, кроме этого могут иметь место и другие клинические проявления: лицевая асимметрия, волчья пасть, монохромазия, глухота, крипторхизм и аномалии развития надпочечников. Можно относительно легко индуцировать сперматогенез с помощью гормонального лечения.
До начала лечения рекомендуется генетический скрининг. Лечение гонадотропинами в подавляющем большинстве случаев может привести к естественному зачатию (даже при относительно низком количестве сперматозоидов в эякуляте), следовательно, выявление пораженного гена (сцепленного с Х-хромосомой аутосомно-доминантного или аутосомно-рецессивного типа) может обеспечить более точное генетическое консультирование, например позволит определить риск передачи генетических нарушений потомству.
Легкая форма синдрома нечувствительности к андрогенам (ЛСНА). Ген рецептора андрогенов (РА) располагается на длинном плече Х-хромосомы. Мутации этого гена могут привести к различным формам синдрома нечувствительности к андрогенам (СНА) – от легкой до полной. Фенотипическими признаками полной формы синдрома нечувствительности к андрогенам (ПСНА) являются наличие женских наружных половых органов и отсутствие волос на лобке (синдром Морриса). Неполная форма СНА имеет различные фенотипические проявления – от преимущественно женского фенотипа, наружных половых органов промежуточного типа до преимущественно мужского фенотипа с микропенисом, промежностной гипоспадией и крипторхизмом. Последний вариант фенотипа носит название синдрома Рейфенштейна.
При вышеприведенных тяжелых формах нечувствительности к андрогенам отсутствует риск передачи генетических нарушений в связи с тем, что такие мужчины не могут иметь биологических детей. У пациентов с ЛСНА мужское бесплодие – первичное и иногда единственное клиническое проявление. Дефекты гена РА, вызывающие бесплодие при отсутствии каких-либо других клинических проявлений, – редкая форма болезни. Описано только несколько подобных мутаций у бесплодных мужчин.
Другие аберрации Х-хромосомы. На Х-хромосоме, особенно на премейотических генах, по сравнению с аутосомными хромосомами было выявлено неожиданно большое количество генов со специфическим для яичек или с обогащенным типом экспрессии, которые были гиперэкспрессированы на Х-хромосоме. К настоящему времени в малых популяционных исследованиях проведен скрининг только по 2 новым генам – USP26 и TAF7L. Связи какого-либо из них с мужским бесплодием выявлено не было.
Y-хромосома и мужское бесплодие
Впервые связь между азооспермией и делецией длинного плеча Y-хромосомы, обнаруженной микроскопически, была установлена Tiepolo и Zuffardi в 1976 г. Сообщения о микроделециях в Y-хромосоме и мужском бесплодии были опубликованы в 1992 г., в дальнейшем был описан еще ряд подобных случаев. Микроделеции были обнаружены в 3 несовпадающих участках Y-хромосомы: AZFa-b-c. Всего через несколько лет после открытия 3 субрегионов AZF, после точного распознавания Y-структуры в Yq11, стало очевидным, что субрегионы AZFb и AZFc накладываются друг на друга, а субрегион AZFd не существует. Делеции, проявляющиеся клинически, захватывают частично или в подавляющем большинстве случаев полностью 1 или более субрегион AZF. Именно они, как правило, представляют собой молекулярно-генетическую основу тяжелой олигозооспермии и азооспермии. В каждом регионе (a, b, c) выявлены разные кандидатные гены, однако их роль в сперматогенезе по большей части остается неизвестной. Так как делеции возникают в нескольких генах, а не в 1, роль гена AZF не может быть достоверно экстраполирована на основании фенотипа AZF-делеции. Поэтому остается неясным, все ли эти гены вовлечены в контроль за сперматогенезом. Геноспецифические делеции, при которых выпадает только 1 ген, обнаруживались только в субрегионе AZFa. Эти исследования позволяют предположить, что ген USP9Y не является необходимым для сперматогенеза и что он, скорее всего, «тонкий настройщик» выработки сперматозоидов. В субрегионе AZFc был описан новый тип Yq-делеций, ему было дано название «gr/gr-делеция». При этой делеции выпадает половина субрегиона AZFc, что приводит к изменению процента мультикопий генов, расположенных внутри этого субрегиона (таких как DAZ, CDY1, BPY2).
Клиническая значимость Yq-делеций долгое время обсуждалась в основном из-за больших различий в их встречаемости по данным различных авторов, а также из-за наличия этих делеций у фертильных мужчин. Сейчас после более 10 лет клинических исследований можно заключить, что:
• делеции Y-хромосомы не встречаются у мужчин с нормоспермией, поэтому очевидным является ее негативное влияние на сперматогенез;
• делеции Y-хромосомы наиболее часто встречаются у мужчин с азооспермией (8-12%), затем далее – у мужчин с олигозооспермией (7%);
• делеции крайне редко обнаруживаются у мужчин с концентрацией сперматозоидов >5 млн/мл (около 0,7%);
• делеции наиболее часто возникают в субрегионе AZFc (приблизительно 65-70%), затем далее – в субрегионах AZFb и AZFb+c или AZFa+b+c (25-30%), в то время как делеции в субрегионе AZFa встречаются значительно реже (5%);
• полная делеция субрегионов AZFa и AZFb связана с тяжелым тестикулярным фенотипом, синдромом клеток Сертоли и сперматогенным блоком соответственно. Полная делеция субрегиона AZFc приводит к различному фенотипу, от азооспермии до олигозооспермии;
• классическая делеция AZF не связана с повышенным риском крипторхизма или рака яичка.
Специфичность и вышеприведенные генотипические/фенотипические корреляции дают основания для проведения анализа делеций Y-хромосомы в диагностических и прогностических целях при выделении сперматозоидов из яичек.
Благодаря клиническим рекомендациям Европейской ассоциации андрологов (ЕАА) и программе внешнего контроля за качеством , тестирование Y-хромосомы становится более гомогенным и доступным в различных генетических лабораториях. Показания для скрининга AZF-делеций основываются на количестве сперматозоидов и включают в себя азооспермию и тяжелую олигозооспермию (<5млн сперматозоидов/мл эякулята). Клинические рекомендации ЕАА устанавливают праймеры, которые способны выявить >95% клинически значимых делеций.
Некоторые унаследованные мутации связаны с тяжелыми или множественными генерализованными нарушениями в состоянии здоровья, которые сочетаются с бесплодием. Такие пациенты находятся под наблюдением врачей с раннего возраста. Даже при больших возможностях лечения целесообразность последнего должна рассматриваться в контексте заботы о человеке в целом и способностью пары в последующем заботиться о ребенке надлежащим образом.
Мутации при муковисцидозе и мужское бесплодие
Основной причиной муковисцидоза служат мутации гена белка CFTR (cystic fibrosis transmembrane regulator) – трансмембранного регулятора муковисцидоза. Муковисцидоз – одно из наиболее частых в европейской популяции наследственных заболеваний с аутосомно-рецессивным типом передачи; 4% больных муковисцидозом являются носителями мутации гена – CFTR. Этот ген локализуется на коротком плече 17 хромосомы. Он кодирует мембранный белок, который функционирует как ионный канал, одновременно оказывая влияние на формирование семявыбрасывающих протоков, семенных пузырьков, семявыносящих протоков и дистальных 2/3 придатков яичек. С мутацией гена CFTR ассоциировано врожденное двустороннее отсутствие семявыносящего протока (ВДОСП, CBAVD – сongenital bilateral absence of the vas deferens). ВДОСП обнаружено у 2% мужчин с ОА, наблюдающихся в клинике Эдинбурга. В различных странах доля таких мужчин среди больных с ОА варьирует. У каждого 2-го пациента с ВДОСП отмечаются заболевания верхних дыхательных путей. Клинически отсутствие семявыносящих протоков часто не выявляется, поэтому для исключения ВДОСП всех пациентов с азооспермией следует очень тщательно обследовать, особенно мужчин с объемом спермы <1,5 мл и pН <7. Опубликовано большое количество работ с результатами исследований мужчин с ВДОСП на наличие различного рода мутаций. Результаты исследований говорят о том, что чем больше объем и число определений (тестов), тем выше процент мужчин, у которых эти мутации обнаруживаются. Среди 449 мужчин с ВДОСП мутация Delta F508 была обнаружена у 244, мутация R117H у 54, а мутация W1282X – у 37 мужчин; 63 другие мутации были найдены у 19 мужчин, даже при неполном объеме генетических исследований. Поскольку найденных и изученных мутаций у этих больных больше числа определений, следует предполагать, что у всех мужчин с ВДОСП высока вероятность обнаружения тех или иных мутаций. Проводить анализ на все возможные мутации не целесообразно, так как большинство из них в этой специфической популяции мужчин встречается крайне редко. Мутации могут быть найдены в обеих копиях гена CFTR, однако у большинства мужчин с ВДОСП мутация обнаруживается только в 1 аллеле. У некоторых из этих, предположительно гетерозиготных, случаев носительства, может присутствовать неизвестная 2-я мутация. Наличие другого механизма наследования подтверждается тем, что у 2/3 мужчин с ВДОСП также обнаруживается отличающаяся последовательность ДНК (5-я аллель) в некодирующей области гена CFTR. Наличие аллеля 5Т признается скорее «мягкой» мутацией, чем полиморфизмом. У каждого пациента с ВДОСП небходимо проводить анализ гена CFTR. Мужчины с ВДОСП часто имеют умеренной степени выраженности клинические проявления муковисцидоза (например, наличие в анамнезе частых легочных инфекций). Следует проводить наблюдение за детьми, являющимися гомозиготными или гетерозиготными носителями по наличию мутации в гене CFTR, родившимися после ИКСИ, в тех случаях, когда у отца имеется ВДОСП.
В случае выявления у мужчины ВДОСП важно проверить его и его партнершу на наличие мутаций муковисцидоза. Если женщина будет являться носителем мутации гена CFTR, пара должна очень тщательно взвесить необходимость использования спермы мужа для ИКСИ, поскольку шанс рождения ребенка с муковисцидозом составит 25%, если ребенок будет гетерозиготным и 50% – если гомозиготным носителем. Если у партнерши искомые мутации не выявлены, шанс наличия у нее неизвестной ранее мутации составляет приблизительно 0,4%.
Одно- или двустороннее отсутствие или патология семявыносящего протока и аномалии почек
Односторонняя аплазия семявыносящего протока обычно сочетается с отсутствием ипсилатеральной почки, что, вероятно, являет собой пример сцепленного наследования. При односторонней аплазии семявыносящего протока мужчины, как правило, остаются фертильными. Чаще всего данное состояние диагностируется как случайная находка во время вазэктомии. У мужчин с односторонним отсутствием семявыносящего протока и мутациями муковисцидоза могут встречаться те же генетические болезни, что и у мужчин с истинным ВДОСП. Тем не менее следует помнить, что у мужчин с двусторонним отсутствием семявыносящего протока и аномалиями развития почек дефектов в гене CFTR не обнаруживается. Мутации гена CFTR являются наиболее частой причиной мужского бесплодия, связанного с врожденным дву- или односторонним нарушением проходимости или отсутствием семявыносящих протоков. Мужчины, у которых выявлено одностороннее отсутствие семявыносящего протока и нормальные почки, или же двустороннее отсутствие, или двусторонние нарушения со стороны семявыносящих протоков, должны быть протестированы на наличие мутаций муковисцидоза. Если результаты отрицательные, а состояние почек ранее не было определено, показано выполнение ультразвукового исследования (УЗИ). Диагностические находки могут варьировать от сочетания одностороннего отсутствия ипсилатеральной почки и семявыносящего протока до двусторонней аномалии со стороны семявыносящих протоков и почек. Данные примеры показывают, что ВДОСП является генетически гетерогенным заболеванием.
Неизвестные генетические нарушения
Принимая во внимание, что большое количество предполагаемых генов вовлечено в сперматогенез, можно предположить, что мутации или полиморфизм генов-кандидатов, регулирующих сперматогенез, лежат в основе большинства идиопатических форм нарушения сперматогенеза. Тем не менее, несмотря на интенсивные поиски новых генетических факторов, никаких клинически значимых мутаций/полиморфизма генов (кроме тех, которые связаны с Y-хромосомой) до сих пор выявлено не было. Внедрение новых аналитических методов, вероятно, приведет к существенному продвижению в этой области. В случаях недостаточного числа сперматозоидов использование метода ИКСИ позволяет мужчинам с тяжелыми нарушениями сперматогенеза иметь детей в тех ситуациях, которые прежде рассматривались как безнадежные. Это привело к озабоченности тем, что дети, которые появились на свет благодаря ИКСИ, могут рождаться с врожденными аномалиями, так как при данном методе дефектные сперматозоиды могут обойти защитные барьеры женского полового тракта и яйцеклетки. При этом, если ранее яйцеклетка не могла быть оплодотворена, то ИКСИ дает ей такую возможность. Кроме того, статистика врожденных аномалий, предоставленная центрами, применяющими технологию ИКСИ, не демонстрирует какого-либо превышения частоты встречаемости врожденных пороков по сравнению с общей популяцией.
Тем не менее дети, рожденные с использованием ИКСИ, имеют повышенный риск развития хромосомных аберраций de novo (почти в 3 раза выше, чем при естественном зачатии) и врожденных структурных аномалий, переданных от отца. Показания к ИКСИ постоянно расширяются, включая оплодотворение с использованием незрелых форм сперматозоидов. Это подчеркивает важность дальнейшего мониторинга частоты встречаемости аномалий развития плода путем детального анализа генов разных подгрупп, соответствующих клиническому и молекулярному диагнозу отца.
Фрагментация ДНК сперматозоидов
Частота повреждения ДНК в генах сперматозоидов мужчин с олигозооспермией повышена. Это снижает возможность оплодотворения естественным путем и, в меньшей степени, оплодотворяющую способность сперматозоидов при применении таких методов, как ИКСИ. В этих случаях (фрагментация ДНК, повреждение ДНК) отмечается более высокая частота ранних выкидышей. Частота ранних выкидышей может уменьшаться после перевязки варикозно расширенных вен семенного канатика.
Генетическое консультирование и ИКСИ
Бесплодие – это проблема пары, и лучше ее решать совместно, усилиями обоих партнеров. Лучший вариант лечения тот, с которым согласились оба партнера после полного обсуждения деталей генетического риска. Исходно паре необходимо дать полную информацию о рисках для ребенка и помочь им решить вопрос о применении ИКСИ или об отказе от него. В случае конфликта пожеланий пары и интересов будущего ребенка отказ пары от применения ИКСИ может быть этически оправданным. Когда оба партнера являются носителями генетических дефектов (например, мутации гена, вызывающего муковисцидоз), вероятность того, что у ребенка разовьется клиническое проявление патологии и наступит смерть в раннем возрасте после нескольких лет болезни, может достигать 50%. Тем не менее ряд клиницистов и персонал клиник, занимающихся лечением бесплодия, признают неэтичной ситуацию, когда интересы общества, связанные с обязанностями по отношению к будущему ребенка, перевешивают пожелания конкретной пары. Если противоречия подобного рода разрешаются консенсусом, то интересы будущего ребенка, по всей видимости, должны иметь приоритет над интересами пары. Пара также должна рассмотреть возможность предимплантационной диагностики возможной патологии с целью наступления беременности изначально здоровым плодом.
Обструктивная азооспермия
Обструктивная азооспермия – отсутствие сперматозоидов и герминогенных клеток в эякуляте и постэякуляторной моче в связи с двусторонней обструкцией семявыносящих протоков. ОА встречается реже, чем НОА и наблюдается у 15-20% мужчин с азооспермией.
Интратестикулярная обструкция составляет 15% всех ОА. Чаще встречаются приобретенные (например, поствоспалительные или посттравматические обструкции), нежели врожденные формы (например, нарушение соединения сети яичка (rete testis) и выносящих протоков). Приобретенные формы более характерны для нарушений проходимости на уровне придатков яичек и семявыносящих протоков.
Обструкция на уровне придатка яичка
Чаще всего ОА обусловлена обструкцией на уровне придатка яичка и наблюдается у 30-67% мужчин с азооспермией и снижением уровня ФСГ в 2 раза по сравнению с нормой. Врожденная обструкция на уровне придатка яичка чаще всего манифестирует как ВДОСП, которое в 82% случаях ассоциировано как минимум с одной мутацией гена муковисцидоза. ВДОСП часто сочетается с отсутствием дистальной части придатка яичка и агенезией семенных пузырьков.
Приобретенные формы ОА носят вторичный характер и являются следствием острых (например, гонококкового) или субклинических форм (например, хламидиозного) эпидидимита, наблюдаются чаще, чем врожденные.
Обструкция на уровне семявыносящих протоков является наиболее частой причиной приобретенной ОА после вазэктомии с целью хирургической контрацепции и возможным последующим повреждением герминогенных клеток и фиброзом. Приблизительно 2-6% мужчин после хирургической контрацепции обращаются за восстановлением проходимости семявыносящих протоков. У пациентов, которым ранее выполнялась вазовазостомия, в 5-10% случаев развивается обструкция на уровне придатков яичек в результате разрыва канальцев, что обязательно требует выполнения эпидидимовазостомии. Обструкция семявыносящего протока также может являться осложнением операций по поводу паховых грыж. Полипропиленовая сетка, применяемая при герниопластике, может вызывать фибропластический ответ в окружающих тканях с вовлечением или полной облитерацией семявыносящих протоков.
Наиболее частая врожденная причина обструкции семявыносящих протоков – ВДОСП – часто сопровождается муковисцидозом. Односторонняя агенезия или частичный дефект семявыносящего протока ассоциируется с аномалиями контралатерального протока или агенезией почек в 80 и 26% случаев соответственно. Обструкции на уровне дистальной части семявыносящего протока включают ВДОСП и случайное повреждение семявыносящего протока при выполнении герниопластики.
Обструкция на уровне семявыбрасывающего протока наблюдается приблизительно у 1-3% мужчин с ОА. Эти обструкции могут быть следствием воспаления или сдавления кистами. Обструкции из-за кист обычно носят врожденный характер (например, киста мюллерова протока или киста мочеполового синуса/семявыбрасывающего протока) и локализуются в медиальной части простаты между семявыбрасывающими протоками. В мочеполовом синусе измененные один или оба семявыбрасывающих протока опорожняются в кисту, тогда как при аномалиях мюллерова протока семявыбрасывающие протоки смещены латерально и сдавлены кистой.
Парамедианные или латеральные внутрипростатические кисты – кисты вольфовых протоков – редкая патология в клинической практике. Поствоспалительные обструкции семявыбрасывающего протока носят вторичный характер и являются следствием острого, подострого или хронического уретропростатита.
Врожденные или приобретенные полные обструкции семявыбрасывающих протоков зачастую сопровождаются небольшим объемом эякулята, уменьшением уровня или отсутствием семенной фруктозы и кислым pH семенной плазмы. Семенные пузырьки обычно расширены (переднезадний диаметр >15 мм).
Функциональная обструкция дистальной
части семявыносящих протоков
Группа Европейской ассоциации урологов (ЕAU), занимающаяся разработкой Клинических рекомендаций по лечению мужского бесплодия, подготовила этот документ в помощь медицинским работникам, основываясь на данных доказательной медицины. Чаще всего урологи первыми обследуют мужчин при подозрении на наличие бесплодия. Мужское бесплодие может быть многофакторной проблемой, требующей привлечения специалистов смежных областей.
Функциональная обструкция дистальной части семявыносящих протоков может быть связана с локальной нейропатией. Это патологическое состояние часто ассоциируется с уродинамическими расстройствами, так как наблюдаются ампуловезикальная атония или повышение давления в семявыбрасывающем протоке, подтверждаемое данными вазографии. Функциональные нарушения проходимости в дистальной части семявыносящих протоков отмечаются при ювенильном сахарном диабете и поликистозной болезни почек; однако в большинстве случаев какой-либо общей патологии обнаружить не удается. Результаты анализа эякулята варьируют между азооспермией, криптозооспермией и тяжелой формой OAT-синдрома.
Обследование
Сбор анамнеза проводится по тем же пунктам, что и при мужском бесплодии в целом. Необходимо целенаправленно выяснить наличие или отсутствие:
• гемоспермии;
• болей после эякуляции;
• предшествующего или текущего уретрита или простатита;
• ирритативных симптомов и симптомов обструкции мочевых путей;
• предшествующего увеличения мошонки, болей или операций на ней;
• предшествующей грыжи или травм;
• хронических синопульмональных инфекций.
Клинический осмотр необходимо проводить по тем же принципам, как и при мужском бесплодии. На ОА указывают следующие признаки:
• объем по крайней мере 1 яичка >15 мл (хотя при ОА в сочетании с частичной тестикулярной недостаточностью могут обнаруживаться и меньшие по объему яички);
• увеличенный и уплотненный придаток яичка;
• узелки в придатке яичка или в семявыносящих протоках;
• отсутствие или частичная атрезия семявыносящего протока;
• признаки уретрита;
• изменения в предстательной железе.
В соответствии с рекомендациями ВОЗ необходимо проведение по крайней мере 2 анализов эякулята с интервалом в 2-3 мес. Азооспермия подразумевает отсутствие сперматозоидов после центрифугирования при 400-кратном оптическом увеличении. Требуется тщательное повторное исследование мазков после повышения концентрации эякулята. Отсутствие сперматозоидов и незрелых герминогенных клеток в эякуляте позволяет предполагать наличие обструкции на уровне проксимальной или дистальной части семявыносящего протока.
Уровень ФСГ в сыворотке крови может быть нормальным, что не исключает тестикулярную природу азооспермии (например, нарушение сперматогенеза). У 40% мужчин с первичными нарушениями сперматогенеза уровень ФСГ находится в пределах нормы. Уровень ингибина В имеет более высокую прогностическую ценность в отношении состояния сперматогенеза.
УЗИ мошонки обязательно и помогает выявить признаки обструкции (например, расширение сети яичка, увеличение придатка яичка с кистозными изменениями или отсутствие семявыносящего протока) и исключить признаки дисгенезии яичка (например, негомогенность гистоархитектоники яичка и наличие микрокальцинатов). Для пациентов с маленьким объемом эякулята и подозрением на дистальную (высокую) обструкцию показано проведение трансуретрального ультразвукового исследования (ТРУЗИ). Инвазивное обследование, включая биопсию яичка, ревизию мошонки и дистальных отделов семявыносящего протока, показано для всех пациентов с ОА, у которых имеется подозрение на приобретенную обструкцию семенных путей. Эксплоративный этап и восстановительные реканализационные операции желательно выполнять одномоментно.
В ряде случаев для исключения нарушений сперматогенеза показано выполнение биопсии яичка. Биопсию яичка следует комбинировать с экстракцией тестикулярных сперматозоидов (например, TESE) с целью их криоконсервации и последующего применения при ИКСИ в случаях, когда невозможно выполнить хирургическую реканализацию или ее результаты оказались неэффективными.
Продолжение в следующем номере.