7 квітня, 2017
Маастрихт V: що нового у веденні інфекції Helicobacter pylori?

Міжнародний оглядовий курс із внутрішньої медицини (MIRCIM) – початковий семінар для лікарів, який проводить у Польщі медичний факультет Університету Макмастера (Канада), що є колискою сучасної доказової медицини. На MIRCIM-2016 провідний європейський фахівець з Helicobacter pylori (H. pylori), професор Петер Мальфертайнер (Університет Отто фон Геріке, м. Магдебург, Німеччина) прочитав лекцію, присвячену ключовим моментам нового керівництва з ведення інфекції H. pylori – Маастрихту V. Зазначимо, що саме професор Мальфертайнер є першим автором цього фундаментального документа, нещодавно надрукованого в журналі Gut (Malfertheiner P. et al. Management of Helicobacter pylori infection — the Maastricht V/Florence Consensus Report. Gut 2016 Oct 5).
Сьогодні відомо, що H. pylori, колонізуючи шлунок, викликає гастрит у всіх людей. Залежно від факторів вірулентності, сприйнятливості макроорганізму і способу життя ця інфекція може мати різні наслідки – від безсимптомного перебігу (80% випадків) до розвитку злоякісних новоутворень.
П’ятий Маастрихтський консенсус (Маастрихт V / Флоренція 2015) містить важливі зміни у підходах до ведення цієї інфекції.
Кіотський глобальний консенсус із хелікобактерного гастриту (Sugano et al., 2015) визначає H. pylori-гастрит як інфекційне захворювання і специфічний тип диспепсії. У Маастрихті V також зазначається, що H. pylori-гастрит є інфекційним захворюванням незалежно від симптомів і ускладнень (рівень доказів ІВ, сильна рекомендація). Під час обговорення цього положення з ним погодилися 85% експертів.
Також H. pylori-гастрит є окремим захворюванням і в деяких пацієнтів викликає симптоми диспепсії. Ерадикація H. pylori забезпечує довготривале полегшення диспепсії майже у 10% пацієнтів (рівень доказів ІА, сильна рекомендація). Механізми, що призводять до гастриту й диспепсії, включають порушення моторики (акомодації, звільнення шлунка), розвиток гіперчутливості із закисленням дванадцятипалої кишки, зміни рівнів гормонів (гастрину, греліну, лептину, соматостатину) та ін.
Алгоритм діагностики H. pylori-асоційованої диспепсії є доволі простим. У разі наявності диспепсії та виявлення H. pylori призначається ерадикаційна терапія. За умови стійкого полегшення (після 6-12 міс) діагностується H. pylori-асоційована диспепсія. Якщо симптоми рецидивують або не змінюються, у пацієнта наявна функціональна диспепсія. При недослідженій диспепсії може застосовуватися стратегія test-and-treat («діагностуй і лікуй») (рівень доказів А). Проте цей підхід має враховувати регіональну ситуацію з H. pylori і співвідношення користь/витрати. Крім того, він не рекомендований літнім хворим і пацієнтам із небезпечними симптомами.
Наявні дані свідчать, що H. pylori негативно і позитивно асоціюється з багатьма захворюваннями або станами, не пов’язаними зі шлунком чи дванадцятипалою кишкою. Зокрема, тестування на H. pylori рекомендується пацієнтам з целіакією або залізодефіцитною анемією з виключеною крововтратою.
Найважливішим завданням ерадикації H. pylori є запобігання раку шлунка. Щорічно у світі діагностується майже 1 млн випадків цього захворювання. Проактивний підхід до профілактики починається з усвідомлення того, що інфекція H. pylori є найбільш вивченим етіологічним фактором раку шлунка (рівень доказів ІА, сильна рекомендація) і що ерадикація H. pylori знижує ризик розвитку раку шлунка (рівень доказів ІА, сильна рекомендація). Метааналіз низки великих контрольованих досліджень показав, що ерадикаційна терапія знижує майбутній ризик раку шлунка на 34% (р=0,02). Масова ерадикація H. pylori на рівні популяції знижує цей ризик на 25% на додаток до зменшення ймовірності атрофічного гастриту і пептичної виразки. H. pylori-гастрит вважається передраковим станом, тож дуже важливо здійснювати ерадикацію на ранніх стадіях інфекції (гастрит), до розвитку інтраепітеліальної неоплазії.
Для діагностики Нр-асоційованого гастриту принаймні необхідна стандартна біопсія: два біоптати з антрального відділу (на великій і малій кривизні, 3 см проксимальніше до пілоричного відділу) і два біоптати із середини тіла шлунка. Додаткова біопсія з ділянки вирізки шлунка рекомендується для діагностики передпухлинних змін (рівень доказів ІІВ, рекомендація середньої сили).
З метою підвищення точності й селективності біопсії рекомендується застосовувати ендоскопію високої чіткості. За наявності вираженої атрофії опціональним є серологічний скринінг із визначенням гастрину, антихелікобактерних антитіл і співвідношення пепсиногену I і пепсиногену II (так звана гастропанель). Дослідження у США – країні з відносно низькою захворюваністю на рак шлунка – показало, що серологічний скринінг (визначення сироваткового пепсиногену) в загальній популяції у віці 50 років знижує ризик аденокарциноми шлунка на 26,4% порівняно з 21,2% у разі ендоскопічного скринінгу.
У дорослих пацієнтів із діагностованою інфекцією H. pylori ерадикація повинна здійснюватись якомога раніше, проте вона ніколи не є занадто пізньою. Так, метааналіз п’яти досліджень показав, що навіть після ендоскопічної резекції ерадикація H. pylori знижує ризик метахронного раку шлунка на 61% (р<0,0001).
У регіонах з низьким або середнім ризиком розвитку раку шлунка рекомендується стратегія screen-and-treat («проводь скринінг і лікуй») (рівень доказів ІА, сильна рекомендація). Серологічний скринінг інфекції H. pylori в рамках стратегії screen-and-treat можна проводити одночасно з ендоскопічним скринінгом колоректального раку.
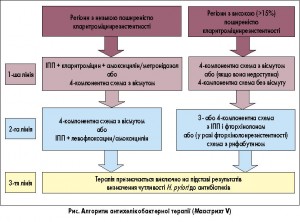
Останніми роками спостерігається істотне підвищення резистентності до кларитроміцину. На цій підставі в регіонах, де рівень резистентності до кларитроміцину перевищує 15%, не слід використовувати трикомпонентну схему з інгібітором протонної помпи (ІПП) і кларитроміцином без попереднього визначення чутливості до антибіотиків (сильна рекомендація).
У регіонах з високою (>15%) резистентністю до кларитроміцину рекомендується проведення квадротерапії з препаратом вісмуту або одночасної квадротерапії без вісмуту (ІПП, амоксицилін, кларитроміцин, нітроімідазол). У регіонах з високою подвійною резистентністю до кларитроміцину і метронідазолу як терапія першої лінії рекомендується чотирикомпонентна схема з вісмутом (рівень доказів ІІВ, сильна рекомендація).
Раніше як один з підходів до подолання кларитроміцинрезистентності вивчалася послідовна терапія (спочатку ІПП і амоксицилін, потім ІПП, кларитроміцин і метронідазол). Проте нещодавно проведений метааналіз показав, що одночасна терапія на 51% ефективніша за послідовну (р=0,02). Серед чотирикомпонентних схем, які не містять препарату вісмуту, одночасна 14-денна терапія ІПП, амоксициліном, кларитроміцином і нітроімідазолом є терапією вибору, оскільки вона найбільш ефективна в подоланні антибіотикорезистентності (рівень доказів ІА, сильна рекомендація).
У попередньому Маастрихті як друга лінія терапії рекомендувалася комбінація левофлоксацину, препарату вісмуту, амоксициліну й езомепразолу. Проте сьогодні цей підхід не завжди є оптимальним унаслідок зростання резистентності до фторхінолонів. Замість левофлоксацину у чотирикомпонентних вісмутвмісних схемах можна використовувати тетрациклін або рифабутин.
Алгоритм антихелікобактерної терапії, згідно з Маастрихтом V, подано на рисунку. У більшості випадків ці схеми призначаються тривалістю 14 днів.
З відеодоповіддю П. Мальфертайнера, присвяченою основним моментам Маастрихту V (англійською мовою), можна ознайомитися тут:
http://empendium.mp.pl/mircim/2016-presentations/143232, maastricht-v-what-is-new-in-the-management-of-h-pylori-infection
Підготував Олексій Терещенко