6 березня, 2017
Диета и Helicobacter pylori

Небольшая спиралевидная грамотрицательная бактерия, известная как Helicobacter pylori (Hp), продолжает волновать умы ученых во всем мире, несмотря на то что в центре пристального внимания исследователей оказалась относительно недавно. По мнению L. Holubiuk и соавт. (2016), Нр сосуществует вместе с человеком на протяжении 58 000 лет. Именно такая длительная колонизация дает некоторые преимущества организму человека: инфицирование Нр ассоциировано со снижением распространенности бронхиальной астмы, целиакии, синдрома раздраженного кишечника, гастроэзофагеальной рефлюксной болезни, эзофагеальной аденокарциномы. Однако эта бактерия обладает не только протекторными, но и агрессивными свойствами.
В настоящее время Нр считают причастной к возникновению целого ряда заболеваний: неалкогольного стеатогепатита, инсулинорезистентности, сахарного диабета 2 типа, полипов кишечника, аденокарциномы толстого кишечника, рака желчных протоков, деменции, псориаза. Если при обнаружении вышеперечисленных заболеваний эрадикация Нр не является строго обязательной, то больным пептической язвой, функциональной диспепсией, атрофическим гастритом, раком желудка, MALT-лимфомой, иммунной тромбоцитопенией, железодефицитной анемией неизвестного генеза, дефицитом витамина В12, а также пациентам с отягощенным семейным анамнезом по этим заболеваниям показано проведение комплексной антихеликобактерной терапии (АХБТ).
Традиционная АХБТ
АХБТ появилась на протяжении нескольких последних десятилетий, но за это время она прочно обосновалась в стандартах лечения и стала неотъемлемой частью повседневной гастроэнтерологической практики. В настоящее время АХБТ предусматривает назначение не менее двух антибактериальных препаратов в комбинации с ингибитором протонной помпы. Ожидаемая эффективность этой терапии колеблется от 82% (тройной режим) до 92% (последовательная терапия). Новые терапевтические режимы, предусматривающие назначение фторхинолонов (левофлоксацина, моксифлоксацина), характеризуются достаточно высокой эффективностью (85 и 90% соответственно) и хорошим профилем безопасности, но их широкое клиническое применение ограничено высокой стоимостью препаратов. Проведение АХБТ сопряжено с целым рядом нежелательных явлений: ростом антибиотикорезистентных штаммов Нр, появлением значительного количества побочных эффектов, особенно со стороны гастроинтестинальной системы (диарея, тошнота, нарушение вкуса), изменением качественного и количественного состава кишечной микрофлоры. Возможные негативные последствия АХБТ вынуждают некоторых пациентов отказаться от терапии / прервать лечение досрочно, а врачей – вести поиски дополнительных средств, увеличивающих эффективность эрадикационной терапии.
Альтернативные методы лечения
На протяжении последних нескольких лет большой популярностью стала пользоваться альтернативная терапия Нр с использованием обычных продуктов питания, бактериостатические и бактерицидные свойства которых были доказаны в условиях in vivo и in vitro. Основными отличительными характеристиками этого метода являются относительно небольшая стоимость, доступность, минимальное количество побочных эффектов.
В качестве альтернативного метода лечения Нр используются самые разнообразные продукты: вещества растительного происхождения, пробиотики, пептиды, полисахариды и др. Несмотря на то что альтернативная терапия не приводит к полной эрадикации Нр, она уменьшает степень бактериальной колонизации, снижает активность воспалительного процесса и степень атрофии слизистой оболочки желудка (СОЖ). Некоторые продукты питания способны повышать эффективность традиционной АХБТ и предотвращать появление побочных действий.
Продукты питания: вред и польза
Результаты последних научных изысканий и молекулярных исследований доказывают, что продукты питания способны модулировать активность патологического процесса благодаря наличию у них выраженных антиоксидантных свойств или комплексного антикарциногенного действия.
Оказывается, длительное употребление некоторых продуктов питания может предрасположить к инфицированию Нр. Например, в одном крупном кросс-секционном исследовании (n=10 407) убедительно доказано, что риск инфицирования Нр наиболее высок у лиц, пристрастившихся к потреблению легкодоступных углеводов и сладостей (отношение шансов (ОШ) 1,65; 95% ДИ 1,27-2,17), по сравнению с пациентами, принимающими эти продукты в минимальном количестве (Xia Y. et al., 2016). По мнению авторов этого исследования, рацион питания лиц, входящих в группу риска по развитию Нр-ассоциированных заболеваний, следует обогатить пищей, богатой белком/холестерином: риск инфицирования Нр при употреблении субпродуктов, крови животных, рыбы, морепродуктов минимален (ОШ 0,75; 95% ДИ 0,57-0,98).
Соль
Известно, что употребление поваренной соли в больших количествах ассоциировано с увеличением риска возникновения рака желудка. В ряде исследований in vivo доказано, что высокое содержание соли в продуктах питания приводит не только к непосредственному повреждению СОЖ, но и к увеличению степени колонизации Нр, что, в свою очередь, провоцирует утрату париетальных клеток, усиливает выраженность атрофии и интестинальной метаплазии.
Интересные результаты получили американские ученые, изучавшие изменения мембранного протеома Нр в зависимости от содержания соли в микробиологической среде (Voss B. J. et al., 2015). Оказалось, что высокое содержание соли вызывает ряд изменений в мембранном протеоме бактерии: оно способствует увеличению количества экспрессируемых белков, в том числе CagA, а также белка наружной мембраны HopQ, белка, содержащего домен фибронектина, НР0746. В среде с низким содержанием соли у хеликобактерий возрастала экспрессия других белков: VacA, двух VacA-подобных протеинов (ImaA, FaaA), белка-переносчика железа через внешнюю мембрану FecA3, а также различных белков, ответственных за активность жгутиков. Основываясь на полученных данных, исследователи утверждают, что бактерии Нр, выращенные в условиях с высоким содержанием соли, обладают меньшей подвижностью и большей вирулентностью по сравнению с бактериями, культивирующимися в среде с низким уровнем соли. Подобные изменения мембранного протеома Нр могут привести к увеличению риска развития рака желудка.
Другая группа американских ученых исследовала влияние диеты, богатой солью, на состояние СОЖ у лабораторных животных – монгольских песчанок (Gaddy J. A. et al., 2013). В соответствии с дизайном исследования одним животным вводили дикий штамм CagA+ Нр, других инфицировали изогенным, мутантным штаммом CagA- Нр. Спустя 4 мес после инфицирования у 100% грызунов, инфицированных диким штаммом Нр и получавших большое количество соли, была диагностирована аденокарцинома желудка; у животных, зараженных диким штаммом Нр и получавших обычную диету, эта патология выявлена в 58% случаев; инфицирование мутантным штаммом CagA- Нр и содержание на обычной диете не привело к неопластическому поражению желудка ни у одной монгольской песчанки (р<0,0001). Инфицирование диким штаммом Нр на фоне потребления большого количества соли сопровождалось увеличением активности воспалительного процесса, снижением уровня рН, значительной потерей париетальных клеток, увеличением экспрессии интерлейкина 1β, снижением экспрессии гепсидина в СОЖ по сравнению с приемом небольшого количества соли. У подопытных животных, поедавших много соли, отмечено также увеличение транскрипции CagA в условиях in vivo по сравнению с грызунами, находившимися на обычной диете.
 Подобные результаты несколько позже получили J. Loh и соавт. (2015). Эти ученые также избрали объектом своих научных изысканий монгольских песчанок. Перед инфицированием лабораторных животных исследователи провели протеомный анализ и полигеномное секвенирование штаммов Нр, предназначенных для введения подопытным грызунам. После инфицирования Нр грызунов на протяжении 4 мес содержали на диете, богатой солью. По завершении исследования штаммы Нр, выделенные у лабораторных животных, значительно отличались от первоначально использованных: увеличилось количество белков, ответственных за поступление железа и устойчивость к окислительно-восстановительному стрессу. «Диета с высоким содержанием соли приводит к значительному усилению воспалительного процесса в СОЖ и способствует селекции более агрессивных штаммов Нр, способных выживать в данных условиях и провоцировать неопластическое поражение органа», – утверждает J. Loh.
Подобные результаты несколько позже получили J. Loh и соавт. (2015). Эти ученые также избрали объектом своих научных изысканий монгольских песчанок. Перед инфицированием лабораторных животных исследователи провели протеомный анализ и полигеномное секвенирование штаммов Нр, предназначенных для введения подопытным грызунам. После инфицирования Нр грызунов на протяжении 4 мес содержали на диете, богатой солью. По завершении исследования штаммы Нр, выделенные у лабораторных животных, значительно отличались от первоначально использованных: увеличилось количество белков, ответственных за поступление железа и устойчивость к окислительно-восстановительному стрессу. «Диета с высоким содержанием соли приводит к значительному усилению воспалительного процесса в СОЖ и способствует селекции более агрессивных штаммов Нр, способных выживать в данных условиях и провоцировать неопластическое поражение органа», – утверждает J. Loh.
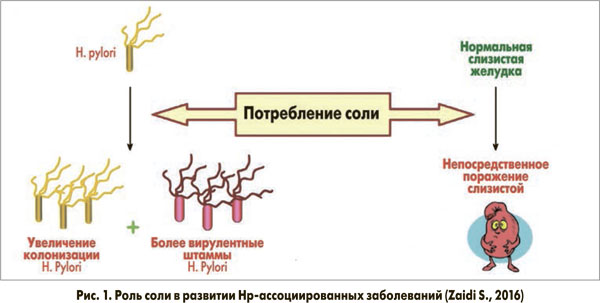
По мнению S. Zaidi (2016), значительное потребление соли приводит к увеличению степени колонизации Нр и появлению более агрессивных/вирулентных штаммов хеликобактерий, что в сочетании с прямым токсическим действием избытка соли на СОЖ приводит к росту Нр-ассоциированных заболеваний (рис. 1).
Производные фенолов: фрукты, ягоды
В условиях in vitro у многих фруктов выявлена бактериостатическая активность в отношении Нр; считается, что данные свойства обусловлены содержанием в этих продуктах производных фенолов.
Известно, что экстракт черники щитковой уменьшает адгезивные свойства Нр. Chatterjee и соавт. (2004) доказали наличие у экстрактов малины, клубники, ежевики, черники выраженной бактериостатической активности в отношении кларитромицинрезистентных штаммов Нр. В проспективном рандомизированном двойном слепом исследовании, выполненном под руководством Zhang (2005), установлено, что ежедневный прием 250 мл сока черники в течение 90 дней приводит к спонтанному разрешению Нр-инфекции в 14,46% случаев.
Наиболее полные сведения относительно протективной роли фруктов можно найти в работе Т. Wang и соавт. (2017), которые выполнили обобщенный анализ результатов 810 проспективных исследований. Оказалось, что увеличение потребления фруктов ассоциировано с уменьшением риска развития некардиального рака желудка (ОШ 0,71; 95% ДИ 0,52-0,95; р=0,02). Минимальный риск развития рака желудка зафиксирован у любителей фруктов, не имеющих антител к Нр (ОШ 0,12; 95% ДИ 0,06-0,25), по сравнению с пациентами, инфицированными CagA+ штаммами Нр и употребляющими небольшое количество фруктов. Исследователи рекомендуют лицам, находящимся в группе риска по развитию Нр-ассоциированной патологии, потреблять больше фруктов, чтобы избежать развития неопластического поражения желудка. Эти выводы, сделанные Т. Wang и соавт., полностью противоречат вышеприведенным результатам, полученным Y. Xia и соавт. (2016). Вероятно, точный ответ на вопрос о целесообразности употребления большого количества фруктов и овощей будет получен несколько позже.
Изотиоцианаты: брокколи
На протяжении многих веков в народной медицине сок (рассол) квашеной капусты используется для лечения язвенной болезни. Различные виды капусты (цветная, белокочанная), а также брюква, рапс, редис содержат изотиоцианаты – вещества, обладающие антиканцерогенной активностью. Изотиоцианаты индуцируют апоптоз, ингибируют клеточную пролиферацию, модулируют активность цитохромов печени, вовлеченных в метаболизм карциногенов. Авторы широкомасштабного (n=18000) проспективного исследования – К. Моу и соавт. (2009) – установили, что риск развития рака желудка у пациентов с высоким содержанием изотиоцианатов в моче гораздо меньше, чем у лиц с низкой концентрацией этого вещества в урине. Исследователи отметили интересный факт: выявленный эффект не зависел от массы тела, однако не наблюдался у курильщиков и пациентов, регулярно употреблявших алкогольные напитки.
Одним из наиболее известных изотиоцианатов является сульфорафан, максимальные концентрации которого содержатся в брокколи и ее ростках (в виде предшественника глюкорафанина). В условиях in vivo сульфорафан обладает выраженной антибактериальной активностью в отношении Нр (минимальная подавляющая концентрация – 2 мкг/мл), включая кларитромицинрезистентные штаммы.
Интересны результаты клинического применения сульфорафана. Одной из таких работ является исследование, выполненное Р. Mirmiran и соавт. (2014). Ученые отобрали больных сахарным диабетом 2 типа, инфицированных Нр (n=86), и разделили их на 3 группы. Пациентам первой группы назначили стандартную тройную терапию (СТТ) (омепразол 20 мг, кларитромицин 500 мг, амоксициллин 1000 мг 2 р/сут на протяжении 14 дней). Другим больным рекомендовали принимать порошок из измельченной капусты брокколи (ПИКБ) (6 г/сут в течение 28 дней). Участники, вошедшие в состав третьей группы, получали комбинацию СТТ и ПИКБ. Исследование завершили 77 пациентов (СТТ: n=28, ПИКБ: n=25; СТТ+ПИКБ: n=24). У 89,3% пациентов, получавших СТТ, эрадикационная терапия была признана эффективной, в группах ПИКБ и СТТ+ПИКБ этот показатель составил 56,0 и 91,7% соответственно. Кроме того, в группе СТТ+ПИКБ исследователи зафиксировали достоверное снижение систолического и диастолического артериального давления в динамике лечения (р<0,05). В группе СТТ имело место увеличение концентрации триглицеридов и индекса ТГ/ ХС ЛПВП (р<0,05), тогда как в группе ПИКБ отмечено снижение концентрации высокочувствительного С-реактивного белка (р<0,05). Основываясь на полученных данных, ученые рекомендуют СТТ сочетать с приемом экстракта брокколи, поскольку такая комбинация не только приводит к увеличению эффективности эрадикационной терапии, но и оказывает благоприятное воздействие на кардиоваскулярные факторы риска у больных СД 2 типа.
Y. Chang и соавт. (2015) также использовали экстракт брокколи, но в отличие от своих американских коллег корейские ученые назначали сульфорафан без сопутствующей АХБТ. Пациентов разделили на 3 группы в зависимости от инфицирования Нр: одним Нр+ больным рекомендовали принимать экстракт брокколи (группа А; n=33), другим Нр+ пациентам назначили плацебо (группа В; n=28), Нр- участники также получали экстракт брокколи (группа С; n=28). Впоследствии оказалось, что брокколи не оказывает значимого влияния на результаты уреазного дыхательного теста и концентрацию аммиака в желудочном соке в группе А (р=0,634 и р=0,505 соответственно), но способствует снижению концентрации малонового диальдегида в СОЖ у больных из групп А (р<0,05) и С (р<0,001). Несмотря на то что экстракт брокколи не уменьшает степень колонизации Нр, он позволяет снизить активность перекисного окисления липидов в СОЖ и может использоваться в качестве цитопротективного средства при Нр-ассоциированном гастрите.
Мед и чай
Антибактериальная активность меда объясняется его высокой осмолярностью, низким рН и содержанием перекиси водорода. В условиях in vitro некоторые виды меда, такие как мед мануки и дуба, обладают мощным ингибирующим бактериостатическим действием в отношении Нр, ингибируя активность уреазы.
Зеленый чай, один из самых почитаемых напитков во всем мире, также способен ингибировать рост Нр. Антибактериальные свойства зеленого чая в отношении Нр подтверждены в условиях in vitro и in vivo; их объясняют содержанием катехинов, в частности эпигаллокатехин‑3-галлатом, который обладает наиболее выраженными антибактериальными свойствами (средняя ингибирующая концентрация – 8 мкг/мл).
Относительно недавно были опубликованы результаты исследования болгарских ученых, которые проанализировали пищевые привычки 150 пациентов, предъявлявших диспепсические жалобы (Boyanova L. et al., 2015). Оказалось, что у участников, употреблявших мед чаще одного дня в нед (50,6%), реже выявляли антитела к Нр по сравнению с больными, не имевшими такой привычки (70,8%). Подобная ситуация наблюдалась в отношении пациентов, предпочитавших пить зеленый/черный чай чаще одного дня в нед (45,2%), по сравнению с остальными больными (64,8%). Данные зависимости носили статистически значимый характер: употребление меда (ОШ 0,38; 95% ДИ 0,19-0,78) и зеленого/черного чая (ОШ 0,45; 95% ДИ 0,21-0,95) сопровождалось более низкой вероятностью заражения Нр.
Лактоферрин
Лактоферрин – это гликопротеин из семейства трансферринов, обладающий антибактериальными свойствами. Он образует комплексные соединения с ионами железа, ограничивая тем самым доступность этого элемента бактериям. Лактоферрин обнаруживается в женском и коровьем молоке, слюне, слезной жидкости; он является составляющим элементом неспецифического иммунитета.
В ряде исследований было показано, что лактоферрин снижает степень бактериальной колонизации и активность Нр-индуцированного гастрита. Метаанализ результатов проспективных РКИ, изучавших целесообразность дополнения тройной / квадротерапии АХБТ назначением лактоферрина, доказал способность последнего увеличивать частоту успешной эрадикации и снижать выраженность побочных действий. Несмотря на незначительное уменьшение биодоступности ионов железа, лактоферрин обладает синергизмом действия с антибактериальными препаратами, облегчая их проникновение сквозь бактериальную мембрану.
Масла и жирные кислоты
В 1994 г. Thompson и коллеги доказали, что в условиях in vitro полиненасыщенные жирные кислоты, омега‑3 и омега‑6 ингибируют рост Нр. Масла растительного происхождения содержат большое количество полифенолов, обладающих бактериостатической активностью в отношении Нр. Оливковое масло, масла из косточек черной смородины, семян моркови и грейпфрута, а также рыбий жир обладают умеренной бактериостатической активностью в отношении Нр. Высказывается мнение, что полиненасыщенные жирные кислоты уменьшают степень тяжести атрофического гастрита.
Чеснок
Фитонцидные свойства чеснока объясняют его активное использование в различных исследованиях. Целесообразность назначения чеснока больным, инфицированным Нр, исследовали М. Zardast и соавт. (2016). Дизайн анализа предполагал двукратное проведение уреазного дыхательного теста: до начала исследования и 3 дня спустя после его завершения. В этом изучении приняли участие пациенты, инфицированные Нр и предъявлявшие гастроинтестинальные жалобы (n=15); всем больным рекомендовали ежедневно на протяжении 3 дней принимать вместе с едой 3 г чеснока днем и вечером. Проанализировав полученные результаты, исследователи пришли к такому выводу: «Прием чеснока несколько улучшил результаты дыхательного уреазного теста в динамике наблюдения».
Пробиотики
Считается, что некоторые пробиотические штаммы обладают антибактериальной активностью в отношении Нр благодаря своей способности модифицировать иммунную систему организма хозяина, секретировать антибиотикоподобные вещества, изменять адгезивные свойства бактерий.
На страницах авторитетного международного журнала Helicobacter в 2016 г. были опубликованы результаты одного очень интересного исследования. Ученые под руководством М. Emara доказали, что длительный прием пробиотиков сопровождается уменьшением количества бактерий Нр, снижением активности воспалительного процесса в теле и антральном отделе желудка. Этот эффект сохраняется на протяжении длительного периода времени и объясняется, вероятно, иммунными механизмами.
Авторы систематического обзора и метаанализа результатов 45 рандомизированных контролированных исследований (РКИ; n=6997) установили, что частота достижения эффективной эрадикации при применении пробиотиков составляет 82,31%, а при отсутствии их использования – 72,08% (Zhang М. et al., 2015). Сочетанное применение пробиотиков со стандартной АХБТ ассоциировано с увеличением эффективности эрадикации как по данным анализа per-protocol (отношение рисков (ОР) 1,11; 95% ДИ 1,08-1,15; р<0,001), так и по результатам анализа intention-to-treat (ОР 1,13; 95% ДИ 1,10-1,16; р<0,001). Ученые подчеркнули, что назначение пробиотиков позволяет снизить частоту возникновения побочных эффектов по сравнению с контрольной группой (21,44 vs 36,27% соответственно). Комбинация пробиотиков со стандартной АХБТ приводит к уменьшению риска развития нежелательных явлений (ОР 0,59; 95% ДИ 0,48-0,71; р<0,001), но не позволяет значительно увеличить приверженность пациентов к лечению (ОР 0,98; 95% ДИ 0,68-1,39; р=0,889).
 По мнению М. Homan и соавт. (2015), при проведении эрадикационной терапии следует использовать наиболее эффективные и безопасные пробиотические штаммы: Saсcharomyces boulardii, Lactobacillus GG, L. reuteri.
По мнению М. Homan и соавт. (2015), при проведении эрадикационной терапии следует использовать наиболее эффективные и безопасные пробиотические штаммы: Saсcharomyces boulardii, Lactobacillus GG, L. reuteri.
Таким образом, особенности пищевого рациона могут облегчить или затруднить инвазию Нр (рис. 2).
В настоящее время установлена антихеликобактерная активность различных пищевых продуктов: пробиотиков, брокколи, черники, черной смородины, различных растительных масел, меда, чая. Однако количество РКИ, в которых была доказана целесообразность и эффективность насыщения этими продуктами пищевого рациона пациентов с Нр-индуцированными заболеваниями, остается очень небольшим. Улучшение здоровья общества посредством уменьшения инфицированности и колонизации Нр, снижения вероятности развития предопухолевых состояний и неопластических заболеваний посредством употребления дешевых, легкодоступных продуктов питания представляется перспективным направлением в гастроэнтерологии. Весьма вероятно, что в скором времени клиницисты будут не просто назначать АХБТ, но и делать акцент на обязательном исключении/потреблении определенных продуктов.
Список литературы находится в редакции.
Медична газета «Здоров’я України 21 сторіччя» № 3 (400), лютий 2017 р.


