7 червня, 2017
Мельдоний при сердечно-сосудистых и метаболических заболеваниях: новые механизмы действия и перспективы клинического применения
Мельдоний – популярный кардиопротектор, антиишемическое действие которого обычно связывают с ингибированием биосинтеза L-карнитина и оптимизацией путей получения энергии клетками. Исследования последних лет показывают, что терапевтический потенциал этой удивительной молекулы еще не до конца раскрыт. В данном обзоре рассмотрены менее известные клиницистам, но перспективные для клинической практики механизмы действия мельдония, которые могут быть использованы при лечении сердечной недостаточности, инфаркта миокарда (ИМ), аритмий, атеросклероза и сахарного диабета (СД).
L-карнитин участвует в переносе жирных кислот (ЖК) на внутренние мембраны митохондрий, где происходит их окисление с образованием АТФ. Мельдоний ограничивает биодоступность карнитина, в результате чего интенсивность β-окисления ЖК в митохондриях снижается в пользу усиления метаболизма глюкозы. Аэробный гликолиз является наиболее эффективным путем продукции АТФ при дефиците кислорода, и это способствует выживанию кардиомиоцитов в условиях ишемии и гипоксии.
Снижение уровня L-карнитина также сопровождается снижением внутриклеточной концентрации недоокисленных токсичных метаболитов ЖК – длинноцепочечных ацилкарнитинов и триметиламина-N-оксида – ТМАО (M. Dambrova et al., 2016).
Изначально карнитин-подавляющий эффект мельдония связывали с его свойством ингибировать последний фермент в цепочке биосинтеза L-карнитина – γ-бутиробетаингидроксилазу. Позже выяснилось, что мельдоний также способен ингибировать катион / карнитиновый транспортный протеин 2 типа (OCTN2) – транспортер L-карнитина в почках (M. Spaniol et al., 2001). Ингибирование OCTN2 в почках под действием мельдония ограничивает поступление L-карнитина из плазмы крови в ткани и усиливает его выведение с мочой, как показано на рисунке (J. Kuka et al., 2012).
Недавно было продемонстрировано, что ингибирование OCTN2 является более эффективным механизмом снижения биодоступности L-карнитина и что это свойство мельдония играет важную роль в ограничении размеров ИМ при острой ишемии (E. Liepinsh et al., 2014).
В условиях ишемии мельдоний предотвращает снижение экспрессии протеинов Ca2+-АТФазы саркоплазматического ретикулума, которая является ионным насосом, отвечающим за депонирование кальция. Этот эффект доказан в экспериментальных исследованиях и имеет прямое отношение к терапии сердечной недостаточности (Y. Hayashi et al., 2000).
Устранение перегрузки кардиомиоцитов кальцием реализуется в клинические эффекты – предупреждение аритмий, нарушений сократимости и расслабления миокарда (M. Dambrova et al., 2002).
В последние годы установлено, что при метаболизме L-карнитина, поступающего с пищей, под действием кишечной микрофлоры образуется TMAO, и доказана связь этого метаболита с развитием атеросклероза и сердечно-сосудистых заболеваний (R.A. Koeth et al., 2013). Мельдоний не влияет на бактериальный транспорт L-карнитина, однако препятствует образованию триметиламина – ТМА (предшественника TMAO), вероятнее всего, посредством ингибирования бактериального фермента карнитиноксигеназы (рис.) (J. Kuka et al., 2014).
Уменьшение биодоступности L-карнитина под действием мельдония стимулирует основные ферменты аэробного окисления глюкозы. Этот эффект не только обеспечивает «переключение» путей образования АТФ на энергетически более выгодный гликолиз, что имеет важное значение при лечении ишемической болезни сердца (ИБС), но и играет важную роль в повышении чувствительности периферических тканей к действию инсулина, что является перспективным направлением терапии СД 2 типа. Растет число работ, в которых показано, что доступность недоокисленных метаболитов ЖК – ацилкарнитинов – определяет баланс между метаболизмом ЖК и глюкозы и может иметь важное значение в развитии инсулинорезистентности (M.G. Schooneman et al., 2013; M. Makrecka et al., 2014).
Мельдоний на сегодняшний день является единственным препаратом, одобренным для клинического использования, который снижает биодоступность ацилкарнитинов. Предполагается, что этот механизм лежит в основе противодиабетического эффекта мельдония (M. Dambrova et al., 2016).
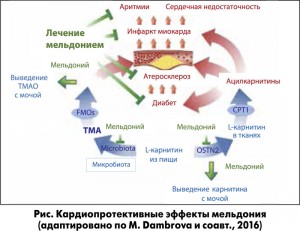
На рисунке обобщены биохимические механизмы кардиопротективного действия мельдония.
Ингибирование OCTN2 в почках под действием мельдония ограничивает поступление L-карнитина из плазмы крови в ткани и усиливает его выведение с мочой.
Снижение биодоступности L-карнитина ограничивает образование токсичных ацилкарнитинов под действием карнитин-пальмитоилтрансферазы (CPT1). Кроме того, мельдоний нарушает образование ТМА из L-карнитина и стимулирует почечную экскрецию его проатерогенного метаболита TMAO, который образуется под действием флавоносодержащих монооксигеназ (FMO) кишечной микрофлоры. Снижение концентраций ацилкарнитинов и TMAO определяет кардиопротективные, антиатеросклеротические и противодиабетические эффекты мельдония.
Фармакологические эффекты мельдония
Сердечно-сосудистые заболевания
Кардиопротективные эффекты мельдония хорошо изучены на моделях ИМ и сердечной недостаточности у животных. Эксперименты подтвердили, что терапия мельдонием способствует сохранению продукции АТФ в условиях гипоксии за счет оптимизации энергетического метаболизма (E. Liepinsh et al., 2013), ограничивает расширение зоны ИМ без влияния на гемодинамику (C. Sesti et al., 2006), предотвращает ишемические и реперфузионные аритмии (N.N. Aye et al., 2000; R. Vilskersts et al., 2009), замедляет темпы постинфарктного ремоделирования камер сердца и формирования сердечной недостаточности (Y. Hayashi et al., 2000).
В нескольких клинических исследованиях оценивали эффективность мельдония при лечении хронической сердечной недостаточности (ХСН). Так, М.Е. Стаценко и соавт. (2007) изучали эффекты мельдония, который назначали дополнительно к базисной терапии пациентов с ХСН и СД 2 типа в постинфарктный период. На фоне приема мельдония отмечали улучшение симптоматики ХСН, что позволило перевести пациентов в низший функциональный класс (ФК), увеличение пройденного расстояния в тесте 6-минутной ходьбы, тенденцию к нормализации диастолической функции и повышение фракции выброса левого желудочка.
Результаты клинических исследований у пациентов с хронической ИБС (стабильной стенокардией) указывают на то, что прием мельдония в дозе 1000 мг/сут в составе комплексной терапии уменьшает частоту приступов стенокардии и потребность в короткодействующих нитратах, повышает толерантность к нагрузкам и в конечном счете улучшает качество жизни пациентов (V. Dzerve et al., 2010).
Метаболический синдром и СД
Дозозависимый эффект снижения уровня глюкозы в плазме крови без повышения уровня инсулина в результате терапии мельдонием наблюдали в экспериментальных исследованиях на модели СД 2 типа (E. Liepinsh et al., 2009).
Лечение мельдонием также предотвращало ассоциированную с СД эндотелиальную дисфункцию и потерю болевой чувствительности вследствие диабетической нейропатии.
Введение мельдония в течение 6 нед крысам со стрептозотоциновым СД 1 типа ассоциировалось с улучшением гликемического статуса, снижением содержания гликозилированного гемоглобина и частоты случаев развития нейропатии (J. Sokolovska et al., 2011).
На экспериментальной модели ожирения и инсулинорезистентности сравнивали метаболические эффекты мельдония и метформина – сахароснижающего препарата первой линии для лечения СД 2 типа (E. Liepinsh et al., 2011). Мельдоний не уступал метформину по способности снижать уровень глюкозы у экспериментальных животных после кормления и натощак. Оба препарата сопоставимо уменьшали инсулинорезистентность. Более того, комбинация мельдония с метформином проявляла синергичное действие, снижая концентрацию инсулина в плазме крови и повышая содержание гликогена в печени в большей степени, чем оба препарата по отдельности. Стимуляция депонирования гликогена свидетельствует о повышении чувствительности печеночной ткани к инсулину, что имеет ключевое значение в терапии СД 2 типа. Кроме того, комбинированная терапия предотвращала увеличение массы тела, а мельдоний сглаживал такой побочный эффект метформина, как лактатацидоз. Эти данные указывают на двойное преимущество мельдония у пациентов с коморбидностью сердечно-сосудистых заболеваний и СД 2 типа.
Выводы
1. Терапия мельдонием способствует адаптации энергетического обмена кардиомиоцитов к условиям ишемии/гипоксии, ограничивает зону инфаркта и противодействует патологическому ремоделированию сердца.
2. Дополнительным преимуществом мельдония является ингибирование образования проатерогенного фактора TMAO под действием ферментов кишечной микробиоты, что может сдерживать прогрессирование атеросклероза.
3. Снижение концентрации ацилкарнитинов под влиянием терапии мельдонием лежит в основе повышения чувствительности тканей к действию инсулина и имеет важное значение при лечении пациентов с коморбидным СД.
4. Экспериментальные и клинические исследования подтверждают эффективность мельдония в комплексной терапии ИБС, ХСН и СД 2 типа.
Подготовил Дмитрий Молчанов