9 травня, 2017
Генная терапия сердечной недостаточности: отдаленная перспектива
С появлением инновационного метода генной терапии открывается перспектива воздействия на тонкие молекулярные механизмы патогенеза сердечной недостаточности (СН), недоступные для медикаментозного лечения. Достижения в области векторных технологий сделали возможным безопасный и эффективный перенос генетического материала в миокард. Параллельно с совершенствованием способов доставки эти достижения приблизили клиническую реальность генной терапии. Однако после успехов исследований ранних фаз результаты последующих клинических испытаний разочаровали и заставили пересмотреть подходы к выбору векторов, доставочных систем, оптимальных мишеней и конечных точек. В данном обзоре рассматриваются некоторые разработки генной терапии, по которым проведены или проводятся в настоящее время клинические исследования.
Мишени
При СН на разных уровнях нарушается связь между возбуждением и сокращением миокарда. Воздействие на различные каналы, транспортеры и белки, критически необходимые для реализации функции, представляется перспективным способом восстановления сократительной способности. Еще одна группа мишеней включает факторы ангиогенеза, цитопротекции и факторы, облегчающие внедрение стволовых клеток.
Усиление сократимости сердечной мышцы
Мишень — β-адренергическая система
β-адренергическая система является ключевым регулятором сократимости сердца. При СН β-адренорецепторы теряют чувствительность, в частности из-за повышенной активности киназы GRK2. В экспериментах на грызунах и крупных животных экспрессия ингибитора GRK2 (bARKct) ассоциировалась с улучшением сократительной функции несостоятельного миокарда (J. Reinkober et al., 2012).
Перспективным направлением β-адренергической стимуляции также является активация аденилатциклазы типа 6 (AC6). На модели СН у свиней перенос гена AC6 с помощью аденовирусного вектора приводил к улучшению функции левого желудочка (ЛЖ) и параметров ремоделирования (N.C. Lai et al., 2004).
Мишень — белки циркуляции кальция
Множественные дефекты белков-переносчиков Ca2+ изучены как причина разобщения процессов возбуждения и сокращения миокарда при СН. Gwathmey и соавт. первыми сообщили о том, что нарушение циркуляции кальция может быть обусловлено сниженной активностью Ca2+-АТФазы саркоплазматического ретикулума (SERCA2a) независимо от этиологии СН (J.K. Gwathmey et al., 1987). В серии экспериментов продемонстрировано улучшение сократимости после переноса гена SERCA2a в миокард свиней (Y. Kawase et al., 2008). Кроме того, трансгенная экспрессия SERCA2a сопровождалась восстановлением энергетического статуса сердца (S. Sakata et al., 2007), снижением частоты развития желудочковых аритмий (F. Prunier et al., 2008) и усилением коронарного кровотока через активацию NO-синтазы в эндотелиоцитах (L. Hadri et al., 2010). Недавно была установлена важная роль мелкого убиквитин-подобного модификатора типа 1 (SUMO1) в регуляции активности SERCA2a в кардиомиоцитах. Уровень SUMO1 уменьшается при СН, а перенос кодирующего гена с помощью аденоассоциированного вируса 9 типа (AAV9) приводил к восстановлению уровня SERCA2a, улучшению гемодинамической эффективности миокарда и снижению смертности в экспериментах на мелких и крупных животных (C. Kho et al., 2011).
Ингибирование фосфоламбана (PLN) — еще один способ улучшения обмена Ca2+ в кардиомиоцитах. Повышенная активность протеинфосфатазы‑1 (РР1), обнаруженная при СН у человека, приводит к дефосфориляции PLN. Гиперэкспрессия РР1 или устранение ее ингибитора у морских свинок ассоциировались со сниженным β-адрено-опосредованным сократительным ответом, угнетением функции сердца и преждевременной смертью от СН. Напротив, у трансгенных мышей, экспрессирующих конститутивно активный ингибитор‑1 (I1c), наблюдали ингибирование РР1, фосфориляцию PLN и улучшение сократимости сердца (A. Pathak et al., 2005).
S100 также относится к семейству Ca2+-модулирующих протеинов. S100A1 — наиболее распространенная в миокарде изоформа, участвующая в процессах сокращения и релаксации посредством усиления активности как рианодиновых рецепторов, так и SERCA2a. Длительная экспрессия S100A1 при помощи вектора AAV6 приводила к стабильному регрессу дисфункции и ремоделирования ЛЖ на модели СН у крыс (S.T. Pleger et al., 2007). А недавно на доклинической модели ишемической кардиомиопатии перенос гена S100A1 при помощи вектора AAV9 вызвал драматическое улучшение сократительной функции сердца (S.T. Pleger et al., 2011).
Мишень — миофиламенты
Сокращение кардиомиоцитов происходит в результате высвобождения энергии химических связей АТФ, которая трансформируется в кинетическую энергию скольжения миозина вдоль филаментов актина. В исследованиях на животных было показано, что замещение АТФ на 2-деокси-АТФ улучшает сократимость поперечно исчерченной мышечной ткани за счет улучшения взаимодействия миозина с актином (S.G. Nowakowski et al., 2013). Продукция 2-деокси-АТФ в норме ограничена, но может быть повышена гиперэкспрессией фермента рибонуклеотидредуктазы (R1R2). Гиперэкспрессия R1R2 приводила к усилению сократимости изолированных кардиомиоцитов крыс и ткани миокарда от пациентов с СН (F. Moussavi-Harami et al., 2015). У трансгенных мышей, экспрессирующих в большом количестве R1R2, наблюдали улучшение систолической функции ЛЖ (S.G. Nowakowski et al., 2013).
Усиление ангиогенеза
Эндотелиальные факторы роста сосудов (VEGF) широко использовались для стимулирования ангиогенеза в ишемизированном миокарде без отчетливых положительных клинических исходов. Предполагается, что длительная гиперэкспрессия VEGF-A приводит к образованию «протекающих» сосудов. Временная гиперэкспрессия VEGF-A с использованием модифицированной РНК стимулировала образование полноценных «непротекающих» сосудов и улучшала выживание мышей в опытах на модели инфаркта миокарда (L. Zangi et al., 2013). Другие изоформы VEGF также продемонстрировали положительные эффекты при стенокардии.
Цитопротекция
Цитопротективная генная терапия недавно продемонстрировала обнадеживающие результаты в клинически релевантных экспериментах на крупных животных. Hinkel и соавт. впервые показали цитопротективную роль гиперэкспрессии гемоксигеназы‑1 при постишемическом реперфузионном повреждении миокарда (R. Hinkel et al., 2015). Изоформы VEGF (B и D) также проявляют кардиопротективные свойства. Внедрение гена VEGF-B167 посредством вирусного вектора AAV способствовало сохранению функции сердца и предотвращало повышение конечно-диастолического давления в ЛЖ у собак с тахикардитической моделью СН (F. Woitek et al., 2015).
Облегчение внедрения стволовых клеток
Комплекс фактора‑1 стволовых клеток (SDF‑1) и C-X-C-хемокинового рецептора (CXCR) 4 типа способствует хоумингу стволовых клеток в инфарцированном миокарде (S.K. Ghadge et al., 2011). SDF‑1 стимулирует миграцию стволовых клеток из костного мозга в зону повреждения миокарда и, по всей видимости, является важным регулятором эндогенных процессов заживления ткани. Доклинические исследования показали, что гиперэкспрессия SDF‑1 в пограничной зоне хронически ремоделированного постинфарктного миокарда приводит к улучшению функции сердца и плотности кардиальной васкуляризации (S. Sundararaman et al., 2011).
Векторы
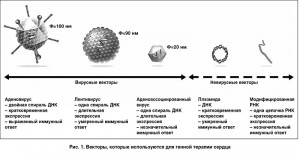
Успех генной терапии во многом зависит от эффективности проникновения генетического материала в миокард. Прицельное внедрение нуклеиновых кислот в кардиомиоциты остается чрезвычайно трудной задачей. Доставочные средства (векторы) можно разделить на две группы: невирусные и вирусные. Каждая векторная система имеет свои недостатки и преимущества (рис. 1).
Невирусные векторы
На сегодняшний день возможности невирусной переноски генов практически эксклюзивно представлены технологией получения обнаженной плазмидной ДНК. К преимуществам плазмидной ДНК относятся: 1) простота производства в больших масштабах; 2) неограниченный размер переносимой ДНК; 3) ограниченный иммунный ответ человеческого организма. Отсутствие выработки значимого гуморального иммунитета позволяет вводить этот вектор повторно без потери эффективности генного переноса. Но, к сожалению, эффективность трансфекции при использовании данного вектора остается низкой.
Перспективным безвирусным переносчиком является мРНК с модифицированными нуклеотидами (модРНК). В отличие от нативных нуклеиновых кислот модРНК не связывается с толл-подобными рецепторами, что ограничивает иммунную реакцию на трансфекцию (K. Kariko et al., 2005). Поэтому модРНК можно вводить повторно. Кроме того, поскольку мРНК доступна для трансляции генетического кода в цитоплазме, не обязательно вводить ее в ядро клетки. МодРНК вызывает интенсивную, но относительно кратковременную трансгенную экспрессию, определяемую в течение 2-6 дней (L. Zangi et al., 2013). Недавно Turnbull и соавт. показали, что модРНК в сочетании с наночастицами индуцирует экспрессию уже через 20 мин после введения в миокард грызунов и свиней (I. Turnbull et al., 2015).
Вирусные векторы
Большинство исследований генной терапии проводились с аденовирусными векторами. Они способны внедрять генетический материал в разные клетки, включая кардиомиоциты, и вызывать обильную, но кратковременную (1-4 нед) экспрессию генов. Применение аденовирусных векторов ограничивает выраженный иммунный ответ реципиента.
Лентивирусные векторы не вызывают выраженной иммунной реакции (S. Nayak, R. W. Herzog, 2010) и могут заражать неделящиеся клетки, включая кардиомиоциты. Поскольку лентивирусы внедряют генетический материал непосредственно в геном клетки-хозяина, они способны генерировать длительную экспрессию. Ни аденовирусы, ни лентивирусы не проявляют специфической тропности к клеткам сердечно-сосудистой системы, поэтому для их внедрения требуются интрамиокардиальные инъекции. Лентивирусные векторы еще не изучались в клинических исследованиях.
Весьма многообещающей доставочной формой для генной терапии сердца считаются аденоассоциированные вирусы (AAV). Это мелкие непатогенные вирусы семейства Parvoviridae, несущие одну спираль ДНК. В миокарде вызывают длительную трансгенную экспрессию даже без интеграции в геном. Главным преимуществом ААV является природная тропность к кардиомиоцитам, выявленная у некоторых серотипов (C. Zincarelli et al., 2008). Это позволяет удобно вводить их в кровоток, а не в миокард, и эксперименты на грызунах подтвердили эффективный генный перенос при системном применении ААV (S. Sakata et al., 2007; C. Kho et al., 2011). К рекомбинантным ААV не вырабатывается иммунитет, но нейтрализующие антитела к диким серотипам вирусов (очевидно, в результате инфицирования на протяжении жизни) представляют серьезное препятствие на пути широкого применения ААV для генной терапии. Более половины населения, а в некоторых регионах Европы до 80%, имеют высокие титры нейтрализующих антител. Несмотря на этот недостаток, а также сравнительно малую емкость для «упаковки» ДНК (≤5 кДа), векторы на основе AAV, вероятно, являются самыми перспективными для генной терапии в кардиологии.
Пути доставки
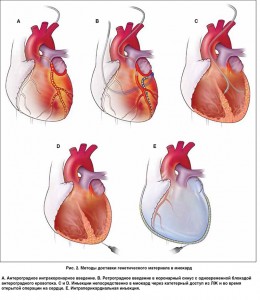
К сожалению, ни одна из векторных технологий не обеспечивает достаточного насыщения миокарда генетическим материалом при системном внутривенном введении, поэтому применяются специальные пути доставки к сердцу (рис. 2). Оптимальный способ зависит от используемого вектора, гена, а также от заболевания и стратегии ведения пациента. Например, хирургическое введение подходит пациентам, у которых проводятся плановые операции на открытом сердце, такие как шунтирование или замена клапанов. При интрамиокардиальном введении происходит локальная трансгенная экспрессия, обычно в радиусе 5-10 мм вокруг хода инъекционной иглы. Преимуществом хирургического доступа является точность доставки генетического материала, в то время как эндоваскулярный путь является менее инвазивным. Системная утечка вектора неизбежна даже при прямой инъекции в миокард. Препарат покидает сердце через венозный дренаж, лимфатическую систему и отверстия от инъекционной иглы.
При антероградной доставке через коронарные артерии инструментарий и техника такие же, как при чрескожных коронарных вмешательствах. Вектор поступает к миокарду физиологическим путем с током крови, чем достигается равномерное его распределение. Однако простые болюсные инъекции вектора в коронарные артерии вызывают очень незначительную трансгенную экспрессию. Более высокая эффективность переноса получена при кратковременных коронарных окклюзиях, однако это может вызвать оглушение миокарда вследствие ишемии, что неприемлемо для пациентов с выраженной СН.
Еще один способ доставки — ретроградные инъекции в коронарный синус. При этом требуется одновременная баллонная окклюзия коронарной артерии и синуса для предотвращения быстрого вымывания векторов. Предполагается, что эффективность экспрессии терапевтических генов тем выше, чем дольше длится окклюзия, однако пользу следует соотносить с риском развития осложнений. Эффективность трансдукции также может повышаться при одновременном введении препаратов, повышающих проницаемость (F. Woitek et al., 2015).
Клинические исследования
Программа исследований по переносу гена SERCA2a (CUPID, AGENT-HF, SERCA-LVAD)
Исследование I-II фазы CUPID (Calcium Upregulation by Percutaneous Administration of Gene Therapy in Cardiac Disease) было первым с участием человека, в котором изучали клинические эффекты восстановления экспрессии SERCA2a у пациентов с далеко зашедшей СН. Ген, кодирующий SERCA2a, с помощью вектора на основе AAV1 вводили путем однократной внутрикоронарной инфузии (M. Jessup et al., 2011). 39 пациентов с СН поздних стадий, у которых не выявили нейтрализующих антител против AAV1, рандомизировали для интракоронарного введения AAV1.SERCA2a в разных дозах или плацебо. В течение 6 мес наблюдалась тенденция к уменьшению частоты клинических событий. Эта тенденция подтвердилась при более длительном наблюдении пациентов (K. Zsebo et al., 2014). Количество повторных сердечно-сосудистых событий было достоверно меньшим в группе высокодозовой терапии AAV1.SERCA2a по сравнению с группой плацебо. Изучение трансгенной экспрессии в подгруппе пациентов, у которых проводился забор ткани миокарда, подтвердило длительную (до 31 мес) персистенцию AAV.
Впоследствии было спланировано более крупное исследование CUPID2, в котором оценивалось влияние интракоронарного введения AAV1.SERCA2a в дозе 1×1013 ДНКазо-резистентных частиц на клинические исходы у пациентов с СН поздних стадий (B. Greenberg et al., 2016). CUPID2 — двойное слепое плацебо-контролируемое рандомизированное многоцентровое международное исследование IIb фазы. Включали пациентов со стабильным течением СН II-IV функциональных классов по NYHA ишемической или неишемической этиологии, с фракцией выброса (ФВ) ЛЖ <35%. 250 пациентов рандомизировали в соотношении 1:1 на базе более 50 клинических центров США и Европы. По первичной конечной точке — времени до повторных событий, связанных с СН, — между группами не было получено статистически достоверных различий (отношение рисков 0,93; 95% доверительный интервал 0,53-1,65; р=0,81). По вторичным конечным точкам, включая время до первого терминального события, группы также не различались. В целом результаты CUPID2 были нейтральными и не подтвердили эффективность генного переноса AAV1.SERCA2a в улучшении клинических исходов у пациентов с СН.
Начаты два других исследования AAV1.SERCA2a. AGENT-HF (NCT01966887) — одноцентровое двойное слепое рандомизированное плацебо-контролируемое исследование, в котором изучается влияние генной терапии AAV1.SERCA2a на объемы и функцию сердца с использованием разных модальностей кардиальной визуализации. Компьютерная томография с выполнением 256 срезов определяет изменения конечно-систолических объемов ЛЖ в течение 6 мес после генного переноса. В исследовании SERCA-LVAD (NCT00534703) изучаются эффекты генной терапии AAV1.SERCA2a у пациентов с СН, которым были имплантированы устройства помощи ЛЖ (LVAD). Оценивается степень восстановления сократительной функции миокарда при попытках отключения LVAD. Однако набор пациентов в оба исследования был приостановлен после получения нейтральных результатов CUPID2. Ожидается подробный анализ данных CUPID2 для объяснения причин нейтральных результатов.
Клинические исследования с SDF‑1 (STOP-HF, RETRO-HF)
После положительных результатов пилотного исследования I фазы с использованием разных доз плазмидного генетического материала, кодирующего SDF‑1, было проведено рандомизированное двойное слепое плацебо-контролируемое исследование II фазы STOP-HF. В нем оценивали безопасность и эффективность однократного переноса гена SDF‑1 пациентам с ишемической СН и ФВ ЛЖ ≤40% (E.S. Chung et al., 2015). Материал вводили посредством 15 эндомиокардиальных инъекций. Тестировали две дозы pSDF‑1 (15 и 30 мг), каждую из которых сравнивали с плацебо. Общее количество пациентов — 93.
Комбинированная первичная конечная точка включала различия изменений дистанции 6-минутной ходьбы и результатов Миннесотского опросника качества жизни с СН по сравнению с группой плацебо на четвертом месяце. В результате по первичной конечной точке различий между группами получено не было (р=0,89).
У пациентов с наименьшими исходными значениями ФВ ЛЖ (<26%) терапия pSDF‑1 в дозе 30 мг вызвала достоверное увеличение этого показателя на 11% (р=0,01) по сравнению с плацебо. Этот эффект, однако, наблюдался через 1 год после введения pSDF‑1, в то время как экспрессия данного вектора на доклинических моделях ишемической СН продолжалась менее 1 мес. Ретроградные инфузии pSDF‑1 в настоящее время изучаются в похожем исследовании RETRO-HF.
Продолжающиеся и ожидаемые клинические исследования сердечно-сосудистой генной терапии
После положительных результатов доклинических экспериментов на крупных животных (S.T. Pleger et al., 2011) продолжается работа по генно-терапевтическому продукту AAV9-S100A1, вызывающему гиперэкспрессию кальций-модулирующего протеина S100A1. В ближайшие годы ожидается старт первого клинического исследования.
Планируется клиническое исследование реинжинирингового вектора AAV (AAV2i8) с высокой тропностью к сердцу (K. Ishikawa et al., 2014). Полезной нагрузкой будет ген I1c, безопасность переноса которого будет оцениваться в четырех разных дозах у 12 пациентов с далеко зашедшей СН.
Эффекты гиперэкспрессии человеческой AC6 при переносе гена AC6 интракоронарным путем изучаются в рандомизированном плацебо-контролируемом исследовании I-II фазы у пациентов с хронической СН (NCT00787059). Эффективность и безопасность должны быть оценены через 4 и 12 нед после введения. Набор пациентов завершен, и результаты этого исследования ожидаются в скором времени.
Нерешенные проблемы и будущие возможности
Несмотря на обнадеживающие результаты, полученные в экспериментах на адекватных моделях у крупных животных, а также в небольших клинических исследованиях I и ранней II фазы, ни одно из более крупных исследований II фазы не подтвердило пользу генной терапии у пациентов с СН. Отрицательные результаты могут быть обусловлены многими факторами. В исследовании CUPID захват вирусных векторов миокардом варьировал от <20 до 561 копий на 1 мг ДНК. Это намного меньше, чем наблюдалось на моделях у животных (20 000-350 000 копий вектора на 1 мг ДНК) и соответствует инфицированию менее 1% кардиомиоцитов.
Данный уровень инфицирования, скорее всего, не способен вызвать сколь-либо заметные изменения глобальной функции желудочка сердца. Возможно, требуется более высокая доза (>1×1013 частиц), однако при близких к 1×1014 значениях может произойти активация Т-клеточного иммунного ответа.
Данные, полученные на свиньях, овцах, собаках и даже приматах, не означают, что похожие результаты будут получены у людей. Несоответствия обусловлены различиями инфицирующей способности, разнообразием и сложностью происхождения заболевания у человека, а также различиями конечных точек. Возможно, для исследований необходимо отбирать более специфические подгруппы пациентов с СН. Ожидается, что детальный анализ данных CUPID2 прольет свет на эти вопросы и даст ключ к совершенствованию генной терапии.
В предстоящих клинических исследованиях будут изучаться новые мишени генной терапии, которые продемонстрировали обнадеживающие результаты в экспериментах на крупных животных. И в этих исследованиях будут применяться более кардиоспецифичные векторы, чем в CUPID. Кроме того, ведется работа по оптимизации методов доставки. Также необходимо разработать стратегии преодоления гуморального иммунитета к AAV, поскольку значительная доля пациентов имеет нейтрализующие антитела ко всем серотипам вируса. Возможные пути решения проблемы — применение плазмафереза, введение пустых капсидов для абсорбирования анти-ААV-антител перед инъекцией генно-инженерного материала, а также разработка новых векторов, ускользающих от иммунного контроля.
Заключение
Несмотря на обескураживающие результаты CUPID2, авангард генной терапии сердца продолжает движение вперед. Получена ценная информация о том, что векторы на основе AAV способны доставить генетический материал в кардиомиоциты, и это вмешательство является безопасным для пациентов с СН. Обозначилась потребность в новых векторах с высокой тропностью к сердцу и способностью ускользать от иммунной защиты реципиента. Достижение высокой эффективности трансдукции генного материала является первостепенной задачей для обеспечения клинически значимых результатов. При использовании улучшенных векторов, новых мишеней и более эффективных технологий доставки в исследованиях с участием тщательно отобранных групп пациентов ожидается получить доказательства терапевтической пользы генной терапии уже в ближайшие годы.
European Heart Journal, 2016; 37: 1651-1658.
Сокращенный перевод с англ. Дмитрия Молчанова