2 квітня, 2017
Сірководень – нова мішень антигіпертензивної та антиангінальної терапії
Зофеноприл – сучасний інгібітор ангіотензинперетворювального ферменту (ІАПФ), прийом якого може знижувати смертність і захворюваність хворих на гострий інфаркт міокарду (ІМ) більшою мірою, ніж інші ІАПФ. Від решти препаратів цього класу він відрізняється наявністю двох сульфгідрильних груп. Зофеноприл є унікальним ІАПФ, оскільки він підвищує біодоступність двох дуже важливих сигнальних молекул – сірководню (H2S) та оксиду азоту (NO) – через брадикінінзалежну систему.
Якщо роль NO в патогенезі захворювань серцево-судинної системи добре відома широкому колу лікарів, то далеко не всі поки що мають чітке уявлення щодо патофізіологічного значення іншої субстанції – H2S, яка, так само як і молекула NO, належить до класу так званих газотрансмітерів, або ендогенних газів. Традиційно до газотрансміттерів відносять оксид азоту, оксид вуглецю і сірководень, патофізіологічне значення якого було розкрите останньою з трьох вищезгаданих молекул. Ці газоподібні речовини утворюються ендогенно (причому ферментативним шляхом), а не надходять ззовні, їхні ефекти не залежать від впливу на мембранні рецептори.
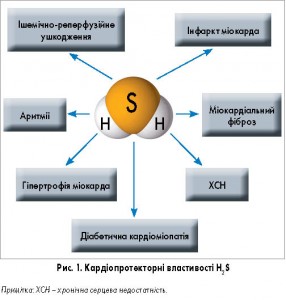 Ендогенний сірководень сьогодні вважається одним з важливих факторів, що захищають організм від серцево-судинних захворювань. Недавні дослідження показали, що H2S може мати протекторний ефект на міокард при інфарктах, аритміях, гіпертрофії, фіброзі, ішемічно-реперфузійних ушкодженнях і серцевій недостатності. Деякі механізми (рис. 1), такі як антиоксидантна дія, збереження функції мітохондрій, захист від апоптозу, протизапальні властивості, позитивний вплив на процеси ангіогенезу, здатність регулювати функцію іонних каналів, а також взаємодія з NO, можуть відповідати за кардіопротекторну дію H2S. Цікаво, що відомі кардіопротекторні властивості часнику, як виявилося, пов’язані з розпадом полісульфідних груп саме до сірководню.
Ендогенний сірководень сьогодні вважається одним з важливих факторів, що захищають організм від серцево-судинних захворювань. Недавні дослідження показали, що H2S може мати протекторний ефект на міокард при інфарктах, аритміях, гіпертрофії, фіброзі, ішемічно-реперфузійних ушкодженнях і серцевій недостатності. Деякі механізми (рис. 1), такі як антиоксидантна дія, збереження функції мітохондрій, захист від апоптозу, протизапальні властивості, позитивний вплив на процеси ангіогенезу, здатність регулювати функцію іонних каналів, а також взаємодія з NO, можуть відповідати за кардіопротекторну дію H2S. Цікаво, що відомі кардіопротекторні властивості часнику, як виявилося, пов’язані з розпадом полісульфідних груп саме до сірководню.
Серед величезного розмаїття біологічних функцій цієї молекули особливе місце приділяють її ролі в регуляції роботи серцево-судинної системи, зокрема в забезпеченні нормального рівня артеріального тиску (АТ). Виявлення такої властивості молекули H2S поклало початок новому напряму у фармакології, пов’язаному з пошуком і створенням принципово нової групи антигіпертензивних препаратів, дія яких ґрунтувалася б на вивільненні молекул H2S.
H2S, як і NO, бере участь у регуляції артеріального тонусу, зумовлюючи розслаблення непосмугованих м’язів судин. Водночас молекулярні механізми дії H2S ще донедавна залишалися нерозкритими. Якщо NO спричиняє розслаблення судин, активуючи фермент непосмугованих м’язів гуанілатциклазу, то H2S викликає той же ефект зовсім іншим шляхом. Під дією H2S, що синтезується ферментативним шляхом, підвищується проникність так званих АТФ-залежних калієвих каналів білкових комплексів, вбудованих у мембрану клітин (зокрема, непосмугованих м’язів судин), які пропускають іони калію. У результаті вихід калію з клітини посилюється, її заряд змінюється. Це призводить до зниження проникності інших – кальцієвих – каналів. Як наслідок, вхід кальцію в клітину знижується, а це сприяє розслабленню непосмугованих м’язів і розширенню судин. В експериментах у мишей з підвищеним АТ, зумовленим віковими змінами судин, при введенні сірководню тиск знижувався, що дозволило зробити висновок про важливу роль H2S у регуляції рівня АТ. Нещодавно був виявлений фермент цистатіонін-гамма-ліаза, що відповідає за утворення сірководню в клітинах непосмугованих м’язів. У подальшому він був знайдений і в ендотеліальних клітинах як експериментальних тварин, так і людини, причому навіть у більшій кількості, ніж у непосмугованих м’язах.
Сірководень не лише сприяє вазорелаксації, він має ще й протизапальну дію, механізм якої пов’язують зі здатністю H2S нейтралізувати прояви запалення, індуковані інтерлейкіном-1.
Цікаво звернути увагу на низку недавніх досліджень, результати яких забезпечили розуміння захисної дії H2S в розвитку ішемічно-реперфузійних ушкоджень міокарда. Було продемонстровано, що H2S покращує відповідь інтими на гіперплазію в кровоносних судинах після балонно-опосередкованого ушкодження судин. Крім того, встановлено, що фізіологічно відповідні дози H2S сприяють посиленню ангіогенезу. Таким чином, H2S може виявитися корисним для гальмування рестенозу коронарних артерій та індукції ангіогенезу.
Профілактичне введення речовин, що є донорами H2S, зменшує частоту виникнення реперфузійних аритмій і покращує виживаність міоцитів. Декілька років тому в експериментах на тваринах було продемонстровано, що болюсна ін’єкція речовини – донора H2S як до початку ішемії, так і під час реперфузії має помітний позитивний вплив на розвиток ішемічно-реперфузійних ушкоджень.
Обидві молекули – H2S і NO – мають потужну цитопротекторну та антиоксидантну дію, що в клінічній практиці трансформується в антиангінальний і антиішемічний ефекти. Так, в одному з клінічних досліджень порівнювали результативність двох ІАПФ, зофеноприлу і периндоприлу, у хворих зі стабільною стенокардією та артеріальною гіпертензією. Було показано, що лише прийом зофеноприлу забезпечував підвищення стійкості ліпопротеїнів низької щільності до переокислення, що свідчило про зменшення інтенсивності процесу перекисного окислення ліпідів (ПОЛ). Своєю чергою, зменшення накопичення високотоксичних продуктів ПОЛ у судинній стінці найсприятливішим чином позначалося на вазодилатуючих властивостях ендотелію, що супроводжувалося поліпшенням показника ендотелійзалежної вазодилатації артерій. Так, показник потікзалежної дилатації плечової артерії (ПЗВД) у хворих, які приймали зофеноприл, достовірно збільшився майже на третину, при цьому прийом периндоприлу не впливав на ПВЗД. Відсутність здатності несірковмісних ІАПФ впливати на даний показник була продемонстрована й на фоні лікування раміприлом. Більш того, тільки зофеноприл зменшував експресію так званих молекул адгезії, що відіграють ключову роль у запаленні судин, пов’язаному з артеріальною гіпертензією (АГ) та атеросклерозом.
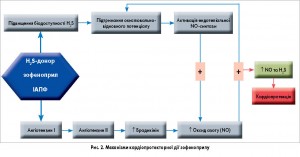 Цікаво, що кардіо- та вазопротекторна дія зофеноприлу не залежить від його антигіпертензивної активності, зумовленої блокадою ренін-ангіотензин-альдостеронової системи (РААС). У реалізації судинних ефектів зофеноприлу певне значення може мати і його високий рівень ліпофільності, в декілька разів вищий, ніж у раміприлу та периндоприлу. Ця властивість дозволяє препарату проникати в клітини й ефективно пригнічувати активність тканинних РААС. Крім того, як уже зазначалося вище, зофеноприл стимулює здатність ендотелію судин до ангіогенезу. На рисунку 2 відображені найактуальніші з клінічної точки зору механізми дії зофеноприлу.
Цікаво, що кардіо- та вазопротекторна дія зофеноприлу не залежить від його антигіпертензивної активності, зумовленої блокадою ренін-ангіотензин-альдостеронової системи (РААС). У реалізації судинних ефектів зофеноприлу певне значення може мати і його високий рівень ліпофільності, в декілька разів вищий, ніж у раміприлу та периндоприлу. Ця властивість дозволяє препарату проникати в клітини й ефективно пригнічувати активність тканинних РААС. Крім того, як уже зазначалося вище, зофеноприл стимулює здатність ендотелію судин до ангіогенезу. На рисунку 2 відображені найактуальніші з клінічної точки зору механізми дії зофеноприлу.
Для вивчення питання щодо зниження загального ішемічного ризику при застосуванні ІАПФ, що містять SH-групу, було проведено спеціально сплановане дослідження SMILE-3, присвячене саме антиішемічним ефектам нової на той час молекули – зофеноприлу. У цьому рандомізованому подвійному сліпому плацебо-контрольованому дослідженні брали участь 349 хворих з ішемічною хворобою серця (ІХС) через 6 тиж після перенесеного гострого ІМ із фракцією викиду лівого шлуночка (ЛШ) >40%, тобто хворі без ХСН. Пацієнти були розподілені на дві групи: стандартної терапії + зофеноприл (30-60 мг/добу) та стандартної терапії + плацебо. Період спостереження тривав 6 міс. Первинною кінцевою точкою були різні клініко-інструментальні прояви ішемії міокарда, а саме: нові ішемічні зміни на стандартній ЕКГ (12 відведень), нові зміни сегмента ST-T при 48-годинному моніторуванні ЕКГ, ЕКГ-ознаки і симптоми стенокардії при пробі з навантаженням, повторний ІМ, потреба в процедурах реваскуляризації міокарда через стенокардію або інші клінічні ознаки ішемії міокарда.
У дослідженні SMILE-3 були переконливо продемонстровані потужні антиішемічні ефекти зофеноприлу у хворих із хронічними формами ІХС, які раніше перенесли гострий ІМ. Через 6 міс терапії в групі пацієнтів, які отримували зофеноприл, відбулося достовірне зменшення первинної кінцевої точки на 48%, а також багатьох її складових. Депресія сегмента ST при амбулаторному запису ЕКГ спостерігалась у 10,7% хворих у групі зофеноприлу проти 22,2% пацієнтів у групі плацебо (р=0,027). У групі зофеноприлу відмічалося суттєве зменшення тривалості ЕКГ-проявів ішемії. Достовірно рідше у хворих групи зофеноприлу мали місце випадки ангінозного болю в грудній клітці (4,7 проти 14,3%; р=0,024). Частота шлуночкових аритмій також була значно нижчою в групі зофеноприлу (3,8 проти 10,5% в групі плацебо; р=0,048).
Зниження ризику виникнення основних серцево-судинних подій у групі зофеноприлу становило 64,6% (4,5% пацієнтів у групі зофеноприлу мали ускладнення проти 12,7% учасників у групі плацебо; р=0,041). Ще раз слід звернути особливу увагу на той факт, що в цьому дослідженні зофеноприл призначався за показанням ІХС, а не у зв’язку з наявністю зниження фракції викиду ЛШ.
Розглядаючи можливості та переваги зофеноприлу в лікуванні хворих на ІХС, не можна не зупинитися ще на одній дуже важливій і досить поширеній у повсякденній клінічній практиці проблемі. Йдеться про розвиток толерантності до нітратів – поступове зниження їх антиангінальних і гемодинамічних ефектів у разі тривалого застосування. Не секрет, що, незважаючи на широке впровадження в клінічну практику сучасних препаратів, які довели свій вплив на клінічні прояви і прогноз ІХС, поширеність призначення нітратів як симптоматичних засобів залишається високою. Багато хворих зберігають прихильність до застосування антиангінальних засобів цього класу. Однак, як згадувалося раніше, їх довгостроковий прийом часто призводить до розвитку толерантності, частота якої, за даними різних авторів, сягає 60-75%, при цьому повна відсутність терапевтичного ефекту реєструється в 10-15% спостережень.
Механізми розвитку толерантності до нітратів складні, наразі є декілька гіпотез, що пояснюють цей феномен. Одна з них – метаболічна, згідно з якою постійно високий рівень нітратів у крові веде до виснаження запасів SH-груп, що забезпечують перетворення молекул нітратів у NO, внаслідок чого знижується реактивність судин і послаблюється вазодилатуюча дія нітратів. Це супроводжується зниженням ниркового кровотоку і підвищенням продукції контррегуляторних нейрогуморальних факторів у нирках. У першу чергу підвищується активність РААС. Саме ці механізми багато в чому пояснюють той факт, що для подолання толерантності до нітратів поряд з іншими заходами використовують призначення так званих препаратів-коректорів, які можуть служити донорами SH-груп. Безперечно, до таких препаратів належать ІАПФ, що містять SH-групу, – каптоприл і зофеноприл. Саме завдяки наявності в молекулі двох сульфгідрильних груп зофеноприл може посилювати вплив нітратів на ендотелійрелаксуючий фактор, що було показано в експериментальних і клінічних дослідженнях. У клінічній практиці це дозволяє підвищити толерантність до фізичних навантажень при тривалому лікуванні нітратами незалежно від системних судинних ефектів. З огляду на те, що зофеноприл може зменшувати кількість ангінозних нападів більше ніж утричі, і з урахуванням його здатності гальмувати розвиток толерантності до нітратів є всі підстави розглядати саме цю молекулу як ІАПФ вибору в пацієнтів з вираженими клінічними проявами хронічної ІХС.
Крім того, ефективність зофеноприлу на відміну від такої більшості ІАПФ не зменшується при одночасному прийомі з аспірином, що дуже важливо саме у хворих на ІХС, оскільки практично всі вони повинні приймати аспірин, а більшість з них – й ІАПФ. Усе це робить зофеноприл привабливим препаратом не тільки для лікування хворих на АГ, але й для вторинної профілактики ІХС.
Медична газета «Здоров’я України 21 сторіччя» № 5 (402), березень 2017 р.


