15 березня, 2017
Кардиологический пациент перед хирургическим вмешательством: коррекция терапии и профилактика осложнений

17 ноября 2016 г. в преддверии традиционной конференции «Дни аритмологии в Киеве», которую ежегодно проводит Ассоциация аритмологов Украины, на базе киевского Института сердца состоялся мультидисциплинарный симпозиум «Медикаментозное сопровождение и осложнения кардиохирургических вмешательств». Кардиохирурги, кардиологи, анестезиологи и терапевты приняли участие в обсуждении различных аспектов предоперационной подготовки и профилактики осложнений у пациентов с сердечно-сосудистыми заболеваниями.
 Генеральный директор ГУ «Институт сердца МЗ Украины», член-корреспондент НАМН Украины, доктор медицинских наук, профессор Борис Михайлович Тодуров во вступительной лекции охарактеризовал достижения и проблемы украинской кардиохирургии, а также поделился опытом внедрения перспективных технологий лечения в клинике Института сердца.
Генеральный директор ГУ «Институт сердца МЗ Украины», член-корреспондент НАМН Украины, доктор медицинских наук, профессор Борис Михайлович Тодуров во вступительной лекции охарактеризовал достижения и проблемы украинской кардиохирургии, а также поделился опытом внедрения перспективных технологий лечения в клинике Института сердца.
Кардиохирургические центры Украины еще очень далеки от показателей европейских стран по охвату населения необходимыми видами вмешательств, в частности при такой социально значимой патологии, как ишемическая болезнь сердца (ИБС). При потребности 200 тыс. коронарографий в год реально выполняется около 29 тыс. процедур, операций на сердце – 140 и 24 тыс. соответственно. Региональную представленность центров кардиохирургической помощи лектор охарактеризовал как «вынужденную централизацию»: три мощнейших клиники находятся в г. Киеве, в то время как на больших территориях страны население вообще не имеет доступа к центрам кардиохирургии в радиусе 90 км, что делает невозможной доставку в течение 2 ч для проведения экстренной реваскуляризации при остром инфаркте миокарда (ОИМ).
Вместе с тем крупные центры демонстрируют высокие показатели выживаемости и реабилитации пациентов после хирургического лечения ИБС. В Институте сердца выполняется около трети всех операций аортокоронарного шунтирования (1235 за 2015 г.) и практически каждое пятое стентирование коронарных артерий в стране (1693 вмешательства за 2015 г.). С 2014 г. действует программа «Стоп инфаркт», по которой клиника дежурит в режиме 24 ч в сутки 7 дней в неделю, принимая больных с ОИМ для проведения ургентной коронарографии и стентирования или аортокоронарного шунтирования.
Госпитальную летальность при ОИМ удалось снизить до 4,2% за счет спасения пациентов с кардиогенным шоком и поражениями коронарных артерий сложных локализаций, что стало возможным благодаря внедрению методов временной поддержки кровообращения – экстракорпоральной мембранной оксигенации (ЭКМО) и внутриаортальной баллонной контрапульсации.
Из достижений последних лет профессор Б.М. Тодуров отметил освоение специалистами Института сердца прогрессивных методик операций на крупных сосудах и клапанах сердца: эндоваскулярного протезирования дуги аорты с брахиоцефальными сосудами и брюшного отдела аорты при больших аневризмах, операции Дэвида (протезирование восходящей аорты без замены клапана) и операции Озаки (формирование аортального клапана из аутоперикарда), а также первые успешные имплантации механических устройств поддержки желудочков сердца, выполненные в 2016 г. Следует также упомянуть о разработке материалов и устройств для нужд кардиохирургии украинского производства, которые, возможно, станут заменой дорогостоящих импортных аналогов. Это опорные кольца для пластики клапанов сердца, кава-фильтры для профилактики венозной тромбоэмболии.
 Заведующий кафедрой анестезиологии и интенсивной терапии НМАПО им. П.Л. Шупика, доктор медицинских наук, профессор Олег Анатольевич Лоскутов осветил вопросы профилактики кардиальных осложнений в общей хирургии. Осложнения со стороны сердечно-сосудистой системы составляют до 42% от всех периоперационных осложнений. Например, у пациента, который перенес ИМ за 3 мес до операции, риск получить повторный интраоперационный ИМ достигает 30%, по данным статистики общей анестезиологической практики.
Заведующий кафедрой анестезиологии и интенсивной терапии НМАПО им. П.Л. Шупика, доктор медицинских наук, профессор Олег Анатольевич Лоскутов осветил вопросы профилактики кардиальных осложнений в общей хирургии. Осложнения со стороны сердечно-сосудистой системы составляют до 42% от всех периоперационных осложнений. Например, у пациента, который перенес ИМ за 3 мес до операции, риск получить повторный интраоперационный ИМ достигает 30%, по данным статистики общей анестезиологической практики.
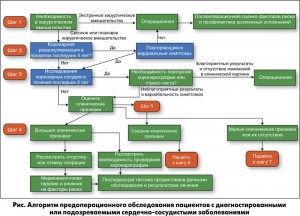
Безусловно, риск осложнений определяется объемом хирургического вмешательства, величиной кровопотери, длительностью и видом анестезии. Однако европейские рекомендации по предоперационной подготовке кардиологических больных (ESC/ESA, Eur. Heart. J. 2014; 35: 2383-2431) исходят из того, что пациент-специфические факторы более значимы для оценки риска и возможности выполнения вмешательства, чем вид операции. Разработан четкий алгоритм принятия решений, основанный на данных анамнеза и клинических признаках сердечно-сосудистой патологии (рис.).
Большие клинические признаки, при наличии которых оперативное вмешательство однозначно противопоказано до стабилизации состояния больного, – это острый или свежий (от 7 до 30 дней) ИМ, нестабильная или тяжелая стенокардия, декомпенсированная сердечная недостаточность (СН), угрожающие аритмии и тяжелая клапанная патология.
К средним клиническим признакам относятся легкая стенокардия (II класс по канадской классификации), ИМ в анамнезе или патологический зубец Q на электрокардиограмме, компенсированная СН, инсулин-зависимый сахарный диабет, почечная недостаточность (креатинин ≥2 мг/дл). При наличии признаков этой группы следует перейти к шагу 6 – определению функциональных возможностей пациента (толерантности к нагрузкам) согласно методике метаболических эквивалентов (МЭ).
При оценке <4 МЭ в сочетании со средними клиническими признаками рекомендуется отсрочка операции до стабилизации состояния пациента оптимальной медикаментозной терапией. При оценке >4 МЭ (полное самообслуживание, возможность выполнять легкую работу по дому и подняться по лестнице на 1 этаж) пациента можно оперировать, если хирургический риск операции средний или низкий. Если же планируемая операция относится к категории высокого хирургического риска, то для уточнения степени сердечно-сосудистого риска и принятия дальнейших решений показано нагрузочное тестирование, по результатам которого также может быть рассмотрена необходимость выполнения коронарографии.
Авторы европейских рекомендаций вместе с тем отмечают, что применение инвазивного метода может вызвать ненужную и непредсказуемую задержку выполнения уже запланированной операции, к тому же коронарография сама по себе может вызвать осложнения, которые дополняют периоперационный риск. Поэтому диагностические тесты должны назначаться только в том случае, если полученные с их помощью результаты повлияют на тактику периоперационного ведения пациента.
Показания класса I (настоятельно рекомендуется) для проведения коронарографии при подготовке к плановой операции следующие:
– стенокардия, стойкая к лекарственной терапии;
– нестабильная стенокардия при планировании операции средней или высокой степени хирургического риска;
– сомнительные результаты неинвазивных тестов при высокой степени хирургического риска.
Комментируя набор обязательных предоперационных лабораторных анализов у пациентов с сердечно-сосудистыми заболеваниями, лектор обратил внимание на то, что анемия (гемоглобин <110 г/л, эритроциты <2,5×1012/л) ограничивает доставку кислорода к миокарду в условиях гипоперфузии и поэтому требует обязательной коррекции перед вмешательством.
Также перед плановой операцией следует убедиться в том, что содержание тромбоцитов в крови составляет не менее 150×109/л. Диуретическая терапия, например, у пациентов с СН, существенно влияет на электролитный состав крови. Согласно американским стандартам подготовки пациента анестезиолог не может начинать вводный наркоз при уровне сывороточного калия <4 ммоль/л. Низкое содержание калия может иметь фатальные последствия из-за высокого риска жизнеугрожающих нарушений сердечного ритма.
Успех операции во многом зависит от совместного планирования сопровождающей терапии хирургом, анестезиологом и лечащим врачом, который ведет пациента. Первое и обязательное условие безопасного гемостаза – это своевременная отмена антикоагулянтов и антиагрегантов перед операцией (табл.).
Рекомендации по новым оральным антикоагулянтам (дабигатран, ривароксабан, апиксабан):
– при операциях без значимого риска кровотечений (офтальмологические, поверхностные, дерматологические) отменить за 18-24 ч, продолжить прием через 6 ч;
– при минимальном риске кровотечений (биопсии, грыжесечение) отменить за 24 ч или раньше, продолжить прием через 24 ч;
– при высоком риске кровотечений (операции в брюшной полости, грудной клетке, нейрохирургия) отменить за 48 ч или раньше, продолжить прием через 48-72 ч при условии стабильного гемостаза.
 О значении артериальной гипертензии (АГ) как фактора операционного риска и принципах периоперационной коррекции антигипертензивной терапии более подробно рассказала руководитель отдела гипертонической болезни ГУ «ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины», доктор медицинских наук, профессор Евгения Петровна Свищенко.
О значении артериальной гипертензии (АГ) как фактора операционного риска и принципах периоперационной коррекции антигипертензивной терапии более подробно рассказала руководитель отдела гипертонической болезни ГУ «ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины», доктор медицинских наук, профессор Евгения Петровна Свищенко.
АГ не относится к большим факторам операционного риска, но повышает вероятность осложнений или смерти после операции на 35% по сравнению с нормотензивными пациентами. Особенно плохой прогноз у пациентов с высоким пульсовым давлением; это, как правило, лица пожилого возраста с атеросклерозом и повышенной жесткостью сосудов. Последствия неконтролируемой АГ можно условно разделить на две группы: обусловленные операцией (кровотечение, расхождение швов, расслоение аорты) и обусловленные поражением органов-мишеней (ИМ, инсульт, почечная недостаточность, острая СН).
У всех пациентов с АГ при планировании операции обязательно следует оценить уровень креатинина в сыворотке крови и скорость клубочковой фильтрации (СКФ), так как скрытое поражение почек в виде микроальбуминурии или снижения СКФ <60 мл/мин согласно данным исследований обнаруживается у 42% больных, а почечная недостаточность входит в число больших факторов операционного риска. Также целесообразно выполнить электро- и эхокардиографическое исследования для оценки степени дисфункции левого желудочка.
АГ 1 и 2 степени (артериальное давление (АД) <180/110 мм рт. ст.) не является поводом для отсрочки оперативного вмешательства. Только при АГ 3 степени операцию по возможности следует отложить для оптимизации терапии и снижения АД.
Что касается лечения АГ в предоперационном периоде, то нет доказательств преимущества одних антигипертензивных препаратов перед другими. Долгое время бета-адреноблокаторы (БАБ) считались обязательным компонентом предоперационной подготовки пациентов с высоким сердечно-сосудистым риском. Эти рекомендации основывались на результатах нескольких исследований, которые продемонстрировали снижение послеоперационной смертности в результате назначения БАБ. Но в исследовании POISE при приеме метопролола (100 мг до и 100 мг после операции) смертность увеличилась на 33%, а частота инсультов – в 2 раза. Поэтому вопрос пользы или вреда БАБ на сегодняшний день остается открытым.
Европейские рекомендации (ESC/ESA, 2014) сформулированы так:
– продолжать прием, если БАБ был назначен ранее для лечения АГ, ИБС, аритмии или СН;
– можно рассмотреть начало приема БАБ перед операцией у пациентов с АГ, ИБС, СН, но начинать не менее чем за 24 ч до операции, лучше за 7-30 дней с постепенной титрацией дозы;
– не начинать лечение БАБ в день операции;
– не начинать лечение БАБ перед операцией низкого хирургического риска.
Ингибиторы ангиотензинпревращающего фермента (АПФ) и блокаторы рецепторов ангиотензина II (БРА) вызывают гипотензию во время анестезии. Согласно европейским рекомендациям (ESC/ESA, 2014) у пациентов с АГ следует временно отменять ингибиторы АПФ за 24 ч до операции и возобновлять прием как можно раньше после вмешательства, но при условии стабильного АД и нормоволемии. Исследование VISION (2016) подтвердило, что отмена ингибиторов АПФ или БРА за сутки до операции уменьшает риск смерти и сердечно-сосудистых осложнений на 18%, а риск гипотензии – на 20%. У пациентов с СН, которые постоянно принимают ингибиторы АПФ, следует рассмотреть возможность продолжения терапии перед операцией под контролем гемодинамики. Начинать терапию ингибиторами АПФ или БРА у пациентов с СН следует не ранее чем за неделю до плановой операции.
Не рекомендуется назначать дигидропиридиновые антагонисты кальция короткого действия перед операцией. Больные, которые не переносят БАБ, могут продолжать прием недигидропиридиновых препаратов; при необходимости их прием можно инициировать перед операцией.
Прием диуретиков для лечения СН можно продолжать до дня операции, но не принимать в день операции, так как гиповолемия затрудняет работу анестезиолога. Электролитные нарушения (гипокалиемию, гипомагниемию) следует устранить до операции.
Если пациент принимает статины, не следует прерывать лечение перед операцией. Перед плановой операцией на сосудах рекомендуется назначить статины, если пациент их еще не принимал, но не менее чем за 2 нед. Убедительно доказано, что статины уменьшают риск развития ИМ, инсультов и снижают смертность в послеоперационном периоде, вероятно, за счет стабилизации атеросклеротических бляшек.
Как правило, чтобы добиться быстрой стабилизации АД, особенно при исходно высоких значениях, приходится сразу назначать комбинированную антигипертензивную терапию. Фиксированные комбинации повышают приверженность, помогают быстрее достигать целевых уровней АД и удерживать их длительное время. В Украине появилась первая трехкомпонентная фиксированная комбинация отечественного производства – препарат Тиара Трио (Фармацевтична фірма «Дарниця»), который содержит в одной таблетке 160 мг валсартана, 5 или 10 мг амлодипина и 12,5 мг гидрохлортиазида. Сочетание БРА, антагониста кальция и диуретика признано лучшей комбинацией для нормализации АД при исходных цифрах 180/110 мм рт. ст. и выше. В сравнении с импортными аналогами Тиара Трио значительно доступнее по цене для украинских пациентов.
Эффективность препарата изучалась в предрегистрационном многоцентровом исследовании, проведенном по поручению Фармкомитета МЗ Украины. В рамках исследования за 28 дней было достигнуто снижение среднесуточного систолического АД на 15 мм рт. ст., диастолического – на 13 мм рт. ст. согласно данным амбулаторного мониторирования. Важно отметить, что лечение препаратом Тиара Трио обеспечивало нормализацию суточного профиля АД, включая значимое снижение показателей в ночное время, в том числе у пациентов, которые исходно оценивались как нон-дипперы. Также очень важно, что было достигнуто снижение вариабельности АД. Среди всех параметров, определяемых при суточном мониторировании, вариабельность АД в наибольшей степени влияет на прогноз пациентов. Высокая вариабельность АД связана с повышением риска развития мозговых инсультов в 5-6 раз (P.M. Rothwell, 2010). Специальные исследования показали, что на вариабельность АД практически не влияет монотерапия такими препаратами, как БАБ, ингибиторы АПФ и БРА; в то же время диуретики и антагонисты кальция, в частности амлодипин, существенно снижают этот показатель (T.R. Smith, 2013).
Вероятно, за счет наличия в составе амлодипина и гидрохлортиазида препарат Тиара Трио продемонстрировал выраженное положительное влияние на вариабельность АД в нашем исследовании. Таким образом, препарат Тиара Трио успешно подтвердил высокую антигипертензивную эффективность и рекомендован для применения в Украине.
 Заведующий кафедрой пропедевтики внутренней медицины Винницкого национального медицинского университета им. Н.И. Пирогова, доктор медицинских наук, профессор Юрий Михайлович Мостовой осветил вопросы выбора антибактериальных препаратов для лечения инфекционных осложнений в кардиологии и кардиохирургии.
Заведующий кафедрой пропедевтики внутренней медицины Винницкого национального медицинского университета им. Н.И. Пирогова, доктор медицинских наук, профессор Юрий Михайлович Мостовой осветил вопросы выбора антибактериальных препаратов для лечения инфекционных осложнений в кардиологии и кардиохирургии.
Одно из наиболее частых показаний к антибиотикотерапии – это госпитальная пневмония у пациентов, длительно находящихся на постельном режиме в связи с декомпенсированным заболеванием или в послеоперационном периоде. Согласно украинскому клиническому протоколу (Приказ МЗ Украины № 128 от 19.03.2007) стартовая эмпирическая терапия ранней пневмонии с факторами риска наличия полирезистентных штаммов возбудителей должна включать цефалоспорин с антисинегнойной активностью (цефтриаксон) или защищенный аминопенициллин (амоксициллин/клавуланат, ампициллин/сульбактам) в комбинации с фторхинолоном III-IV поколения (левофлоксацин, моксифлоксацин). Наиболее распространенная схема с хорошо изученной эффективностью и безопасностью – амоксициллин/клавуланат + левофлоксацин.
При инфекционном эндокардите на интактных клапанах или через 12 ч и более после протезирования рекомендуется начинать терапию с комбинации антистафилококковых антибиотиков – ампициллина и оксациллина. Альтернативная комбинация – ванкомицин + гентамицин. При инфекционном эндокардите протезированных клапанов, который развивается позже чем через 12 ч после операции, или у больных с нозокомиальной инфекцией рекомендуется тройная терапия ванкомицин + гентамицин + рифампицин (Рекомендации ESС по лечению инфекционного эндокардита, 2015; Приказ МЗ Украины № 436 от 03.07.2006).
Для лечения гнойного перикардита рекомендуется комбинация ванкомицин + ципрофлоксацин. Альтернативная комбинация – ванкомицин + цефепим. Обязательным является дренирование полости перикарда (Рекомендации ESC по лечению заболеваний перикарда, 2015).
Для профилактики инфекционных осложнений при кардиохирургических вмешательствах рекомендуются три антибиотика – цефазолин, цефуроксим или ванкомицин. В мире самым назначаемым является цефуроксим (1,5 г внутривенно однократно или каждые 12 ч до суммарной дозы 6 г). Его спектр антимикробной активности против грамотрицательных и грамположительных возбудителей более сбалансированный, чем у популярного в Украине цефтриаксона.
Кардиологам и терапевтам важно помнить о некоторых нежелательных взаимодействиях антибиотиков с кардиологическими препаратами. Так, антагонисты кальция в комбинации с макролидами могут вызывать гипотензию. Одновременное лечение цефалоспоринами II-III поколений повышает риск геморрагических осложнений антикоагулянтной и антиагрегантной терапии.
Поэтому, если у пациента с показаниями к приему варфарина или клопидогреля (например, после стентирования) возникает пневмония или отит, лучше назначить альтернативные препараты – защищенные аминопенициллины или левофлоксацин. Также цефалоспорины повышают риск нефротоксичности аминогликозидов, петлевых диуретиков и нестероидных противовоспалительных препаратов.
Респираторные фторхинолоны и макролиды могут удлинять интервал QT и вызывать желудочковую пируэт-тахикардию – редкое, но опасное осложнение, поэтому применение этих антибиотиков у пациентов с нарушениями ритма нежелательно. Из фторхинолонов самым безопасным является моксифлоксацин, а самым сильным проаритмогенным потенциалом обладает ципрофлоксацин.
 Заведующий кафедрой анестезиологии, интенсивной терапии с последипломной подготовкой Одесского национального медицинского университета, доктор медицинских наук, профессор Олег Александрович Тарабрин продемонстрировал возможности низкочастотной пьезоэлектрической тромбоэластографии (НПТГ) в диагностике состояний, связанных с риском тромботических осложнений. На сегодняшний день это золотой стандарт определения гемостатического потенциала в образце цельной крови, который оценивает кинетику тромбообразования в реальном масштабе времени. Результаты тромбоэластографии помогают оперативно контролировать действие антикоагулянтов и антиагрегантов у постели больного и выбирать оптимальную стратегию терапии. Полное исследование занимает 90-95 мин, но в некоторых ситуациях достаточно 20 минут для принятия решений о коррекции терапии. При НПТГ измеряется более 20 показателей, среди которых интенсивность контактной коагуляции (дает представление о тромбоцитарном звене гемостаза), константа тромбиновой активности (характеризует скорость нарастания тромбинообразования, интенсивность протеолитического этапа образования сгустка), интенсивность полимеризации сгустка, время образования поперечно сшитого фибрина, интенсивность ретракции и лизиса сгустка. Лектор продемонстрировал на клинических примерах, как НПТГ помогает индивидуализировать антикоагулянтную и антиагрегантную терапию в сложных случаях.
Заведующий кафедрой анестезиологии, интенсивной терапии с последипломной подготовкой Одесского национального медицинского университета, доктор медицинских наук, профессор Олег Александрович Тарабрин продемонстрировал возможности низкочастотной пьезоэлектрической тромбоэластографии (НПТГ) в диагностике состояний, связанных с риском тромботических осложнений. На сегодняшний день это золотой стандарт определения гемостатического потенциала в образце цельной крови, который оценивает кинетику тромбообразования в реальном масштабе времени. Результаты тромбоэластографии помогают оперативно контролировать действие антикоагулянтов и антиагрегантов у постели больного и выбирать оптимальную стратегию терапии. Полное исследование занимает 90-95 мин, но в некоторых ситуациях достаточно 20 минут для принятия решений о коррекции терапии. При НПТГ измеряется более 20 показателей, среди которых интенсивность контактной коагуляции (дает представление о тромбоцитарном звене гемостаза), константа тромбиновой активности (характеризует скорость нарастания тромбинообразования, интенсивность протеолитического этапа образования сгустка), интенсивность полимеризации сгустка, время образования поперечно сшитого фибрина, интенсивность ретракции и лизиса сгустка. Лектор продемонстрировал на клинических примерах, как НПТГ помогает индивидуализировать антикоагулянтную и антиагрегантную терапию в сложных случаях.
Подготовил Дмитрий Молчанов