14 березня, 2017
Европейские рекомендации по лечению дислипидемий (2016): прежние цели – новые пути
По материалам X ежегодного заседания Украинского общества атеросклероза «Многофакторная профилактика атеросклероза и его осложнений» (23 ноября 2016 года, г. Киев)
Летом 2016 года вышли в свет обновленные рекомендации Европейского общества кардиологов (ESC) и Европейского общества по изучению атеросклероза (EAS) по ведению пациентов с дислипидемиями. В более широком контексте рекомендации ориентированы на предупреждение атеросклероза и его осложнений, поэтому полезны в работе врачей на всех уровнях медицинской помощи.
 Об изменениях, которые произошли в рекомендованных схемах липидоснижающей терапии, сообщил руководитель отдела атеросклероза и хронической ишемической болезни сердца ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины, доктор медицинских наук, профессор Михаил Илларионович Лутай.
Об изменениях, которые произошли в рекомендованных схемах липидоснижающей терапии, сообщил руководитель отдела атеросклероза и хронической ишемической болезни сердца ННЦ «Институт кардиологии им. Н.Д. Стражеско» НАМН Украины, доктор медицинских наук, профессор Михаил Илларионович Лутай.
По сравнению с предыдущей редакцией (2011) новый документ содержит ряд важных изменений и дополнений. Как и прежде, во главу угла поставлена оценка общего сердечно-сосудистого риска. Результаты этой оценки (а не исходный уровень холестерина) служат основанием для принятия решения о назначении статинов. Цели лечения остались практически без изменений, как и принцип интенсивной терапии для их достижения, но изменились рекомендации и по выбору, и по комбинированию традиционных липидоснижающих средств (статинов, ингибиторов абсорбции холестерина), а также предложены схемы терапии с использованием препаратов нового класса – ингибиторов PCSK9. Тем не менее статины остаются основой терапии.
Последовательность действий врача и основные принципы лечения в новых рекомендациях сформулированы следующим образом:
1) оценить общий сердечно-сосудистый риск пациента;
2) вовлечь пациента в решения по управлению факторами риска;
3) определить целевой уровень холестерина липопротеинов низкой плотности (ХС ЛПНП) для данного уровня риска;
4) выбрать статин и дозу, которая могла бы обеспечить необходимое снижение уровня ХС ЛПНП;
5) ответ на лечение статинами является вариабельным, поэтому может потребоваться титрование дозы;
6) если наибольшая переносимая доза статина не позволяет достичь цели, рассмотреть комбинацию препаратов;
7) снижение уровня ХС ЛПНП ≥50% от исходного должно быть достигнуто у пациентов очень высокого и высокого риска.
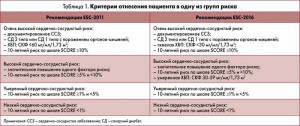
Изменились по сравнению с предыдущими рекомендациями критерии оценки риска, в частности уровень сердечно-сосудистого риска при наличии хронической болезни почек (ХБП) теперь определяется величиной скорости клубочковой фильтрации (СКФ) (табл. 1).
Цели и средства
Авторы рекомендаций еще раз обращают внимание на то, что достижение целевых показателей липидов крови – не самоцель, но важная часть комплексной стратегии снижения сердечно-сосудистого риска, которая должна также включать полноценное питание, умеренные физические нагрузки, контроль массы тела и артериального давления.
Снижение уровня ХС ЛПНП является первичной целью липидоснижающей терапии. Общий холестерин (ОХС) следует рассматривать в качестве цели лечения, если другие показатели не доступны. Аполипопротеин B (Апо-В) следует рассматривать в качестве вторичной цели, только если определение его уровня доступно.
Холестерин липопротеинов высокой плотности (ХС ЛПВП), а также соотношения Апо-B/Апо-A1 или ХС не ЛПВП/ХС ЛПВП не рекомендуются в качестве целей лечения. Не доказано, что повышение уровня ХС ЛПВП с помощью лекарственных средств напрямую ассоциируется с профилактикой сердечно-сосудистых событий, хотя высокие значения этого показателя рассматриваются как благоприятный предиктор. Что касается терапии, направленной на повышение уровня ХС ЛПВП, то никотиновая кислота больше не считается эффективным средством. Статины и фибраты одинаково эффективно повышают ХС ЛПВП.
Липопротеин (а) – независимый генетический фактор риска развития инфаркта миокарда, инсульта, заболеваний периферических артерий, кальцинирующего стеноза аортального клапана. Но его не рекомендуется использовать для скрининга риска в общей популяции.
Категории пациентов, рассматриваемые для скрининга:
– раннее начало ССЗ;
– семейная гиперхолестеринемия;
– раннее ССЗ и/или повышение липопротеина (а) в анамнезе;
– рецидив ССЗ, несмотря на оптимальное гиполипидемическое лечение;
– 10-летний риск развития фатальных ССЗ при оценке по шкале SCORE ≥5%.
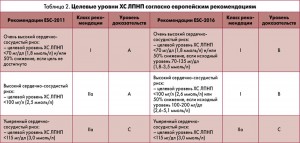
Целевые уровни ХС ЛПНП не изменились, но получили уточнения в новых рекомендациях (табл. 2).
Для достижения поставленных целей настоятельно рекомендуется лечение статином в самой высокой рекомендованной дозе или в наивысшей переносимой дозе (класс рекомендации I, уровень доказательств А).
Данная рекомендация основывается на результатах исследований, которые показали, что интенсивная терапия статинами приводит к клинически значимому снижению уровня атерогенных фракций холестерина, стабилизации атеросклеротических бляшек и даже к уменьшению их размеров. Так, в исследовании ASTEROID у 349 пациентов с ишемической болезнью сердца (ИБС), которые принимали розувастатин в дозе 40 мг в сутки, повторные измерения просвета коронарных артерий с использованием внутрисосудистого ультразвука (IVUS) показали достоверное уменьшение среднего объема атером на 6,1 мм3 за 24 мес. Это происходило на фоне существенного снижения уровня ХС ЛПНП (со 130,4 до 60,8 мг/дл; -53%) и повышения содержания антиатерогенной фракции холестерина – ХС ЛПВП (с 43,1 до 49,0 мг/дл; +14,7%). Главным же аргументом в пользу назначения статинов является их доказанное благоприятное влияние на прогноз пациентов высокого и очень высокого СС-риска.
Все остальные липидоснижающие средства являются дополнительными или альтернативными, а их уровень доказательств в лечении дислипидемий остается невысоким. При непереносимости статина следует рассмотреть возможность назначения эзетимиба или секвестранта желчных кислот либо эти два препарата в комбинации (IIa, C). Если цель не достигнута на терапии статином в адекватной дозе, следует рассмотреть дополнительное назначение ингибитора абсорбции холестерина эзетимиба (IIa, B). Также может быть рассмотрена комбинация статина с секвестрантом желчных кислот (IIb, B).
У пациентов с очень высоким риском и сохраняющимся высоким уровнем ХС ЛПНП, несмотря на лечение статином в максимальной переносимой дозе в сочетании с эзетимибом, а также у пациентов, которые плохо переносят статины, может быть рассмотрено назначение ингибитора PCSK9 (IIb, C).
Ингибиторы PCSK9 (пропротеиновой конвертазы субтилизин-кексинового типа 9) – новый класс препаратов для снижения уровня ХС ЛПНП, успешно прошедший клинические испытания. В рамках исследования ODYSSEY пациенты, которые принимали максимальные дозы статинов и других липидоснижающих препаратов, с высоким сердечно-сосудистым риском или семейной гиперхолестеринемией (n=1553), получали алирокумаб в дозе 150 мг 1 раз в 2 нед. Через 24 нед было достигнуто снижение уровня ХС ЛПНП на 61%. У 79% пациентов достигнуты целевые уровни ХС ЛПНП (<1,8 ммоль/л). За 65 нед расчетное снижение относительного риска сердечно-сосудистых событий в группе алирокумаба составило 54%. Но с учетом высокой стоимости неизвестно, будут ли использоваться ингибиторы PCSK9 в Украине.
Значительным изменениям подвергся раздел рекомендаций по лечению гипертриглицеридемии. Рассмотреть лечение следует у пациентов высокого риска с уровнем триглицеридов (ТГ) >2,3 ммоль/л (IIa, B). Фибраты больше не являются препаратами выбора, из рекомендаций исключена никотиновая кислота. На первый план выдвинута терапия статинами (I, A). У пациентов высокого риска, принимающих статины, с уровнем ТГ >2,3 ммоль/л, можно рассмотреть комбинацию фенофибрата со статином (IIa, B).
Большой раздел рекомендаций посвящен лечению дислипидемий у различных категорий пациентов, часто встречающихся в работе кардиологов, терапевтов и семейных врачей.
У пациентов с острым коронарным синдромом (ОКС) и лиц, которым были проведены перкутанные коронарные вмешательства (ПКВ), настоятельно рекомендуется начать или продолжить терапию высокими дозами статинов в ранние сроки после госпитализации при отсутствии противопоказаний или непереносимости, независимо от начальных значений ХС ЛПНП (I, A). Если у пациентов после ОКС целевой уровень ХС ЛПНП не достигается на самой высокой переносимой дозе статина, следует рассматривать усиление терапии эзетимибом (IIa, B).
Если же целевой уровень ХС ЛПНП не достигается на самой высокой переносимой дозе статина и/или эзетимиба, следует рассмотреть возможность назначения ингибитора PCSK9 – отдельно либо в сочетании с эзетимибом у пациентов с непереносимостью статинов или когда они противопоказаны (IIb, C).
Следует повторно проанализировать липидограмму через 4-6 нед после ОКС, чтобы определить, достигнут ли целевой уровень ХС ЛПНП <1,8 ммоль/л, снизился ли он на 50%, если начальный уровень составлял от 1,8 до 3,5 ммоль/л, и существуют ли какие-либо вопросы безопасности. Терапевтическая доза должна быть затем соответствующим образом адаптирована.
Рутинный короткий курс предварительного лечения (на фоне базовой терапии) высокими дозами статинов следует рассматривать перед проведением ПКВ у пациентов с ОКС без элевации сегмента ST (IIa, A).
Влияние интенсивной терапии статинами на объем атеросклеротической бляшки показано в исследовании YELLOW, в которое были включены 87 пациентов со многососудистым поражением коронарных артерий после стентирования с неполной реваскуляризацией и сохраняющимся гемодинамически значимым стенозом FFR ≤0,8. 44 пациента принимали 40 мг розувастатина, 43 – статины в прежней дозе. Оценивали индекс содержания липидов (LCBI) в ядре бляшки с помощью инфракрасной спектроскопии (NIRS) и внутрисосудистого ультразвука. Интенсивная липидоснижающая терапия высокой дозой розувастатина приводила к существенному уменьшению индекса содержания липидов в атеросклеротической бляшке через 6-8 нед.
Для первичной профилактики инсульта у пациентов высокого и очень высокого риска рекомендуется терапия статинами с достижением целевых уровней липидов (I, A). Липидоснижающая терапия рекомендуется также больным с другими проявлениями ССЗ для первичной профилактики инсульта (I, A). Для вторичной профилактики инсульта рекомендуется интенсивная терапия статинами пациентам, которые перенесли некардиоэмболический ишемический инсульт или транзиторную ишемическую атаку (I, A).
Заболевания периферических артерий, включая сонные артерии, ассоциируются с очень высоким сердечно-сосудистым риском, и этим пациентам настоятельно рекомендована липидоснижающая терапия, прежде всего статины (I, A). Терапия статинами должна быть рассмотрена для предупреждения и замедления прогрессирования аневризмы брюшной аорты (IIa, B).
В разделе по лечению дислипидемий у больных СД всем пациентам с СД 1 типа и микроальбуминурией
и/или болезнью почек рекомендуется назначение статинов с целью снижения уровня ХС ЛПНП на 50%, независимо от исходного уровня ХС ЛПНП (I, C).
У больных с СД 2 типа и ССЗ или ХБП, а также у лиц старше 40 лет без ССЗ, но с одним и более факторами риска или маркерами поражения органов-мишеней рекомендуются как первичная цель снижение уровня ХС ЛПНП <1,8 ммоль/л (<70 мг/дл), вторичная цель – снижение уровня ХС не ЛПВП <2,6 ммоль/л (<100 мг/дл) и Апо-B <80 мг/дл (I, B).
У всех пациентов с СД 2 типа без дополнительных факторов риска и/или очевидного поражения органов-мишеней уровень ХС ЛПНП <2,6 ммоль/л – первичная цель. Уровень ХС не ЛПВП <3,4 ммоль/л (<130 мг/дл) и Апо-B <100 мг/дл – вторичные цели.
Пациентов с ХБП III-V стадий следует относить к категориям высокого или очень высокого сердечно-сосудистого риска (I, A) (см. также табл. 1). Использование статинов или комбинации статин + эзетимиб показано больным с ХБП, которым не проводится диализ (I, A). Больным с диализ-зависимой ХБП и отсутствием атеросклеротических ССЗ статины не показаны.
Пациентам с ССЗ, которые на момент начала диализа принимают статины, эзетимиб или комбинацию статин + эзетимиб, терапию этими препаратами следует продолжать.
Некоторые особенности имеют рекомендации по лечению дислипидемий при сердечной недостаточности (СН) и патологии клапанов сердца. Терапия статинами не рекомендуется (но не наносит вреда) пациентам с СН при отсутствии других показаний к их применению. Омега‑3-полиненасыщенные жирные кислоты (1 г в сутки) можно добавлять к основной терапии у больных СН. Липидоснижающая терапия не рекомендуется пациентам со стенозом аортального клапана без ИБС при отсутствии других показаний к их применению.
У пациентов с хронической СН уровень ОХС и ХС ЛПНП обычно ниже, чем у пациентов без СН. Низкий уровень ОХС – плохой прогностический признак при СН.
Лечение статинами рекомендуется пожилым пациентам с установленными ССЗ, так же, как и молодым (I, A). У пожилых людей часто наблюдаются коморбидные заболевания и нарушения фармакокинетики лекарств. Липидоснижающие препараты должны назначаться с низких доз, с последующей титрацией до достижения целевого уровня липидов. Терапия статинами должна быть рассмотрена у пожилых пациентов без ССЗ, в частности при наличии таких факторов риска и состояний, как артериальная гипертензия, курение, СД и дислипидемии (IIa, B).
Традиционная тема для обсуждений – побочные эффекты статинов. В новых рекомендациях эксперты ESC ссылаются на ряд контролируемых и наблюдательных исследований, в которых проводилась оценка частоты и клинической значимости основных побочных эффектов. Рабдомиолиз – опасное, но очень редкое осложнение со стороны скелетных мышц, которое встречается с частотой 1-3 случая на 100 тысяч пациентов в год. Миалгии – более распространенное явление с частотой 10-15% согласно данным открытых наблюдений и 5% в контролируемых исследованиях (M. Law, A.R. Rudnicka, 2006; B.A. Parker et al., 2013).
Для пациентов с побочными эффектами со стороны мышечной системы предлагается альтернативный режим приема статинов – 2 раза в неделю.
Со стороны печени возможно повышение активности маркеров цитолиза: уровень АЛТ повышается в >3 раза у 0,5-2% пациентов, принимающих статины. Это дозозависимый эффект, при котором может потребоваться коррекция дозы, но он не ассоциируется с гепатотоксичностью и не должен служить поводом к отмене терапии (N. Chalasani et al., 2004).
Очень редко на фоне приема статинов регистрировались новые случаи СД. По данным метаанализа, относительный риск составляет 9%, абсолютный – 0,2%. Это 1 случай СД на 255 пациентов в течение 4 лет (N. Sattar et al., 2010).
Таким образом, статины остаются краеугольным камнем липидоснижающей терапии с лучшим на сегодняшний день соотношением эффективности и безопасности. Идея интенсивной терапии статинами до достижения обозначенных целевых уровней липидов проходит через все разделы рекомендаций ESC. Вместе с тем, как показало исследование EUROASPIRE IV, более 80% пациентов категорий высокого и очень высокого риска не достигают целевых уровней липидов крови, то есть не получают максимальной пользы от статинотерапии. Стартовая доза не обеспечивает необходимого эффекта, а максимальная редко используется, что связано как с низкой приверженностью пациентов, так и с опасениями врачей назначать высокие дозы. Поэтому продолжаются поиски оптимальной схемы титрации дозы статинов для преодоления данного парадокса.
Одна из возможностей заключается в использовании промежуточных дозировок розувастатина – 15 и 30 мг, которые позволяют оптимизировать гиполипидемическую терапию и увеличить ее эффективность. Учитывая, что большинство пациентов получает терапию минимальными дозами статинов без последующего их повышения, дозировка 15 мг может рассматриваться в качестве начальной для пациентов высокого и очень высокого риска. Cубмаксимальная дозировка розувастатина (30 мг) может стать хорошей альтернативой максимальной в случае необходимости интенсивной статинотерапии и наличия у врача опасений в отношении последней.
С целью изучения эффективности промежуточных дозировок розувастатина (15 и 30 мг) и их места в клинической практике было спланировано международное многоцентровое открытое проспективное рандомизированное клиническое исследование ROSU-PATH.
В этом исследовании 472 пациента были рандомизированы в 2 группы: для лечения розувастатином по стандартной схеме титрования дозы (10 мг → 20 мг → 40 мг) или по альтернативной схеме (15 мг → 30 мг → 40 мг). На 4-й, 8-й и 12-й неделях проводили повторные оценки эффективности и безопасности.
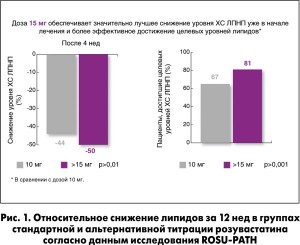
Исследование продемонстрировало, что стартовая доза Роксеры 15 мг в сравнении с дозой 10 мг обеспечивает достоверные преимущества в снижении уровня ХС ЛПНП уже в начале лечения.
В группе со стартовой дозировкой Роксеры 15 мг по сравнению с группой, в которой лечение начиналось с дозы 10 мг в сутки, достоверно больше пациентов достигли целевых уровней липидов: 81 против 67% (P<0,0001) при сопоставимой переносимости (рис. 1).
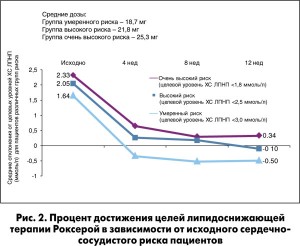
Показана также более высокая эффективность альтернативной схемы титрования по влиянию на весь липидный профиль. При анализе в подгруппах в зависимости от исходного сердечно-сосудистого риска закономерно меньше пациентов достигали целевых уровней липидов, имея очень высокий риск (рис 2). Но в целом получены удовлетворительные результаты даже в этой подгруппе: эффективность лечения оценена положительно у 96% пациентов.
Таким образом, в исследовании ROSU-PATH впервые дана клиническая оценка эффективности и безопасности розувастатина (Роксера®, КRКА) в дозах 15 и 30 мг. Результаты клинического исследования ROSU-PATH продемонстрировали преимущества применения промежуточных доз розувастатина (15 и 30 мг). Значительно большее количество пациентов, получавших розувастатин в дозах 15 и 30 мг, достигли целевых уровней липидов в сравнении с пациентами, получавшими лечение дозами 10 и 20 мг. Назначение препарата Роксера в дозе 15 мг является эффективной и безопасной начальной стратегией, особенно при наличии высокого и очень высокого риска, обеспечивающей более эффективное достижение целевого уровня ХС ЛПНП у большего количества пациентов.
Подготовил Дмитрий Молчанов