30 січня, 2017
Ретроспективный анализ влияния веса на эффективность десвенлафаксина 50 и 100 мг/сут у пациентов с депрессией
По данным литературы, частота ожирения среди лиц с депрессией выше, чем в общей популяции. Метаанализы (F.S. Luppino et al., 2010; L. de Wit et al., 2010) показали, что как ожирение ассоциируется с повышенным риском депрессии, так и депрессия является предиктором избыточного веса и ожирения. Связь между ними усложняется антидепрессантами, при применении которых часто отмечается повышение массы тела, которое может отрицательно влиять на приверженность терапии. И хотя достижение ремиссии является наиболее важной задачей при ведении пациентов с большим депрессивным расстройством (БДР), среди антидепрессантов с сопоставимой эффективностью рекомендуется отдавать предпочтение препаратам, нейтральным в отношении веса, особенно если речь идет о больных с избыточным весом или ожирением. И наконец, исходный индекс массы тела (ИМТ) может влиять как на динамику массы тела во время лечения антидепрессантами, так и на эффективность терапии.
Десвенлафаксин (применяемый в виде десвенлафаксина сукцината) является ингибитором обратного захвата серотонина и норадреналина (ИОЗСН), одобренным для лечения взрослых пациентов с БДР. Основными задачами данного анализа была оценка влияния исходного ИМТ на эффективность терапии и динамику веса у взрослых лиц с БДР, получавших десвенлафаксин 50 мг или 100 мг/сут, по сравнению с плацебо.
Материалы и методы
В анализ были включены индивидуальные данные участников 8 краткосрочных многоцентровых рандомизированных двойных слепых плацебо-контролируемых исследований, в которых изучали эффективность фиксированной дозы десвенлафаксина при БДР. Продолжительность 6 исследований составила 8 недель, по одному исследованию продолжались 10 и 12 недель. Первичной конечной точкой всех исследований было изменение от исходного уровня показателя по шкале депрессии Гамильтона (HDRS‑17).
Отдельно был проведен анализ 12-месячного рандомизированного исследования – только для оценки динамики веса на фоне терапии десвенлафаксином. В ходе этого исследования пациенты сначала открыто получали десвенлафаксин 50 мг/сут в течение 8 недель, после чего участники, ответившие на лечение, продолжали терапию в открытом режиме еще 12 недель. Затем пациентов с сохраняющимся устойчивым улучшением включали в 6-месячное двойное слепое плацебо-контролируемое исследование и рандомизировали в две группы (1:1), одна из которых продолжала прием десвенлафаксина, а вторая переводилась на плацебо.
Что касается критериев включения, то во все исследования привлекались взрослые амбулаторные пациенты с диагнозом БДР в соответствии с критериями DSM-IV, длительностью депрессивных симптомов не менее 30 дней, показателем по шкале HDRS‑17 ≥20 баллов или по шкале Монтгомери-Асберга (MADRS) ≥25 баллов. Критерии исключения в каждом исследовании предполагали отбор стабильных с общемедицинской точки зрения пациентов с основным диагнозом БДР (за исключением биполярной и психотической депрессии).
Результаты
В краткосрочных исследованиях как минимум одну дозу исследуемого препарата в общей сложности приняли 3399 пациентов, которые были включены в объединенный ретроспективный анализ безопасности. Из них 2/3 имели избыточный вес или ожирение. Так, у 1131 пациента (33,3%) ИМТ был в нормальном диапазоне или ниже нормы; 964 (28,4%) имели избыточный вес; 1304 (38,4%) страдали ожирением. По крайней мере одна оценка эффективности получена у 3384 пациентов, которые составили ITT-популяцию (1122 с нормальным или сниженным весом, 960 с избыточным и 1302 с ожирением).
В продолжительном исследовании в открытом этапе приняли участие 874 пациента, в том числе 345 (39,5%) с нормальной массой тела, 271 (31,0%) с избыточной и 258 (29,5%) с ожирением. Рандомизированы для продолжения терапии или приема плацебо после завершения открытого этапа 548 пациентов, из которых у 542 проведена как минимум одна оценка массы тела в динамике; этих пациентов и включили в анализ изменения веса.
Исходные демографические и клинические характеристики в целом были сопоставимы между группами лечения во всех исследованиях.
Эффективность
Через 8 недель терапии улучшение показателя по шкале HDRS‑17 от исходного уровня было достоверно большим при приеме десвенлафаксина 50 и 100 мг/сут по сравнению с плацебо во всех подгруппах ИМТ (все р≤0,0027, рис.). Такие же результаты получены при оценке эффективности по шкале MADRS и Шкале общего клинического впечатления о тяжести заболевания (CGI-S). Частота ответа на терапию (по изменению показателя HDRS‑17) через 8 недель была значительно выше для обеих доз десвенлафаксина по сравнению с плацебо в каждой подгруппе ИМТ.
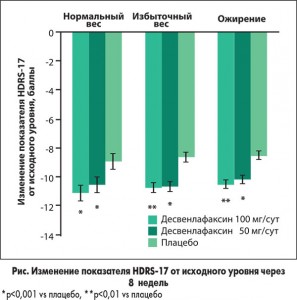
Исходный ИМТ был достоверным предиктором изменения показателя HDRS‑17 (выше ИМТ – меньше изменение HDRS‑17) для групп десвенлафаксина 50 мг/сут (р=0,048) и 100 мг/сут (р=0,031), но не плацебо (р=0,097). Также исходный ИМТ оказался значимым предиктором вероятности ответа на десвенлафаксин 50 мг/сут (р=0,0397): у больных с более высоким ИМТ было меньше шансов ответить на лечение по сравнению с пациентами с более низким ИМТ. В то же время исходный уровень ИМТ не влиял на вероятность достижения ремиссии или время до получения ответа на терапию.
Изменение массы тела
Согласно объединенному анализу краткосрочных исследований, в каждой из подгрупп ИМТ через 8 и 16 недель после начала терапии у пациентов, принимавших десвенлафаксин 50 или 100 мг/сут, отмечено небольшое снижение веса. В то же время пациенты с нормальным и избыточным весом в группе плацебо продемонстрировали небольшое, но статистически значимое увеличение веса с течением времени. Разница по изменению веса от исходного уровня между группами открытого лечения (десвенлафаксин 50 и 100 мг/сут) и плацебо была небольшой, но статистически значимой (р≤0,0195 во всех подгруппах). Исходный уровень ИМТ был значимым предиктором изменения веса и ИМТ в общей популяции исследования (р≤0,0035) и в группе десвенлафаксина 100 мг/сут (р≤0,0354).
В открытой фазе продолжительного исследования прием десвенлафаксина 50 мг/сут сначала привел к снижению, а затем небольшому повышению массы тела (в среднем на 0,47 кг от исходного уровня). Что касается подгруппового анализа, то через 8 недель приема десвенлафаксина 50 мг/сут в открытой фазе исследования у лиц с нормальным и избыточным весом не наблюдалось статистически значимого изменения массы тела от исходного уровня, а у пациентов с ожирением она достоверно снизилась (–0,38±0,15 кг; р=0,012). Через 20 недель открытой фазы у лиц с исходно нормальным и избыточным весом масса тела немного увеличилась (+0,67±0,18 кг и +0,58±0,19 кг соответственно, все р≤0,003 по сравнению с исходным уровнем), а у лиц с ожирением достоверно не изменилась.
За время двойной слепой фазы исследования при продолжении лечения десвенлафаксином 50 мг/сут отмечено значительно меньшее увеличение веса по сравнению с переводом на плацебо (0,24 vs 0,52 кг соответственно, р=0,004). У лиц с исходно нормальным весом, но не у лиц с избыточной массой тела или ожирением, прием десвенлафаксина ассоциировался с небольшим, но статистически значимым увеличением веса за 26 недель двойной слепой фазы (0,97±0,26 кг, р<0,001). Тем не менее не было обнаружено статистически значимых различий между пациентами, принимавшими десвенлафаксин и плацебо, в любой подгруппе ИМТ.
Исходный уровень ИМТ был значимым предиктором изменения веса и ИМТ в общей популяции долгосрочного исследования (все р≤0,009) и в группе десвенлафаксина 50 мг/сут (все р≤0,0112). Пациенты с более высоким исходным ИМТ и ожирением в частности имели меньше шансов на прибавку веса в долгосрочной перспективе.
Обсуждение
Результаты данного анализа согласуются с другими исследованиями и метаанализами, показавшими несколько меньшую эффективность терапии антидепрессантами (селективными ингибиторами обратного захвата серотонина (СИОЗС), ИОЗСН, трициклическими антидепрессантами, миртазапином) у пациентов с ожирением и избыточной массой тела по сравнению с лицами с нормальным весом.
Динамика массы тела на фоне терапии десвенлафаксином, показанная в данном анализе, согласуется с данными для десвенлафаксина в дозах до 400 мг/сут в других исследованиях, а также с исследованиями дулоксетина, венлафаксина и некоторых СИОЗС (флуоксетин, пароксетин). В долгосрочных исследованиях (≥4 мес) ранняя потеря веса сопровождалась последующим возвратом к исходному уровню массы тела у пациентов, получавших дулоксетин или СИОЗС.
Связь между исходным ИМТ и изменением веса в динамике, наблюдавшаяся в этом анализе (пациенты с высоким исходным ИМТ имели большую потерю веса в начале лечения и меньшую прибавку в долгосрочной перспективе), также согласуется с результатами исследований других антидепрессантов.
Перевод с английского Вячеслава Килимчука
Список литературы находится в редакции.
Статья печатается в сокращении.
R.S. McIntyre, R.S. Fayyad, C.J. Guico-Pabia, M. Boucher. A Post Hoc Analysis of the Effect of Weight on Efficacy in Depressed Patients Treated With Десвенлафаксин 50 mg/d and 100 mg/d. Prim Care Companion CNS Disord. 2015; 17(3): 10.
Выводы
Десвенлафаксин 50 и 100 мг/сут эффективно уменьшает выраженность симптомов депрессии при любом исходном ИМТ.
Во всех подгруппах ИМТ десвенлафаксин ассоциировался со статистически значимым снижением веса (<1 кг) после краткосрочного курса терапии БДР и не вызывал достоверного изменения веса по сравнению с плацебо после длительного лечения.
Исходный ИМТ был предиктором ответа на лечение и изменения веса в ходе лечения: несколько большее снижение выраженности симптомов депрессии наблюдалось у пациентов с нормальным ИМТ, а потеря веса при краткосрочной терапии была наибольшей у пациентов с ожирением.


