30 січня, 2017
Ключові питання інтенсивної терапії хворих з гострими мозковими катастрофами
За матеріалами III Міжнародного конгресу з інфузійної терапії
6-7 жовтня у м. Києві відбувся III Міжнародний конгрес з інфузійної терапії, який став однією з найбільших наукових подій року. В межах наукового заходу провідні вітчизняні науковці та відомі зарубіжні спеціалісти прочитали велику кількість доповідей, присвячених гострим та дискусійним питанням інфузійної терапії критичних станів. Чимало повідомлень стосувалися особливостей ведення пацієнтів з мозковим інсультом, черепно-мозковою травмою (ЧМТ) та іншими гострими пошкодженнями головного мозку. Про аспекти лікування хворих з гострими мозковими катастрофами розповів завідувач кафедри анестезіології та інтенсивної терапії Івано-Франківського національного медичного університету, доктор медичних наук, професор Іван Іванович Тітов.
На початку своєї доповіді професор зазначив, що інтенсивна терапія інсульту та тяжкої ЧМТ має єдині концептуальні підходи, що зумовлено монопатогенетичністю реакцій мозку на патологічні впливи. Однак кожна мозкова катастрофа має свої, притаманні їй характерні риси.
У пацієнтів з ішемічним інсультом важливо підтримувати на належному рівні об’єм циркулюючої крові (ОЦК) та не допускати розвитку гіповолемії у зв’язку із зростанням ризику гіпотензії, зниженням центрального перфузійного тиску, що призводить до вазодилатації і підвищення внутрішньочерепного тиску. Доведено, що від’ємний баланс рідини в перші три доби лікування значно знижує виживаність пацієнтів з інсультом. Тому у пацієнтів з гострим ішемічним інсультом введення рідини повинно становити не менше добової потреби для збереження загального водно-електролітного балансу та забезпечення достатнього кровотоку в мозкових судинах. Для корекції водно-електролітного балансу не рекомендується використовувати розчини, які містять глюкозу, оскільки гіперглікемія посилює ацидоз в ішемізованих ділянках мозку, а розчини глюкози є джерелом вільної рідини, яка може сприяти набряку мозку.
Зазвичай для підтримки нормоволемії достатньо вводити рідину в об’ємі 30-35 мл/кг/добу. Якщо на момент госпіталізації у пацієнта є ознаки гіповолемії (низький артеріальний тиск, підвищений гематокрит (Ht), сухість слизових оболонок) і немає протипоказів (декомпенсована серцева недостатність), інфузійна терапія може бути призначена в об’ємі 1000-1500 мл 0,9% розчину хлориду натрію або розчину Рінгера. Для проведення інфузійної терапії у непритомних пацієнтів рекомендована постановка центрального венозного катетера. Це дозволить проводити моніторинг центрального венозного тиску (ЦВТ), який бажано підтримувати на рівні 80-100 мм водного стовпчика.
За даними Івано-Франківської обласної клінічної лікарні, майже всі пацієнти, що були госпіталізовані з діагнозом гострого порушення мозкового кровотоку, при поступленні мали гіповолемію різного ступеня (у 38,4% пацієнтів показник гематокриту був в межах 0,35-0,55 л/л, у 44,8% пацієнтів ≥0,55 л/л, 12% пацієнтів ≥0,65 л/л). Тобто близько 95% хворих з гострим порушенням мозкового кровотоку потребували інфузійної корекції агрегатного стану крові (рис. 1).
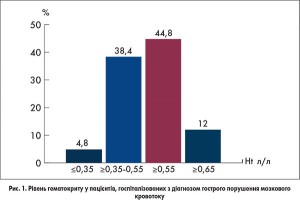
Показом до проведення терапевтичної гемодилюції є гематокрит більше 0,45 л/л. Залежно від величини цього показника виділяють гіперволемічну (при Ht >0,45 л/л) та ізоволемічну (при Ht >0,55 л/л) гемодилюцію. Методика проведення гіперволемічної гемодилюції включає інфузію 500 мл 0,9% розчину хлориду натрію впродовж 1 години з наступним переходом на інфузію 1000-1500 мл розчину Рінгера до кінця доби. При цьому пацієнт повинен отримувати рідину перорально (як правило, через зонд) в об’ємі фізіологічної потреби. Для швидкого проведення ізоволемічної гемодилюції рекомендують спочатку виконати ексфузію 300-500 мл крові, після чого виконати інфузію 500-1000 мл 0,9% розчину хлориду натрію чи розчину Рінгера впродовж 1-2 годин. Надалі проводять введення рідини в об’ємі фізіологічної потреби перорально (через зонд).
Говорячи про інфузійну терапію у пацієнтів з ішемічним інсультом, обов’язково слід враховувати осмолярність плазми крові. Гіпоосмолярність <285 мосм/л вказує на надлишок рідини, який веде до набряку мозку, гіперосмолярність >310 мосм/л спричиняє дегідратацію, гіповолемію, гемоконцентрацію та зниження перфузії передусім у пошкоджених структурах мозку. У неврологічних пацієнтів рекомендовано підтримувати осмолярність в межах 300-320 мосм/л. Осмолярність крові можна розрахувати, застосовуючи нескладні формули:
1,86 × (Na + глюкоза + сечовина) + 9 = … мосм/л;
2 × Na + глюкоза + сечовина = … мосм/л;
2 × (Na +К) = … мосм/л.
Проводячи корекцію гіповолемії, необхідно обов’язково зважати на осмолярність застосовуваних розчинів. Так, розчини з високою осмолярністю (альбумін 5% – 350 мосм/л, глюкоза 10% – 586 мосм/л, маннітол – 1382 мосм/л) з цією метою використовувати не можна. Рекомендується застосовувати 0,9% розчин NaCI (308 мосм/л) та розчин Рінгера (309 мосм/л), Нейроцитин (288 мосм/л) та інші нормоосмолярні розчини. При застосуванні осмотично-активних речовин осмолярність плазми не повинна перевищувати 320 мосм/л (рівень обґрунтованості C) [4]. В нормі рівень осмолярності крові становить 285-310 мосм/л (Наказ МОЗ України від 03.08.2012 № 602 «Про затвердження та впровадження медико-технологічних документів зі стандартизації медичної допомоги при ішемічному інсульті»).
Застосування 7,5% розчину NaCI, Гекотону, Сорбілакту можливе з метою зниження внутрішньочерепної гіпертензії.
Більш точне уявлення про церебральну гемодинаміку дає визначення церебрального перфузійного тиску (ЦПТ), нормальне значення якого становить 90-95 мм рт. ст. Цей показник можна визначити розрахунковим методом: ЦПТ = САТ – ЛТ; або ЦПТ =САТ – ЦВТ (де САТ – середній артеріальний тиск, що дорівнює сумі діастолічного артеріального тиску та 1/3 пульсового тиску; ЛТ – лікворний тиск; ЦВТ – центральний венозний тиск. Для перерахунку мм водн. ст. в мм рт. ст. використовують коефіцієнт 13,6). В ідеалі слід проводити безперервний моніторинг центральної перфузії.
Стратегічним напрямом у лікуванні інсульту вважається нейропротекція. Це мінімально інвазивний метод, який можна безпечно застосовувати за будь-якого виду інсульту та на будь-якому етапі лікування без попередніх діагностичних досліджень. Беззаперечною перевагою нейропротекції є її безпечність та ефективність.
Існує багато груп лікарських препаратів, які застосовують з метою нейропротекції (антагоністи кальцію, антагоністи глутамату, непрямі модулятори глутамату, антиоксиданти тощо). Але лише деякі продемонстрували ефективність в міжнародних клінічних рандомізованих дослідженнях. Крім того, результати експериментальних робіт вказують на те, що важливим є терапевтичний вплив на найважливіші точки ішемічного каскаду. Зокрема було доведено, що комплекс електролітів в комбінації з цитиколіном (Нейроцитин) мінімізує активність фосфоліпази А2, стимулює синтез глутатіону та пригнічує процеси пероксидації ліпідів та білків, нормалізує роботу натрій-калієвого насосу, активує енергетичні процеси в нейронах, нормалізує процеси тканинного дихання, інгібує глутамат-індукований апоптоз, активує біосинтез лецитину та попереджує його катаболізм, відновлює нормальний рівень фосфоліпідних компонентів внутрішньої мітохондріальної мембрани.
Щодо ефективності, безпечності та переносимості цитиколіну в лікуванні пацієнтів з інсультом свідчать перші результати власного дослідження комплексної нейропротекції. В дослідження увійшли дві групи пацієнтів з ішемічним інсультом: контрольна група, пацієнти якої отримували стандартну терапію інсульту згідно з наказом № 602 МОЗ України; основна (дослідна) група, пацієнти якої окрім стандартної терапії згідно з наказом № 602 МОЗ України отримували з метою комплексної нейропротекції комбінацію електролітів з цитиколіном (Нейроцитин) в дозі по 1000 мг 2 рази на добу внутрішньовенно з 1-ї по 14-ту добу лікування.
Методи дослідження включали: загальноклінічний та неврологічний огляд (шкала NIHSS, індекс Бартела, шкала Ренкіна); КТ (МРТ) з контролем при виписці; ЕКГ; визначення нейронспецифічної енолази; BIS-індекс; церебральну оксиметрію.
Доповідач зазначив, що досить чутливим індикатором пошкодження нейронів є рівень нейронспецифічної енолази – спільного маркеру усіх диференційованих нейронів. У нормі цей показник становить 10-11 нг/мл. Величина зростання рівня цього білка в сироватці крові чи у спинномозковій рідині свідчить про ступінь ушкодження нейронів та порушення цілісності гематоенцефалічного бар’ єру. Згідно з результатами дослідження у пацієнтів основної групи вже з перших днів лікування спостерігалося суттєве зниження цього маркера відносно вихідного рівня (69,17 нг/мл) та порівняно з пацієнтами контрольної групи (38,46 vs 61,33 нг/мл відповідно). З часом ця розбіжність ставала дедалі більшою, досягнувши максимуму на 14-й день терапії (19,26 нг/мл в основній групі та 48,32 нг/мл в групі контролю) (рис. 2).
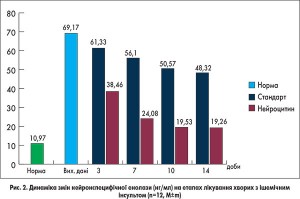
Також вивчалась динаміка BIS-індексу на тлі інфузії Нейроцитину при ішемічному інсульті. Зазвичай методику BIS-моніторингу використовують для визначення глибини пригнічення свідомості під час загальної анестезії (в нормі BIS-індекс становить 97-98). Але оскільки BIS-індекс є відображенням інтегральної оцінки біоелектричної активності мозку, цей метод можна використовувати і у хворих з інсультом. У пацієнтів, які брали участь у дослідженні, BIS-індекс знаходився в межах 45-48, що свідчить про стан коми чи сопору. У пацієнтів, що отримували терапію Нейроцитином, вже на другу добу лікування відмічалось стрімке зростання BIS-індексу до середнього значення 60, тоді як в групі стандартної терапії він все ще залишався на рівні 45. Після завершення курсу терапії різниця між групами перевищувала 26 (85 в основній групі та 58 в групі контролю) (рис. 3.).
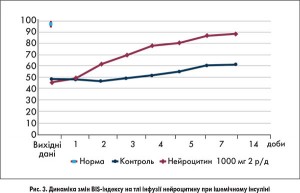
Таким чином, Нейроцитин нормалізує показники біоелектричної активності мозку при ішемічному інсульті та створює сприятливі умови для перебігу процесів нейрорепарації.
Терапія Нейроцитином суттєво покращувала оксигенацію мозку, про що свідчать показники церебральної оксиметрії. Починаючи з другого дня дослідження була відмічена суттєва різниця між групами у насиченні гемоглобіну киснем в мікроциркуляторному руслі тканин мозку.
Наприкінці своєї доповіді професор І.І. Тітов зауважив, що підтримка вітальних функцій та гомеостазу в поєднанні з ранньою комплексною нейропротекцією та нейрореабілітацією є найбільш реальною і доступною стратегією лікування гострих порушень мозко вого кровообігу в умовах сучасної медицини. З метою нейропротекції доцільно застосовувати лікарський препарат Нейроцитин. Він об’єктивно продемонстрував високу ефективність у лікуванні гострих порушень мозкового кровообігу та є перспективним з точки зору включення в терапевтичні схеми невідкладної допомоги при гострому порушенні мозкового кровообігу.
Підготував В’ячеслав Килимчук



