22 березня, 2017
Сучасний погляд на особливості діагностики та лікувальної тактики набрякових форм раку грудної залози
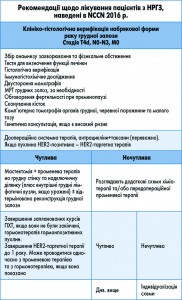
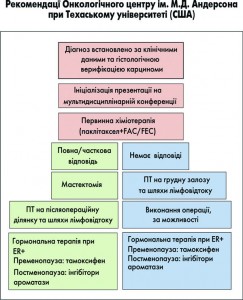
Набряковий рак грудної залози (НРГЗ) відносять до агресивних варіантів перебігу захворювання. Діагностика набрякових форм може становити певні труднощі. Обов’язковим етапом є виконання трепан-біопсії з пухлини чи підпахвинних лімфатичних вузлів. Неоад’ювантна терапія має включати системну поліхіміотерапію (ПХТ) на основі таксанів, антрациклінів, препаратів платини. При відповіді на лікування наступним етапом проводиться хірургічне втручання. Методом вибору оперативної техніки є радикальна мастектомія з контролем країв резекції. Органозбережні втручання та підшкірні ендопротезування при цій формі не виправдані. Реконструктивно-відновні операції мають бути відтерміновані і проведені після закінчення ад’ювантного лікування. При прогресуванні на фоні неоад’ювантної ПХТ призначається неоад’ювантна радіотерапія до 70 Грей. Гормонотерапія призначається за наявності гормоночутливих пухлин в ад’ювантному режимі.
Рак грудної залози (РГЗ) є найпоширенішим онкологічним захворюванням серед жінок більшості країн світу. Головну проблему становлять запущені форми й агресивні варіанти перебігу РГЗ, що мають несприятливий прогноз. До них відносять місцевопоширений рак грудної залози (МПРГЗ) (у тому числі й набрякові форми). Згідно з визначенням [1], МПРГЗ характеризується наявністю пухлини >5 см, конгломератом залучених іпсілатеральних лімфатичних вузлів та/або збільшеними підключичними й парастернальними солітарними лімфатичними вузлами. Для пацієнток з набряковим раком грудної залози (НРГЗ), крім того, картина захворювання нагадує запальний процес. Відзначається потовщення й гіперемія шкіри, збільшення розмірів ураженої залози, місцеве підвищення температури, дифузне ущільнення тканини залози. Специфічною ознакою є виникнення набряку, що вражає більше ніж третину грудної залози. Також характерним є виражене ураження регіонарних лімфатичних колекторів. За спостереженням низки авторів [2], регіонарні пахвові лімфатичні вузли уражаються в 95% випадків, а надключичні лімфовузли – у 40% випадків. Заведено розрізняти дифузну (істинну) і вузлову форму НРГЗ. У першому випадку спостерігається набряк без солідної пухлини, у другому визначається пухлинний вузол з набряком навколишніх тканин.
Діагностика НРГЗ. Діагностика НРГЗ базується на загальноприйнятих методах клініко-інструментальних досліджень і гістологічної верифікації. Обов’язковим є виконання мамографії, а за необхідності – мамосцинтіграфії. На мамограмі зазвичай відмічають ущільнення тканини грудної залози, яке поширюється більше ніж на її третину, що може спостерігатися як за наявності, так і за відсутності пухлинного утвору. Ультразвукова діагностика виконує допоміжну функцію і використовується при надщільній тканині грудних залоз, коли можливості рентгенівських променів знижуються. Також важко перебільшити значення цієї методики для оцінки стану регіонарних лімфатичних колекторів. Гістологічна верифікація діагнозу передбачає проведення трепан-біопсії з подальшим мікроскопічним дослідженням пунктату. Певні складнощі можливі за відсутності пухлинного вузла (істинно набрякова форма РГЗ). При цьому виникає необхідність пункційної біопсії регіонарних лімфатичних колекторів або дослідження зразків тканини грудної залози в зоні набряку. При НРГЗ обов’язково має бути виконане імуногістохімічне дослідження біопсійного матеріалу, а проведення цитологічного дослідження для цієї форми РГЗ недоцільно. Для уточнення діагнозу використовується доплерівське сканування, комп’ютерна томографія, магнітно-резонансна томографія, позитронно-емісійна томографія.
Лікування пацієнток з НРГЗ є актуальним та складним завданням сучасної онкології, при чому серед онкологів досі немає одностайної думки щодо доцільності тих чи інших методик лікування та їх послідовності, хоча більшість фахівців вважають за потрібне застосовувати до хворих цієї категорії комбінацію з трьох основних методів лікування.
Хіміотерапевтичне лікування. Хіміотерапія НРГЗ наразі вважається методикою, яку використовують як перший етап лікування для цієї форми РГЗ. Це пов’язано з прихованою генералізацією онкопроцесу при НРГЗ, яку визнають майже всі сучасні дослідники та спеціалісти. Використання хіміотерапії в лікуванні пацієнтів з НРГЗ дозволяє впливати як на первинну пухлину, так і на мікрометастази пухлини. Нині використовують комбінації хіміопрепаратів з різним механізмом дії, що потенціює протипухлинний ефект і зменшує ризик розвитку лікарської резистентності. Слід зауважити, що суттєвого зростання показника загальної виживаності для цієї форми вдалося досягти саме за умови використання неоад’ювантної ПХТ. Згідно з міжнародними консенсусами, призначається системна ПХТ на основі антрациклінів і таксанів, краще в послідовному порядку. Відповідь пухлини на лікування є єдиним беззаперечним критерієм, що зумовлює продовження лікування в такому форматі, а за його неефективності – перехід на інші хіміотерапевтичні схеми або до інших лікувальних методик.
Променева терапія. Променева терапія на певному етапі була методом вибору для хворих на НРГЗ, зважаючи на агресивний перебіг хвороби, залучення лімфатичних судин дерми й незадовільні результати хірургічних операцій. Променева терапія дозволяла уникнути хірургічної травми, проте, як і операція, лишалася чинником локального лікування і не впливала на віддалене метастазування. Для досягнення певного ефекту променевої дії, за даними багатьох авторів, потрібне підведення до пухлини й регіонарних зон дози не менше 60-70 Гр. Проте це не виключало розвитку місцевих і регіонарних рецидивів, частка яких до озброєння сучасними опромінювачами сягала 46-88%. Наразі загальноприйнято призначення променевих методик у неоад’ювантному режимі за відсутності відповіді на неоад’ювантну ПХТ або при прогресуванні процесу. Також променева терапія має бути призначена в ад’ювантному режимі як завершальний етап комплексного лікування, якщо вона не проводилася в неоад’ювантному режимі.
Гормонотерапія. Наявність у тканинах пухлини рецепторів стероїдних гормонів служить критерієм її гормональної чутливості і є показанням до призначення гормонотерапії. Відсутність рецепторів супроводжується гормонорезистентністю пухлини, за винятком 8-10%, коли пухлина все ж виявляється гормоночутливою.
За даними популяційного аналізу 308 хворих на НРГЗ, проведеного M. Panades і співавт. у 2005 р. [3], велику прогностичну значущість у досягненні 10-річної безрецидивної виживаності має наявність позитивних рецепторів естрогену. Проте в дослідженні, проведеному J.A. Low і співавт. у 2004 р. [4], показана відсутність впливу рецепторного й менопаузального статусів на загальну виживаність хворих. Також не відзначено статистично значущого впливу позитивних або негативних рецепторів естрогенів у хворих як у пременопаузі, так і в період постменопаузи. Нині гормонотерапія переважно застосовується в поєднанні з іншими методами лікування з використанням найсучасніших препаратів, включаючи інгібітори та інактиватори ароматаз, аналоги гіпоталамічних гормонів. Позиціювання гормонотерапії як допоміжної лінії терапії пацієнтів з НРГЗ відповідає думці більшості представників міжнародних дослідницьких кіл щодо значного превалювання гормон-негативних пухлин при НРГЗ.
Таргетна терапія. Останнім часом широкого застосування набуває таргетна терапія РГЗ. Таргетні препарати впливають на молекулярні структури – зовнішні і внутрішньоклітинні рецептори, білки, які продукують клітини пухлини, а також на кровоносні судини пухлини. Ураження цих «мішеней» призводить до загибелі клітин пухлини. З 1990 р. уже зареєстровано близько 15 таргетних препаратів [5]. Зростаюче розуміння молекулярних явищ, характерних для раку, призвело до виявлення великої кількості нових мішеней і паралельно до розвитку безлічі нових методів протиракової терапії. Таргетна терапія сфокусована на специфічних молекулах у злоякісній клітині, включаючи ключові молекули, залучені в процеси клітинної інвазії, метастазування, апоптозу, контролю клітинного циклу і пухлинного ангіогенезу. Безліч таргетних препаратів проходять випробування в клінічних дослідженнях. Таргетна терапія в більшості випадків переноситься істотно краще, ніж препарати хіміотерапії та гормонотерапії.
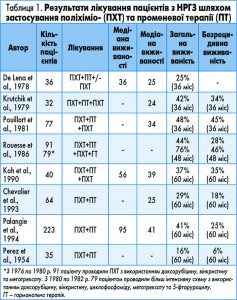
Хірургічне лікування. Найбільш суперечливі підходи при НРГЖ донедавна існували щодо хірургічного етапу. Розуміння системності природи НРГЖ породжувало в деяких дослідників певний скепсис щодо доречності хірургічного лікування як етапу взагалі. Низка авторів [6, 7] висловлювалися на користь обмеження лікувальних заходів при НРГЗ комбінацією хіміопроменевого лікування, наводячи дані про практично ідентичні показники загальної та безрецидивної виживаності у групах пацієнтів, яким була виконана відповідно неоад’ювантна хіміотерапія з подальшим хірургічним лікуванням або неоад’ювантна хіміотерапія з подальшою радіотерапією. Так, DeBoer і співавт. [9] наводили результати лікування 59 пацієнток, під час якого першій групі (35 хворих) після курсу ПХТ проводилася радіотерапія, тоді як пацієнткам другої групи (24 хворих) проводилося хірургічне лікування в поєднанні з радіотерапією. Медіана загальної виживаності була ідентична для обох груп і становила 35 міс. Ознаки повернення хвороби у вигляді метастазування відзначені у 69% пацієнток, які отримали радіотерапію, і у 79%, які лікувалися поєднанням променевого та хірургічного методів. Локорегіонарний рецидив спостерігали в 34 і 42% випадків відповідно. Був зроблений висновок про відсутність будь-яких переваг при введенні в схему комплексного лікування хірургічного етапу. Однак дослідження R.Y. Fleming і співавт., M. Panades і співавт., B. Chevallier і співавт. [8, 9, 10] показали переваги комплексного підходу, за якого неоад’ювантна (ад’ювантна) хіміотерапія поєднувалася з радикальним хірургічним лікуванням та променевою терапією. При цьому показник загальної виживаності досягав 41%.
Слід відзначити, що ця перевага актуальна тільки для пацієнтів, у яких була досягнута повна або часткова регресія у відповідь на неоад’ювантну ПХТ. M. Pandes і співавт. [9] повідомили про переваги включення мастектомії в схему лікування хворих на НРГЗ: 10-річна виживаність без ознак регіонарного рецидиву склала 62,8 проти 34,4%, а 10-річна виживаність без ознак хвороби 36,9 проти 22,5% відповідно в групах пацієнток, яким проводилося оперативне лікування поряд з хіміопроменевим на відміну від тих, що отримали комбіновану хіміопроменеву терапію. За даними B. Chevallier і співавт. [10], медіана безрецидивної і загальної виживаності в пацієнток, прооперованих з приводу НРГЗ після завершення неоад’ювантної ПХТ, склала 38,3 і 60,1 міс відповідно, тоді як у тих, що отримали після неоад’ювантної ПХТ радіотерапію, – 19 і 38,3 міс.
Адекватним обсягом оперативного втручання при НРГЗ беззаперечно вважається радикальна мастектомія. Існують поодинокі повідомлення щодо виконання органозбережних операцій у пацієнток з НРГЗ [6], але немає жодних даних щодо успішності такої тактики. Натомість є інформація про зростання кількості випадків локорегіонарного рецидивування майже втричі. Суть проблеми полягає в тому, що при явищах «набряку», тобто лімфогенної дисемінації пухлинних клітин у тканину залози та підшкірно, достеменна оцінка лікувального ефекту утруднена. Наводяться дані [11, 12], що клініко-рентгенологічна регресія при неоад’ювантному лікуванні корелює із залишком елементів пухлини більш ніж у 60% пацієнтів. Саме тому при цій формі РГЗ вкрай важливим є дослідження чистоти країв резекції, навіть при виконанні радикальних мастектомій.
Наразі, на думку багатьох авторів [13, 14, 15], питання щодо необхідності хірургічного етапу вважається вирішеним, але за певної умови. Помічено, що показники виживаності зростають тільки для тих хворих, що отримали відгук на попередню неоад’ювантну терапію. Тому сучасні рекомендації щодо лікування пацієнтів з НРГЗ (ASCO, NCCN, SentGallen) включають хірургічний етап тільки після оцінки результатів попередньої ПХТ. За умов досягнення повної або часткової регресії наступним етапом виступає хірургічне лікування. За відсутності динаміки або прогресування хвороби призначається ПХТ за додатковими схемами та радіотерапія. Якщо динаміка позитивна, пропонується хірургічне лікування, але немає розуміння щодо лікування НРГЗ за відсутності відгуку на попередню неоад’ювантну ПХТ.
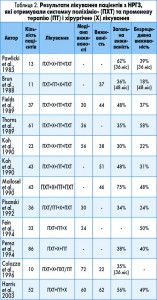
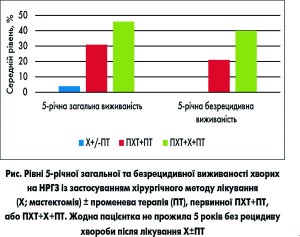
Комплексне лікування. У порівняльному аспекті наводилися результати досліджень лікування хворих на НРГЗ [16] із застосуванням як двох методів (хіміо- та променевої терапії), так і трьох (хіміо- та променевої терапії і хірургічного втручання). Попри невелику кількість задіяних у дослідженнях хворих і певний розкид результатів, можна помітити тенденцію до зростання безрецидивної та загальної виживаності для хворих, які лікувалися з використанням усіх трьох методів (табл. 1, 2, рис.).
Таким чином, сучасним стандартом лікування НРГЗ є комплексний підхід з використанням усіх наявних методик. Найкращі результати отримані при поєднанні неоад’ювантної хіміотерапії з хірургічним або променевим методом лікування або з тим і іншим разом. При цьому вирішальне значення має відповідь пухлини на проведену неоад’ювантну хіміотерапію. Методом вибору оперативної техніки є радикальна мастектомія. Краї операційної рани мають бути досліджені на «чистоту». Органозбережні втручання та підшкірні ендопротезування при цій формі раку не виправдані. Реконструктивно-відновні операції мають бути відтерміновані і проведені після закінчення ад’ювантного лікування. Немає ясності щодо лікування хворих, у яких не отриманий ефект від неоад’ювантної хіміотерапії. При прогресуванні на фоні неоад’ювантної ПХТ зазвичай призначається неоад’ювантна радіотерапія до 70 Грей. Гормонотерапія призначається за наявності гормоночутливих пухлин в ад’ювантному режимі.
Отже, НРГЗ був і лишається серйозним викликом онкологічній спільноті, але разом з тим надає широке поле для інтенсифікації та вдосконалення тактики лікування.
Література
1. Справочник по онкологи / Под ред. Шалимова С.А., Гриневич Ю.А., Возианова А.Ф. – 2-е изд., перераб. и доп. – К.: Здоров’я, 2008. – 256 с.
2. Jaiyesimi I.A., Buzdar A.U., Hortobagyi G. Inflammatory breast cancer: a review // J Clin Oncol 1992. – Vol.10. – P. 1014-1024.
3. Panades M., Olivotto I.A., Speers C.H. et al. Evolving treatment strategies for inflammatory breast cancer: A population based survival analysis // J Clin Oncol 2005. – Vol.23 (9). – P. 1941-1950.
4. Low J.A., Berman A.W., Steinberg S.M. et al. Long-term follow-up for locally advanced and inflammatory breast cancer patients treated with multimodality therapy // J Clin Oncol 2004. – Vol.22(20). – P. 4067-4074.
5. Longo R., Torino F., Gasparini G. Target Therapy of Breast Cancer. Current Pharmaceutical Design 2007. – Vol.13. – Р. 497-517.
6. De Boer R.H., Allum W.H., Ebbs S.R. et al. Multimodality therapy in inflammatory breast cancer: is there a place for surgery? // Ann Oncol 2000. – Sep. – Vol.11(9). – P. 1147-1153.
7. Fisher E.R., Gregorio R.M., Fisher B. еt al. The pathology of invasive breast cancer: a syllabus derived from findings of the National Surgical Adjuvant Breast Project (protocol № 4) // Cancer 1975. – Vol.36. – P. 1-85.
8. Fleming R.Y., Asmar L., Buzdar A.U. et al. Effectiveness of mastectomy by response to induction chemotherapy for control in inflammatory breast carcinoma // Ann Surg Oncol 1997. – Vol.4. – P. 452-461.
9. Panades M., Olivotto I.A., Speers C.H. et al. Evolving treatment strategies for inflammatory breast cancer: A population based survival analysis // J Clin Oncol 2005. – Vol.23(9). – P. 1941-1950.
10. Chevallier B., Bastit P., Graic Y. et al. The Centre H. Becquerel studies in inflammatory non metastatic breast cancer: combined modality approach in 178 patients // Br J Cancer 1993. – Vol.67. – P. 594-601.
11. Hortobagyi G., Singletary S.E., Strom E.A. Treatment of locally advanced and inflammatory breast cancer in: J.R. Harris, M.E. Lippman, M. Morrow (Eds.) Treatment of locally advanced and inflammatory breast cancer. Lippincott, Williams & Wilkins, Philadelphia; 2000: 645-660.
12. Vlastos G., Fornage B.D., Mirza N.W. et al., The correlation of axillary ultrasonography with histologic breast cancer downstaging after induction chemotherapy. Am J Surg 2000; 179: 446-452.
13. Chevallier B., Bastit P., Graic Y. et al. The Centre H. Becquerel studies in inflammatory non metastatic breast cancer: combined modality approach in 178 patients // Br J Cancer 1993. – Vol.67. – P. 594-601.
14. Hennessy B.T., Gonzalez-Angulo A.M., Hortobagyi G.N. et al. Disease-free and overall survival after pathologic complete disease remission of cytologically proven in flammatory breast carcinoma axillary lymph node metastases after primary systemic chemotherapy // Cancer 2006. – Vol.106(5). – P. 1000-1006.
15. Kim T., Lau J., Erban J. Lack of uniform diagnostic criteria for inflammatory breast cancer limits interpretation of treatment outcomes: a systematic review // Clin Breast Cancer 2006. – Vol.7(5). – P. 386-395.
16. Singletary S.E., Surgical management of inflammatory breast cancer // Seminars in oncology. – Vol.35, № 1, February 2008: 72-77.