22 березня, 2017
Терапия никотиновой зависимости
 Рекомендации Национальной онкологической сети США (NCCN), 2015
Рекомендации Национальной онкологической сети США (NCCN), 2015
Обзор
По статистике, в США курят 42,1 млн человек, что составляет около 18% взрослого населения страны. Ежегодно от причин, связанных с курением, преждевременно умирают 480 тыс. человек. Курение является фактором риска развития рака легкого, гортани, глотки, желудка, матки, яичника, мочевого пузыря, прямой кишки и других органов. На момент постановки диагноза 39% пациентов с раком легкого и 14% пациентов с колоректальным раком являлись курильщиками, из них 14 и 9% соответственно продолжали курить в течение 5 мес после постановки диагноза. По меньшей мере 30% всех случаев смерти онкологических больных связаны с курением.
В докладе по общей хирургии «Последствия курения для здоровья – 50 лет прогресса» (2014) были представлены выводы о том, что курение способствует:
• повышению риска смерти:
• развитию второй первичной опухоли;
• худшему ответу на специфическую терапию;
• более выраженным токсическим проявлениям на фоне лечения.
Поэтому, несомненно, важны отказ от курения всех пациентов с онкологическими заболеваниями и неукоснительное выполнение ими рекомендаций, адаптированных к их потребностям и проблемам.
Несмотря на то что доказано негативное влияние курения на противораковую терапию, многие пациенты продолжают курить во время лечения и после него. Распространенность курения среди пациентов онкологического профиля широко варьирует в зависимости от типа рака и других факторов, таких как пол, раса и возраст.
Риски, ассоциированные с курением у больных раком
Необходимо информировать пациентов о преимуществах отказа от курения, которые включают в себя увеличение выживаемости, улучшение клинического прогноза и качества жизни, уменьшение нежелательных эффектов терапии, таких как токсичные проявления и побочные действия на фоне приема препаратов, хирургические осложнения.
Перед началом терапии, до принятия решений относительно методики лечения, дозировки препаратов и сроков терапии, следует учитывать стаж курения в анамнезе и потенциальные риски, связанные с курением.
Хирургическое лечение
Курение негативно влияет на результаты хирургического лечения, затрагивая такие аспекты, как послеоперационные осложнения, качество жизни, продолжительность пребывания в стационаре, а также риск смерти.
В ходе исследований было доказано, что при раке легкого курение негативно влияет на успешность хирургической резекции, снижает качество послеоперационной жизни; постоянная одышка и боль в груди беспокоят пациентов и через 12 мес после операции. Хирургические осложнения включают в себя: инфицирование, сосудистые осложнения (тромбоэмболия, инсульт / нарушение мозгового кровообращения, инфаркт миокарда), а также легочные осложнения. При анализе данных пациентов, которым были проведены операции по поводу рака легкого, желудочно-кишечного тракта и мочевыводящих путей, выявлено, что у некурящих пациентов частота возникновения осложнений была значительно ниже, чем у курящих. Послеоперационные заболеваемость и смертность были выше среди курильщиков, наблюдался дозозависимый эффект при стратификации риска серьезных осложнений в зависимости от полученного показателя курящего человека «пачко-годы».
Среди пациентов, перенесших трансплантацию гемопоэтических стволовых клеток при остром лейкозе, у курящих чаще наблюдались легочные осложнения и период их пребывания в стационаре был более длительным.
Вследствие курения также может замедляться заживление ран и возникает предрасположенность к хирургическим осложнениям у лиц, которым проводятся реконструктивные операции после основного лечения. У пациентов с IІІ и IV стадией плоскоклеточного рака головы и шеи концентрация никотина в сыворотке была дозозависимо связана с повышенным риском развития раневых осложнений после реконструктивных операций головы и шеи, в то же время отказ от курения за 4 нед до операции существенно снижал риск их развития.
Лучевая терапия
Курение снижает ответ на лучевую терапию (ЛТ), уменьшает выживаемость, способствует возникновению осложнений, особенно у пациентов с раком головы и шеи.
У пациентов с ларингофарингеальным раком курение в период лечения было ассоциировано с повышенной заболеваемостью лучевым остеонекрозом и более частой госпитализацией.
По данным исследований, у пациенток, получавших ЛТ как часть лечения I или II стадии рака шейки матки, курение (>1 пачки в день) было наиболее сильным независимым фактором при прогнозировании долгосрочных осложнений со стороны мочевого пузыря, прямой или тонкой кишки. Отмечено, что даже минимальное/умеренное курение (<1 пачки в день) предполагает развитие осложнений со стороны тонкой кишки.
Курение во время ЛТ немелкоклеточного рака легкого приводило к значительному ухудшению локорегионарного контроля. Курение и ЛТ способствуют возникновению отдаленных сердечно-сосудистых осложнений у пациентов с раком грудной железы с 10-летней выживаемостью. Активное курение может также уменьшить эффективность ЛТ при раке простаты, прямой кишки и т.д.
Химиотерапия
Курение увеличивает риск развития осложнений, связанных с токсическим воздействием химиопрепаратов на легкие и сердечно-сосудистую систему (фиброз легких, кардиомиопатия). Сильнее проявляются такие симптомы, как потеря веса, кахексия, усталость. Более выраженным становится иммуносупрессивный эффект системных препаратов, что приводит к подавлению адаптивного и врожденного иммунитета, повышению риска развития инфекционных заболеваний, таких как пневмония, грипп. Активно изучается потенциальная связь между курением и химиорезистентностью.
Курение также может повлиять на метаболизм определенных химиотерапевтических препаратов. Оно воздействует на систему цитохрома Р450, вследствие чего может изменяться концентрация препарата в плазме крови и время элиминации, что негативно сказывается на эффективности препаратов. Таким образом, изменение метаболизма препаратов связано с определенными рисками и требует коррекции. К примеру, у курильщиков наблюдается быстрый клиренс эрлотиниба и иринотекана, поэтому им для достижения эквивалентного системного воздействия необходимы более высокие дозы этих препаратов, чем некурящим.
В то же время курение не изменяет фармакокинетических свойств таксансодержащих химиопрепаратов (доцетаксел, паклитаксел) и даже оказывает парадоксальное защитное действие, снижая риск развития лекарственно индуцированной нейтропении.
Преимущества отказа от курения для онкологических пациентов
Положительный эффект отказа от курения проявляется сразу и характеризуется такими изменениями, как снижение уровня оксида азота в крови, уменьшение проявлений респираторных симптомов (кашель, одышка), а также улучшение функции легких. В долгосрочной перспективе снижается риск развития сердечно-сосудистых, легочных заболеваний и злокачественных новообразований. По данным исследований, сравнение пациентов, продолжавших курить в период терапии, и тех, кто бросил курить незадолго до ее начала, показало, что во второй группе меньше риск смерти, рецидива и формирования второй первичной опухоли, показатель 5-летней выживаемости выше, а также лучше качество жизни.
Определение статуса курения
Врач должен регулярно оценивать статус курения пациента и попытки бросить курить, делая соответствующую запись в истории его болезни. Необходимо изначально выяснить:
• курил ли пациент когда-либо, и если да, то как часто;
• курит ли пациент в настоящее время;
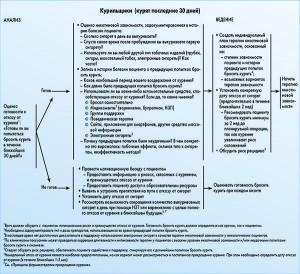
• курил ли пациент на протяжении последних 30 дней.
Вся информация должна быть отражена в медицинской документации.
Некурящим пациентам и тем, кто бросил курить ранее, следует настоятельно рекомендовать вести здоровый образ жизни, предоставляя информацию об обеспечиваемых им преимуществах.
Пациенты, продолжающие курить
У пациентов, которые курят в настоящее время, в первую очередь оценивается готовность бросить курить в течение ближайших 30 дней. У тех, кто готов отказаться от вредной привычки, следует определить степень зависимости от никотина, что обусловливает шансы на успех и риск рецидива. Для этого необходимо получить такую информацию: количество выкуриваемых в день сигарет, время с момента пробуждения до выкуривания первой сигареты, использует ли пациент другие формы табака (трубка, сигары, нюхательный табак, электронные сигареты), и если да, то как часто. Нужно также собрать информацию о предыдущих попытках бросить курить и выяснить, почему они были успешными/неуспешными. В частности, необходимо установить самый длительный период воздержания, дату последней попытки отказа от курения и какие вспомогательные средства в это время использовались, а также причину возврата к курению. При работе с пациентом необходимо оговорить конкретную дату отказа от сигарет или возможность сокращения курения с целью прекращения в ближайшем будущем. По данным метаанализа 10 рандомизированных исследований с участием 3760 онкологических пациентов, бросивших курить, эффективным является как резкий отказ от курения, так и постепенное уменьшение количества выкуриваемых сигарет вплоть до полного отказа от них. Таким образом, оба варианта могут быть использованы в терапии никотиновой зависимости. Медикаментозная терапия при помощи никотинзамещающих препаратов (НЗП) или варениклина может использоваться в качестве промежуточного шага на пути от сокращения курения к полному прекращению.
Мотивационное интервьюирование
Если пациент не выражает готовности бросить курить, рекомендуется провести с ним мотивационный диалог, цель которого – убедиться в том, что пациент знает о возможных рисках, связанных с курением, и преимуществах отказа от него. Врач должен учитывать отмечаемые пациентом препятствия на пути к отказу от курения. Подчеркивается важность поощрения и непосредственности в общении с пациентами, которые курят. При ведении мотивационного интервьюирования необходимо придерживаться таких принципов:
• сопереживать пациенту;
• выявлять противоречия;
• уменьшать сопротивление;
• поощрять самостоятельность пациента.
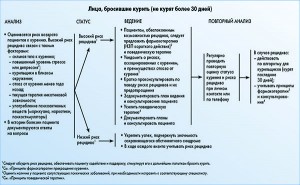
Пациенты, курившие в прошлом
У пациентов, которые не курили последние 30 дней, необходимо оценить риск рецидива. Высокий риск связан с такими факторами: сильная тяга к курению, повышенный уровень стресса или депрессия, наличие курильщиков в близком окружении, отказ от курения менее года назад, текущая терапия никотиновой зависимости, употребление психоактивных веществ. Необходимо обсудить риск рецидива с пациентами и содействовать им в повторных попытках бросить курить.
Ведение пациентов, демонстрирующих повышенный риск рецидива, включает в себя применение фармакотерапии (НЗП короткого действия). При необходимости могут быть предложены краткие консультации о факторах риска рецидива и профилактике рецидивов, применение поведенческой терапии. У пациентов с низким риском рецидива необходимо укреплять веру в успех, подчеркивая важность воздержания от сигарет. Риск рецидива должен быть перепроверен при последующих посещениях.
Важно регулярно пересматривать статус курения пациентов при личном контакте или в ходе разговора по телефону.
Прекращение курения в ходе терапии онкологических заболеваний
Необходимо составить персонализированный план терапии никотиновой зависимости, в котором учитывается степень зависимости, предыдущие попытки бросить курить, а также возможные варианты терапии. Рекомендуемые сроки отказа от курения – 2 нед до каких-либо плановых операций. Наиболее эффективной является фармакотерапия в комбинации с поведенческой терапией.
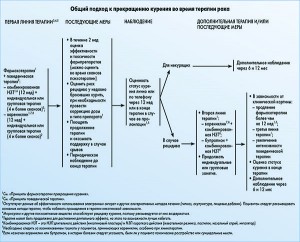
Первая линия терапии
По рекомендациям, основанным на данных метаанализа клинических исследований, наиболее эффективным является комбинированный подход, включающий фармакотерапию и поведенческую терапию никотиновой зависимости у онкологических пациентов. К первой линии терапии относится применение комбинации НЗП (длительного и короткого действия) или варениклина и поведенческих тренингов. Никотинзаместительная терапия (НЗТ) включает в себя использование никотинового пластыря и НЗП короткого действия, таких как никотиновая жевательная резинка, пастилки, ингалятор или назальный спрей, которые используются по мере необходимости.
Дальнейшее наблюдение
В течение первых двух недель после прекращения курения оценивается эффективность и безопасность фармпрепаратов. Это можно делать как во время визита пациента, так и по телефону. В дальнейшем следует оценивать возможный риск рецидива, при необходимости корректируя дозу или назначая другой препарат. Дальнейшая оценка статуса курения проводится на 12-й неделе, на 6-м и 12-м месяце. Для пациентов, которые вернулись к курению, может быть рассмотрена возможность применения второй линии терапии.
Вторая и третья линии терапии
Вторая линия терапии включает применение варениклина или бупропиона в сочетании с комбинированной НЗТ. Третья линия терапии состоит из трех подходов: комбинированная терапия варениклином, бупропионом и НЗТ, монотерапия нортриптилином или клонидином.
Терапия в случае рецидива
Рекомендуется продолжить поведенческую терапию с любым альтернативным препаратом, применяемым в первой, второй или третьей линии терапии. Статус курения должен быть пересмотрен в конце каждого курса терапии с дополнительным обследованием на 6-м и 12-м месяце после успешного отказа от курения.
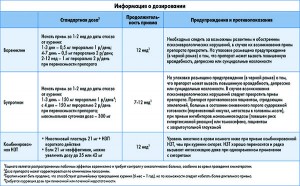
Общие рекомендации по фармакотерапии
Начальная продолжительность лечения составляет 12 нед для варениклина и комбинации НЗП и 7-12 нед для бупропиона. Допустима более длительная терапия, но следует избегать неоправданно продолжительного лечения. Коррекция дозы проводится в зависимости от клинической картины. Положительным результатом считается воздержание от курения не менее 6 мес с начала терапии никотиновой зависимости.
Варениклин
Препарат является частичным агонистом α4β2Н-холинорецепторов. Варениклин частично имитирует воздействие никотина на головной мозг и конкурентно ингибирует связывание никотина.
Может использоваться как монотерапия, так и в сочетании с НЗП. По данным метаанализа, варениклин увеличивает вероятность отказа от курения почти в три раза по сравнению с плацебо. Курс варениклина продолжительностью 24 нед эффективно способствует отказу от курения у пациентов, которые не собирались бросать курить, но готовы постепенно сокращать потребление сигарет. Метаанализ рандомизированных контролируемых исследований по прекращению курения, проведенный в 2015 г., не выявил никаких свидетельств того, что варениклин увеличивает риск самоубийства или попыток самоубийства, возникновения суицидальных наклонностей или депрессии.
Побочные эффекты при приеме варениклина: тошнота, бессонница и необычные сновидения, головная боль, сердечно-сосудистые события.
Комбинированная никотинзаместительная терапия
НЗТ – альтернативный способ доставки никотина. Он используется для уменьшения симптомов отмены, вызванных отказом от курения. Наиболее эффективной является комбинация НЗП длительного и короткого действия.
В качестве НЗП в настоящее время используются: никотиновый пластырь, жевательная резинка, ингаляторы, пастилки, спрей и таблетки. Польза от НЗТ перевешивает потенциальные риски. Уровень никотина в крови при проведении НЗП значительно ниже, чем при курении. НЗП не являются значимыми предикторами развития рака легких, в отличие от сигарет. Добавление поведенческой терапии к НЗТ повышает шансы на успех почти в три раза.
Бупропион
Бупропион ранее был одобрен для лечения депрессии, но также стала очевидной его эффективность в лечении никотиновой зависимости. Помимо воздействия на дофаминергические и адренергические системы, препарат действует также в качестве ингибитора Н-холинорецепторов. По некоторым данным, бупропион особенно эффективен в лечении никотиновой зависимости у лиц, страдающих депрессией.
Среди побочных эффектов наиболее значимыми являются развитие судорожного синдрома и психоневрологических нарушений.
Поведенческая терапия
Поведенческая терапия может повысить мотивацию пациента и способствовать соблюдению фармакотерапии.
В качестве общего принципа интенсивная поведенческая терапия предпочтительнее кратких консультаций. Данные подтверждают, что более частые или более длительные сеансы дают лучшие результаты. Интенсивная поведенческая терапия состоит из по крайней мере 4 сеансов (групповых или индивидуальных) продолжительностью не менее 10 мин – обычно 30 мин или дольше. Даже короткие 3-минутные консультации дают свой, хоть и незначительный, результат в борьбе с пагубной привычкой, поэтому не следует ими пренебрегать.
Наиболее успешными стратегиями поведенческой терапии считаются консультирование, социальная поддержка и мотивационное интервьюирование. Следует учитывать степень никотиновой зависимости, предыдущие попытки бросить курить и вспомогательные средства, которые использовались ранее при попытках отказа от курения. Пациенту предоставляются такие методы терапии, которые помогут справиться с симптомами отмены, триггерами окружающей среды и стрессовыми ситуациями. Например, добавление когнитивно-поведенческой терапии, направленной на овладение навыками управления стрессом, дает лучшее результаты в терапии зависимости по сравнению с одной лишь стандартной терапией. Кроме того, можно использовать мобильные приложения или печатные материалы. Пациенты с сопутствующими психическими заболеваниями или зависимостью от других препаратов должны быть направлены к соответствующему специалисту.
Консультирование проводится при личном контакте, по телефону, либо в формате групповой терапии. В любом случае при выборе методик терапии следует руководствоваться предпочтениями пациента, данными истории болезни, а также наличием ресурсов.
Полный текст Руководства на www.nccn.org
Перевела с англ. Екатерина Марушко