22 березня, 2017
Исследование BIRCH (II фаза): эффективность атезолизумаба у пациентов с немелкоклеточным раком легкого, отобранных по PD-L1
Обновленные данные об эффективности
Первичный анализ результатов исследования показал клинически значимую частоту объективного ответа при применении атезолизумаба у пациентов с немелкоклеточным раком легкого (НМРЛ), причем как предварительно получавших терапию, так и ранее не леченных.
В настоящее время озвучены обновленные результаты исследования, касающиеся эффективности атезолизумаба.
Критерием включения пациентов в клиническое несравнительное исследование II фазы BIRCH по применению атезолизумаба (антитела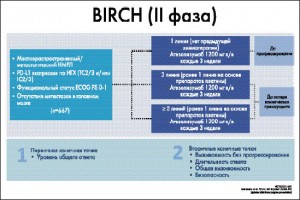 против PD-L1) в качестве 1-й или последующей линии терапии при распространенном НМРЛ являлся иммуногистохимически подтвержденный уровень экспрессии PD-L1. В исследование были включены пациенты с IIIB/IV стадией заболевания или рецидивировавшим НМРЛ без метастазов в центральной нервной системе.
против PD-L1) в качестве 1-й или последующей линии терапии при распространенном НМРЛ являлся иммуногистохимически подтвержденный уровень экспрессии PD-L1. В исследование были включены пациенты с IIIB/IV стадией заболевания или рецидивировавшим НМРЛ без метастазов в центральной нервной системе.
В исследовании приняли участие 659 пациентов, разделенных на три группы. В первую группу вошли пациенты, ранее не получавшие химиотерапии. Критерием включения во вторую и третью группу было прогрессирование заболевания после предшествующей терапии, то есть атезолизумаб назначался во второй или третьей линии терапии соответственно. Пациенты ранее получали терапию на основе препаратов платины, а при наличии в опухоли мутаций EGFR – терапию ингибиторами тирозинкиназы.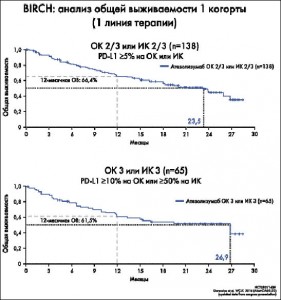
Выраженность экспрессии PD-L1 оценивалась с использованием иммуногистохимического теста VENTANA SP142. Для участия в исследовании отбирались пациенты, у которых уровень экспрессии PD-L1 на опухолевых или инфильтрующих опухоль иммунных клетках (ОК и ИК соответственно) составлял 5% или более. Проводилась стратификация в зависимости от уровня экспрессии PD-L1 и оценка клинических результатов как у всех участников исследования, так и в подгруппе с максимальной экспрессией PD-L1 (ОК 3 или ИК 3). Участники исследования получали 1200 мг атезолизумаба внутривенно каждые 3 недели. Терапию продолжали до тех пор, пока сохранялась клиническая польза, при условии отсутствия неприемлемой токсичности или ухудшения симптомов в связи с прогрессированием заболевания.
Первичной конечной точкой исследования являлась частота объективного ответа (ЧОО), подтвержденная независимой группой наблюдателей. Дополнительные конечные точки включали в себя ЧОО по оценке исследователя, длительность ответа (ДО), общую выживаемость (ОВ), выживаемость без прогрессирования (ВБП) и оценку биомаркеров.
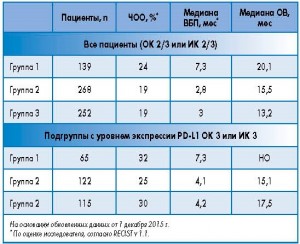
Эффективность атезолизумаба оценивалась у всех 659 пациентов. Анализ данных показал, что показатель ЧОО выше у больных, получавших атезолизумаб в качестве терапии первой линии, и составляет 24, 19 и 19% для первой, второй и третьей группы соответственно (табл.). Медиана ДО составила 13,1 мес (95% ДИ 9,9-17,5) для первой группы и 14,1 мес (95% ДИ 10,5 – не определено) для второй и третьей групп. Большинство пациентов продолжают отвечать на терапию. При медиане последующего наблюдения 14,6 мес отмечено значительное преимущество в ОВ у пациентов, получавших атезолизумаб в качестве терапии первой линии по сравнению с пациентами, получавшими атезолизумаб в качестве терапии второй и третьей линии: медиана ОВ составила 20,1, 15,5 и 13,2 мес для первой, второй и третьей групп соответственно.
Улучшение показателей наблюдалось у пациентов с максимальной экспрессией PD-L1 (ОК 3 или ИК 3): ЧОО составила 32, 25 и 30% у первой, второй и третьей групп соответственно, а ВБП – 7,3 мес для первой группы, 4,1 и 4,2 мес для второй и третьей (табл.).
Ответ на терапию атезолизумабом наблюдался независимо от EGFR- и KRAS-статуса или результатов гистологического исследования опухоли. Побочные эффекты, связанные с лечением, соответствовали наблюдаемым в предыдущих исследованиях, посвященных изучению атезолизумаба, и были сопоставимы по группам наблюдения. Наиболее распространенными побочными явлениями были усталость (18%) и тошнота (10%).
Таким образом, при более длительном наблюдении монотерапия атезолизумабом продолжает демонстрировать положительные клинические результаты в отношении НМРЛ. Эти данные способствуют дальнейшему исследованию атезолизумаба в качестве первой или последующей линии терапии распространенного НМРЛ у пациентов, отобранных по уровню экспрессии PD-L1.
Wakelee H. et al. Phase II trial of atezolizumab for patients with PD-L1 selected advanced NSCLC (BIRCH): updated efficacy and exploratory biomarker results, 2016.
Перевела с англ. Екатерина Марушко