11 квітня, 2017
Сучасні можливості лікування гострих респіраторних вірусних інфекцій у дітей з алергічною патологією
Віруси – причина розвитку більшості гострих інфекцій дихальних шляхів, які в сукупності забирають понад 4 млн людських життів на рік. Причому реальна кількість хворих перевищує офіційну статистику в 1,5-2 рази. За даними Всесвітньої організації охорони здоров’я (ВООЗ), у світі в міжпандемічні періоди на грип хворіє в середньому близько 1 млрд осіб на рік, причому в 3-5 млн із них розвиваються тяжкі форми інфекції, а від 300 тис. до 500 тис. пацієнтів помирають. Максимальна летальність від респіраторних інфекцій відзначається у хворих раннього дитячого та літнього віку. Втрати дитячих життів унаслідок розвитку пневмонії, які сягають 1,4-1,8 млн щороку (що перевищує сумарну летальність від малярії, інфекції вірусу імунодефіциту людини / синдрому набутого імунодефіциту і кору), значною мірою асоційовані з грипом (17% випадків) та респіраторно-синцитіальною вірусною (RSV) інфекцією (29%). Це визначає провідні – за медико-соціальною значущістю – позиції цих гострих респіраторних вірусних інфекцій (ГРВІ) у переліку захворювань людини [2].
Високий рівень захворюваності на ГРВІ та грип завдає істотної шкоди як економіці країни загалом, так і сімейному бюджету кожної родини, насамперед через втрату хворими працездатності. Часті випадки респіраторних захворювань асоційовані із соціальною дезадаптацією дитини та несуть потенційні ризики виникнення педагогічних проблем, змін психологічного клімату в родині та зниження якості життя всіх її членів [13, 14].
ГРВІ являють собою групу захворювань із подібними епідеміологічними та клінічними особливостями, але різноманітною етіологією (вірусною, вірусно-бактеріальною, змішаною). Сьогодні відомо понад 300 збудників респіраторних інфекцій, серед яких найпоширенішими є віруси: на них припадає до 90% від загальної кількості всіх дитячих захворювань.
Збудники ГРВІ вірусної етіології належать до різних родин. Серед них найбільш відомими є РНК-віруси: віруси грипу, парагрипу, респіраторно-синцитіальні віруси (РСВ), метапневмовіруси, коронавіруси, риновіруси, ентеровіруси та ротавіруси; ДНК-віруси: аденовіруси, бокавіруси. Йдеться як про давно відкриті та добре вивчені, так і про нові штами вірусів, ідентифіковані останніми роками завдяки більш широкому використанню в дослідженнях молекулярно-біологічних методів [3, 15, 20].
Ще одна актуальна проблема сучасної медицини – важко контрольоване поширення алергічної патології у світі, особливо в пацієнтів дитячого віку. У зв’язку з недавнім відкриттям нових етіопатогенетичних механізмів розвитку алергічної патології, зокрема бронхіальної астми (БА), стало зрозуміло, що частина загострень хронічних алергічних захворювань пов’язана з епізодами ГРВІ та складною взаємодією генетичної схильності пацієнта і факторів навколишнього середовища. Проте особливе значення приділяється саме респіраторній інфекції, зокрема вірусній, яка відіграє значну роль у реалізації впливу навколишнього середовища на розвиток алергічного захворювання та його загострення, що було встановлено під час багатьох епідеміологічних досліджень [3, 4]. Зокрема, чітко простежується зв’язок між сезонним зростанням рівня захворюваності на ГРВІ та частотою госпіталізацій, пов’язаних із загостренням БА. Насамперед це характерно для дітей [7]. Результати низки клініко-епідеміологічних досліджень підтверджують, що приблизно в 80-85% усіх випадків загострення астми в дітей та в 60-75% – у дорослих основними тригерами є респіраторні віруси [7, 8]. Ці віруси виступають у ролі основного чинника і здатні опосередковано спричиняти обструкцію дихальних шляхів [9-11]. C.S. Murray і співавт. вказують на те, що причиною загострення БА у дорослих і дітей старшого віку найчастіше є риновіруси – до 80% випадків, віруси грипу – до 15%, ентеровіруси – 4%, а також метапневмовірус і РСВ – 2% випадків усіх вірус-індукованих загострень. Також причиною розвитку бронхообструкції можуть бути аденовіруси, віруси парагрипу 1-го і 3-го типу, коронавіруси [4].
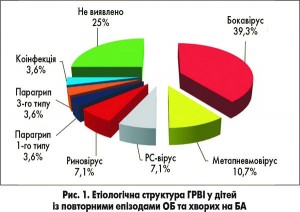
ГРВІ не тільки є тригером загострення астми та коморбідної патології, а й значно ускладнюють їх перебіг. Результати відповідних досліджень свідчать про те, що у хворих на БА з симптомами ГРВІ спостерігається більш тяжкий ступінь порушення вентиляційної функції легень. Також виявлено безпосередній зв’язок між вірусною інфекцією та летальністю внаслідок загострення БА, зокрема, в тому випадку, коли пацієнт не отримував необхідної терапії [2, 3, 5, 6, 9]. Показники поширеності та вираженості ураження респіраторними вірусами значно відрізняються у різних вікових групах пацієнтів. Так, за результатами дослідження, проведеного О.М. Охотніковою та спіавт., було встановлено, що найчастіше у дітей з обструктивним бронхітом (ОБ) виявляли бокавірус 1-го типу (39,3%). Другим за частотою ідентифікації був метапневмовірус, який було визначено у 10,7% дітей Риновіруси та РС-вірус виявили у 7,1% дітей відповідно. У 3,6% випадків ідентифіковано віруси парагрипу 1-го і 3-го типу, у 3,6% випадків зафіксовано коінфекцію (метапневмовірус та вірус парагрипу 1-го типу) (рис. 1).
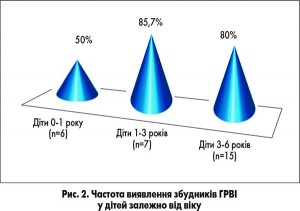
При розподілі частоти ідентифікованих респіраторних вірусів залежно від віку пацієнтів (рис. 2) було виявлено 80-85,7% позитивних проб у дітей старше 1 року, тоді як у хворих віком до 1 року кількість позитивних проб на наявність збудників ГРВІ складала 50%, але різниця у показниках не була статистично значущою (р>0,05).
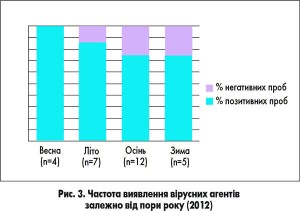
Ідентифікація респіраторних вірусів здійснювалася упродовж року. У зразках, взятих у дітей навесні 2012 р., віруси виявили у 100% випадків захворювання, влітку – у 86%, восени віруси ідентифікували у 75%, тоді як узимку тільки у 40% випадків (рис. 3).
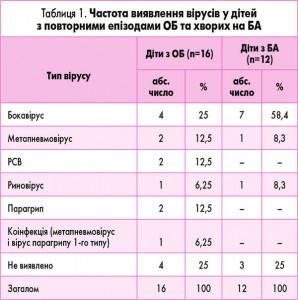
У результаті дослідження частоти виявлення респіраторних вірусів залежно від діагнозу отримано дані, подані у таблиці 1. У дітей обох груп віруси було ідентифіковано у 75% випадків. Як у дітей із ОБ, так і у дітей із загостренням БА найчастіше виявляли бокавірус 1-го типу. У пацієнтів з ОБ кількість випадків виявлення бокавірусу – 25%, тоді як у дітей з БА – 58,4%. Частота виявлення бокавірусів у групах дітей з ОБ та БА вірогідно значимо не відрізнялася (р>0,05), але клінічно значущу відмінність усе ж таки встановлено.
Загострення БА у дітей у 2,3 раза частіше було пов’язане з бокавірусною інфекцією порівняно з хворими на ОБ (відносний ризик – ВР – 2,3; 95% довірчий інтервал – ДІ – 0,9-6,2).
Незважаючи на значні досягнення сучасної медицини, проблема ефективного контролю за захворюваністю на ГРВІ і сьогодні залишається актуальною. Одна з основних проблем сучасної вірусології– постійні зміни антигенної структури вірусів, що приводять до формування високотоксичних, резистентних до лікування штамів. Окрім цього, якщо на сучасному етапі негативну роль вірусних агентів у розвитку та загостренні БА і коморбідних захворювань визнано безумовною, то питання діагностики, лікування та профілактики вірус-індукованого загострення БА й досі не вирішено остаточно [3, 5, 9] через низку причин: це й велика різноманітність респіраторних вірусів, і складність їх верифікації (у рутинній практиці методи експрес-діагностики грипу, ГРВІ та бактеріальних респіраторних інфекцій поки що є малодоступними) та визначення особливостей патогенезу, і недостатня кількість противірусних препаратів із доведеною клінічною ефективністю відносно респіраторних збудників тощо [1-3]. Цим, власне, і можна пояснити практично повну відсутність у міжнародних і вітчизняних рекомендаціях відомостей про діагностику та лікування вірус-індукованого загострення БА [3, 5, 9, 10].
Загальновідомо, що один з найбільш обґрунтованих та ефективних заходів боротьби з щорічними епідеміями грипу – вакцинопрофілактика. Водночас вакцини, які могли б допомогти в контролі та запобіганні розвитку інших вірусних захворювань, відсутні.
Зауважимо, що сьогодні педіатри обмежені у виборі противірусних препаратів для терапії ГРВІ та грипу у дітей. Спектр противірусних препаратів із доведеною клінічною ефективністю складають переважно блокатори М2-каналів та інгібітори нейрамінідази, а також рибавірин, який застосовують у терапії тяжких форм РСВ-інфекції. Однак у зв’язку з розвитком у циркулюючих штамів резистентності препарати адамантанового ряду (амантадин, ремантадин), які застосовують у лікуванні грипу А, помітно втратили свої позиції в його терапії. У деяких країнах частка резистентних до них штамів вірусу грипу А сягає 90%, що в США з минулого епідемічного сезону стало причиною заборони використання адамантанів для лікування і профілактики грипу [9, 10]. Інгібітори нейрамінідази (осельтамівір, занамівір), які застосовують у лікуванні грипу А і В, є ефективними відносно більшості вірусів грипу, у тому числі пандемічного, але останніми роками відзначається суттєве зростання числа резистентних до осельтамівіру штамів вірусу грипу А/H1N1. Найбільше таких штамів виділено в Норвегії (64%), Франції (39%), а також у США (9%), Гонконгу та Австралії [10].
Наявна ситуація актуалізує пошук нових препаратів із широким спектром противірусної активності та з іншими істотними для лікування ГРВІ терапевтичними ефектами (протизапальними, антигістамінними). Очевидно, що препарати для терапії ГРВІ, у тому числі грипу, мають сприяти елімінації збудника, стимулювати захисні сили людського організму та корегувати функціональні порушення, що виникають у процесі хвороби [11].
Ґрунтуючись на аналізі вітчизняних та закордонних опублікованих праць щодо цього питання, вважаємо перспективним використання інноваційних лікарських препаратів, створених на основі реліз-активних антитіл до ендогенних регуляторів. Завдяки особливій технології виробництва цим препаратам притаманна специфічна фармакологічна активність, яка отримала назву «реліз-активність». Саме ця властивість забезпечує їх високу безпеку та широкий терапевтичний коридор [12].
У 2011 р. фармацевтична науково-виробнича компанія ТОВ «НПФ «Матеріа Медика Холдінг» випустила комбінований противірусний препарат Ергоферон®, який містить реліз-активні афінно-очищені антитіла до інтерферону-гама людини (РА АТ до ІФН-γ), гістаміну (РА АТ до гістаміну) і CD4 (РА АТ до CD4) і чинить комплексну дію (посилену противірусну, протизапальну та антигістамінну) [13, 14].
Посилена противірусна дія препарату Ергоферон реалізується за рахунок впливу РА АТ до ІФН-γ на систему інтерферонів у поєднанні з активацією процесів розпізнавання вірусів системою CD4. Експериментально і клінічно доведено, що РА АТ до ІФН-γ підвищують вірус-індуковану продукцію ІФН-γ та ІФН-γ та асоційованих із ними інтерлейкінів (ІЛ‑2, ІЛ‑4, ІЛ‑10 тощо), поліпшують ліганд-рецепторну взаємодію ІФН, відновлюють цитокіновий статус. РА АТ до ІФН-γ також сприяють активації фагоцитозу і NK-клітин, відновленню балансу T-хелперної (1-го і 2-го типу) активності імунної відповіді та В-лімфоцитів з підвищенням продукції захисних антитіл – IgG і IgA, включаючи секреторний sIgА, який сприяє посиленню місцевого імунітету, і гальмуванням продукції алергічних антитіл – IgЕ [15-19].
РА АТ до CD4 регулюють функціональну активність CD4-рецептора, представленого на антиген-презентуючих клітинах (макрофагах, дендритних клітинах) і Т-хелперах 1-го і 2-го типу, що призводить до підвищення функціональної активності CD4-лімфоцитів, нормалізації імунорегуляторного індексу CD4/CD8, а також субпопуляційного складу імунокомпетентних клітин (CD3, CD4, CD8, CD16, CD20) [13, 17].
Таким чином, поєднання РА АТ до ІФН-γ і РА АТ до CD4 впливає на універсальні механізми противірусного захисту, які відіграють ключову роль у розвитку імунної відповіді незалежно від типу вірусу.
У низці відповідних експериментальних досліджень показано високу противірусну активність препарату Ергоферон та його компонентів. Так, наприклад, доведено порівняно з oсельтамівіром противірусний ефект РА АТ до ІФН-γ стосовно вірусу пандемічного грипу А(H1N1) (2009), що проявлявся пригніченням реплікації вірусу в легеневій тканині, збільшенням тривалості життя і зниженням летальності лабораторних тварин [20]. Також in vitro на моделі РСВ-інфекції продемонстровано, що Ергоферон інгібує реплікацію РСВ, достовірно знижуючи вірусне навантаження на клітини лінії HeLa, і є нетоксичним [21]. Отримані результати зазначених досліджень свідчать про противірусну активність препарату Ергоферон стосовно РСВ і можливості його використання у складі комплексної терапії і профілактики цього захворювання, що було підтверджено і в ході проведення клінічних досліджень у дітей, наприклад, такого компонента препарату Ергоферон, як РА АТ до ІФН-γ [22].
Противірусну активність препарату Ергоферон доповнюють ефекти РА АТ до гістаміну, які чинять протизапальну та антигістамінну дію. Завдяки модифікуючій дії на гістамін-залежну активацію периферичних і центральних H1-рецепторів РА АТ до гістаміну сприяють зменшенню проникності судин і зниженню агрегації тромбоцитів у реакціях на контакт із алергеном, пригніченню вивільнення гістаміну з опасистих клітин і базофілів, оптимізації продукції лейкотрієнів. Як наслідок, знижується тонус гладенької мускулатури бронхів і виразність супутніх інфекційному процесу алергічних реакцій. Клінічно це приводить до скорочення тривалості і виразності ринореї, набряку слизової оболонки носа, кашлю і чхання [13, 18].
Таким чином, 3-компонентний склад препарату Ергоферон дозволяє впливати на різні механізми інфекційно-запального процесу і формувати адекватний противірусний ефект широкого спектру без ризику розвитку резистентності.
Терапевтичну ефективність цього препарату підтверджено численними експериментальними і клінічними випробуваннями [18, 21, 23-31, 34]. Слід відзначити, що дослідження безпеки та ефективності препарату Ергоферон, результати яких опубліковано, було проведено відповідно до чинних стандартів дослідження лікарських препаратів та принципів доказової медицини.
З метою вивчення терапевтичної ефективності препарату Ергоферон у лікуванні ГРВІ і грипу проведено низку рандомізованих досліджень, у тому числі золотий стандарт дизайну досліджень із позицій доказової медицини – рандомізовані багатоцентрові подвійні сліпі плацебо-контрольовані дослідження [18, 25, 27].
Упродовж 2-х епідемічних сезонів (2010/2011 і 2011/2012 рр.) за участю 213 хворих було проведено багатоцентрове порівняльне рандомізоване клінічне дослідження ефективності препарату Ергоферон та осельтамівір у лікуванні грипу у дорослих.
Максимальну ефективність препарату Ергоферон відзначали на 2-гу добу лікування, що проявилося нормалізацією температури тіла у 48% хворих, які отримували цей препарат, проти 28% пацієнтів, яких лікували осельтамівіром (p=0,008). Застосування препарату Ергоферон зменшувало необхідність використання антипіретиків із 1-го дня терапії, а також частоту розвитку бактеріальних ускладнень і необхідність застосування антибіотиків. Число пацієнтів, які потребували антипіретичної терапії, на 2-й день лікування у групі пацієнтів, які отримували Ергоферон, було втричі менше, ніж у групі тих, кого лікували осельтамівіром. У ході дослідження у 1-й групі не виявлено жодного випадку розвитку ускладнень, які потребували б призначення антибіотиків або госпіталізації, а також не відзначено небажаних ефектів, пов’язаних із прийомом цього препарату. На підставі отриманих результатів автори зробили висновок про те, що ефективність препарату Ергоферон у лікуванні грипу можна порівняти з ефективністю осельтамівіру [25].
Оцінку ефективності та безпеки профілактичного застосування препарату Ергоферон здійснено у відкритому проспективному порівняльному рандомізованому дослідженні за участю хворих на бронхіальну астму дітей віком 3-7 років, яке проводилося в епідемічний сезон ГРВІ. За його результатами встановлено, що профілактичний прийом препарату Ергоферон упродовж 1 міс дозволяє удвічі (р<0,05) знизити частоту епізодів ГРВІ та загострень БА у дітей дошкільного віку. На тлі застосування препарату не зареєстровано жодного випадку розвитку бактеріальних ускладнень, погіршення перебігу респіраторної інфекції та небажаних змін біохімічних і загальноклінічних лабораторних показників [1, 7, 8, 31].
Ергоферон продемонстрував хорошу сумісність із препаратами симптоматичної терапії ГРВІ та препаратами інших груп, які дозволені для застосування у лікуванні дітей (антипіретиками, інгаляційними кортикостероїдами, препаратами кромогліцієвої кислоти, антагоністами лейкотрієнових рецепторів, β2-агоністами короткої дії та місцевими антисептиками).
Мета дослідження, проведеного на кафедрі педіатрії № 1 на базі НДСЛ «ОХМАТДИТ» і Республіканської консультативної поліклініки, – оцінка клінічної ефективності та безпеки використання препарату Ергоферон у комплексній терапії ГРВІ у дітей з БА і коморбідною патологією.
Згідно з критеріями включення до дослідження увійшли діти віком від 6 міс до 6 років із діагнозом БА або рецидивного синдрому бронхіальної обструкції (РБОС), у яких відмічалося підвищення температури тіла ≥ 37,5 °С та наявність щонайменше одного катарального симптому (кашлю, риніту, почервоніння, болю у горлі) та одного з симптомів інтоксикації (зниження апетиту, нудоти, головного болю, в’ялості, болю у м’язах, пітливості або ознобу). За методом випадкової вибірки із загального числа хворих (40 пацієнтів) сформували 2 групи дітей (по 20 дітей – у кожній). Усі пацієнти отримували лікування згідно з чинними протоколами та необхідну симптоматичну терапію з урахуванням клінічних симптомів ГРВІ. Крім цього, пацієнти основної групи отримували препарат Ергоферон за лікувальною схемою з 1-ї доби визначення симптомів хвороби: 1-ша доба лікування – 8 таблеток (згідно з інструкцією).
Оцінка ефективності препарату Ергоферон у лікуванні БА та РБОС здійснювалася за низкою критеріїв. Як основний критерій використано показники тривалості підвищеної температурної реакції та тривалості синдрому БОС. Крім цього, визначали частку пацієнтів, у яких розвинулись вторинні (бактеріальні ускладнення, які вимагали призначення антибіотиків), додатково оцінювали інтоксикаційний та катаральний синдроми.
Статистична обробка результатів дослідження проводилася за допомогою програм Statistica 6,0.
Аналіз отриманих результатів показав, що клінічна картина типового перебігу ГРВІ характеризувалась гострим початком захворювання, наявністю синдрому інтоксикації та катарального синдрому та розвитком загострення у вигляді БОС з 2-го (або 3-го) дня захворювання. Своєчасне призначення препарату Ергоферон сприяло нормалізації температури тіла в 2,5 раза швидше, ніж у групі контролю (табл. 2). У цілому завдяки застосуванню цього препарату у дітей основної групи вдалося запобігти розвитку бактеріального ускладнення порівняно з дітьми контрольної групи (р>0,05).
Отже, на підставі проведеного аналізу літератури та власних спостережень щодо ролі нових респіраторних вірусів у провокації БОС у дітей та можливостей сучасної противірусної терапії можна зробити висновок про доцільність призначення препарату Ергоферон у комплексній терапії ГРВІ у дітей з хронічною алергічною патологією: висока ефективність цього препарату та відсутність небажаних явищ у період терапії роблять його препаратом вибору етіотропної, патогенетичної терапії ГРВІ і грипу у дітей різних вікових груп.
Список літератури знаходиться в редакції.