5 лютого, 2017
Эволюция базисной терапии бронхиальной астмы и ХОЗЛ

По материалам 26-го конгресса Европейского респираторного общества,
3-7 сентября, г. Лондон, Великобритания
 26-й конгресс Европейского респираторного общества (ERS) стал значимым глобальным событием для респираторной медицины. Учитывая масштабность мероприятия (количество делегатов в этом году превысило 20 тыс.), в качестве площадки для его проведения был выбран London Excel – один из крупнейших выставочных центров Великобритании.
26-й конгресс Европейского респираторного общества (ERS) стал значимым глобальным событием для респираторной медицины. Учитывая масштабность мероприятия (количество делегатов в этом году превысило 20 тыс.), в качестве площадки для его проведения был выбран London Excel – один из крупнейших выставочных центров Великобритании.
Пульмонология является одним из приоритетных направлений научно-исследовательской работы немецкой фармацевтической компании Boehringer Ingelheim. На ERS-2016 при поддержке Boehringer Ingelheim прошли симпозиумы, на которых были представлены новейшие достижения в ведении хронической бронхообструктивной патологии – бронхиальной астмы (БА) и хронического обструктивного заболевания легких (ХОЗЛ).
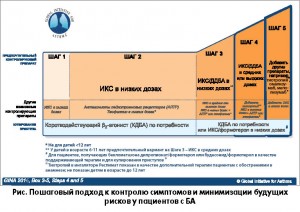
Профессор Сорен Педерсен (Дания) рассказал о важных изменениях в рекомендациях по ведению БА Глобальной инициативы по борьбе с астмой (GINA), касающихся фармакотерапии. В частности, новыми препаратами, рекомендуемыми на шаге 5, стали омализумаб и меполизумаб. В GINA-2015 на шаге 5 тиотропия бромид наравне с оральными кортикостероидами рекомендовался в качестве «других возможных контролирующих препаратов»; в GINA-2016 статус тиотропия на этом шаге был повышен до «предпочтительного контролирующего препарата» (рис.). Кроме того, тиотропий теперь рекомендуется для применения у детей в возрасте 12 лет и старше (прим. ред. – в Украине лекарственный препарат Спирива Респимат пока разрешён к применению только с 18 лет).
По словам докладчика, уже получены данные об эффективности и безопасности тиотропия и у детей в возрасте до 11 лет. Так, результаты исследования CanoTinA-asthma показали, что назначение тиотропия Респимат в качестве дополнительной терапии детям в возрасте от 6 до 11 лет, которые уже используют ингаляционные кортикостероиды (ИКС) или же сочетают ИКС с другими лекарственными средствами для поддерживающей терапии астмы, значительно улучшает легочную функцию. При этом безопасность и переносимость тиотропия Респимат были сопоставимы с таковыми показателями плацебо. Кроме того, новый post-hoc анализ исследования NinoTinA-asthma свидетельствует о том, что эффективность и безопасность тиотропия Респимат у детей в возрасте от 1 года до 5 лет при добавлении его к поддерживающей терапии сравним с соответствующими показателями, зафиксированными у более старших детей и у взрослых.
О значимости обострений ХОЗЛ для прогноза и способах их профилактики рассказал профессор Гарвардского Университета, доктор Бартоломе Селли (США).
В соответствии с определением Американского торакального общества (ATS) и Европейского респираторного общества (ERS) обострение – это событие в течении заболевания, характеризующееся острым изменением имеющихся у пациента одышки, кашля и/или отделения мокроты по сравнению с обычным уровнем, которое выходит за рамки ежедневных колебаний и является основанием для изменения плановой терапии.
Похожее определение дает GOLD (2013): «острое событие, характеризующееся усугублением симптомов пациента, выходящее за рамки ежедневных колебаний и требующее изменения лечения».
Согласно Национальному институту клинического мастерства Великобритании (NICE) под обострением следует понимать ухудшение симптомов, превышающее обычную вариабельность, имеющее острое начало и часто требующее модификации терапии; указывается, что основными симптомами обострения являются усугубление одышки, повышение продукции мокроты и изменение ее цвета.
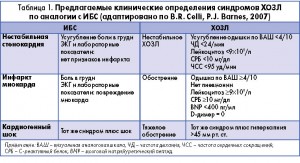
Проблема всех вышеуказанных определений состоит в том, что они не учитывают синдромы ХОЗЛ, как это имеет место, например, при классификации ишемической болезни сердца (табл. 1).
В проспективном исследовании J.J. Soler-Cataluna и соавт. (2005) была показана четкая взаимосвязь между количеством обострений ХОЗЛ и выживаемостью пациентов. Исследование этой зависимости у 604 пациентов показало, что у больных ХОЗЛ без серьезных обострений выживаемость в течение 5 лет достигала около 70%, при возникновении 1-2 обострений этот показатель снижался до 50%, а при наличии 3-4 обострений составил только 25%.
Влиянию частоты обострений на течение ХОЗЛ было посвящено крупное популяционное исследование S. Suissa и соавт. (2012). Общая выборка включила 73 106 пациентов, период наблюдения составил 17 лет. Было установлено, что риск развития последующего обострения значительно возрастал с каждым новым обострением – от 3-кратного после второго перенесенного обострения до 24-кратного после десятого обострения по сравнению с риском после первого обострения. В свою очередь, риск летального исхода возрастал по мере увеличения числа перенесенных обострений: после второго тяжелого обострения ХОЗЛ летальность была в 1,9 раза выше, чем после первого обострения, а после десятого обострения – в 4,5 раза выше. Летальность после тяжелого обострения ХОЗЛ была максимальной (40 случаев на 10 тыс. пациентов в день) в течение первой недели после поступления пациентов в стационар и постепенно снижалась в течение последующих трех месяцев (до пяти случаев на 10 тыс. пациентов в день).
В руководстве по профилактике обострений ХОЗЛ Американской коллегии торакальных врачей и Канадского торакального общества (ACCP/CTS, 2015) указывается, что частоту обострений снижают: вакцинация против гриппа и пневмококка, отказ от курения, легочная реабилитация, обучение пациентов, длительнодействующие β2-агонисты (ДДБА) vs короткодействующих β2-агонистов, длительнодействующие антагонисты мускариновых рецепторов (ДДАМ) vs плацебо, ДДАМ vs ДДБА, макролиды vs плацебо, ингибиторы фосфодиэстеразы-4 vs плацебо, ацетилцистеин vs плацебо, ИКС/ДДБА vs плацебо и ИКС/ДДБА vs антагонистов лейкотриенов. Эти стратегии нацелены на два ключевых патогенетических фактора ХОЗЛ: воспаление и нарушенную механику дыхания.
Роль ДДАМ в профилактике обострений ХОЗЛ была продемонстрирована в масштабном 4-летнем исследовании UPLIFT, в котором тиотропий снижал риск обострений в целом на 14% и также на 14% – риск обострений, требовавших госпитализации. Кроме того, терапия тиотропием статистически значимо снижала общую смертность на 16%.
В других исследованиях тиотропий показал преимущество в снижении частоты тяжелых обострений над гликопирронием (исследование SPARK), индакатеролом (INVIGORATE), салметеролом (POET-COPD), комбинацией гликопирроний/индакатерол (SPARK) и флутиказон/салметерол (INSPIRE).
По сравнению с монотерапией ДДБА комбинированные препараты ИКС/ДДБА в большей степени снижают риск обострений, однако они не влияют на смертность и частоту госпитализаций и к тому же повышают риск развития пневмонии.
Таким образом, обострения ХОЗЛ, развивающиеся вследствие усугубления локального и системного воспаления, повышают респираторную нагрузку и без того дисфункциональной дыхательной системы. Центральным клиническим событием обострения является повышение респираторного драйва и частоты дыхания с увеличением гиперинфляции и одышки, и главная задача лечения обострения состоит в том, чтобы разорвать этот порочный круг. Для профилактики обострений следует использовать мультидисциплинарный подход (табл. 2), обязательно включающий бронходилататоры.
О поддерживающей терапии ХОЗЛ рассказал профессор Университета Ливерпуля (Великобритания), доктор Питер Каверли. По его словам, на сегодня в ведении ХОЗЛ стоят два важных вопроса: какие пациенты должны получать ИКС и какой препарат следует использовать для стандартной бронходилатационной терапии.
Проблемой при назначении ИКС пациентам с ХОЗЛ является повышение риска пневмонии. Например, в исследовании M.T. Dransfield и соавт. (2013) комбинация вилантерол/флутиказона фуроат ассоциировалась с двукратным увеличением частоты развития пневмонии по сравнению с монотерапией вилантеролом, при этом наблюдалось дозозависимое повышение риска фатальной пневмонии в группах более высоких доз флутиказона. В то же время в исследовании WISDOM ступенчатая, в течение 3 месяцев, отмена ИКС с сохранением терапии салметеролом и тиотропием не выявила большей частоты обострений у пациентов с тяжелым и среднетяжелым ХОЗЛ по сравнению с продолжением терапии ИКС.
Тем не менее существует небольшая подгруппа пациентов с ХОЗЛ, которые могут получить пользу от назначения ИКС, – это больные с повышенной эозинофилией мокроты (≥300 клеток/мкл) и ≥2 обострениями за прошлый год (P.M.A. Caverley, 2016). У таких пациентов ИКС при регулярном использовании снижают частоту среднетяжелых и тяжелых обострений, однако их влияние на другие значимые клинические исходы является сомнительным. Альтернативой ИКС может быть поддерживающая терапия двумя бронходилататорами.
Как известно, сниженный уровень физической активности у пациентов с ХОЗЛ является достоверным предиктором ухудшения заболевания и риска смерти. В исследовании III фазы PHYSACTO после 8 нед лечения препаратом Spiolto (тиотропий/олодатерол) Respimat в сочетании с программой тренировок у пациентов с тяжелым и среднетяжелым ХОЗЛ значительно уменьшилась выраженность одышки и на 45,8% улучшилась переносимость физических нагрузок по сравнению с группой плацебо (р<0,001).
Краткий обзор фармакологических аспектов ведения терапии ХОЗЛ сделал профессор Кай-Майкл Бех (Германия). По его словам, в настоящее время основу поддерживающей терапии ХОЗЛ составляют бронходилататоры – ДДБА и ДДАМ. Эти препараты отличаются высокой безопасностью и клинической эффективностью.
Сравнительной оценке эффективности и безопасности ДДБА и ДДАМ было посвящено исследование POET-COPD. На протяжении 1 года пациенты с ХОЗЛ II-IV стадии по GOLD (от средней тяжести до очень тяжелого течения) получали тиотропий (Спирива) или салметерол.
Ключевым результатом исследования POET-COPD стало доказательство того, что тиотропий значительно отдалял время до первого обострения ХОЗЛ (первичная конечная точка): снижение риска составило 17% в пользу тиотропия. В отношении времени до первого тяжелого обострения ХОЗЛ преимущество тиотропия составило 28%. Кроме того, был подтвержден благоприятный профиль безопасности тиотропия, о чем свидетельствовало снижение общей смертности на 19% и значительно более низкая частота досрочного прекращения лечения в группе тиотропия по сравнению с группой салметерола.
Более низкая эффективность ДДБА в отношении профилактики обострений ХОЗЛ может быть обусловлена зависимостью их эффекта от полиморфизмов гена ADRB2, кодирующего β2-адренорецептор. В частности, K.F. Rabe и соавт. установили, что у пациентов с полиморфизмами Gly16Gly и Arg16Gly вероятность обострения значительно выше, чем у больных с полиморфизмом Arg16Arg. В отличие от ДДБА тиотропий и ДДАМ демонстрируют стабильную эффективность независимо от генетического профиля пациентов.
 Роль ДДАМ как основы поддерживающей терапии ХОЗЛ была продемонстрирована в крупнейшем исследовании UPLIFT. После 48 нед терапии тиотропия бромидом (Спирива) наблюдалось снижение общей смертности на 11%, снижение кардиоваскулярной и респираторной заболеваемости. Наиболее выраженное замедление снижения объема форсированного выдоха за 1-ю секунду (ОФВ1) при лечении тиотропием наблюдалось у пациентов с II стадией ХОЗЛ по GOLD (–12%; р=0,024), у больных, ранее не получавших поддерживающей терапии (–20%; р=0,026), и у пациентов в возрасте до 50 лет (–34%; р=0,01).
Роль ДДАМ как основы поддерживающей терапии ХОЗЛ была продемонстрирована в крупнейшем исследовании UPLIFT. После 48 нед терапии тиотропия бромидом (Спирива) наблюдалось снижение общей смертности на 11%, снижение кардиоваскулярной и респираторной заболеваемости. Наиболее выраженное замедление снижения объема форсированного выдоха за 1-ю секунду (ОФВ1) при лечении тиотропием наблюдалось у пациентов с II стадией ХОЗЛ по GOLD (–12%; р=0,024), у больных, ранее не получавших поддерживающей терапии (–20%; р=0,026), и у пациентов в возрасте до 50 лет (–34%; р=0,01).
По мнению профессора Беха, алгоритм фармакотерапии у пациентов с впервые установленным диагнозом ХОЗЛ должен выглядеть следующим образом. В качестве стартового лечения всем пациентам следует назначить поддерживающую терапию ДДАМ (например, тиотропий). При недостаточном контроле симптомов и/или обострениях следующим шагом является комбинированная терапия ДДАМ + ДДБА или ДДАМ + ИКС/ДДБА. Комбинация ИКС/ДДБА может быть показана во 2-й линии терапии небольшой подгруппе пациентов с неконтролируемым заболеванием и повышенной эозинофилией мокроты.
Доклад профессора Оксфордского Университета, доктора Ричарда Рассела (Великобритания) был посвящен значимости выбора ингалятора для пациентов с ХОЗЛ. Он отметил, что необходимым условием эффективного ведения ХОЗЛ является приверженность пациентов к соблюдению врачебных рекомендаций. Это относится не только к лекарственным препаратам, но и к образу жизни (диета, физические нагрузки), вакцинациям, легочной реабилитации, отказу от курения и т.д.
Вопрос приверженности пациентов к терапии требует комплексного подхода. Если ранее считалось, что активным участником лечебного процесса является врач, а пациенту отводилась второстепенная роль, то сегодня такой подход больше не является эффективным. Понятие приверженности больного к терапии также претерпело изменения: ранее использовали термин compliance, под которым понимали желание пациента следовать выбранному курсу терапии, теперь предполагается более активная позиция больного, что выражается термином adherence, подразумевающим сочетание комплайенса и четкого соблюдения пациентом врачебных назначений, осознания последствий отказа от терапии.
В многочисленных исследованиях, проведенных начиная с 1980-х годов и до сегодняшних дней, было продемонстрировано, что пациенты с хронической легочной патологией отличаются низкой приверженностью к лечению. В частности, врачебные рекомендации соблюдают всего 40% больных, и 50-60% пациентов используют ингаляторы неэффективно. В реальной клинической практике эти цифры, очевидно, еще более удручающие.
Основными факторами, негативно влияющими на приверженность к терапии, являются недостаточная информированность пациента, сложность схем лечения и полипрагмазия, страх побочных эффектов, переносимость и стоимость препаратов.
У пациентов с обструктивными заболеваниями легких важнейшим фактором, определяющим приверженность к лечению и его эффективность, является выбор доставочного устройства – ингалятора. При БА и ХОЗЛ способность пациента правильно применять ингалятор достоверно коррелирует с риском госпитализации, особенно при переходе на другой препарат (O. Turan et al., 2016). В то же время в клиниках, в которых больных обучают правильной технике ингаляции, регистрируется снижение частоты госпитализаций и обострений ХОЗЛ (C. Xin et al., 2016).
Для пациента значимыми факторами при выборе ингалятора являются легкость и комфорт в использовании, ощущаемый эффект, портативность, стоимость, наличие индикатора принятой дозы и возможность контроля оставшихся доз.
На правильность использования ингалятора влияют тяжесть заболевания пациента, сопутствующая патология (физические ограничения, расстройства памяти и т.д.), способность выполнить технику ингаляции и опыт применения конкретного устройства. В свою очередь, факторы, связанные с ингалятором, включают скорость потока и размер частиц препарата, форму мундштука, непосредственные побочные эффекты, ощущаемые пациентом (вкус, болезненность, высыпания в ротовой полости), а также количество необходимых шагов. Например, при использовании дозированных аэрозольных ингаляторов больной должен выполнить 10 шагов: снять колпачок, хорошо встряхнуть баллон, держать баллон вертикально, свободно выдохнуть, поместить мундштук в рот, привести в действие устройство в момент начала вдоха, медленно и глубоко вдохнуть, задержать дыхание по крайней мере на 10 с, медленно выдохнуть. Для сравнения, современный ингалятор Respimat требует всего трех шагов: повернуть прозрачное основание, снять колпачок и нажать кнопку.
Чтобы помочь пациенту с БА или ХОЗЛ правильно выбрать препарат и, соответственно, доставочное устройство, врач сам должен досконально знать, как использовать разные типы ингаляторов, то есть выступать экспертом в данном вопросе. Тем не менее исследования показывают, что 85,8% пульмонологов не имеют адекватных знаний об ингаляторах и только 28% проверяют технику ингаляции при переводе на новый препарат (V. Plaza et al., 2012).
Эффективность ингаляционной терапии определяется депозицией препарата в легких, которая, в свою очередь, зависит от ограничения воздушного потока. Среди наиболее часто используемых доставочных устройств (Respimat, Turbohaler, Ellipta, Genuair, Diskus, Breezhaler) ингалятор Respimat имеет самую низкую рекомендованную скорость воздушного потока (30 л/мин), благодаря чему со стороны пациента требуется минимальное инспираторное усилие. За счет малого размера частиц (1-5 мкм) и медленной ингаляции Respimat по сравнению с дозированными ингаляторами под давлением обеспечивает более эффективную легочную депозицию дозы препарата (53 vs 21% соответственно) (P. Brand et al., 2008).
Таким образом, при лечении БА и ХОЗЛ выбор доставочного устройства является не менее важным, чем выбор препарата. Этот выбор должен сделать не врач, а пациент при всесторонней помощи и поддержке врача. Следует проверять технику использования ингалятора при каждом визите пациента и помнить о том, что «самый дорогой» ингалятор – не тот, который стоит больше, а тот, который неправильно используется.
Подготовил Алексей Терещенко