7 червня, 2017
Ураження опорно-рухового апарату у хворих на цукровий діабет і способи їх корекції
Діабетичні артропатії є частим ускладненням цукрового діабету (ЦД) і зустрічаються, за даними літератури, у більш ніж половини хворих на ЦД 1 типу та у 20-25% пацієнтів із ЦД 2 типу. Найчастішими ураженнями кістково-суглобової системи при діабеті є остеоартроз колінних суглобів, котрий виникає як наслідок особливостей метаболічного синдрому, а також плечолопатковий періартрит із синдромом обмеження рухомості суглобів та іноді супутнім теносиновіїтом долонь. Крім того, серед цих хворих досить поширені синдром діабетичної стопи й остеопороз [1].
Головною причиною залучення кістково-м’язової системи є абсолютний дефіцит інсуліну, що призводить до зниження вироблення остеобластами колагену й лужної фосфатази (ЛФ), необхідних для утворення кісткового матриксу та його мінералізації; зменшення стимуляції остеокластів, опосередкованої інсуліноподібним фактором росту. При цьому відзначають прямий вплив високої концентрації глюкози на опорно-руховий апарат за рахунок кінцевих продуктів глікозилювання й посилення резорбції кістки остеобластами. Крім того, при зниженні секреції інсуліну спостерігають нестачу активних метаболітів вітаміну D, що призводить до зниження всмоктування кальцію в кишківнику. При цьому розвивається негативний баланс неорганічних елементів в організмі й посилення резорбції кісткової тканини. Нейрогенна остеоартропатія у хворих на ЦД наразі є найпоширенішою формою з усіх нейрогенних артропатій [2-4].
Донедавна в літературі було описано дві конкуруючі теорії розвитку артропатій при ЦД: нейросудинну та нейротравматичну. Згідно з нейросудинною теорією процес остеоартропатії є трофічним розладом, який виникає внаслідок посилення кровотоку в кістковій тканині з надмірною неконтрольованою активізацією остеокластів [5, 6]. Нейротравматична теорія говорить, що відсутність захисної чутливості сприяє неоптимальному навантаженню на кінцівку, в результаті чого виникають мікропереломи. Посилення шунтового кровотоку та ендотеліальна дисфункція при ЦД активують окремі цитокіни, які, у свою чергу, активують остеобласти [7]. Ідентичні механізми остеолізу й руйнування кістки характерні для ревматоїдного артриту та для системних захворювань сполучної тканини. Виявлено також, що в процесі кальцифікації судин беруть участь цитокіни запалення та порушення кальцій-фосфорного гомеостазу [8, 9].
Слід зазначити, що у хворих на ЦД 2 типу вказані ураження комбінуються з порушеннями, характерними для остеоартрозу: зміна ремоделювання кісткової тканини, що призводить на ранніх стадіях захворювання до розрідження, а потім до потовщення кістки, погіршення її якості, синовіальне запалення, при якому виявляється збільшення експресії прозапальних медіаторів і збільшення катаболізму матриксу суглобового хряща. Синовіїт активує сенсорні нервові волокна, спричиняє біль та нейрогенне запалення [10, 11]. Тобто формується хронічне запальне захворювання, при якому переважну роль відіграє дисбаланс цитокінів (інтерлейкіну – ІЛ‑1, -6, -17, фактора некрозу пухлин-α – ФНП-α). При цьому хондроцити експресують рецептори для ІЛ‑1, що підвищує їх чутливість до цього цитокіну [12-15]. Роль ІЛ‑1 полягає в його впливі на плазміноген, що сприяє перетворенню останнього на активний плазмін, який, у свою чергу, переводить неактивні прометалопротеази в активну форму, посилюючи деградацію позаклітинного матриксу. Катаболічна дія ІЛ‑1 проявляється в його здатності стимулювати вироблення хондроцитами й синовіоцитами оксиду азоту (NO), який ушкоджує позаклітинний матрикс. Крім того, NO, знижуючи концентрацію антагоніста рецептора ІЛ‑1, сам активує ІЛ‑1 і впливає на апоптоз хондроцитів. ІЛ‑1β підвищує екскрецію кальцію, активує остеобласти, що призводить до зниження інтенсивності формування кісткової тканини. Зменшення під його впливом концентрації остеокальцину зумовлює руйнування субхондральної кістки [16-18]. Також при цьому спостерігають гіперекспресію ферменту циклооксигенази‑2, який індукує синтез простагландинів, що беруть участь у розвитку запалення.
Хронічне запалення призводить до активації кісткової резорбції, зумовленої системою RANK/RANKL, що забезпечує розвиток, активність і виживання остеокластів. ІЛ‑1β, ФНП-α і RANKL конкурентно підвищують активність ядерного фактора каппа В (NF-κB) у клітинах-мішенях, що спричиняє посилення запалення і/або кісткову деструкцію [15, 16]. Усе це є свідченнями різноманітного патофізіологічного впливу прозапальних цитокінів на катаболізм хряща, субхондральної кістки та робить їх мішенню терапевтичної стратегії при лікуванні вказаних порушень.
На сучасному етапі головною метою лікування ЦД є забезпечення належної якості життя хворого [19, 20]. Цього можна досягти шляхом повної компенсації порушеного обміну речовин: нормалізації обміну вуглеводів, ліпідів, білків та мінералів. Саме з цією метою у комплексній терапії хворих на ЦД із наявністю ураження опорно-рухового апарату доцільно використовувати препарати кальцію з провітаміном D3, бісфосфонати, а також хондропротектори, що позитивно впливають на стан хрящової тканини [21, 22]. Згідно з рекомендаціями Асоціації ревматологів України хондропротектори, до складу яких входять глюкозамін та хондроїтину сульфат, є важливою складовою лікування пацієнтів із захворюваннями кісткової системи. Вони є компонентами суглобового хряща, входять до складу протеогліканів і глюкозаміногліканів хрящової тканини [23-25].
Аналіз механізмів розвитку уражень суглобів при ЦД наводить на думку щодо можливості позитивного впливу хондропротекторів, які містять хондроїтин та глюкозамін. Досить ефективними є ін’єкційні форми для внутрішньосуглобового застосування, завдяки яким ліки можна вводити безпосередньо в місце ураження, зокрема препарат Алфлутоп. Він є біологічним коктейлем, його розчин містить біоактивний концентрат із дрібної морської риби, до складу котрого входять: хондроїтинсульфат, амінокислоти, поліпептиди, солі макро- та мікроелементів (Na, К, Са, Mg, Fe, Zn, Cu), сполуки групи гліцерофосфоліпідів. Тобто можна відзначити, що цей засіб містить природні глюкозаміноглікани [26]. Слід зауважити, що досліджень щодо ефективності Алфлутопу у хворих на діабетичну остеоартропатію досі практично не проводили.
Мета дослідження – оцінити ефективність застосування хондропротектора Алфлутоп у хворих на ЦД з ураженнями опорно-рухового апарату.
Матеріали та методи
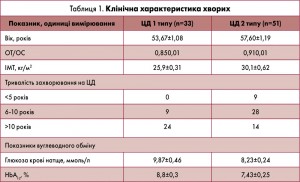
В умовах ендокринологічного відділення комунального закладу охорони здоров’я «Обласна клінічна лікарня – центр екстреної медичної допомоги та медицини катастроф» м. Харкова (база кафедри внутрішньої медицини № 3 Харківського національного медичного університету) під наглядом перебували 84 хворі на ЦД із проявами остеоартриту (38 чоловіків, 46 жінок), переважно в стадії субкомпенсації, з них 33 хворі на ЦД 1 типу та 51 хворий на ЦД 2 типу. Тривалість захворювання – від 4 до 27 років, середній вік пацієнтів становив 56,42±1,17 року. Під наглядом перебували хворі з переважним ураженням плечових (56 осіб) і колінних суглобів (28 осіб).
Клінічне обстеження пацієнтів включало аналіз скарг, збір анамнезу, фізикальний огляд та оцінку антропометричних показників – зросту, маси тіла, обхвату талії (ОТ), обхвату стегон (ОС), визначення індексу маси тіла (ІМТ = вага, кг / зріст, м2) і співвідношення ОТ/ОС. Відповідно до загальноприйнятих критеріїв при визначенні ОТ >94 см у чоловіків та >80 см у жінок констатували абдомінальне ожиріння. Згідно з індексом Кетле діагноз «ожиріння» встановлювали хворим при ІМТ ≥30 кг/м2 (табл. 1).
Обстеження хворих проводили згідно з протоколами Міністерства охорони здоров’я (Наказ від 12.10.2006 № 676 та Наказ від 21.12.2012 № 1118). План обстеження містив вивчення показників вуглеводного обміну з визначенням рівня глюкози крові натще (ГКН), рівня глікозильованого гемоглобіну (HbA1c); біоелементного балансу (біохімічним методом) – вміст калію (К), кальцію (Са), магнію (Mg), фосфору (Р); активності ЛФ, рівня серомукоїдів (CM) орциновим методом, сіалових кислот (СК) калориметричним резорциновим методом та С-реактивного протеїну (СРП) за реакцією преципітації в капілярах. Усім хворим проводили рентгенологічне дослідження опорно-рухової системи. Інтенсивність болю в суглобах у спокої та під час рухів оцінювалася за візуальною аналоговою шкалою (ВАШ) і становила 40 мм у всіх хворих.
До початку дослідження хворі не отримували терапії Алфлутопом. На момент дослідження 45 хворих із 84 приймали нестероїдні протизапальні препарати (НПЗП) для зменшення виразності больового синдрому, прийом їх був ситуаційним або курсовим протягом 5-7 днів. З метою вивчення впливу Алфлутопу на перебіг артропатії пацієнтів розподілили на дві групи. На тлі стандартної терапії ЦД (дієта, інсулінотерапія чи цукрознижувальні препарати) перша група хворих (n=41) отримувала лікування з призначенням НПЗП, у другій групі (n=43) додатково до терапії НПЗП було застосовано хондропротектор Алфлутоп.
Групи були зіставними за основними демографічними та клінічними характеристиками й не мали відмінностей щодо характеру й частоти супутніх захворювань. Зважаючи на обмежені терміни перебування хворих у стаціонарі, ми дещо модифікували й інтенсифікували схему призначення Алфлутопу (патент України на корисну модель від 25.04.2013 № 79795 Л.В. Журавльової, В.О. Федорова, Н.К. Александрової, М.О. Олійник «Спосіб лікування остеоартропатій у хворих на цукровий діабет»). Препарат застосовували за схемою: по 1 мл внутрішньосуглобово через день, 5 ін’єкцій (курс лікування в стаціонарі), в подальшому – щоденно по 1 мл внутрішньом’язово загальним курсом 20 ін’єкцій. НПЗП приймали протягом 10 днів.
Ефективність терапії оцінювали за виразністю болю в суглобах у спокої та під час рухів за ВАШ, індексом WOMAC (Western Ontario and McMaster University), який включає визначення виразності болю, скутості, порушення функції суглобів і сумарний бал. Дослідження проводили на початку лікування, через 2 тиж (лікування в стаціонарі) та через 8 тиж після початку лікування.
Результати та обговорення
ІМТ був значно вищий у хворих на ЦД 2 типу. Усі обстежені пацієнти з ЦД переважно перебували в стані субкомпенсації. Середній рівень ГКН у хворих на ЦД 1 типу становив 9,87±0,46 ммоль/л, 2 типу – 8,24±0,24 ммоль/л; рівень HbA1c при ЦД 1 типу становив 8,8±0,3%, 2 типу – 7,43±0,25% (табл. 1).
Основними клінічними проявами ураження суглобів були біль, обмеження рухів та припухлість над суглобами, в окремих випадках – їх деформація, осалгії.
На тлі проведеної терапії позитивну динаміку спостерігали в обох групах хворих після закінчення курсу лікування в стаціонарі. Було відзначено зменшення больового синдрому в уражених суглобах (перша група – 32 хворі, друга – 39), збільшення обсягу рухів (22 та 31 хворий відповідно), зменшення припухлості над суглобами (15 та 26 хворих відповідно), зникнення осалгій (8 та 11 хворих відповідно). Аналіз показників болю за ВАШ виявив достовірне зниження болю через 4 тиж після початку лікування в обох групах. До 8-го тижня після початку лікування в групі хворих, які отримували Алфлутоп, біль у спокої зменшився на 58%, під час рухів – на 31%, тоді як у групі хворих, котрі приймали НПЗП, біль у спокої зменшився на 44%, під час рухів – на 23%, що може свідчити про вплив Алфлутопу на виразність больового синдрому. На тлілікування відзначали зменшення болю за WOMAC у першій групі на 14,12%, у другій – на 26,5%. Статистично значущо зменшилася скутість у суглобах (p<0,05) та покращився функціональний індекс WOMAC (p<0,05) в обох групах, але виразнішу позитивну динаміку спостерігали у другій групі (p<0,05) (табл. 2).

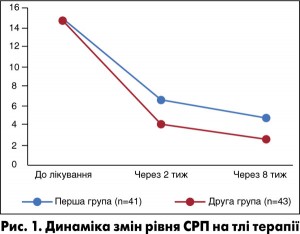
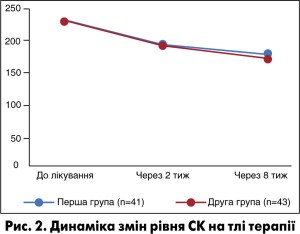
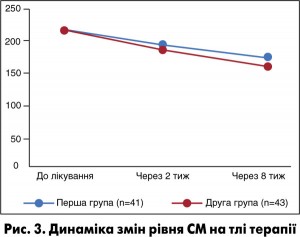
Як ми можемо побачити з рисунків 1-3, на тлі терапії відзначали достовірне зниження рівня СРП через 2 тиж після початку лікування в обох досліджуваних групах (р<0,05), проте через 8 тиж після початку лікування виразніше його зниження спостерігали у другій групі хворих, які отримували Алфлутоп (р=0,006). Також за даними досліджень рівня СМ та СК виявлено позитивну динаміку цих показників у хворих обох груп, але за період лікування в стаціонарі повної нормалізації цих показників не відбулося.
При визначенні біоелементного балансу спостерігали зниження вмісту фосфору (0,73±0,04 ммоль/л) у сироватці крові та гіперкальційурію (6,21±0,33 ммоль/л), які були більш виражені у хворих на ЦД 1 типу та за тяжкого перебігу захворювання (табл. 3). Виявлені зміни можуть бути зумовлені абсолютною чи відносною недостатністю інсуліну, що призводить до порушення метаболічних процесів і відіграє негативну роль щодо стану кісткової матриці. У свою чергу, підвищення осмотичного діурезу за декомпенсації ЦД призводить до порушення реабсорбції Са та Р у ниркових канальцях (наявність гіперкальційурії та гіперфосфатурії), тобто до негативного балансу Са, Р, іноді Mg в організмі (табл. 3).

За даними біохімічних досліджень сироватки крові (ЛФ, рівнів кальцію, магнію та фосфору) виявлено незначну позитивну динаміку у хворих обох груп, але за період лікування в стаціонарі повної нормалізації цих показників не спостерігали. Проте під час проведення контрольного обстеження через 8 тиж було зафіксовано вірогідну нормалізацію мінеральних показників, особливо у другій групі, що свідчить про нормалізацію фосфорно-кальцієвого балансу. Також у хворих, які приймали Алфлутоп, через 8 тиж відзначали покращення рівня загальних хондроїтинсульфатів до 0,15±0,03 г/л, що може свідчити про здатність Алфлутопу до структурно-модифікувальної дії.
Треба зауважити, що переносимість Алфлутопу була задовільною. Побічних ефектів та алергічних реакцій при введенні препарату не спостерігали. Також у хворих, які отримували додатково Алфлутоп, відміна НПЗП проходила в коротший термін, ніж у хворих на монотерапії НПЗП.
Висновки
1. Оцінювання ефективності терапії Алфлутопом за показниками болю за ВАШ, а також індексом WOMAC продемонструвало позитивну динаміку в зменшенні болю, вранішньої скутості та функціональної недостатності.
2. У хворих на діабетичну артропатію на тлі терапії було відзначено покращення показників СК, СМ та рівня СРП.
Отже, використання препарату Алфлутоп у хворих на ЦД дає швидкий клінічний ефект, що проявляється у зменшенні больового синдрому й покращенні функції суглобів у більш стислі терміни порівняно з іншими препаратами. У зв’язку з цим вважаємо доцільним хворим на ЦД з ураженням опорно-рухового апарату призначати комплексну медикаментозну корекцію з використанням у схемах лікування хондропротекторів, зокрема Алфлутопу.
Література
1. Журавльова Л.В. Застосування хондропротекторної терапії при лікуванні діабетичних остеоартропатій / Л.В. Журавльова, В.О. Федоров, М.О. Олійник, О.Ю. Ткачук, А.І. Щічка // Експериментальна і клінічна медицина. – 2012. – № 4 (57). – С. 74-78.
2. Балаболкин М.И. Диабетическая остеоартропатия и синдром диабетической стопы //Диабетология. – М.: Медицина, 2000. – С. 439-452.
3. Ahmadi M.E., Morrison W.B., Carrino J.A., et al. Neuropathic arthropathy of the foot with and without superimposed osteomyelities: MR imaging characteristics. Radiology. 2006; Vol. 238, № 2: 622-631.
4. Baker N., Green A., Krishman S., Rayman G. Microvascular and C-fiber function in diabetic Charcot neuroarthropathy and diabetic peripheral neuropathy. Diabetes Care. 2007; Vol. 30 (12): 3077-3079.
5. Jeffcoate W.J., Game F., Cavanagh P.R. The role of proinflammatory cytokines in the cause of neuropathic osteoarthropathy (acute Charcot foot) in diabetes. Lancet. 2005; Vol. 366 (10): 2058-2061.
6. Mabilleau G., Petrova N.I., Edmonds M.E., Sabokbar A. Increased osteoblastic activity in acute Charchot’s osteoarthropathy: the role of receptor activator of nuclear factor-kappaB ligand. Diabetologia. 2008; Vol. 51 (6): 1035-1040.
7. Huang P.J., Fu Y.C., Lu C.C., et al. Hindfoot arthrodesis for neuropathic deformity. Kaohsiung J. Med. Sci. 2007; Vol. 23 (3): 120-127.
8. Vattikuti R., Towler D. Osteogenic regulation of vascular calcification: an early perspective. Am. J. Physiol. Endocrin. Metab. 2004; Vol. 286 (5): E686-E696.
9. Wu S.C., Driver V.R., Wrobel J.C. Foot ulcers in the diabetic patient, prevention and treatment. Vasc. Health and Risk Manag. 2007; Vol. 3 (1): 65-76.
10. Журавльова Л.В. Роль прозапальних цитокінів у розвитку остеоартрозу та цукрового діабету 2 типу / Л.В. Журавльова, М.О. Олійник // Український ревматологічний журнал. – 2015. – № 2 (60). – С. 31-35.
11. Балабанова Р.М. Роль интерлейкина‑1 при остеоартрозе и возможности его блокирования / Р. М. Балабанова // Совр. ревматология. – 2011. – № 1. – С. 58-62.
12. Головач И.Ю. Остеоартрит: фундаментальные и прикладные аспекты этиопатогенеза заболевания. Ничего не стоит на месте / И.Ю. Головач // Український ревматологічний журнал. – 2014. – № 2 (56). – С. 4-11.
13. Franchimont N., Lambert C., Huynen P., et al. IL‑6 receptor shedding is enhanced by IL‑1b and TNF-α and is partially mediated by TNFa-converting enzyme in osteoblast-like cells. Arthr. Rheum. 2005; Vol. 52: 84-93.
14. Kapoor M., Martel-Pelletier J., Lajeunesse D., et al. Role of proinflammatory cytokines in the pathophysiology of osteoarthritis. Nat. Rev. Rheumatol. 2011; Vol. 7: 33-42.
15. Національний підручник з ревматології / За ред. В.М. Коваленка, Н.М. Шуби. – К.: Моріон, 2013. – 672 с.: іл., табл., бібліогр.
16. Santangelo K.S., Nuovo G.J., Bertonein A.L. Vivo reduction or blockade of interleukin‑1β in primary osteoarthritis influences expression of mediators implicated in pathogenesis. Osteoarthritis and Cartilage. 2012; Vol. 20 (12): 1610-1618.
17. Wang X., Hunter D., Xu J., et al. Metabolic triggered inflammation in osteoarthritis. Osteoarthritis and Cartilage. 2015; Vol. 23, № 1: 22-30.
18. Коваленко В.М. Ревматичні захворювання в Україні: стан проблеми та шляхи вирішення / В.М. Коваленко / Український ревматологічний журнал. – 2012. – № 3 (49). – C. 84-86.
19. Журавльова Л.В. Остеоартроз та цукровий діабет 2 типу: спільні ланки патогенезу / Л.В. Журавльова, М.О. Олійник // Ендокринологія. – 2015. – Том 20, № 1. – С. 79-83.
20. McAlindon T.E., Bannuru R.R., Sullivan M.C., et al. OARSI guidelines for the non-surgical management of knee osteoarthritis. Osteoarthritis and Cartilage. 2014; Vol. 22, Issue 3: 363-388.
21. Hochberg M. C. Structure-modifying effects of chondroitin sulfate in knee osteoarthritis: an updated meta-analysis of randomized placebo-controlled trials of 2-year duration. Osteoarthritis Cartilage. 2010; Vol. 18 (Suppl. 1): S28-31.
22. Hochberg M.C., Altman R.D., April K.T., et al. American College of Rheumatology 2012 recommendation for the use of nonpharmacologic and pharmacologic therapies in osteoarthritis of the hand, hip, and knee. Arthritis Care Res (Hoboken). 2012; Vol. 64 (4): 465-474.
23. Шуба Н.М. Выбор структурно-модифицирующих и противовоспалительных препаратов у пациентов с остеоартрозом / Н.М. Шуба, Т.Д. Воронова, А.С. Крылова // Український ревматологічний журнал. – 2013. – № 2 (52). – C. 67-73.
24. Wildi I.M., Raynauld J.P., Martel-Pelletier J., et al. Chondroitin sulfate reduces both cartilage volume loss and bone marrow lesions in knee osteoarthritis patients starting as early as 6 months after initiation of therapy: a randomised, double-blind, placebo-controlled pilot study using MRI. Ann Rheum Dis. 2011 Jun; Vol. 70 (6): 982-989. doi: 10.1136/ard.2010.140848. Epub 2011 Mar 1.
25. Lee Y.H., Woo J.H., Choi S.J., et al. Effect of glucosamine or chondroitin sulfate on the osteoarthritis progression: a meta-analysis. Rheumatol. Int. 2010; Vol. 30 (3): 357-363.
26. Бур’янов О.А. Патогенетичне лікування хворих на остеоартроз та вивчення його впливу на стан суглобового хряща / О.А. Бур’янов, І.М. Дикан, Л.А. Міроняк та ін. / Consilium medicum. – 2012. – № 8. – С. 34-40.