7 червня, 2017
Вибір НПЗП при остеоартриті: доказова чи персоналізована медицина?
За матеріалами науково-практичної конференції «Ревматичні хвороби: межі повноважень популяційних
та персоніфікованих методів лікування» (16-17 березня, м. Київ)
Остеоартрит (ОА) – найпоширеніша форма ревматичних захворювань суглобів та одна з основних причин хронічного болю й інвалідності у пацієнтів середнього та похилого віку. На підставі тривалих досліджень патогенезу цього захворювання його було визначено не просто як хворобу зношення тканин (хвороба wear and tear), а як патологічне ремоделювання суглобових тканин, кероване безліччю прозапальних факторів, що продукуються насамперед субхондральною кісткою із синовією.
Знеболювальна терапія відіграє важливу роль у терапії ОА: з неї розпочинається лікування цього захворювання, від неї залежить його ефективність, а також успішність реабілітаційних заходів. У багатьох пацієнтів знеболювальна терапія не обмежується кількома днями: лікарі змушені призначати кілька курсів лікування, найчастіше використовуючи нестероїдні протизапальні препарати (НПЗП). Проте призначення останніх потребує вкрай обережного підходу, ретельної оцінки всіх ризиків, а отже, вибору найбезпечнішого препарату.
 Доктор медичних наук, професор Ірина Юріївна Головач (Клінічна лікарня «Феофанія» ДУС, м. Київ) присвятила свою доповідь вибору НПЗП у пацієнтів з ОА і навела клінічний приклад, котрий демонструє, як багато факторів має враховувати лікар, перш ніж прийняти остаточне рішення.
Доктор медичних наук, професор Ірина Юріївна Головач (Клінічна лікарня «Феофанія» ДУС, м. Київ) присвятила свою доповідь вибору НПЗП у пацієнтів з ОА і навела клінічний приклад, котрий демонструє, як багато факторів має враховувати лікар, перш ніж прийняти остаточне рішення.
Біль – ключовий симптом ОА, якому властиві гетерогенність та мультимодальність. Прояви болю дуже різноманітні й залежать від його походження (табл.).
Упродовж багатьох років знайти альтернативу НПЗП так і не вдалося: ці препарати залишаються важливим компонентом комплексної терапії ОА завдяки впливу на патогенетичні механізми захворювання і швидкому симптоматичному ефекту. Наразі не стоїть питання відмови від препаратів цієї групи, проте надзвичайно актуальним питанням є запобігання розвиткові ускладнень НПЗП-терапії, на чому наголошують у всіх сучасних наукових роботах у цій галузі та в рекомендаціях із лікування пацієнтів з ураженнями опорно-рухового апарату. До загальних принципів призначення НПЗП при ОА, що формувалися впродовж багатьох років і застосовуються сьогодні в клінічній практиці, належать такі:
– препарат слід вибирати з урахуванням результатів оцінки гастроінтестинальної, кардіоваскулярної, ренальної безпеки та вікових особливостей пацієнта;
– слід поміркувати про вплив конкретного НПЗП на стан суглобового хряща, адже представники цієї групи мають відмінності щодо цього;
– перевагу необхідно віддавати мінімальній ефективній дозі НПЗП;
– слід уникати одночасного призначення декількох НПЗП;
– через місяць лікар має оцінити ефективність лікування і змінити його за відсутності ефекту;
– не слід призначати НПЗП, якщо пацієнт з ОА не скаржиться на біль.
Остеоартрит (ОА) – найпоширеніша форма ревматичних захворювань суглобів та одна з основних причин хронічного болю й інвалідності у пацієнтів середнього та похилого віку. На підставі тривалих досліджень патогенезу цього захворювання його було визначено не просто як хворобу зношення тканин (хвороба wear and tear), а як патологічне ремоделювання суглобових тканин, кероване безліччю прозапальних факторів, що продукуються насамперед субхондральною кісткою із синовією.
Окрім аспектів безпеки НПЗП-терапії, необхідно оцінити її очікувані переваги й обґрунтувати доцільність призначення лікування результатами глобальної оцінки здоров’я, а саме: якості життя (шкала оцінки якості життя або запитання «Як ви почуваєтеся?»), виразності болю (візуальна аналогова шкала – ВАШ), кількості уражених суглобів (генералізований/локальний ОА), функціональних обмежень у повсякденному житті (індекс Лекена, WOMAC), коморбідності.
Професор І.Ю. Головач зазначила, що підходи до вибору НПЗП при ОА можуть суттєво відрізнятися залежно від характеристик пацієнта (вік, професія), провідного фактора розвитку ОА, його локалізації, стадії та наявності коморбідних станів (захворювання серця, шлунково-кишкового тракту (ШКТ), нирок). ОА – гетерогенне захворювання, швидкість його прогресування істотно варіює, проте сучасні рекомендації щодо лікування ОА не дають чітких відповідей, які препарати і в якій послідовності слід застосовувати в певній ситуації. Утім, результати лікування не завжди задовольняють хворих у реальній клінічній практиці.
У ході доповіді були розглянуті можливості призначення індивідуалізованої терапії у пацієнтки з ОА і коморбідними захворюваннями, які ускладнювали вибір НПЗП.
Клінічний приклад
Пацієнтка В., 65 років. Скарги на болі в колінних суглобах упродовж 5 років; в останні 2 роки відзначає посилення болю та припухання суглобів. Для знеболювання застосовувала «народні» методи лікування й неодноразово – внутрішньом’язове введення бетаметаспану із задовільним ефектом. У зв’язку із підвищенням артеріального тиску (АТ) після ін’єкцій бетаметаспану була змушена відмовитися від його використання і деякий час неконтрольовано приймала різні НПЗП. Побічна реакція цієї терапії – біль у шлунку.
В анамнезі – артеріальна гіпертензія, АГ (призначено комбіновану антигіпертензивну терапію), гіперхолестеринемія (без корекції), ожиріння (індекс маси тіла – 33,5 кг/м2).Встановлено ерозивний гастрит, асоційований із Heliсobacter pylori.
За результатами рентгенографічного дослідження встановлено ОА колінних суглобів ІІ і ІІІ стадії. Результати оцінки суглобового синдрому дали змогу констатувати помірно виразний больовий синдром із помірними функціональними обмеженнями (4 бали за ВАШ у спокої; 6 балів за ВАШ – під час рухів і після навантаження; індекс Лекена – 6,5 бала; індекс WOMAC– 220 балів; шкала скутості – 75 балів; шкала функціонального індексу – 220 балів).
Під час вирішення питання щодо лікування больового синдрому в цьому випадку було враховано наявність факторів ризику гастроінтестинальних ускладнень – похилий вік; одночасний прийом декількох НПЗП в анамнезі, ерозивний гастрит, асоційований із Heliсobacter pylori. Перелічені фактори формують загалом помірний ризик ускладнень НПЗП-терапії.
Крім того, пацієнтка хворіє на АГ і має гіперхолестеринемію, тобто серйозні фактори кардіоваскулярного ризику. Це важливий момент з огляду на те, що частота кардіоемболічних подій майже в 4 рази перевищує частоту шлунково-кишкових ускладнень у пацієнтів похилого віку на тлі прийому НПЗП (A.-M. Schjerning, G.H. Gisiason et al., 2015).
Якщо в цій клінічній ситуації обирати лікування, спираючись на рекомендації ESCEO 2014 року, то пацієнтці не можуть бути призначені неселективні НПЗП (у зв’язку з підвищеним гастроінтестинальним ризиком) і ЦОГ-2-селективні НПЗП (у зв’язку з підвищеним кардіоваскулярним ризиком). Тому після ерадикації Heliсobacter pylori разом із корекцією харчування, статинотерапією та фізичними методами реабілітації було призначено NO-асоційований НПЗП амтолметин гуацил – АМГ (Найзилат) у дозі 600 мг для одноразового вранішнього прийому. Крім того, пацієнтці призначено симптоматичну терапію сповільненої дії у вигляді хондропротекторів.
Призначення NO-асоційованих НПЗП, зокрема АМГ, – новий підхід у НПЗП-терапії, спрямований на підвищення безпеки лікування. Знеболювальний, протизапальний і жарознижувальний ефекти АМГ є зіставними з такими у неселективних і ЦОГ-2-селективних НПЗП. АМГ не тільки є безпечним з огляду на гастроінтестинальні ускладнення, а й має гастропротективні властивості, пов’язані з пригніченням активності інгібіторів індуцибельної NO-синтетази (iNOS) і локальним збільшенням продукції NO в слизовій оболонці шлунка.
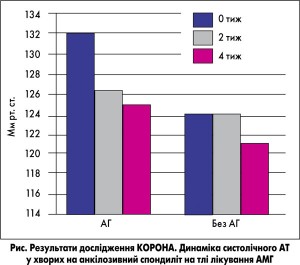
Ефективність і кардіоваскулярна безпека АМГ продемонстровані у клінічному дослідженні КОРОНА за участю пацієнтів з анкілозивним спондилітом та контрольованою АГ. Зокрема, показано, що рівень АТ у пацієнтів незалежно від вихідних значень не тільки не підвищувався, а й навіть знижувався на тлі прийому АМГ (рис.).
Відсутність підвищення рівня АТ під час тривалої терапії АМГ встановлено також у ході дослідження L. Niccoli і співавт. (2002).
Ще одним аргументом на користь застосування АМГ у пацієнтів із підвищеним кардіоваскулярним ризиком є антитромбоцитарний ефект препарату, що був встановлений у ході експерименту (in vitro та ex vivo) і відповідав такому при застосуванні ацетилсаліцилової кислоти (E. Tubaro et al., 1995).
Отже, вибір АМГ для лікування больового синдрому в пацієнтки з ОА та факторами гастроінтенстинального й кардіоваскулярного ризику – цілком обґрунтований.
Якщо окреслювати коло пацієнтів, яким може бути призначено АМГ, то це можуть бути:
– пацієнти з хронічним болем, які потребують тривалого прийому НПЗП;
– пацієнти, що мають високий ризик ерозивно-виразкових ускладнень із боку ШКТ;
– пацієнти з виразковим анамнезом, а також із анамнезом виразкових ускладнень; із диспепсією/ерозіями слизової оболонки ШКТ в анамнезі на тлі прийому інших НПЗП;
– пацієнти з помірним кардіоваскулярним ризиком, АГ (у більшості випадків корекція антигіпертензивної терапії не потрібна).
Отже, персоніфіковане лікування сьогодні залежить від здатності лікаря оцінити всі «за» і «проти» в конкретного пацієнта з урахуванням його індивідуальних особливостей. Вирішення завдання оптимального лікування пацієнтів з ОА полягає у визначенні його фенотипових характеристик, балансу ефективності та безпеки втручання, потреб і преференцій хворого.
Підготувала Наталя Очеретяна