10 травня, 2017
Легочные инфекции при системных ревматических заболеваниях: фокус на оппортунистические инфекции
Для системных ревматических заболеваний (РЗ) характерны высокая заболеваемость и смертность, в значительной мере обусловленные сопутствующими инфекциями. Чаще всего у больных РЗ развиваются легочные инфекции.
Эти пациенты подвержены пневмониям, вызываемым как обычными возбудителями, так и оппортунистической микрофлорой, у них наблюдается повышенная склонность к возникновению инфекционных осложнений. Отчасти это происходит из-за нарушения иммунной регуляции на фоне заболевания, в некоторых случаях – вследствие иммуносупрессивной терапии. Применение ряда лекарственных средств связано с повышением вероятности возникновения инфекций, осложняющих ведение больных с РЗ. Иммуносупрессивная терапия и прием биологических препаратов, особенно назначаемых в комбинации, повышают риск инфицирования оппортунистическими патогенами (Mycobacterium spp., Pneumocystis jiroveci, Histoplasma capsulatum, Coccidioides immitis, Aspergillus spp., Nocardia spp.), а также вероятность развития бактериальных и вирусных респираторных инфекций.
Предрасположенность больных системными РЗ к инфекционной патологии обусловлена 3 основными группами факторов: иммунологическими, связанными с заболеванием и ассоциированными с медикаментозной терапией.
В основе повышения риска инфекционной патологии при РЗ лежат несколько видов иммунологических нарушений. Одно из важнейших – снижение активности системы комплемента. Недостаточность факторов комплемента тесно связана с развитием системной красной волчанки (СКВ) и повышенной восприимчивостью к инфекции, вызываемой капсулообразующими бактериями (Streptococcus pneumoniae и Neisseria meningitidis). Более того, дефицит рецепторов комплемента в эритроцитах, лимфоцитах и нейтрофилах больных СКВ может также препятствовать комплементзависимому клиренсу микроорганизмов. Проявления иммунной дисрегуляции описаны и у больных ревматоидным артритом (РА). В условиях хронического воспаления при РА постоянная антигенная стимуляция сопровождается нарушением гомеостаза Т-клеток, выражающимся в олигоклональной экспансии периферических Т-клеток и глобальном сокращении набора Т-клеточных рецепторов. Эти олигоклональные Т-клетки могут персистировать годами, конкурируя за факторы роста и пространство, что приводит к значительному снижению пула Т-клеток, функционально способных реагировать на чужеродные антигены.
Восприимчивость к инфекции может быть обусловлена органной патологией, вызванной системными РЗ. Поражение органов может привести к появлению locus minoris resistentiae, подверженному воздействию инфекции. Когортные исследования с участием больных идиопатическим фиброзом легких с обострением респираторных симптомов, требующим госпитализации, показали наличие примерно в трети случаев возбудителей, действительно способных вызвать внезапное угнетение функции дыхания. Хорошо известны случаи инфекции при фиброзе легких, сопутствующем РЗ. При мультифакторном анализе когорты больных РА оказалось, что наличие малых признаков интерстициальных заболеваний легких и ревматоидных узелков является важным прогностическим маркером легочной инфекции. Такая патология пищевода, как нарушение моторики или рефлюкс, тоже может быть связана с легочной инфекцией. При системной склеродермии (ССД) наиболее частыми причинами смерти, помимо непосредственно основного заболевания, признаны инфекции, особенно аспирационная пневмония.
Частое использование иммуномодулирующих/иммуносупрессивных препаратов существенно увеличивает риск инфекции у больных РЗ. В терапии данной патологии наиболее часто используются 3 группы лекарственных средств: глюкокортикоиды (ГК), средства базисной терапии и биологические противоревматические препараты.
Глюкокортикоиды
Лечение ГК, оказывающими противовоспалительное и иммуносупрессивное действие, широко практикуется при РЗ. При этом повышается вероятность развития инфекции на фоне угнетения функции фагоцитов и клеточного иммунитета. Метаанализ более 2 тыс. случайно отобранных результатов системного лечения ГК продемонстрировал более высокий риск развития инфекционной патологии у пациентов с различными РЗ независимо от того, получали они малые или высокие дозы препаратов. В обширной когорте больных РА было обнаружено, что использование преднизолона являлось значимым независимым прогностическим фактором госпитализации по поводу пневмонии, причем степень риска коррелировала с повышением дозы. Аналогично среди больных СКВ, которые получали лечение ГК, отмечались большая частота микотических инфекций и более высокая смертность. У пациентов с СКВ и гранулематозом в сочетании с полиангиитом терапия ГК также повышала вероятность развития пневмоцистной пневмонии. Учитывая влияние приема ГК на риск возникновения инфекции, Европейская противоревматическая лига рекомендует выявлять и проводить курс лечения хронических или рецидивирующих инфекций перед назначением данных препаратов и в ходе их применения.
Средства базисной терапии
Средства базисной терапии тоже относятся к факторам, провоцирующим возникновение инфекций, причем степень риска варьирует в зависимости от того, какой из препаратов используют. Так, в большой когорте больных РА прием циклофосфамида был связан с наиболее высокой вероятностью возникновения тяжелых инфекций, требующих госпитализации, тогда как азатиоприн лишь незначительно повышал их частоту. Метотрексат, как оказалось, умеренно увеличивал риск госпитализации по поводу пневмонии, тогда как противомалярийные препараты, лефлуномид, сульфасалазин, циклоспорин и другие средства базисной терапии не повышали риска развития инфекции. Тем не менее в силу сложности ведения больных и необходимости частого комбинирования разных типов препаратов базисной терапии необходим постоянный контроль для своевременного выявления инфекционных осложнений независимо от применяемой схемы лечения.
Биологическая терапия
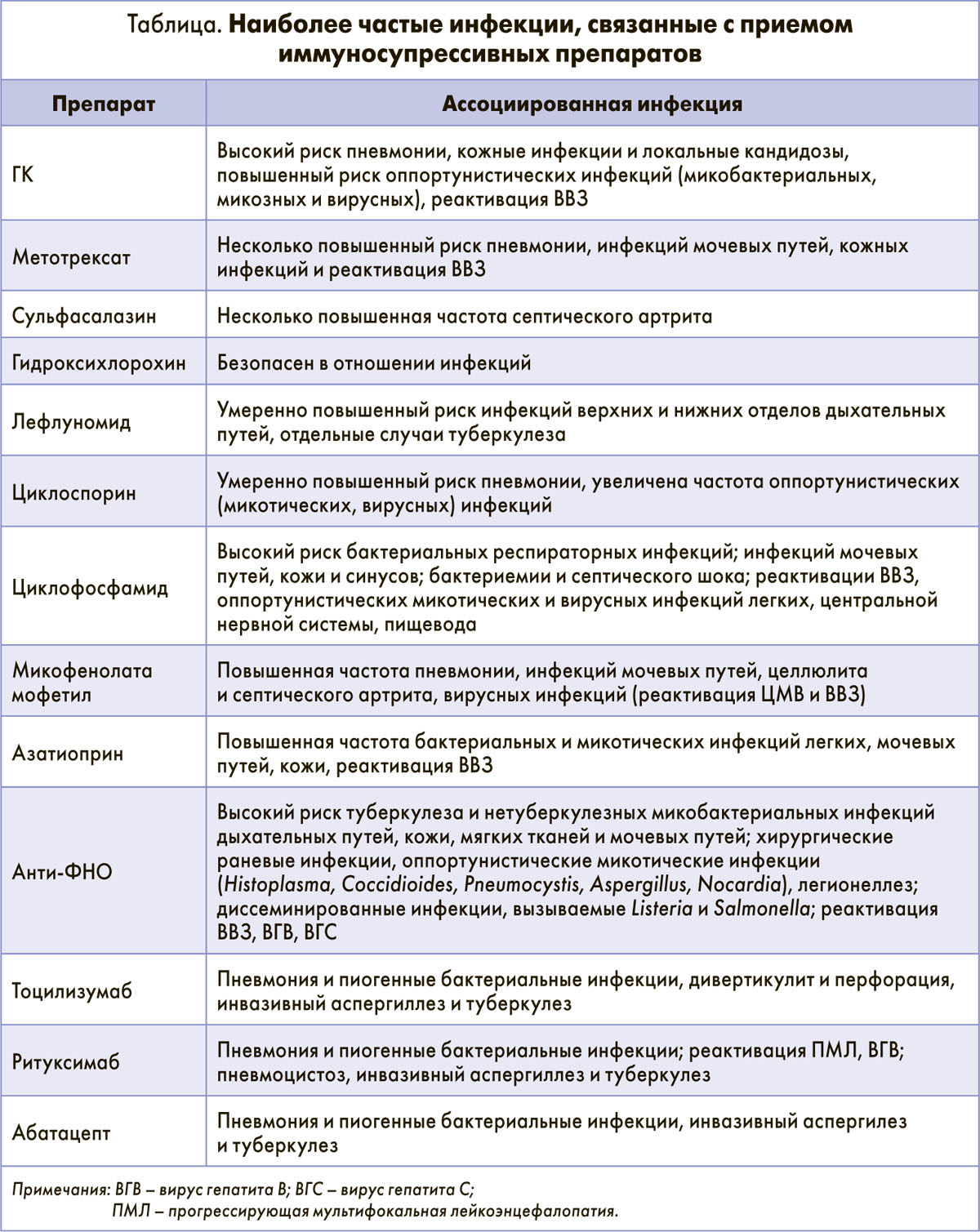 Ингибиторы фактора некроза опухоли (анти-ФНО) считаются терапией выбора при многих РЗ, прежде всего при агрессивных формах РА. Угнетение ФНО может приводить к развитию инфекции или реактивации гранулематозных инфекций наподобие туберкулеза, а также микотических инфекций, таких как Histoplasma, Coccidioides, Aspergillus, Pneumocystis и Nocardia. Нарушение функции макрофагов может также обусловливать предрасположенность к бактериальным инфекциям, как, например, легочным, вызываемым Pneumococcus и Legionella, или диссеминированным, причинами которых являются Salmonella и Listeria. На фоне терапии анти-ФНО препаратами, хотя и реже, могут развиваться вирусные инфекции, вызываемые вирусом Varicella zoster (ВВЗ) и цитомегаловирусом (ЦМВ), как это бывает у больных с иммуносупрессией. Ритуксимаб и анти-CD20-антитела, которые вызывают полное истощение популяции В-клеток, широко используются при лечении системных РЗ. В настоящее время ритуксимаб рекомендуется применять при РА и АНЦА-ассоциированных васкулитах, часто его используют в терапии СКВ с поражением почек или центральной нервной системы, ССД и синдрома Шегрена. Авторы многих работ указывают на повышенную частоту инфекций у больных, принимающих ритуксимаб. Для объяснения этого феномена предложены несколько возможных механизмов. Повышенная восприимчивость к инфекциям может быть связана с нейтропенией и гипогаммаглобулинемией, которые часто возникают при повторных назначениях ритуксимаба. Истощение популяции В-клеток, снижение способности к реализации иммунного ответа на воздействие новых антигенов и антигенпрезентирующей функции В-клеток приводит к нарушению реагирования на влияние микобактерий и пневмоцист. Хотя до сих пор факт повышения частоты микобактериальных и пневмоцистных инфекций у принимающих ритуксимаб достоверно не доказан, рекомендуется проявлять настороженность и проводить постоянное клиническое и лабораторное наблюдение. Наиболее частые инфекционные осложнения, наблюдающиеся на фоне иммуносупрессивной терапии, перечислены в таблице.
Ингибиторы фактора некроза опухоли (анти-ФНО) считаются терапией выбора при многих РЗ, прежде всего при агрессивных формах РА. Угнетение ФНО может приводить к развитию инфекции или реактивации гранулематозных инфекций наподобие туберкулеза, а также микотических инфекций, таких как Histoplasma, Coccidioides, Aspergillus, Pneumocystis и Nocardia. Нарушение функции макрофагов может также обусловливать предрасположенность к бактериальным инфекциям, как, например, легочным, вызываемым Pneumococcus и Legionella, или диссеминированным, причинами которых являются Salmonella и Listeria. На фоне терапии анти-ФНО препаратами, хотя и реже, могут развиваться вирусные инфекции, вызываемые вирусом Varicella zoster (ВВЗ) и цитомегаловирусом (ЦМВ), как это бывает у больных с иммуносупрессией. Ритуксимаб и анти-CD20-антитела, которые вызывают полное истощение популяции В-клеток, широко используются при лечении системных РЗ. В настоящее время ритуксимаб рекомендуется применять при РА и АНЦА-ассоциированных васкулитах, часто его используют в терапии СКВ с поражением почек или центральной нервной системы, ССД и синдрома Шегрена. Авторы многих работ указывают на повышенную частоту инфекций у больных, принимающих ритуксимаб. Для объяснения этого феномена предложены несколько возможных механизмов. Повышенная восприимчивость к инфекциям может быть связана с нейтропенией и гипогаммаглобулинемией, которые часто возникают при повторных назначениях ритуксимаба. Истощение популяции В-клеток, снижение способности к реализации иммунного ответа на воздействие новых антигенов и антигенпрезентирующей функции В-клеток приводит к нарушению реагирования на влияние микобактерий и пневмоцист. Хотя до сих пор факт повышения частоты микобактериальных и пневмоцистных инфекций у принимающих ритуксимаб достоверно не доказан, рекомендуется проявлять настороженность и проводить постоянное клиническое и лабораторное наблюдение. Наиболее частые инфекционные осложнения, наблюдающиеся на фоне иммуносупрессивной терапии, перечислены в таблице.
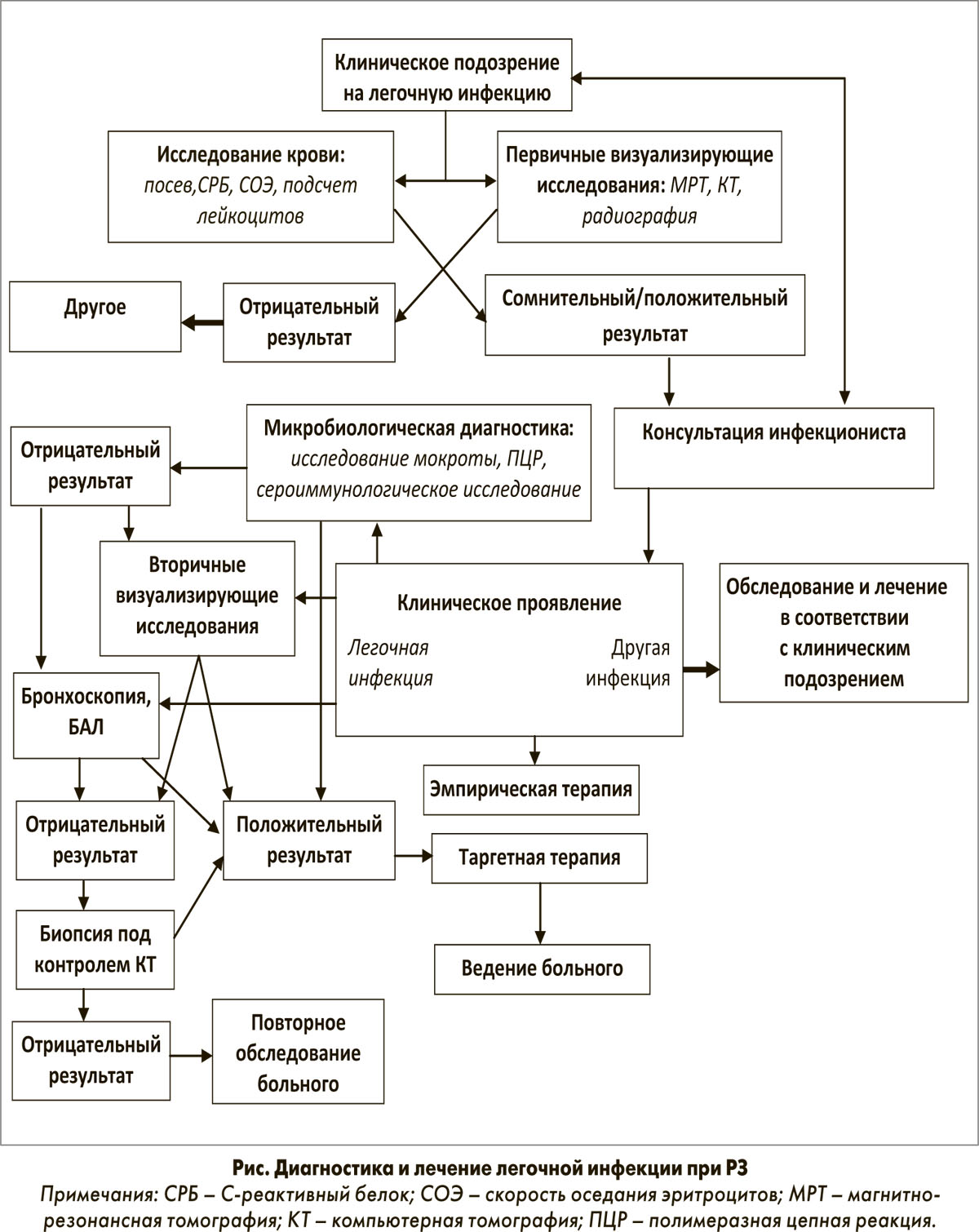 Несмотря на улучшение показателей выживаемости, инфекции лидируют в структуре заболеваемости и смертности больных РЗ. Доминируют нарушения со стороны легких. Пациенты с РЗ предрасположены также к оппортунистическим инфекциям. Ввиду отсутствия специфичности клинических проявлений на ранних стадиях обследование больного должно быть углубленным. При наличии клинических данных, свидетельствующих о легочной инфекции, немедленно должны быть проведены все необходимые исследования и начата соответствующая терапия (рис.).
Несмотря на улучшение показателей выживаемости, инфекции лидируют в структуре заболеваемости и смертности больных РЗ. Доминируют нарушения со стороны легких. Пациенты с РЗ предрасположены также к оппортунистическим инфекциям. Ввиду отсутствия специфичности клинических проявлений на ранних стадиях обследование больного должно быть углубленным. При наличии клинических данных, свидетельствующих о легочной инфекции, немедленно должны быть проведены все необходимые исследования и начата соответствующая терапия (рис.).
Поскольку ведение таких пациентов сопряжено с большими сложностями, необходимо участие мультидисциплинарной команды, включающей специалистов-ревматологов и инфекционистов, имеющих опыт ведения пациентов, получающих иммуносупрессивные препараты. Учитывая потенциально высокую смертность в результате подобных инфекций, исследования должны проводиться быстро, без задержек в диагностике. Для этиологического диагноза необходима тщательная оценка клинических и лабораторных данных, в том числе бронхоальвеолярного лаважа (БАЛ) и биопсии легких, когда это показано. Таргетную терапию следует начинать как можно скорее.
Di Franco M., Lucchino B., Spaziante M. et al. Lung Infections in Systemic Rheumatic Disease:
Focus on Opportunistic Infections. Int. J. Mol. Sci. 2017, 18, 293.
Перевел с англ. Геннадий Долинский
Медична газета «Здоров’я України 21 сторіччя» № 7 (404), квітень 2017 р.


