22 березня, 2017
Тотальная панкреатэктомия при злокачественных новообразованиях поджелудочной железы
В 1960 году в мире было описано всего 97 случаев выполнения тотальной панкреатэктомии (ТПЭ). Сегодня с каждым днем количество этих операций неуклонно растет. Так, при анализе данных реестра Национального института здоровья США с 1998 по 2006 гг. ТПЭ была выполнена 4013 пациентам, при этом количество больных, оперированных ежегодно, возрастало (в 1998 г. – 384, в 2006 г. – 494 пациента), а частота послеоперационной летальности снижалась (1998-2000 гг. – 12,4%, 2002-2006 гг. – 5,9%). В то же время в Украине эти операции выполняются крайне редко.
Несмотря на то что в настоящее время ТПЭ уже признана как опция для ряда клинических ситуаций, консенсус в отношении показаний к выполнению этой операции все еще не достигнут. На сегодняшний день самыми распространенными показаниями в онкологии являются:
1. Рак поджелудочной железы (РПЖ), особенно наследственные его формы (BRCA‑2 синдром, синдром Пейтс-Егерса, наследственный аденоматозный полипоз, наследственный неполипозный колоректальный рак, наследственная атипичная множественная меланома и др.). При этом, если у пациентов ≥3 прямых родственников имели в анамнезе РПЖ, риск его возникновения возрастает в 57 раз. Это заболевание передается аутосомно-доминантным путем, и ТПЭ рассматривается рядом авторов как адекватная профилактическая мера. При этом больным может выполняться одномоментная инсулярная аутотрансплантация.
2. Интрадуктальные папиллярно-муцинозные опухоли составляют около 3-5% от всех первичных опухолей поджелудочной железы (ПЖ); часто полностью поражают главный панкреатический проток. От 30 до 72% этих опухолей при детальном гистологическом исследовании представляют собой инвазивную или неинвазивную карциному. Кроме того, они часто сосуществуют с протоковой аденокарциномой ПЖ. Отмечен ряд случаев появления протокового рака культи железы после резекции по поводу интрадуктальной папиллярно-муцинозной опухоли. В связи с этим показания для ТПЭ при указанном виде опухоли расширяются.
3. Нейроэндокринные опухоли составляют 3-4% от общего числа. Проявляясь в синдроме множественной эндокринной неоплазии первого типа (MEN1), они характеризуются мультицентрическим ростом, в том числе в подслизистом слое дуоденум и хвосте ПЖ с высоким риском малигнизации, что является прямым показанием к ТПЭ.
4. Мультифокальное метастатическое поражение ПЖ. Встречается не чаще чем в 5% всей онкопатологии железы. Наиболее часто наблюдается при раке почки (примерно 50% всех метастатических поражений).
Материалы и методы
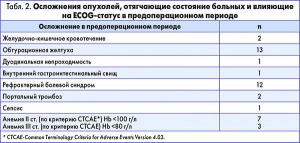
На клинической базе кафедры общей хирургии № 1 НМУ им. А.А. Богомольца, в Киевском центре хирургии печени, поджелудочной железы и желчных протоков им. В.С. Земскова (КГКБ № 10) с 2003 по 2015 гг. ТПЭ была выполнена 35 пациентам (женщин – 16, мужчин – 19; средний возраст больных – 57,3±8,3 года). Гистологические виды и онкологическая стадийность опухолей у пациентов, которым была выполнена ТПЭ, представлены в таблице 1. У большинства оперированых больных отмечались осложнения опухолевого процесса (распад опухоли, кровотечение, непроходимость и др.). В таблице 2 представлен предоперационный статус пациентов. Более 2/3 из них имели клинически значимые симптомы. У пятерых пациентов по шкале ECOG статус был 2, у всех остальных >2.
Учитывая тяжесть предоперационного состояния многих больных, мы сочли необходимым поделить все выполненные нами панкреатэктомии в зависимости от общехирургических показаний на плановые и срочные (табл. 3). Это значительно упростило анализ отдаленных результатов.
В зависимости от сложности панкреатэктомии были поделены на комбинированные и некомбинированные. Среди комбинированных панкреатэктомий наиболее часто выполнялись тотальные дуодено-сплено-панкреато-гастрэктомии. Показанием к этому служило впадение левой желудочной вены в селезеночную вену или вовлечение первой в опухолевый процесс.
Объем лимфаденэктомии при протоковой аденокарциноме ПЖ варьировал. В случаях парааортальной лимфаденопатии он соответствовал расширенной радикальной лимфаденэктомии по классификации Сastelfranco Veneto, 1999.
В последнее время выделение ПЖ нами выполняется начиная от крючковидного отростка без транссекции перешейка. При этом достигается полная мобилизация порто-мезентериального сегмента воротной вены. По нашему мнению, удаление железы «en bloc» позволяет снизить риск локального рецидивирования.
Результаты
Послеоперационная летальность. В нашем исследовании в послеоперационном периоде умерли 7 больных, 5 из них были оперированы в срочном порядке, 4 из них выполнена комбинированная ТПЭ. Общая летальность составила 20% (7 из 35). Среди больных, оперированных в плановом порядке, послеоперационная летальность составила 6,7% (2 из 30).
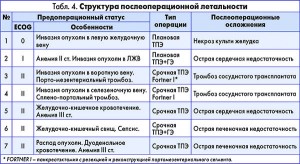
Как видно из таблицы 4, все 5 пациентов, оперированных в срочном порядке, имели тяжелые осложнения в предоперационном периоде, что повлекло за собой декомпенсацию и смерть в течение 1 месяца после операции.
Два случая послеоперационной смерти плановых больных связаны: 1 – с некрозом культи желудка вследствие перевязки левой желудочной вены, атипично впадающей в селезеночную вену, что привело к блоку единственного оставшегося пути венозного оттока от желудка. Во втором случае больной умер от острой сердечной недостаточности, несмотря на адекватную коррекцию анемии до операции и отсутствие значимой интраопреационной кровопотери.
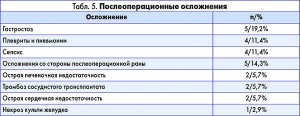
Осложнения. Общая частота послеоперационных осложнений составила 48,6% (17 пациентов). Из них 5 – это пациенты, которым ТПЭ была выполнена в срочном порядке. Таким образом, для плановых ТПЭ частота осложнений составила 40% (12 пациентов). Неспецифические послеопреационные осложнения учитывались начиная с 2 баллов по шкале Clavien-Dindo. Гастростазы определены согласно классификации ISGPS и считались только для 26 пациентов без гастрэктомий. Все осложнения представлены в таблице 5.
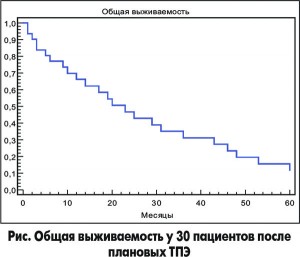
Выживаемость. Анализ выживаемости в нашем исследовании проводился путем построения кривой Каплана-Майера для 30 больных после плановых ТПЭ (рис.), так как все 5 больных, которым ТПЭ была выполнена в экстренном или срочном порядке, умерли в течение 30 дней после операции. Трехлетняя выживаемость составила 40% (12 пациентов), 5-летняя выживаемость – 13,3% (4 больных). Медиана выживаемости – 18 месяцев.
Основными метаболическими последствиями ТПЭ является тяжелая экзокринная недостаточность с синдромом мальассимиляции, нутритивными нарушениями, сахарный диабет со склонностью к гипогликемии, стеатогепатоз и стеатогеапатит.
Экзокринная функция ПЖ после операции отсутствовала у всех пациентов. Адекватной заместительной терапией является пероральный прием панкреатических ферментов до 400 тысяч ЕД (липазы) в сутки.
У всех больных после ТПЭ развился сахарный диабет 3 типа (по классификации ВОЗ), который характеризовался гликемической нестабильностью с частыми эпизодами постпрандиальной гипергликемии, с ночными гипогликемиями, редкими кетоацидозом, ангиопатиями и сравнительно невысокой потребностью в инсулине. На 4-й неделе послеоперационного периода при неосложненном течении доза инсулина составляла от 4 до 40 ЕД/сут. В среднем около 0,5 ЕД/кг/сут.
В случаях резкой гликемической нестабильности в послеоперационном периоде – 6,7% (2 пациента) – была использована система постоянного мониторинга гликемии (CGMS), которая дает возможность выявить скрытые эпизоды гипогликемии и более адекватно оценивать течение диабета. Использование этой технологии позволило существенно улучшить степень компенсации сахарного диабета.
Кроме дефицита инсулина у больных после ТПЭ в развитии эндокринных изменений активную роль также играет дефицит глюкагона и панкреатического пептида (ПП). В этом заключается основное различие между панкреатогенным диабетом (ПД) и диабетом 1 и 2 типа. Считается, что больные ПД более склонны к тяжелым гипогликемиям и более резистентны к развитию кетоацидоза. В их плазме наблюдается более высокий уровень прекурсоров глюконеогенеза, включая аланин и лактат, что связано с отсутствием глюкагона. В отношении ПП предполагают, что он играет ключевую роль в индукции чувствительности гепатоцитов к инсулину и регуляции инсулиновых рецепторов. При ПД происходит дерегуляция инсулиновых рецепторов в тканях, что обусловливает индивидуальную чувствительность пациентов к заместительной терапии инсулином, более высокий риск гипо- и гипергликемий и, как следствие, приводит к сложностям в адекватном контроле гликемии. Предсуществующая патология ПЖ также может играть роль в контроле гликемии после ТПЭ. Недавние исследования показали, что у пациентов после ТПЭ по поводу хронического панкреатита диабет чаще имеет декомпенсированное течение.
Уровень гликозилированного гемоглобина (HbA1c) крови и частота гипогликемий наших пациентов после ТПЭ не отличались от таковых при диабете 1 и 2 типа и соответствовали таковым в других опубликованных наблюдениях. Все пациенты применяют продленный инсулин в сочетании с коротким инсулином препрандиально. Средняя суточная доза инсулина у таких больных составляет около 0,5 ЕД/кг.
Дискуссия
Первые ТПЭ были описаны еще в конце XIX века. Однако ТПЭ, после которой пациент выжил, получая заместительную инсулинотерапию, была выполнена впервые в 1943 году [1]. Без малого 60 лет разделяют в истории первый опыт выполнения этой операции от успешного ее результата! В 1950-х годах бытовало мнение, что им присущ мультицентрический характер. Причиной тому была высокая частота локальных рецидивов в культе ПЖ после резекций. Это побуждало ученых того времени к более широкому внедрению ТПЭ в хирургическую практику [2]. Кроме того, они полагали, что эта процедура позволяет повысить онкологическую радикальность хирургического лечения, а также избежать на то время очень частых и тяжелых осложнений, связанных с несостоятельностью панкреатодигестивных анастомозов при панкреатодуоденальной резекции.
Тем не менее «успех» операции оказался непродолжительным. Результаты ТПЭ были признаны неудовлетворительными из-за неприемлемого уровня послеоперационных осложнений и летальности. Основными проблемами, которые приводили к этому, были панкреатогенный диабет, характеризующийся гликемической нестабильностью со склонностью к гипогликемиям, и экзокринная панкреатическая недостаточность. С 60-х по 80-е годы прошлого века высококачественные ферментативные препараты, необходимые для купирования экзокринной недостаточности, были еще недоступны (в Украине они оставались малодоступными вплоть до конца 1990-х годов). Таким образом, прогрессирующая потеря массы тела, диарея и мальабсорбция способствовали формированию кахексии со значительным снижением качества жизни, физической и социальной активности этих больных. Кроме того, эти же изменения значительно осложняли контроль гликемии у пациентов после ТПЭ. Стеаторея приводила к дефициту жирорастворимых витаминов, в особенности витамина D, что служило причиной развития остеопороза и жирового гепатоза. Совокупность указанных факторов сменила интерес, вызванный этой операцией в 1960 годах, на негативизм в 1980-1990 годах.
Кроме того, негативное отношение к ТПЭ было продиктовано отсутствием улучшения онкологической выживаемости больных РПЖ.
Тем не менее интерес к ТПЭ в последнее время усиливается благодаря многим факторам. Во-первых, развитие морфологии в последние десятилетия расширило наши представления о природе и биологических свойствах опухолей ПЖ. Инвазивная протоковая аденокарцинома ПЖ составляет от 85 до 90% всех злокачественных поражений ПЖ, является самой биологически агрессивной и, как следствие, ассоциируется с наихудшим прогнозом даже после радикальной резекции и адъювантной терапии. При этом диагнозе ТПЭ не приносит улучшения в выживаемости по сравнению с резекциями ПЖ. Однако такие опухоли, как внутрипротоковая папиллярно-муцинозная неоплазия с генерализованным поражением протока ПЖ, мультицентрические нейроэндокринные опухоли и изолированные множественные метастатические поражения ПЖ, являются менее агрессивными и прогностически более благоприятными. Обеспечение адекватного локального контроля посредством ТПЭ является обязательным условием в протоколе онкологического лечения этих больных. Более того, даже при протоковой аденокарциноме, в случае ранней диагностики (путем эндоскопической эксфолиативной (браш) биопсии протокового эпителия ПЖ) рака «in situ» или так называемой PanIN3-стадии дисплазии, а также генетически подтвержденных наследственных онкосиндромов (BRCA-синдром, синдром Пейтс-Егерса, наследственный аденоматозный полипоз, наследственный неполипозный колоректальный рак, наследственная атипичная множественная меланома и др.) ТПЭ может быть оправдана с точки зрения улучшения онкологической выживаемости [3].
Во-вторых, современные хирургические и анестезиологические технологии в комплексе с новыми подходами в диабетологии и заместительной энзимотерапией не только позволяют обеспечить более адекватный уход за больным в раннем послеоперационном периоде, но и обеспечивают ему достаточно высокое качество жизни в последующем.
Успех адекватного контроля гликемии поcле ТПЭ зависит от многих факторов. В первую очередь это раннее обучение и информирование пациента об особенностях ПД. Если вероятность ТПЭ в предоперационном периоде велика, то пациент должен иметь персональный глюкометр еще до операции. В состав мультидисциплинарной команды нашей клиники входит эндокринолог, имеющий опыт совместного с хирургами ведения пациентов после ТПЭ. Он консультирует больного перед операцией и сразу после перевода из отделения реанимации и интенсивной терапии или начала энтерального питания. К этому моменту у пациента уже должна быть его «история сахаров», мониторируемая персональным глюкометром, начиная с момента экстирпации ПЖ. В арсенал эндокринолога также входит CGMS. Особенностью данной системы является имплантируемый на 3-5-й день в подкожную клетчатку брюшной стенки датчик уровня глюкозы, соединенный с компьютерным чипом. Это позволяет с помощью соответствующего программного обеспечения отслеживать гликемические кривые пациента и их корелляцию с приемом пищи и введением инсулина, что значительно упрощает контроль гликемии в сложных случаях, особенно при гнойно-септических осложнениях. Однако на протяжении последних 5 лет в условиях раннего обучения пациента необходимиости в применении CGMS у нас не было.
В отношении использования глюкагона на сегодняшний день четких рекомендаций не существует. В литературе есть данные об эффективности глюкагона в предотвращении постпрандиальной гипогликемии у пациентов с сахарным диабетом 1 типа. Заместительную терапию глюкагоном авторы проводили у малого количества пациентов после ТПЭ и сообщают, что при пропорциональном назначении глюкагона и инсулина у таких больных значительно улучшается утилизация гликогенных аминокислот, липидов и углеводов.
Еще одним довольно частым и серьезным осложнением после ТПЭ является стеатогепатит. Причина его развития является многофакторной, одним из основных патогенетических аспектов выступает снижение чувствительности гепатоцитов к инсулину, в том числе вследствие дефицита ПП. Сегодня продолжается активное изучение этой комплексной проблемы, а консенсус в отношении лечения стеатогепатита у больных после ТПЭ еще не выработан.
И все же сегодня ТПЭ выполняется довольно редко и число наблюдений пациентов после этой операции очень ограничено. Bhayani в 2013 г. анализировал общенациональную базу данных Американского колледжа хирургов США с 2005 по 2011 гг. В результате из 6314 плановых онкологических резекций ПЖ только 198 (3%) припадали на долю ТПЭ. Современные публикации, посвященные ТПЭ, насчитывают 25-198 случаев и представляют собой опыт одной или нескольких клиник за более чем 5-летний период [4].
В последнее время в литературе ТПЭ принято разделять на элективные (плановые, одноэтапные) и завершающие (completing) – выполняемые, как правило, по поводу осложнений со стороны культи уже оперированной ПЖ, либо при рецидивах в культе ПЖ. В силу малого количества наблюдений анализ результатов ТПЭ часто проводится на общей выборке пациентов, которая включает в себя как элективные, так и завершающие ТПЭ. Это, с одной стороны, позволяет повысить силу статистического критерия за счет увеличения числа наблюдений в выборке, но с другой стороны, эта выборка становится менее однородной. Как следствие, часто неудовлетворительные результаты завершающих ТПЭ, выполняемых при панкреонекрозах культи ПЖ, на фоне уже существующих хирургических осложнений (панкреатический свищ, гастростаз, постгеморрагическая анемия и т.д.) экстраполируются на результаты элективных ТПЭ. Это, на наш взгляд, способствует сохранению негативизма в отношении ТПЭ.
ТПЭ – это технически сложная хирургическая процедура. Однако для хирургов-панкреатологов, владеющих техникой дистальной и проксимальной резекции ПЖ и выполняющих не менее 25 этих вмешательств в год, ТПЭ не представляет особой сложности. При тщательном отборе пациентов для этой операции уровень послеоперационных хирургических осложнений и летальности не значительно отличается от таковых после резекций ПЖ. Итальянский опыт 65 ТПЭ, представленный Crippa [5], свидетельствует о 39% послеоперационных осложнений с нулевой летальностью. Клиника Мейо приводит свои данные о 99 ТПЭ с 32% осложнений и 5% летальности [6]. Muller сообщает о 124 элективных ТПЭ, летальность не превышала 5%, а осложнения – 40%, хотя летальность после 23 завершающих ТПЭ, выполненных по поводу осложнений, достигала 39% [7].
Интересное, на наш взгляд, сообщение опубликовали американские коллеги [8]. Был проведен анализ послеоперационных осложнений у 64 пациентов после элективной ТПЭ с летальностью 1,6%. Осложнения оценивались путем вычисления так называемого постоперационного индекса морбидности (PMI). Этот интегральный показатель позволяет оценить не только частоту, но и степень тяжести и риски этих осложнений. Так, для их выборки риск осложнений после ТПЭ составляет 45,3%, при этом тяжесть осложнения составляет 33,3 по 100-бальной шкале. Необходимость выполнения сосудистой или мультивисцеральной резекции в ходе ТПЭ не оказывала влияния на PMI.
Последнее наблюдение противоречит данным Bhayani [9], которые свидетельствуют о 2-кратном увеличении частоты осложнений при расширении ТПЭ с вовлечением еще одного органа брюшной полости. Анализ осложнений проведен на 198 пациентах на протяжении 90 дней после операции. Летальность в этом исследовании составила 6,1%, а общий процент осложнений – 44%. Наш опыт также указывает на тенденцию к увеличению частоты осложнений у больных с комбинированными ТПЭ.
К сожалению, на протяжении последних 20 лет, когда во всем мире возобновился интерес к ТПЭ, более того, эта операция уже заняла свою нишу в арсенале хирургического лечения внутрипротоковых папиллярно-муцинозных нейроэндокринных опухолей ПЖ, а также наследственных форм рака ПЖ и хронического панкреатита, социально-экономические условия в Украине не способствовали научно-практическому развитию хирургии. Как результат, несмотря на доступность практически всего необходимого спектра технологической и фармакологической поддержки для выполнения ТПЭ и адекватного послеоперационного ведения этих больных, сегодня упоминание об этой операции вызывает смятение и негодование многих ведущих украинских хирургов.
Мировой опыт доказал, что ТПЭ не только имеет право на существование, но и в ряде ситуаций является единственным средством лечения и продления жизни больному.
Выводы
Опыт нашей клиники показывает, что сегодняшний уровень развития хирургии в Украине позволяет внедрять эту процедуру в практику с удовлетворительными результатами, соответствующими мировым.
Для обеспечения успешной ТПЭ в наших условиях, что дает пациентам шанс на долгосрочную выживаемость с сохранением физической активности и социальной функции после ТПЭ, необходимо соблюдение следующих условий.
Тщательный предоперационный отбор пациентов, основанный не только на оценке основного диагноза, возраста, сопутствующей патологии, риска удаления соседних органов, но и психологической и финансовой готовности пациента и его родственников обеспечивать заместительную терапию и адъювантное лечение.
Обучение пациента особенностям панкреатогенного диабета, консультация опытного диабетолога в пред- и послеоперационном периоде.
В послеоперационном периоде обязательное совместное ведение больного мультидисциплинарной командой, включающей хирурга, гастроэнтеролога, эндокринолога, онколога, при необходимости психолога, диетолога и других специалистов + диспансерное наблюдение.
Литература
Rockey E.W. Total pancreatectomy for carcinoma: Case Report. Ann Surg 1943; 118: 603-611.
ReMine W.H., Priestley J.T., Judd E.S., et al. Total pancreatectomy. Ann Surg. 1970; 172: 595-604.
Bartsch D.K. Familial pancreatic cancer. Br J Surg 2003; 90: 386-387.
Bhayani N.H., Miller J.L., Ortenzi J., Kaifi J.T., Kimchi E.T., Staveley-O’Carroll K.F., Gusani N.J. Perioperative Outcomes of Pancreaticoduodenectomy Compared to Total Pancreatectomy for Neoplasia. J Gastrointest Surg (2014) 18: 549-554.
Crippa S., Tamburrino D., Partelli S., et al (2011) Total pancreatectomy: indications, different timing, and perioperative and long-term outcomes. Surgery 149: 79-86.
Billings B.J., Christein J.D., Harmsen W.S., et al. Quality-of-life after total pancreatectomy: is it really that bad on long-term follow-up? J Gastrointest Surg. 2005; 9: 1059-1066.
Muller M.W., Friess H., Kleeff J., Dahmen R., Wagner M., Hinz U., Breisch-Girbig D., Ceyhan G.O., Buchler M.W. Is there still a role for total pancreatectomy? Annals of Surgery. 2007; 246(6): 966-74.
Datta J., Lewis Jr R.S., Drebin J.A. et al. Quantifying the Burden of Complications Following Total Pancreatectomy Using the Postoperative Morbidity Index: A Multi-Institutional Perspective J Gastrointest Surg (2015) 19: 506-515.
Bhayani N.H., Kimchi E.T., Kaifi J.T., Staveley-O’Carroll K.F., Gusani N.J. Pancreaticoduodenectomy-multivisceral aresection adds morbidity: a NSQIP analysis. Surgery. 2013; in review.