18 травня, 2017
Диабетическая нейропатия: когда время играет решающую роль
Стоит только попристальнее вглядеться в настоящее,
будущее вдруг выступит само собой.
Н.В. Гоголь
Когда к врачу обращается пациент с выраженной болевой формой диабетической нейропатии (ДН)
или с синдромом диабетической стопы, можно купировать симптомы, но уже мало что можно сделать для существенного улучшения прогноза у данного больного. Означает ли это, что ДН – приговор? Нет, на ситуацию можно существенным образом повлиять при условии своевременного выявления и раннего начала патогенетического лечения этого осложнения. Говорят, что время – единственный фатально невозобновляемый ресурс во вселенной, и при ДН оно действительно играет решающую роль.
Когда же следует предпринимать активные действия и с чего начинать? Постараемся разобраться
в этой статье.
Есть диабет или даже предиабет?
Ищите нейропатию!
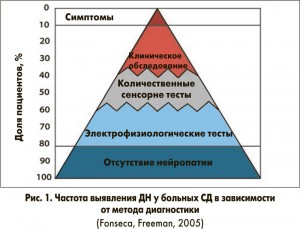
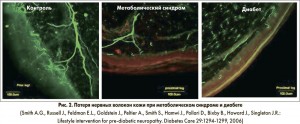
ДН считается самым частым осложнением сахарного диабета (СД). Ее распространенность в популяции больных СД очень высока и, по данным некоторых авторов, может достигать 80%, если для ее выявления использовать электрофизиологические методы диагностики (рис. 1). Таким образом, отсутствие ДН у больного СД можно считать скорее исключением, чем правилом. Следует отметить, что поражение мелких нервных волокон происходит еще до развития самого диабета, то есть на уже на фоне метаболического синдрома (рис. 2).
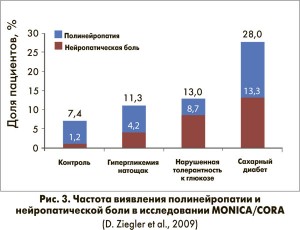
В исследовании MONICA/CORA, проведенном Ziegler и соавт. в 2009 г., было показано, что поражение нервной системы и соответствующие клинические признаки нейропатии могут проявляться даже на этапе предиабета. По их данным частота выявления диабетической полинейропатии и нейропатической боли у лиц с нарушенной толерантностью к глюкозе составляет 13%, с повышенной гликемией натощак – 11,3% (рис. 3).
Nota bene! Точка невозврата
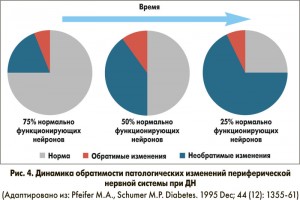
ДН, как и другие хронические осложнения СД, при отсутствии контроля гликемии и адекватной патогенетической терапии представляет собой неуклонно прогрессирующий патологический процесс. На определенном этапе к функциональным отклонениям (нарушение нейротрофики, ухудшение проведения нервного импульса) добавляются структурные изменения нервных волокон (демиелинизация, дегенерация, атрофия), а затем и гибель нервных клеток. С течением времени количество нормально функционирующих нейронов уменьшается, и рано или поздно наступает точка невозврата, когда уже невозможно вернуть исходное состояние нервной системы (рис. 4). Чем больше длительность течения СД и ДН, тем более выражены необратимые органические изменения периферических нервов и тем меньше в распоряжении врачей остается возможностей терапевтического воздействия на функциональные нарушения.
Поэтому выявлять ДН и начинать ее лечение необходимо как можно раньше.
Ранняя диагностика диабетической нейропатии: препятствия и возможности
К сожалению, сегодня в силу ряда причин ДН у большинства больных диагностируют очень поздно, когда время для эффективного вмешательства уже упущено. В целом это неудивительно, если учесть длительное бессимптомное течение этого осложнения. Ведь жалобы на боль и парестезии пациенты начинают предъявлять, как правило, уже на более поздних стадиях заболевания. При СД 2 типа ситуация усугубляется еще и тем, что он также длительно протекает бессимптомно и поздно диагностируется, в результате чего у многих больных уже к моменту установления диагноза имеются признаки ДН.
Таким образом, рассчитывать на своевременное выявление ДН на основании жалоб больных не приходится – необходим активный скрининг.
У пациентов с СД 1 типа его рекомендуется проводить через 5 лет после манифестации заболевания, а вот при СД 2 типа – сразу после установления диагноза. В последующем скрининговые исследования проводятся ежегодно.
Какие методы диагностики следует использовать для скрининга? О том, что неприемлемо опираться на активные жалобы пациентов на боль и парестезии, уже было сказано выше. Более ранние стадии ДН можно выявить с помощью рутинной оценки на наличие неврологического дефицита, то есть исследуя разные виды чувствительности (болевая, тактильная, вибрационная и др.), силу мышц и рефлексы. Однако эти методы оценки достаточно субъективны и их результаты могут быть искажены большим количеством вмешивающихся факторов.
Большей объективностью и высокой чувствительностью обладают электрофизиологические методы (оценка нервной проводимости, электромиография), однако они не являются широкодоступными и поэтому не могут быть использованы для массового скрининга. Это, скорее, полезный инструмент для научно-исследовательских целей. К тому же они предназначены для выявления нарушения функции только крупных миелинизированных нервных волокон, в то время как первыми при ДН повреждаются мелкие волокна.
Нейропатия мелких волокон: сигнал для врача о необходимости активных действий
В последние годы в медицинской литературе, прежде всего англоязычной, все чаще встречается термин «нейропатия мелких волокон». Напомним, что периферические нервные волокна могут быть классифицированы в зависимости от их размера и наличия миелиновой оболочки: миелинизированные нервные волокна большого и среднего диаметра (А-альфа, бета, гамма), слабомиелинизированные нервные волокна среднего диаметра (A-дельта) и немиелинизированные/слабомиелинизированные нервные волокна мелкого диаметра (C). Большие волокна диаметром 6-12 мкм имеют миелиновую оболочку и отвечают за сухожильно-мышечные рефлексы, тактильную, вибрационную и проприоцептивную чувствительность. Мелкие нервные волокна не имеют миелиновой оболочки или слабо миелинизированы и отвечают за температурную и болевую чувствительность, а также за вегетативные функции (потоотделение, вазодилатация и др.). Мелкие волокна составляют примерно 80-90% от всех периферических нервных волокон.
Нейропатия мелких волокон представляет особый интерес для клиницистов, так как мелкие нервные волокна поражаются на более ранних этапах, чем крупные, причем их функция может быть нарушена даже у лиц с нарушенной толерантностью к глюкозе.
Так, в ряде исследований было показано нарушение со стороны мелких нервных волокон при нормальной проводимости крупных волокон (Malik et al., 2005; Smith et al., 2001; Sumner et al., 2003).
Как можно диагностировать это патологическое состояние? Указывать на наличие нейропатии мелких волокон будет болевой синдром и симптомы автономной нейропатии при нормальных показателях вибрационной чувствительности и электрофизиологических тестов (нервной проводимости). Причем не стоит ждать, пока пациент сам придет к врачу с нестерпимой болью или парестезиями, которые не дают ему заснуть по ночам. Тщательно собирайте анамнез, спрашивайте о любых необычных или неприятных явлениях, например «непереносимости постельного белья» или синдроме беспокойных ног, которые будут указывать на пока еще не явно заметные пациенту парестезии. Также пристальное внимание должно быть обращено на симптомы нарушения вегетативных функций, которые на первый взгляд могут казаться не связанными с СД: частые диарея или запор, сухость кожи или гипергидроз, приливы крови к лицу, половая дисфункция и др. Важно помнить, что и симптомы вегетативной дисфункции часто выражены умеренно, поэтому пациенты не всегда придают им значение и сообщают о них самостоятельно.
Обнаружить нейропатию нервных волокон еще до появления симптомов помогают специализированные исследования мелких нервных волокон: оценка температурного порога (специальным прибором) и судомоторной функции (индикаторным пластырем), ортостатическая проба (изменение АД при изменении положения тела), биопсия с оценкой интраэпидермальной плотности нервных волокон. Интересно, что в исследовании Tesfaye и соавт. (2010), в котором использовались методы обнаружения нейропатии мелких волокон, ДН обнаружили у 12,5% пациентов с предиабетом, что заметно выше по сравнению с упомянутой ранее работой Ziegler и коллег.
Лечение: с чего начинать?
Безусловно, краеугольным камнем профилактики развития и прогрессирования всех хронических осложнений является контроль гликемии. Но, увы, обычно этого недостаточно. Как показывает ряд исследований, ДН и другие осложнения могут прогрессировать, несмотря на хорошую компенсацию СД. Вероятно, это обусловлено феноменом метаболической памяти. Под этим термином подразумевают необратимые изменения, развивающиеся при сравнительно коротком периоде воздействия высокой концентрации глюкозы. Причиной данных нарушений является процесс гликозилирования белков митохондрий, приводящий к избыточному формированию свободных радикалов и усугубляющий течение ассоциированных с диабетом осложнений.
Поэтому если врач выявил ДН, как манифестную, так и субклиническую (и даже на стадии предиабета), он должен помимо контроля гликемии и других факторов риска (дислипидемии, артериальной гипертензии и т.д.) и симптоматических средств, не влияющих на течение болезни, обязательно назначить патогенетическую терапию. Под патогенетическим
лечением ДН подразумевают назначение лекарственных средств, способных прервать на том или ином этапе патобиохимический каскад, запущенный гипергликемией, и замедлить утрату функционирующих нейронов. Этот каскад включает такие звенья: активация полиолового пути метаболизма глюкозы с накоплением сорбита и фруктозы с последующим отеком клеток, оксидативный стресс, неэнзиматическое гликозилирование структурных и функциональных белков и др. Их результатами является как непосредственное поражение нервных волокон, так и эндотелия vasa nervorum, что приводит к снижению эндоневрального кровотока и гипоксии.
Ключевая роль в патогенезе ДН отводится оксидативному стрессу, влиять на который можно с помощью альфа-липоевой кислоты (АЛК).
Она не только обладает мощным прямым антиоксидантным эффектом, но и восстанавливает активность других антиоксидантов, а также уменьшает инсулинорезистентность. Все это обеспечивает надежную защиту нервов и сосудов, что подтвердили экспериментальные и клинические исследования.
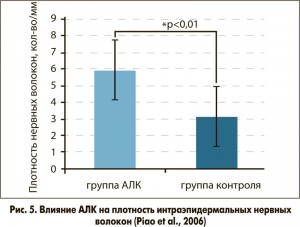
Так, Piao с коллегами провели интересный эксперимент, в котором оценили влияние АЛК на плотность интраэпидермальных нервных волокон и их функцию. Части подопытных животных с индуцированным СД 2 типа давали АЛК перорально в течение 40 недель, а остальным – нет. У крыс с диабетом было отмечено существенное снижение плотности нервных волокон в эпидермисе (рис. 5) и повышение порога вибрационной чувствительности по сравнению с животными, получавшими АЛК.
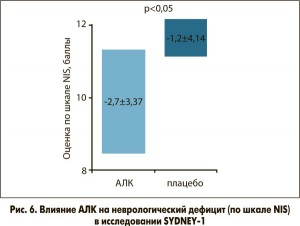
Особого внимания заслуживает тот факт, что именно АЛК имеет сегодня наибольшую доказательную базу клинической эффективности среди средств патогенетической терапии (масштабные контролируемые исследования ALADIN I, ALADIN II, ALADIN III, ORPIL, SYDNEY, SYDNEY II, DEKAN, NATHAN I, NATHAN II). В контексте рассматриваемой темы важно отметить, что в ряде клинических испытаний АЛК показала способность уменьшать не только положительную симптоматику (выраженность боли и парестезий), но и неврологический дефицит (рис. 6). Так, метаанализ Ziegler и соавт., объединивший 4 исследования (ALADIN I, ALADIN III, SYDNEY, NATHAN II) с участием в общей сложности 1258 пациентов, показал улучшение показателя NIS-LL (шкала оценки неврологического дефицита) на 16% по сравнению с плацебо всего через 3 недели терапии. Эти данные подтверждают способность АЛК защищать нервные волокна и даже восстанавливать их функцию.
Украинским врачам и пациентам доступен оригинальный препарат АЛК – Тиоктацид®. Все перечисленные выше клинические исследования по оценке эффективности и безопасности АЛК при полинейропатии были проведены именно с этим препаратом.
Начинать лечение можно как с парентеральной (1 ампула Тиоктацид® 600 Т в сутки в течение 15 дней), так и с пероральной лекарственной формы (3 таблетки Тиоктацид® 600 HR в сутки в течение 15 дней). Первый вариант обеспечивает более быстрый симптоматический эффект, а второй – более удобен в амбулаторных условиях. Далее необходима поддерживающая терапия препаратом Тиоктацид® 600 HR в течение как минимум 1-2 мес, но желательно дольше. Так, в исследованиях SYDNEY‑1 Follow Up и AND было показано, что эффект АЛК в отношении уменьшения неврологического дефицита сохраняется в течении 6 месяцев при условии выполнения стандартной схемы лечения, поэтому длительная пероральная терапия АЛК (непрерывная или курсами) является непременным условием успешного лечения ДН.
Важным преимуществом пероральной формы Тиоктацид® HR (High Release) является высокая биодоступность при пероральном приеме по сравнению с другими препаратами АЛК. По данным S. Bоhm (1999), межиндивидуальная вариабельность концентрации действующего вещества в сыворотке крови при приеме обычной таблетированной формы АЛК у здоровых добровольцев составляет 59%, а у таблеток Тиоктацид® HR – всего 22%, что означает относительное снижение вариабельности на 58%. Стабильная абсорбция препарата Тиоктацид® HR создает достаточный уровень АЛК в плазме крови каждого больного, обеспечивая во всех случаях ожидаемый клинический эффект. В подтверждение этому Podachina и соавт. (2007) продемонстрировали более выраженное действие Тиоктацид® 600 HR на невропатические симптомы, чем взятые для сравнения два других препарата АЛК. В немецком исследовании Fuβ и соавт. (2000) пациенты с симптоматической ДН, не отвечающие на терапию обычными формами АЛК, были переведены на Тиоктацид® HR, результатом чего стало уменьшение выраженности невропатических симптомов и неврологического дефицита. Таким образом, из-за особенностей фармакокинетики этого вещества данные, полученные в исследованиях с препаратом Тиоктацид® HR, некорректно экстраполировать на другие пероральные препараты АЛК.
При обсуждении раннего начала любой терапии, особенно на субклинической стадии, когда пациент еще не предъявляет никаких жалоб, очень актуальным является вопрос безопасности лечения. Если больной с симптомами, нарушающими его качество жизни, еще будет готов мириться с риском побочных эффектов, то у пациента без жалоб, скорее всего, будут очень высокие требования к безопасности и переносимости препарата. В этом отношении АЛК является оптимальным выбором, поскольку, являясь эндогенным биологически активным соединением, она в целом характеризуется высоким профилем безопасности. Тем не менее разные препараты АЛК могут несколько отличаться по этому критерию.
Парентеральная форма Тиоктацид® HR не содержит пропиленгликоль, а АЛК в его составе представлена не этилендиаминовой, а трометамоловой солью. Все это позволило устранить проблемы непереносимости, характерные для препаратов АЛК первого поколения. Частота нежелательных явлений при приеме препарата Тиоктацид® в контролируемых клинических исследованиях соответствовала таковой в группах плацебо.
В завершение следует еще раз напомнить, что чем раньше начать лечение АЛК, тем большего эффекта и лучшего прогноза можно ожидать, поскольку со временем доля необратимых изменений нервных волокон неуклонно увеличивается. Назначая пациентам лечение сегодня, думайте и о будущем.
Список литературы находится в редакции.
Подготовила Наталья Мищенко