18 травня, 2017
Інтенсифікація терапії інсуліном гларгін у пацієнтів з неадекватно контрольованим цукровим діабетом 2 типу покращує глікемічний контроль з високою задоволеністю лікуванням і без збільшення маси тіла
Цукровий діабет (ЦД) є глобальною неінфекційною епідемію. 2010 року у світі нараховувалось близько 285 млн хворих на ЦД 2 типу. За прогнозами, 2030 року цей показник досягне 439 млн за рахунок значного підвищення розповсюдженості серед підлітків і молоді й у деяких регіонах світу [1]. У Швейцарії розповсюдженість ЦД 2 типу становить 5,7-7% від загальної популяції, яка складає приблизно 500 тис. людей [2]. У пацієнтів з ЦД 2 типу гіперглікемія підвищує ризик інфаркту міокарда, інсульту, ампутації нижньої кінцівки і мікроваскулярних ускладнень [2-6]. Американське дослідження, проведене в умовах реальної клінічної практики, показало, що у двох третин пацієнтів концентрація HbA1c перевищує 6,5%, що може викликати значні віддаленні ускладнення і зайві витрати на охорону здоров’я [7].
Пацієнтам, у яких модифікація способу життя і лікування одним або більше пероральним протидіабетичним препаратом не дозволяють досягти цільових значень HbA1c, особливо хворим з високими рівнями глюкози плазми натще, наполегливо рекомендується призначати базальний інсулін [8]. Адекватний глікемічний контроль упродовж тривалого часу необхідний для зниження ризику ускладнень, пов’язаних із діабетом [8, 10]. Нещодавно було опубліковано спільне керівництво з ЦД 2 типу Американської асоціації діабету (ADA) і Європейської асоціації з вивчення діабету (EASD), в якому підкреслюються значення базального інсуліну у веденні захворювання. На основі цього документа Швейцарське товариство ендокринології і діабету (SSED) створило власні рекомендації [12, 13]. У керівництві 2009 року додавання базального інсуліну до пероральних протидіабетичних препаратів рекомендувалось пацієнтам з HbA1c >7% [12], тоді як у новому керівництві 2013 р. рекомендовано використовувати індивідуальні цільові рівні HbA1c у межах 6-8% [13].
У клінічних дослідженнях було продемонстровано, що у пацієнтів з неконтрольованим ЦД 2 типу інсулін гларгін (базальний аналог інсуліну [14]) дозволяє ефективно досягати рівнів HbA1c <7% [8, 15-27]. Оптимізація і довготривалий контроль глікемії за допомогою інсуліну гларгін були підтверджені у великих когортах пацієнтів з ЦД 2 типу [10, 22, 23], і в багатьох дослідженнях були встановлені переваги цього препарату порівняно з іншими інсулінами і пероральними протидіабетичними засобами [8, 15, 17, 19, 20, 24, 25]. Пацієнти, які потребують інсулінотерапії, стикаються з певними труднощами у веденні захворювання. Вони мають постійно вимірювати рівні глюкози плазми і збалансовувати прийом вуглеводів зі щоденними ін’єкціями інсуліну [8].
Низька прихильність до інсулінотерапії є розповсюдженою і важливою причиною недосягнення глікемічних цілей. Використання інсуліну пацієнтами часто обмежується страхом ін’єкцій і гіпоглікемії, а також проблемами, пов’язаними власне з пристроєм для введення інсуліну. Отже, пристрої, легкі у використанні, можуть позитивно впливати на рішення лікаря щодо початку інсулінотерапії і комплаєнс пацієнтів [8]. Зручні і прості у використанні шприц-ручки SoloSTAR® і ClickSTAR® стали значним досягненням у спрощенні самостійного ведення діабету та забезпечили підвищення прихильності до лікування і більш високу задоволеність пацієнтів [8, 26]. Таким чином, призначення інсуліну гларгін за допомогою шприц-ручок SoloSTAR® і ClickSTAR® дозволяє оптимізувати терапію діабету [27]. Крім того, навчання самостійному веденню діабету є важливим аспектом сучасного персоналізованого підходу до лікування. Останній передбачає врахування потреб і можливостей пацієнтів з метою покращення їх знань і навичок щодо схем лікування і модифікації способу життя [8, 28, 29]. Мета цього дослідження – оцінити ефективність 6-місячного курсу лікування інсуліном гларгін стосовно досягнення глікемічного контролю (HbA1c і глюкоза плазми натще) і зміни маси тіла, а також визначити вподобання щодо пристрою введення інсуліну і задоволеність лікуванням у пацієнтів з ЦД 2 типу, які знаходились під наглядом лікарів первинної ланки в різних регіонах Швейцарії.
Методи
У проспективному спостережному дослідженні, що проводилось у період з листопада 2009 по вересень 2011 року, взяли участь 72 лікаря первинної ланки. Щодо пацієнтів, критеріями включення були погано контрольований ЦД 2 типу, незважаючи на попередню терапію пероральними протидіабетичними препаратами або інсуліном; вік ≥18 років й інформована згода пацієнта. Критерії виключення були відсутніми. Лікування інсуліном гларгін (Лантус®, Sanofi) у пристроях для підшкірного введення (SoloSTAR® і CliсkSTAR®, Sanofi) призначалось як частина рутинної медичної допомоги і відповідно до інструкції препарату [30]. Лікарі забезпечували належне навчання пацієнтів щодо призначення інсуліну гларгін, використання шприц-ручок і супутньої модифікації способу життя з метою полегшення самостійного ведення діабету і вибору пристрою – одноразового (SoloSTAR®) або багаторазового (ClickSTAR®). За виключенням першого візиту і візиту після 6 міс лікування інсуліном гларгін, систематичний моніторинг пацієнтів не проводився. Протокол дослідження був схвалений незалежним етичним комітетом.
На першому (вихідному) візиті визначали демографічні характеристики пацієнтів, артеріальний тик, ліпідний профіль, медичний анамнез, ускладнення діабету і супутні захворювання, попереднє лікування і рекомендовану дозу інсуліну гларгін. На заключному візиті (після 6 міс лікування) визначали початкову дозу, схему титрації і фінальну дозу інсуліну гларгін.
Параметри ефективності (HbA1c і глюкозу плазми натще) оцінювали на вихідному і заключному візитах. Про випадки небажаних подій повідомляли безпосередньо в центри Федеральної служби з фармаконагляду Швейцарії (Swissmedic) відповідно до національного законодавства. Задоволеність лікуванням оцінювали за допомогою 4-бальної шкали Лікерта («дуже незадоволений», «незадоволений», «задоволений», «дуже задоволений») шляхом опитування пацієнтів і лікарів. Результати вносились в індивідуальні реєстраційні карти лікарями, які брали участь у дослідженні.
Результати
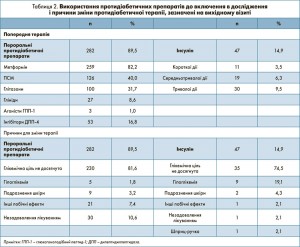
Із 327 пацієнтів, включених у дослідження, 12 (3,7%) не з’явились на заключний візит і були виключенні з аналізу. 9 (2,8%) із 315 пацієнтів завершили лікування передчасно, і 6 пацієнтів мали вихідний рівень HbA1c <7,0%, що не відповідало протоколу. Отже, в заключний аналіз увійшли 300 пацієнтів, які представляли всі основні області і мовні регіони Швейцарії. Вихідні клініко-демографічні параметри наведені в таблиці 1. У таблиці 2 представлені попереднє протидіабетичне лікування і причини його зміни.
Титрація інсуліну гларгін і терапевтичне навчання пацієнтів
Стартова доза інсуліну гларгін становила 10 од. (61,9%) або 0,2 од./кг (26,7%) відповідно до протоколу; у 11,4% пацієнтів (як правило, у тих, які раніше отримували інсулінотерапію) вона була вищою (16,5±8,6 од.). Титрація дози інсуліну гларгін здійснювалась лікарями (71,1%) або пацієнтами (28,9%) 1 раз на тиждень (73,0%) або на 2 од. кожні 3 дні (18,4%).
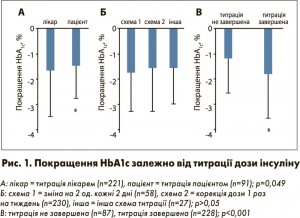
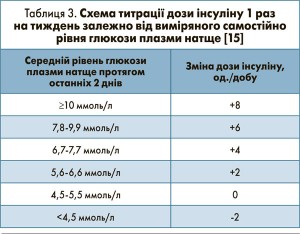
На заключному візиті (після 6 міс лікування) титрація була завершена у 72,4% хворих; ці пацієнти мали нижчі рівні HbA1c порівняно з пацієнтами, які не завершили титрацію. Схему титрації обирав лікар: 1 раз тиждень на підставі значень глюкози плазми натще за останні 2 дні або підвищення на 2 од. кожні 3 дні у разі неконтрольованих рівнів глюкози (табл. 3). Схема титрації не корелювала з рівнями HbA1c, проте титрація лікарем асоціювалась із дещо більш вираженим покращенням HbA1c порівняно з титрацією пацієнтом (рис. 1). Середня добова доза інсуліну гларгін становила 27,7±14,3 од., середня тривалість лікування – 178±56 днів. Шприц-ручки ClickSTAR® і SoloSTAR® використовували 20 і 80% пацієнтів відповідно. Кількість пацієнтів, які отримували пероральні протидіабетичні препарати, залишався стабільним упродовж дослідження.
На вихідному візиті навчання самостійному веденню діабету було проведено у 303 (96,2%) пацієнтів, переважно лікарями (95,4%), експертами з діабету (37,3%), дієтологами (28,1%) і психотерапевтами (1,0%). Аналогічний характер навчальної підтримки зберігався і на заключному візиті.
Ефективність
В ITT-популяції (n=315; пацієнти, які отримали принаймні 1 дозу досліджуваного препарату) середній рівень HbA1c знизився з 8,9±1,6% (вихідний візит) до 7,3±1,0% (заключний візит), що відповідає статистично значимій різниці у – 1,6±1,7% (p<0,0001). Середній рівень глюкози плазми натще знизився з 10,8±4,4 до 7,3±1,8 ммоль/л з достовірною різницею у – 3,6±4,5 ммоль/л (p<0,0001). Кількість пацієнтів з рівнем HbA1c ≤7,0% підвищилась з 4,8 до 43,8% (p<0,0001), кількість пацієнтів з глюкозою плазми натще ≤7,0 ммоль/л – з 9,6 до 50,3% (p<0,0001). Середня маса тіла залишалась стабільною протягом періоду дослідження (85,4±17,2 кг на вихідному візиті vs 85,0±16,5 кг на заключному візиті; p=0,11).
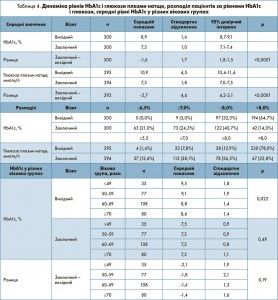
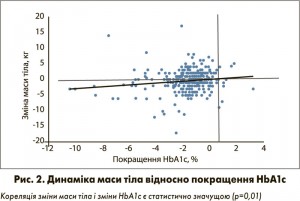
У РР-популяції (n=300; пацієнти, які завершили лікування згідно з протоколом) середній рівень HbA1c знизився з 8,9±1,6% до 7,3±1,0% зі статистично значимою різницею у – 1,6±1,7% (p<0,0001) (табл. 4). На вихідному візиті середній рівень HbA1c достовірно корелював (р=0,022) з віковою групою і був найвищим у пацієнтів у віці ≤49 років (9,5±1,8%) і найнижчим у пацієнтів у віці ≥70 років (8,6±1,4%). Проте тенденція (р=0,19) до більш вираженої різниці між вихідним і заключним рівнем HbA1c у наймолодших пацієнтів порівняно з найстарішими обумовила подібний HbA1c на заключному візиті. Середній рівень глюкози плазми натще знизився з 10,9±4,5 до 7,3±1,8 ммоль/л з достовірною різницею у – 3,6±4,6 ммоль/л (p<0,0001). Кількість пацієнтів з рівнем HbA1c ≤7,0% підвищилась з 3,0 до 45,3% (p<0,0001), кількість пацієнтів з глюкозою плазми натще ≤7,0 ммоль/л – з 9,2 до 50,7% (p<0,0001). Середня маса тіла залишалась стабільною протягом періоду дослідження (85,4±17,2 кг на вихідному візиті vs 85,0±16,5 кг на заключному візиті; p=0,11) (рис. 2).
Переносимість
На початку дослідження лікарі були поінформовані щодо їх обов’язку надсилати звіти про побічні ефекти безпосередньо у центри фармаконагляду Swissmedic із використанням індивідуальних реєстраційних карт. Гіпоглікемія була відмічена лише в 1 одного пацієнта (0,3%); про інші побічні реакції не повідомлялось.
Задоволеність лікуванням
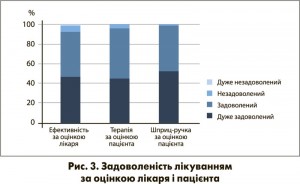
У цілому 92,7% лікарів і 96,3% пацієнтів були задоволені або дуже задоволені терапією інсуліном гларгін (рис. 3). Майже всі пацієнти (99,0%) були задоволені або дуже задоволені користуванням шприц-ручками SoloSTAR® і ClickSTAR®. Більшість пацієнтів (80%) надали перевагу одноразовій шприц-ручці SoloSTAR® порівняно з багаторазовим пристроєм ClickSTAR® (20%).
Обговорення
У цьому проспективному спостережному дослідженні, проведеному в умовах первинної медичної ланки за участі пацієнтів с раніше неконтрольованим ЦД 2 типу, 6-місячний курс інсуліну гларгін, що призначався за допомогою шприц-ручок SoloSTAR® або ClickSTAR®, та навчання ін’єкціям інсуліну і самостійному веденню діабету асоціювались з клінічно значимим покращенням глікемічного контролю (рівнів HbA1c і глюкози плазми натще) без збільшення маси тіла в усій когорті. Переважна більшість пацієнтів і лікарів були задоволені лікуванням.
Порівняння з результатами рандомізованих досліджень
Результати проведеного дослідження отримані в умовах реальної клінічної практики і представляють персоналізований підхід, що передбачає лікування інсуліном гларгін у шприц-ручках SoloSTAR® або ClickSTAR® і навчання пацієнтів самостійному веденню діабету. Початок терапії інсуліном гларгін і титрацію дозу здійснювали у 73% пацієнтів відповідно до схеми Riddle і співавт. [15] і 18% пацієнтів згідно рекомендацій ADA/EASD [11]. Цікаво, що самостійна титрацію дози в цьому дослідженні відбувалась частіше, ніж у попередньому дослідженні [22], проведеному у 2005-2007 роках у Швейцарії (29 vs 17%).
Це є відображенням сучасної тенденції до навчання пацієнтів і їх більшого залучення у терапевтичний процес. Проте наші результати свідчать про те, що титрація лікарем забезпечила дещо більш виражене покращення HbA1c на противагу до вибору схеми титрації, який не впливав на цей показник. Титрація була завершена після 6 міс у 72% пацієнтів із середньою добовою дозою інсуліну гларгін 27,7±14,3 од., або 0,32±0,17 од./кг. Ця доза знаходиться у нижньому діапазоні заміщення інсуліну в пацієнтів з початковою інтенсифікацією лікування. Пацієнти, які завершили титрацію, мали значно нижчий рівень HbA1c.
У відповідності результатів великих клінічних досліджень [15, 17, 20, 21], лікування інсуліном гларгін протягом 24 тиж забезпечило клінічно значиме зниження рівнім HbA1с і глюкози плазми натще. Значне покращення глікемічного контролю не супроводжувалось підвищенням маси тіла; це свідчить на користь того, що інсулінотерапія не обов’язково призводить до збільшення ваги, особливо якщо використовуються не надто високі дози інсуліну.
Керівництво SSED2009 року [12], яке було актуальним на момент початку дослідження, рекомендувало цільовий рівень HbA1c ≤7,0%, тоді як сучасне керівництво [13] рекомендує індивідуальний цільовий рівень у межах 6-8% (втім HbA1c ≤7,0% все ще залишається бажаним для більшості пацієнтів). У нашому дослідженні 45% пацієнтів досягли рівня HbA1c ≤7,0%. Середні значення HbA1c після 6 міс лікування інсуліном гларгін становили 7,3±1,0% і були подібними в усіх вікових групах. Аналогічну частоту відповіді спостерігали й у попередніх дослідженнях [20, 21].
Нещодавні дослідження (ACCORD, ADVANCE і VADT) [32-34] стали підставою для нової спільної рекомендації ADA/EASD [8] щодо використання індивідуальних цільових рівнів HbAc1 >7% у пацієнтів з передіснуючими кардіоваскулярними ускладненнями, великою тривалістю діабету й епізодами гіпоглікемії в анамнезі. Під час проведення нашого дослідження ця рекомендація ще не була опублікована. На сьогодні ідеальним діапазоном HbA1c є 6-7,5% з урахуванням найнижчої части мікро- і макроваскулярних ускладнень за рівнів HbA1c 6,5 і 7% відповідно. Лише у пацієнтів з короткою тривалістю діабету, які не мають кардіоваскулярних ускладнень і частих епізодів гіпоглікемії, рекомендованим рівнем HbA1c залишається рівень <7,0%. Агресивне лікування з цільовим рівнем HbA1c ≤6,5% підвищує рівень смертності, ймовірно за рахунок гіпоглікемії.
У нашому дослідженні середня тривалість діабету становила 6,2 року і значна кількість пацієнтів уже мала кардіоваскулярні захворювання на момент включення, що свідчить про високий ризик кардіоваскулярних подій. Ми не аналізували індивідуальні цільові рівні HbA1c, проте очевидно, що багато лікарів обирали менш суворі цілі у пацієнтів з більшою тривалістю захворювання навіть до публікації нових рекомендацій. В іншому випадку відсоток пацієнтів із завершеною титрацією був би вищим за 72%
Задоволеність лікуванням
Як і в попередньому дослідженні [22], переважна більшість лікарів і пацієнтів були задоволені або дуже задоволені терапією інсуліном гларгін. Цікаво, що 80% пацієнтів надали перевагу одноразовій шприц-ручці для стартової інсулінотерапії. Крім того, 99% пацієнтів були задоволені або дуже задоволені користуванням шприц-ручками SoloSTAR® і ClickSTAR®. Уподобання одноразової шприц-ручки і високий рівень задоволеності підкреслюють простоту навчання і користування цими пристроями, а також їх схвалення пацієнтами.
Висновки
У пацієнтів з ЦД 2 типу, неадекватно контрольованим попередньою терапією, 6-місячне лікування інсуліном гларгін (Лантус®) у шприц-ручках SoloSTAR® або ClickSTAR® у поєднанні з навчанням щодо ін’єкцій інсуліну за допомогою цих пристроїв і самостійного ведення діабету забезпечило клінічно значиме покращення HbA1c і глюкози плазми натще без збільшення маси тіла. В умовах первинної ланки медичної допомоги інсулін гларгін дозволяє ефективно контролювати глікемію за стабільної маси тіла, що сприяє високій задоволеності пацієнтів і лікарів.
Література
1. Magliano D.J., Zimmet P.Z. The worldwide epidemiology of type 2 diabetes mellitus, present and future perspectives. Nat Rev Endocrinol. 2011; 8(4): 228-36.
2. Kaiser A., Vollenweider P., Waeber G., Marques-Vidal P. Prevalence, awareness and treatment of type 2 diabetes mellitus in Switzerland: the CoLaus study. Diabet Med. 202; 29: 190-7.
3. Stratton I.M., Adler A.I., Neil H.A.W. et al. Association of glycaemia with macro- vascular and microvascular complications of type 2 diabetes (UKPDS35): prospective observational study. BMJ. 2000; 321: 405-12.
4. Saydah S., Tao M., Imperatore G., Gregg E. GHb level and subsequent mortality among adults in the U.S. Diabetes Care. 2009; 32: 1440-6.
5. Sarwar N., Gao P., Seshasai S.R. et al. Emerging Risk Factors Collaboration. Diabetes mellitus, fasting blood glucose concentration, and risk of vascular disease: a collaborative meta-analysis of 102 prospective studies. Lancet. 2010; 375: 2215-22.
6. Gerstein H.C., Islam S., Anand S. et al. Dysglycaemia and the risk of acute myocardial infarction in multiple ethnic groups: an analysis of 15,780 patients from the INTERHEART study. Diabetologia. 2010; 53: 2509-17.
7. Blonde L. State of diabetes health. 2006 Available from www.stateofdiabetes.com/state_compare.htm.
8. Inzucchi S.E., Bergenstal R.M., Buse J.B. et al.; American Diabetes Association (ADA); European Association for the Study of Diabetes (EASD). Management of hyperglycemia in type 2 diabetes: a patient-centered approach: position statement of the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2012; 35(6): 1364-79 / Diabetologia. 2012; 55(6): 1577-96.
9. Aschner P., Chan J., Owens D.R. et al., on behalf of the EASIE investigators. Insulin glargine versus sitagliptin in insulin-naive patients with type 2 diabetes mellitus uncontrolled on metformin (EASIE): a multicentre, randomised open-label trial. Lancet. 2012; 379: 2262-6229.
10. Riddle C. (on behalf of the ORIGIN trial investigators). Characteristics Associated With Maintenance of Mean A1C <6.5% in People with Dysglycemia in the ORIGIN Trial. Diabetes Care. 2013; 36(10): 2915-22.
11. Nathan D.M., Buse J.B., Davidson M.B. et al. Medical management of hyperglycaemia in type 2 diabetes mellitus: a consensus algorithm for the initiation and adjustment of therapy: a consensus statement from the American Diabetes Association and the European Association for the Study of Diabetes. American Diabetes Association, European Association for the Study of Diabetes. Diabetologia. 2009; 52(1): 17-30.
12. Philippe J., Brndle M., Carrel J. et al. Massnahmen zur Blutzuckerkontrolle bei Patienten mit Typ‑2-Diabetes-Mellitus: Consensus Statement der Schweizerischen Gesellschaft fr Endokrinologie und Diabetes (SGED): Schweiz Med Forum. 2009; 9(3): 50-5.
13. Lehmann R., Henzen Ch., Christ E. Neue Richtlinien der SGED/SSED zur Therapie des Typ 2 Diabetes mellitus. info@herz+gefss 2013; 4: 20-4.
14. Wang F., Vergara C.M. Insulin glargine: a systematic review of a long-acting insulin analogue. Clin Ther. 2003; 25: 1541-77.
15. Riddle M.C., Rosenstock J., Gerich J. The Treat-to-Target Trial: Randomised addition of Glargine or human NHP insulin to oral therapy of type 2 diabetic patients Diabetes Care. 2003; 26(11): 3080-6.
16. Yki-Jarvinen H., Yki-Jrvinen H., Juurinen L. et al. Initiate Insulin by Aggressive Titration and Education (Initiate a Randomized Study to Compare Initiation of Insulin Combination Therapy in Type 2 Diabetic Patients Individually And in Groups. Diabetes Care. 2007; 30: 1364-70.
17. Bretzel R.G., Nuber U., Landgraf W. et al. Once-daily basal insulin glargine versus thrice-daily prandial insulin lispro in people with type 2 diabetes on oral hypoglycaemic agents (APOLLO): an open randomised controlled trial. Lancet. 2008; 371: 1073-84.
18. Fritsche A. Langwirkende Analoginsuline: Ergebnisse mit Insulin glargine: Dtsch Med Wochenschr. 2008; 133: S101-S105.
19. Davies M., Lavalle-Gonzalez F., Storms F., Gomis R. (on behalf of the AT.LANTUS Study Group). Initiation of insulin glargine therapy in type 2 diabetes subjects suboptimally controlled on oral anti-diabetic agents: results from the AT.LANTUS trial. Diabetes, Obesity and Metabolism. 2008; 10: 387-99.
20. Rosenstock M., Davies P., Home D. et al. A randomised, 52-week, treat-to-target trial comparing insulin detemir with insulin glargine when administered as add-on to glucose-lowering drugs in insulin-naive people with type 2 Diabetes. Diabetologia. 2008; 51: 408-16.
21. Fonseca V., J. Gill J., Zhou R., Leahy J. An analysis of early insulin glargine added to metformin with or without sulfonylurea: impact on glycaemic control and hypoglycaemia. Diabetes Obes Metab. 2011; 13: 814-22.
22. Spirk D., Lareida J., Scheidegger K., Diem P. Optimierung der glykmischen Kontrolle und Dosistitration mit Insulin Glargine (Lantus®) durch frei praktizierende rzte in der Schweiz: Resultate des OPTI-LAN Praxiserfahrungsberichtes. Praxis. 2009; 98: 315-20.
23. Gerber P., Spirk D., Braendle M. et al. Regional differences of glycaemic control in patients with type 2 diabetes mellitus in Switzerland. Swiss Med Wkly. 2011, doi: 10.4414/smw.2011.13218
24. Home P.D., Fritsche A., Schinzel S., Massi-Benedetti M. Meta-analysis of individual patient data to assess the risk of hypoglycaemia in people with type 2 diabetes using NPH insulin or insulin glargine. Diabetes Obes Metab. 2010; 12: 772-9.
25. Polonsky W., Traylor L., Wei W. et al. More satisfied, but why? A pooled patient-level analysis of treatment satisfaction following the initiation of insulin glargine versus comparators in insulin-nave patients with type 2 diabetes mellitus. Diabetes Obes Metab. 2013; doi: 10.1111/dom.12214.
26. Hancu N., Czupryniak L., Genestin E., Sourij H. A Pan-European and Canadian prospective survey to evaluate patient satisfaction with the SoloSTAR insulin injection device in type 1 and type 2 diabetes. J Diabetes Sci Technol. 2011; 5: 1224-34.
27. Bhler S., Landgraf W., Schreiber S.A. Bewertung des neuen Insulin-Fertigpens und Injektionsgewohnheiten von Diabetikern in der tglichen Praxis. MMW-Fortschritte der Medizin Originalen 2009; IV: 179-87.
28. Lagger G., Zoltan P., Golay A. Efficacy of therapeutic patient education in chronic disease and obesity. Patient Educ Couns. 2010; 79: 283-6.
29. Golay A., Lagger G., Chambouleyron., Carrard I., Lasserre-Moutet A. Therapeutic education of diabetic patients. Diabetes Metab Res Rev. 2008; 24: 192-6.
30. www.swissmedicinfo.ch. Fachinformation fr Lantus®ClikSTAR und Lantus® SoloSTAR®. Sanofi-Aventis (Schweiz) AG.
31. American Diabetes Association. Standards of medical care in diabetes – 2012. Diabetes Care. 2012; 35(Suppl 1): S11-63.
32. Effects of Intensive Glucose Lowering in Type 2 Diabetes The Action to Control Cardiovascular Risk in Diabetes Study Group. N Engl J Med. 2008; 358: 2545-59.
33. Intensive Blood Glucose Control and Vascular Outcomes in Patients with Type 2 Diabetes. The ADVANCE Collaborative Group. N Engl J Med. 2008; 358: 2560-72.
34. Duckworth W., Abraira C., Moritz T. et al.; VADT Investigators. N Engl J Med. 2009; 360(2): 129-39. Original article Swiss Med Wkly. 2015; 145: w14114 Swiss Medical.
Стаття друкується у скороченні.
Riebenfeld D., Spirk D., Mathis A. et al. Treatment intensification with insulin glargine in patients with inadequately controlled type 2 diabetes improves glycaemic control with a high treatment satisfaction and no weight gain. Swiss Med Wkly. 2015 Mar 5;145: w14114.
Переклав з англ. Олексій Терещенко