25 липня, 2017
Секнидокс в амбулаторной практике лечения урогенитальных инфекций
В микробиоме влагалища женщины репродуктивного возраста выявлено 282 филотипа микроорганизмов (J. Ravel et al., 2011). Филотипы индигенной флоры (постоянно присутствующей в организме человека) неидентичны у разных индивидуумов и представителей различных этнических групп. Микробиота влагалища сохраняет стабильность в условиях разнородных химических и корпускулярных потоков, пронизывающих муцин вдоль и поперек (при половой жизни, использовании интравагинальных средств, беременности и т.д.). Такая организация обеспечивает ее физиологическую и функциональную стабильность, колонизационную резистентность и, следовательно, является залогом конкурентного выживания в экологической нише.
Количественный состав микроорганизмов в микробиоценозе влагалища в норме динамично изменяется в течение менструального цикла (S. Srinivasan et al., 2010).
Избыточное размножение облигатных вагинальных анаэробов ассоциировано с бактериальным вагинозом (БВ).
БВ (по определению CDC, 2015) – это полимикробный клинический синдром, который развивается в результате замены нормальных, продуцирующих перекись водорода, Lactobacillus spр. во влагалище на анаэробные бактерии, например, Prevotella spp. и Mobiluncus spp., G. vaginalis, Ureaplasma, Mycoplasma и многочисленные труднокультивируемые или некультивируемые анаэробы. Наиболее распространенным маркерным микроорганизмом БВ является G. vaginalis. Это не только самый распространенный, но и самый патогенный из всех ассоциированных с БВ микроорганизмов ввиду возможности образования биопленок, способности к адгезии, продукции цитотоксинов (в том числе вагинолизина), угнетающих лейкоциты. Развитие БВ не сопровождается увеличением количества лейкоцитов во влагалищной среде.
Начиная с 1960-х гг. и по сегодняшний день для лечения анаэробной инфекции наиболее часто применяют препараты группы 5-нитроимидазолов – синтетических низкомолекулярных соединений, содержащих нитрогруппу (NO2) в положении 5-го имидазольного цикла.
Имидазолы проявляют активность в отношении Bacteroides fragilis, Prevotella melaninogenica, Fusobacterium spp., Pеptococcus spp., Peptostreptococcus spp., Clostridium spp., Clostridium difficile, Eubacterium spp., G. vaginalis, Helicobacter pylori. Кроме того, имидазолы оказывают действие на простейших (Trichomonas vaginalis, Entamoeba hystolitica, Lamblia, Leishmania). Действующее вещество имидазолов достигает очага возбудителя, не вредит палочке Додерлейна и неактивно по отношению к Candida albicans.
Подробное изучение биологических и антимикробных свойств 5-нитроимидазолов установило их высокую активность в отношении облигатных анаэробов.
Наибольшее значение имеет их активность в отношении бактероидов, в первую очередь, в отношении Bacteroides fragilis, и различных представителей Clostridium spp.
Вместе с тем высокая биодоступность и оптимальное распределение в организме позволяют успешно применять 5-нитроимидазолы перорально с целью системного действия.
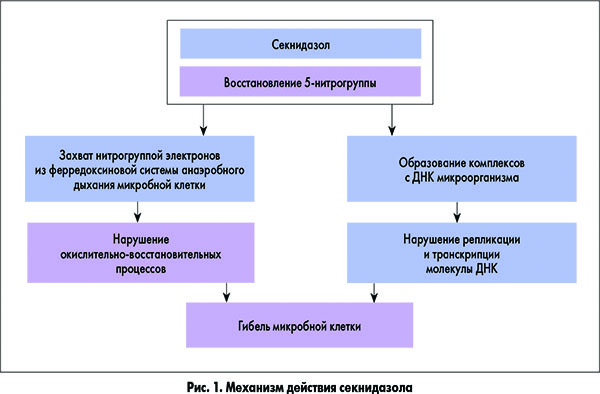 Нитроимидазолы проявляют свое действие только после трансформации в клетках бактерий или простейших. Нитроредуктазы катализируют процесс взаимодействия в микробной клетке белков группы ферридоксинов с нитросоединениями. В результате действия нитроредуктаз в клетке образуются активные метаболиты 5-нитроимидазолов, которые оказывают бактерицидное действие и влияют на цистные формы микроорганизмов. Мишенью этих метаболитов являются ДНК и РНК клеток и клеточные белки. Активные восстановленные формы препаратов нарушают репликацию ДНК и синтез белка в микробной клетке. Этот процесс одновременно сопровождается образованием свободных радикалов, которые также оказывают повреждающее действие на ДНК. Аналогичное действие оказывает и препарат последнего поколения 5-нитроимидазолов – секнидазол (рис. 1).
Нитроимидазолы проявляют свое действие только после трансформации в клетках бактерий или простейших. Нитроредуктазы катализируют процесс взаимодействия в микробной клетке белков группы ферридоксинов с нитросоединениями. В результате действия нитроредуктаз в клетке образуются активные метаболиты 5-нитроимидазолов, которые оказывают бактерицидное действие и влияют на цистные формы микроорганизмов. Мишенью этих метаболитов являются ДНК и РНК клеток и клеточные белки. Активные восстановленные формы препаратов нарушают репликацию ДНК и синтез белка в микробной клетке. Этот процесс одновременно сопровождается образованием свободных радикалов, которые также оказывают повреждающее действие на ДНК. Аналогичное действие оказывает и препарат последнего поколения 5-нитроимидазолов – секнидазол (рис. 1).
Компания World Medicine (Великобритания) представила на рынок Украины препарат секнидазола – Секнидокс, который отличается от других 5-нитроимидазолов тем, что: Секнидокс – противопротозойный препарат с антибактериальным и бактерицидным действием; одна таблетка препарата содержит 1 г секнидазола; таблетки покрыты оболочкой. Секнидазол – первый из нитроимидазолов, обеспечивающий 3-дневную активность после однократного приема.
 Обладая более длительным периодом полураспада, Секнидокс демонстрирует клиническую эффективность и повышает приверженность пациента к терапии ввиду короткого курса лечения.
Обладая более длительным периодом полураспада, Секнидокс демонстрирует клиническую эффективность и повышает приверженность пациента к терапии ввиду короткого курса лечения.
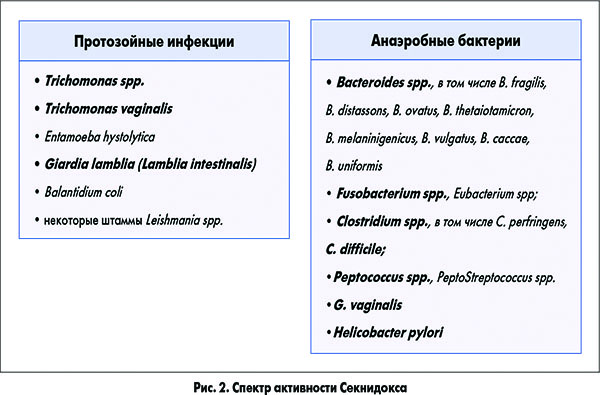
Секнидокс проявляет активность в отношении анаэробных бактерий и простейших (рис. 2).
Секнидокс быстро всасывается после перорального приема. Его биодоступность составляет 80%. Метаболизируется препарат в печени. Максимальный уровень в плазме достигается после 3 ч (t max) после перорального приема 2 г препарата Секнидокс.
Период полувыведения из плазмы составляет 20-25 ч. Большая часть препарата выводится с мочой (50% примененной дозы выводится в течение 120 ч). Выделяется с грудным молоком, проникает через плацентарный барьер.
Фармакокинетика Секнидокса демонстрирует самый длительный период полураспада из всех 5-нитроимидазолов, обеспечивая 72-часовую терапевтическую концентрацию в крови после однократного приема 2 г препарата.
Благодаря ограниченному и однократному приему не развивается резистентность к препарату Секнидокс по сравнению с избыточным приемом других 5-нитроимидазолов.
Не рекомендуется одновременный прием секнидазола с дисульфирамом в связи с риском развития состояний потери ориентации и параноидальных реакций. Применение секнидазола вместе с варфарином требует тщательного наблюдения, так как он усиливает действие оральных антикоагулянтов и может спровоцировать кровотечение.
! Эффективность секнидазола в дозе 2 г однократно равна эффективности метронидазола при режиме дозирования 500 мг в течение 7 дней.
J.M. Bohbot и соавт. (2010) провели двойное слепое плацебо-контролируемое исследование, в котором сравнили эффективность секнидазола (2 г, однократно) с эффективностью метронидазола (500 мг 2 р/день, курс – 7 дней). В общей сложности были рандомизированы 577 пациенток. Результаты продемонстрировали, что однократная доза секнидазола по меньшей мере столь же эффективна, как и прием нескольких доз метронидазола (60,1 vs 59,5%). Профили безопасности были сопоставимы в обеих группах. Авторы сделали вывод о том, что применение секнидазола в дозе 2 г однократно является эффективной и удобной терапевтической альтернативой, которую клиницисты должны учитывать в обычной практике.
! Высокая комплаентность однократного приема наряду с хорошей переносимостью и эффективностью делает секнидазол препаратом выбора в классе нитроимидазолов для терапии БВ и инфекций, вызванных простейшими.
J.C. Gillisand и L.R. Wiseman (1996) провели обзор литературы по антимикробной активности, фармакокинетическим свойствам и терапевтическому использованию секнидазола при лечении протозойных инфекций и БВ. Авторы отмечают, что после введения единственной дозы секнидазола эрадикация возбудителя была достигнута у 92-100% пациентов с урогенитальным трихомониазом. Пациенты с БВ реагируют на однодозовый прием секнидазола тинидазола или 7-дневный курс терапии метронидазолом. Клиническое улучшение и/или микробиологическое излечение было достигнуто у 59-96% пациентов. В рассмотренных клинических исследованиях указывается хорошая переносимость секнидазола. Большинство побочных эффектов отмечались со стороны желудочно-кишечного тракта и не требовали вмешательства в лечение или отмены терапии. Таким образом, имеющиеся данные свидетельствуют о том, что секнидазол столь же эффективен, как и другие препараты 5-нитроимидазола, при лечении БВ и протозойных инфекций. Удобство и простота применения, связанные с однодозовой терапией, в сочетании с хорошим профилем переносимости делают секнидазол оптимальной альтернативой схемам терапии другими препаратами этого класса с множественным дозированием.
! Даже однодозовый прием секнидазола (1 г) характеризуется высокими показателями эффективности при лечении БВ, вызванного G. vaginalis.
С целью определить, можно ли вылечить БВ с помощью однократной пероральной дозы секнидазола 1 г, J.T. Nuez и G. Gomez (2005) провели исследование с участием 80 женщин в амбулаторной гинекологической клинике больницы Мануэля Норьеги, г. Маракайбо, Венесуэла. Диагноз был основан на критериях Амселя. Участницы были рандомизированы в 2 группы. Пациентки 1-й группы (n=44) получили пероральную дозу секнидазола 1 г однократно, второй группы (n=32) – пероральную дозу секнидазола 2 г однократно. Клиническое излечение определяли как отсутствие характерных клинических симптомов (неприятный запах и обильные влагалищные выделения) и по меньшей мере двух из следующих: вагинальный рН <4,5, отсутствие запаха рыбы при добавлении KOH и отсутствие G. vaginalis или ключевых клеток при экспертизе влажных биоптатов.
Клиническое излечение наблюдалось у 95,5% женщин, получивших пероральную дозу секнидазола 1 г, и у 97,4% женщин, получивших пероральную дозу 2 г. Не установлено существенной разницы между группами в клиническом разрешении БВ. После лечения результат бактериоскопии у 94,7% женщин показал отсутствие G. vaginalis. В 1-й группе 41 женщина (93,2%), а во 2-й группе 31 женщина (96,9%), по данным микроскопии влагалищных мазков, имели подтвержденную бактериологическую эффективность препарата. Мазок по Папаниколау выявил G. vaginalis у 3 женщин в 1-й группе и у 1 женщины во 2-й группе (р=0,47). 27 женщин (35,5%) сообщили о слабых побочных эффектах. Большее количество побочных эффектов зарегистрировано у пациенток 1-й группы (n=16), чем 2-й (n=11), но эта разница не была статистически значимой. Таким образом, результаты проведенного клинического исследования показали, что однократная пероральная доза секнидазола 1 г эффективна для лечения БВ, ассоциированного с G. vaginalis.
В США M.A.B. Petrina и соавт. (2017) провели исследование восприимчивости вагиноз-ассоциированных бактерий к секнидазолу по сравнению с метронидазолом, тинидазолом и клиндамицином. В общей сложности 605 уникальных бактерий, ассоциированных с БВ, и 108 изолятов лактобацилл, выделенных из влагалища, у женщин в течение 2009-2015 гг., были протестированы на антимикробную восприимчивость для определения минимальной ингибирующей концентрации (МИК). MИК90 (мкг/мл) для секнидазола была схожа с таковой для метронидазола и тинидазола в случае дифференцирования Anaerococcus tetradius (секнидазол: MИК90 2; метронидазол: MИК90 2; тинидазол: MИК90 4), Atopobium vaginae (32; >128; 128), видов Bacteroides (2; 2; 2), Finegoldia magna (2; 2; 4), G. vaginalis (128; 64; 32), Mageeibacillus indolicus (2; 2; 2), Megasphaera-подобных бактерий (0,5; 0,25; 0,5), Mobiluncus curtisii (128; >128; >128) и Mobiluncus mulieris (>128; >128; >128), Peptoniphilus lacrimalis (4; 4; 4) и Peptoniphilus harei (2; 2; 4), виды Porphyromonas (0,25; 0,5; 0,25), Prevotella bivia (8; 8; 8), Prevotella amnii (2; 1; 2) и Prevotella timonensis (2; 2; 2). В этой оценке 14 (40%) из 35 P. bivia, 5 (14%) из 35 P. amnii и 21 (58%) из 36 штаммов P. timonensis были устойчивы к клиндамицину с величинами MИК >128 мкг/мл. Активность секнидазола, как и метронидазола, превосходила таковую клиндамицина в отношении Prevotella spp., Bacteroides spp., Peptoniphilus spp., Anaerococcus tetradius и Finegoldia magna. Клиндамицин имел большую активность против Atopobium vaginae, G. vaginalis и Mobiluncus spp. по сравнению с нитроимидазолами. Все 27 Lactobacillus crispatus, 26 (96%) из 27 L. jensenii, 5 (19%) из 27 L. gasseri и 18 (67%) изолятов 27 L. iners были восприимчивы к клиндамицину (MИК ≤2), тогда как величины MИК90 для всех тестируемых лактобацилл составляли >128 мкг/мл для секнидазола, метронидазола и тинидазола.
Авторы пришли к выводу о том, что секнидазол обладает аналогичной активностью in vitro против ряда микроорганизмов, ассоциированных с БВ, по сравнению с метронидазолом или тинидазолом. Кроме того, секнидазол сохраняет лактобациллы, что характерно для препаратов, используемых в лечении БВ. При неосложненных формах воспалительных заболеваний органов малого таза (ВЗОМТ), вызванных смешанной аэробно-анаэробной инфекцией в сочетании с Mycoplasma hominis, Ureaplasma (urealyticum + parvum), Chlamidia trachomatis, Trichomonas vaginalis, эффективно применение комбинации препаратов левофлоксацина и секнидазола.
Нами проведено изучение клинической эффективности и переносимости перорального приема комбинации препаратов Левоксимед и Секнидокс при неосложненных формах ВЗОМТ (Е.Н. Носенко, 2016). В исследование были включены 30 пациенток репродуктивного возраста с неосложненными формами ВЗОМТ. Терапию ВЗОМТ проводили препаратами Левоксимед в форме таблеток в дозе 500 мг (1 таблетка) в сутки в течение 14 дней и Секнидокс – в однократной дозе 2 г (2 таблетки). Оценивали клинические показатели, эрадикацию возбудителей, переносимость препаратов и их безопасность. Проведенное лечение привело к элиминации болевого синдрома у 96,67% пациенток; дизурических явлений – у 46,67%; патологических выделений из половых путей – у 86,67%; субфебрильной температуры – у 36,67%. После проведенного лечения была отмечена полная эрадикация облигатных патогенов и элиминация условно-патогенных микроорганизмов в диагностически значимых количествах.
Переносимость комбинации препаратов Левоксимед и Секнидокс была признана отличной у 76,67%, хорошей – у 16,67%, удовлетворительной – у 6,67% пациенток. Таким образом, исходя из результатов проведенного исследования, был сделан вывод о высокой клинической эффективности, широком спектре антимикробной активности препаратов, проявляющих синергизм действия, отличной переносимости и безопасности, что позволяет рекомендовать комбинацию препаратов Левоксимед + Секнидокс для эмпирической терапии неосложненных форм ВЗОМТ в амбулаторных условиях.
Выводы
В амбулаторной практике лечения урогенитальных инфекций Секнидокс является препаратом выбора для терапии БВ, специфического трихомонадного вульвовагинита и неосложненных форм ВЗОМТ. Его рекомендуется применять как в качестве монотерапии, так и в комплексе с левофлоксацином.
Тематичний номер «Гінекологія, Акушерство, Репродуктологія» № 2 (26), червень-липень 2017 р.



